GB 47892-2010
基本信息
标准号: GB 47892-2010
中文名称:食品安全国家标准 食品微生物学检验 菌落总数测定
标准类别:国家标准(GB)
标准状态:现行
出版语种:简体中文
下载格式:.rar .pdf
下载大小:245KB
相关标签: 食品安全 国家标准 食品 微生物学 检验 菌落 总数 测定

标准分类号
关联标准
出版信息
相关单位信息
标准简介
GB 47892-2010 食品安全国家标准 食品微生物学检验 菌落总数测定
GB47892-2010
标准压缩包解压密码:www.bzxz.net
标准图片预览




标准内容
中华人民共和国国家标准
GB4789.2—2010
食品安全国家标准wwW.bzxz.Net
食品微生物学检验菌落总数测定National food safetystandardFood microbiological examination:Aerobic plate count2010-03-26发布
中华人民共和国卫生部
2010-06-01实施
本标准代替GB/T4789.2-2008《食品卫生微生物学检验菌落总数测定》本标准与GB/T4789.2-2008相比,主要修改如下:修改了标准的中英文名称:
-修改了菌落总数计算公式中的解释;修改了培养基和试剂;
菌落总数PetrifilmTM测试片法,-删除了第二法
本标准的附录A是规范性附录。
本标准所代替标准的历次版本发布情况为:GB4789.2-1984、GB4789.2-1994、GB/T4789.2-2003、GB/T4789.2-2008。
GB4789.2—2010
1范围
食品安全国家标准
食品微生物学检验
菌落总数测定
本标准规定了食品中菌落总数(Aerobicplatecount)的测定方法,本标准适用于食品中菌落总数的测定。2术语和定义
2.1菌落总数aerobicplatecountGB4789.2—2010
食品检样经过处理,在一定条件下(如培养基、培养温度和培养时间等)培养后,所得每g(mL)检样中形成的微生物菌落总数。设备和材料
除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:3.1恒温培养箱:36℃±1℃,30℃±1℃。3.2冰箱:2℃~5℃。
3.3恒温水浴箱:46℃±1℃。
3.4天平:感量为0.1g。
5均质器。
3.6振荡器。
3.7无菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)或微量移液器及吸头。3.8无菌锥形瓶:容量250mL、500mL。3.9无菌培养皿:直径90mm。
3.10pH计或pH比色管或精密pH试纸。1放大镜或/和菌落计数器。
4培养基和试剂
4.1平板计数琼脂培养基:见附录A中A.1。4.2
磷酸盐缓冲液:见附录A中A.2。4.3无菌生理盐水:见附录A中A.3。5检验程序
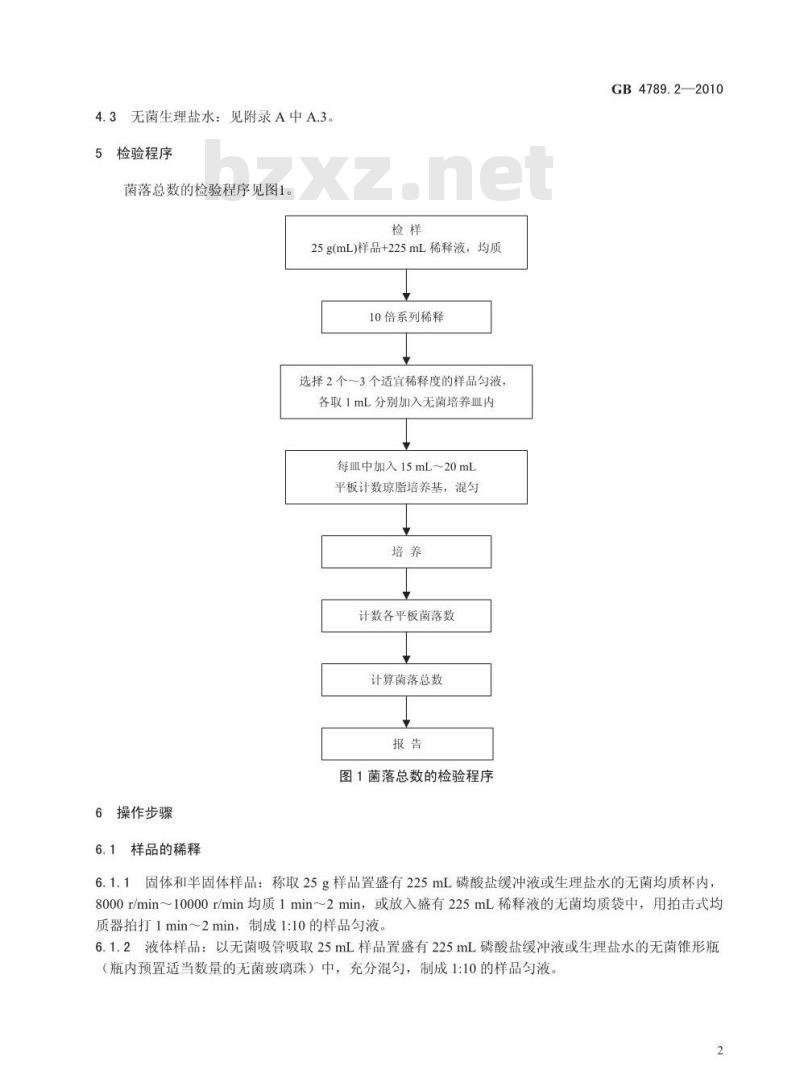
菌落总数的检验程序见图1。
25g(mL)样品+225mL稀释液,均质10倍系列稀释
选择2个~3个适宜稀释度的样品匀液,各取1mL分别加入无菌培养血内
每血中加入15mL~20mL
平板计数琼脂培养基,混匀
计数各平板菌落数
计算菌落总数
图1菌落总数的检验程序
6操作步骤
6.1样品的稀释
GB4789.2—2010
6.1.1固体和半固体样品:称取25g样品置盛有225mL磷酸盐缓冲液或生理盐水的无菌均质杯内,8000r/min~10000r/min均质1min~2min,或放入盛有225mL稀释液的无菌均质袋中,用拍击式均质器拍打1min~2min,制成1:10的样品匀液。6.1.2液体样品:以无菌吸管吸取25mL样品置盛有225mL磷酸盐缓冲液或生理盐水的无菌锥形瓶(瓶内预置适当数量的无菌玻璃珠)中,充分混匀,制成1:10的样品匀液。2
GB4789.2-2010
6.1.3用1mL无菌吸管或微量移液器吸取1:10样品匀液1mL,沿管壁缓慢注于盛有9mL稀释液的无菌试管中(注意吸管或吸头尖端不要触及稀释液面),振摇试管或换用1支无菌吸管反复吹打使其混合均匀,制成1:100的样品匀液。6.1.4按6.1.3操作程序,制备10倍系列稀释样品匀液。每递增稀释一次,换用1次1mL无菌吸管或吸头。
6.1.5根据对样品污染状况的估计,选择2个3个适宜稀释度的样品匀液(液体样品可包括原液),在进行10倍递增稀释时,吸取1mL样品匀液于无菌平皿内,每个稀释度做两个平皿。同时,分别吸取1mL空白稀释液加入两个无菌平血内作空白对照。6.1.6及时将15mL~20mL冷却至46℃的平板计数琼脂培养基(可放置于46℃±1℃恒温水浴箱中保温)倾注平血,并转动平血使其混合均匀。6.2培养
6.2.1待琼脂凝固后,将平板翻转,36℃±1℃培养48h+2h。水产品30℃±1℃培养72h±3h。6.2.2如果样品中可能含有在琼脂培养基表面弥漫生长的菌落时,可在凝固后的琼脂表面覆盖一薄层琼脂培养基(约4mL),凝固后翻转平板,按6.2.1条件进行培养。6.3菌落计数
可用肉眼观察,必要时用放大镜或菌落计数器,记录稀释倍数和相应的菌落数量。菌落计数以菌落形成单位(colony-formingunits,CFU)表示。6.3.1选取菌落数在30CFU~300CFU之间、无蔓延菌落生长的平板计数菌落总数。低于30CFU的平板记录具体菌落数,大于300CFU的可记录为多不可计。每个稀释度的菌落数应采用两个平板的平均数。
6.3.2其中一个平板有较大片状菌落生长时,则不宜采用,而应以无片状菌落生长的平板作为该稀释度的菌落数;若片状菌落不到平板的一半,而其余一半中菌落分布又很均勾,即可计算半个平板后乘以2,代表一个平板菌落数。
6.3.3当平板上出现菌落间无明显界线的链状生长时,则将每条单链作为一个菌落计数。7结果与报告
7.1菌落总数的计算方法
7.1.1若只有一个稀释度平板上的菌落数在适宜计数范围内,计算两个平板菌落数的平均值,再将平均值乘以相应稀释倍数,作为每g(mL)样品中菌落总数结果7.1.2若有两个连续稀释度的平板菌落数在适宜计数范围内时,按公式(1)计算:Ec/
/(n,+0.1n,)d
式中:
N样品中菌落数
ZC平板(含适宜范围菌落数的平板)菌落数之和:ni第一稀释度(低稀释倍数)平板个数;n2—第二稀释度(高稀释倍数)平板个数;d稀释因子(第一稀释度)。
示例:
稀释度
菌落数(CFU)
1:100(第一稀释度)
232,244
/(n,+0.1n2)d
232+244+33+35
[2 + (0.1×2)]×10-2 -
上述数据按7.2.2数字修约后,表示为25000或2.5×104。GB4789.2—2010
1:1000(第二稀释度)
33,35
7.1.3若所有稀释度的平板上菌落数均大于300CFU,则对稀释度最高的平板进行计数,其他平板可记录为多不可计,结果按平均菌落数乘以最高稀释倍数计算。7.1.4若所有稀释度的平板菌落数均小于30CFU,则应按稀释度最低的平均菌落数乘以稀释倍数计算。
7.1.5若所有稀释度(包括液体样品原液)平板均无菌落生长,则以小于1乘以最低稀释倍数计算,7.1.6若所有稀释度的平板菌落数均不在30CFU~300CFU之间,其中一部分小于30CFU或大于300CFU时,则以最接近30CFU或300CFU的平均菌落数乘以稀释倍数计算。7.2菌落总数的报告
7.2.1菌落数小于100CFU时,按“四舍五入”原则修约,以整数报告。7.2.2菌落数大于或等于100CFU时,第3位数字采用“四舍五入”原则修约后,取前2位数字,后面用0代替位数:也可用10的指数形式来表示,按“四舍五入”原则修约后,采用两位有效数学。7.2.3若所有平板上为蔓延菌落而无法计数,则报告菌落蔓延。7.2.4若空白对照上有菌落生长,则此次检测结果无效。7.2.5称重取样以CFU/g为单位报告,体积取样以CFU/mL为单位报告。4
附录A
(规范性附录)
培养基和试剂
A.1平板计数琼脂(platecountagar,PCA)培养基A.1.1成分
胰蛋白陈
酵母浸膏
葡萄糖
蒸馏水
pH 7.0±0.2
A.1.2制法
1000mL
GB4789.2—2010
将上述成分加于蒸馏水中,煮沸溶解,调节pH。分装试管或锥形瓶,121℃高压灭菌15min。A.2
磷酸盐缓冲液
A.2.1成分
磷酸二氢钾(KH2PO4)
蒸馏水
A.2.2制法
贮存液:称取34.0g的磷酸二氢钾溶于500mL蒸馏水中,用大约175mL的1mol/L氢氧化钠溶液调节pH,用蒸馏水稀释至1000mL后贮存于冰箱。稀释液:取贮存液1.25mL,用蒸馏水稀释至1000mL,分装于适宜容器中,121℃高压灭菌15minA3
无菌生理盐水
A.3.1成分
氯化钠
蒸馏水
A.3.2制法
1000mL
称取8.5g氯化钠溶于1000mL蒸馏水中,121℃高压灭菌15min。5
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
GB4789.2—2010
食品安全国家标准wwW.bzxz.Net
食品微生物学检验菌落总数测定National food safetystandardFood microbiological examination:Aerobic plate count2010-03-26发布
中华人民共和国卫生部
2010-06-01实施
本标准代替GB/T4789.2-2008《食品卫生微生物学检验菌落总数测定》本标准与GB/T4789.2-2008相比,主要修改如下:修改了标准的中英文名称:
-修改了菌落总数计算公式中的解释;修改了培养基和试剂;
菌落总数PetrifilmTM测试片法,-删除了第二法
本标准的附录A是规范性附录。
本标准所代替标准的历次版本发布情况为:GB4789.2-1984、GB4789.2-1994、GB/T4789.2-2003、GB/T4789.2-2008。
GB4789.2—2010
1范围
食品安全国家标准
食品微生物学检验
菌落总数测定
本标准规定了食品中菌落总数(Aerobicplatecount)的测定方法,本标准适用于食品中菌落总数的测定。2术语和定义
2.1菌落总数aerobicplatecountGB4789.2—2010
食品检样经过处理,在一定条件下(如培养基、培养温度和培养时间等)培养后,所得每g(mL)检样中形成的微生物菌落总数。设备和材料
除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:3.1恒温培养箱:36℃±1℃,30℃±1℃。3.2冰箱:2℃~5℃。
3.3恒温水浴箱:46℃±1℃。
3.4天平:感量为0.1g。
5均质器。
3.6振荡器。
3.7无菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)或微量移液器及吸头。3.8无菌锥形瓶:容量250mL、500mL。3.9无菌培养皿:直径90mm。
3.10pH计或pH比色管或精密pH试纸。1放大镜或/和菌落计数器。
4培养基和试剂
4.1平板计数琼脂培养基:见附录A中A.1。4.2
磷酸盐缓冲液:见附录A中A.2。4.3无菌生理盐水:见附录A中A.3。5检验程序
菌落总数的检验程序见图1。
25g(mL)样品+225mL稀释液,均质10倍系列稀释
选择2个~3个适宜稀释度的样品匀液,各取1mL分别加入无菌培养血内
每血中加入15mL~20mL
平板计数琼脂培养基,混匀
计数各平板菌落数
计算菌落总数
图1菌落总数的检验程序
6操作步骤
6.1样品的稀释
GB4789.2—2010
6.1.1固体和半固体样品:称取25g样品置盛有225mL磷酸盐缓冲液或生理盐水的无菌均质杯内,8000r/min~10000r/min均质1min~2min,或放入盛有225mL稀释液的无菌均质袋中,用拍击式均质器拍打1min~2min,制成1:10的样品匀液。6.1.2液体样品:以无菌吸管吸取25mL样品置盛有225mL磷酸盐缓冲液或生理盐水的无菌锥形瓶(瓶内预置适当数量的无菌玻璃珠)中,充分混匀,制成1:10的样品匀液。2
GB4789.2-2010
6.1.3用1mL无菌吸管或微量移液器吸取1:10样品匀液1mL,沿管壁缓慢注于盛有9mL稀释液的无菌试管中(注意吸管或吸头尖端不要触及稀释液面),振摇试管或换用1支无菌吸管反复吹打使其混合均匀,制成1:100的样品匀液。6.1.4按6.1.3操作程序,制备10倍系列稀释样品匀液。每递增稀释一次,换用1次1mL无菌吸管或吸头。
6.1.5根据对样品污染状况的估计,选择2个3个适宜稀释度的样品匀液(液体样品可包括原液),在进行10倍递增稀释时,吸取1mL样品匀液于无菌平皿内,每个稀释度做两个平皿。同时,分别吸取1mL空白稀释液加入两个无菌平血内作空白对照。6.1.6及时将15mL~20mL冷却至46℃的平板计数琼脂培养基(可放置于46℃±1℃恒温水浴箱中保温)倾注平血,并转动平血使其混合均匀。6.2培养
6.2.1待琼脂凝固后,将平板翻转,36℃±1℃培养48h+2h。水产品30℃±1℃培养72h±3h。6.2.2如果样品中可能含有在琼脂培养基表面弥漫生长的菌落时,可在凝固后的琼脂表面覆盖一薄层琼脂培养基(约4mL),凝固后翻转平板,按6.2.1条件进行培养。6.3菌落计数
可用肉眼观察,必要时用放大镜或菌落计数器,记录稀释倍数和相应的菌落数量。菌落计数以菌落形成单位(colony-formingunits,CFU)表示。6.3.1选取菌落数在30CFU~300CFU之间、无蔓延菌落生长的平板计数菌落总数。低于30CFU的平板记录具体菌落数,大于300CFU的可记录为多不可计。每个稀释度的菌落数应采用两个平板的平均数。
6.3.2其中一个平板有较大片状菌落生长时,则不宜采用,而应以无片状菌落生长的平板作为该稀释度的菌落数;若片状菌落不到平板的一半,而其余一半中菌落分布又很均勾,即可计算半个平板后乘以2,代表一个平板菌落数。
6.3.3当平板上出现菌落间无明显界线的链状生长时,则将每条单链作为一个菌落计数。7结果与报告
7.1菌落总数的计算方法
7.1.1若只有一个稀释度平板上的菌落数在适宜计数范围内,计算两个平板菌落数的平均值,再将平均值乘以相应稀释倍数,作为每g(mL)样品中菌落总数结果7.1.2若有两个连续稀释度的平板菌落数在适宜计数范围内时,按公式(1)计算:Ec/
/(n,+0.1n,)d
式中:
N样品中菌落数
ZC平板(含适宜范围菌落数的平板)菌落数之和:ni第一稀释度(低稀释倍数)平板个数;n2—第二稀释度(高稀释倍数)平板个数;d稀释因子(第一稀释度)。
示例:
稀释度
菌落数(CFU)
1:100(第一稀释度)
232,244
/(n,+0.1n2)d
232+244+33+35
[2 + (0.1×2)]×10-2 -
上述数据按7.2.2数字修约后,表示为25000或2.5×104。GB4789.2—2010
1:1000(第二稀释度)
33,35
7.1.3若所有稀释度的平板上菌落数均大于300CFU,则对稀释度最高的平板进行计数,其他平板可记录为多不可计,结果按平均菌落数乘以最高稀释倍数计算。7.1.4若所有稀释度的平板菌落数均小于30CFU,则应按稀释度最低的平均菌落数乘以稀释倍数计算。
7.1.5若所有稀释度(包括液体样品原液)平板均无菌落生长,则以小于1乘以最低稀释倍数计算,7.1.6若所有稀释度的平板菌落数均不在30CFU~300CFU之间,其中一部分小于30CFU或大于300CFU时,则以最接近30CFU或300CFU的平均菌落数乘以稀释倍数计算。7.2菌落总数的报告
7.2.1菌落数小于100CFU时,按“四舍五入”原则修约,以整数报告。7.2.2菌落数大于或等于100CFU时,第3位数字采用“四舍五入”原则修约后,取前2位数字,后面用0代替位数:也可用10的指数形式来表示,按“四舍五入”原则修约后,采用两位有效数学。7.2.3若所有平板上为蔓延菌落而无法计数,则报告菌落蔓延。7.2.4若空白对照上有菌落生长,则此次检测结果无效。7.2.5称重取样以CFU/g为单位报告,体积取样以CFU/mL为单位报告。4
附录A
(规范性附录)
培养基和试剂
A.1平板计数琼脂(platecountagar,PCA)培养基A.1.1成分
胰蛋白陈
酵母浸膏
葡萄糖
蒸馏水
pH 7.0±0.2
A.1.2制法
1000mL
GB4789.2—2010
将上述成分加于蒸馏水中,煮沸溶解,调节pH。分装试管或锥形瓶,121℃高压灭菌15min。A.2
磷酸盐缓冲液
A.2.1成分
磷酸二氢钾(KH2PO4)
蒸馏水
A.2.2制法
贮存液:称取34.0g的磷酸二氢钾溶于500mL蒸馏水中,用大约175mL的1mol/L氢氧化钠溶液调节pH,用蒸馏水稀释至1000mL后贮存于冰箱。稀释液:取贮存液1.25mL,用蒸馏水稀释至1000mL,分装于适宜容器中,121℃高压灭菌15minA3
无菌生理盐水
A.3.1成分
氯化钠
蒸馏水
A.3.2制法
1000mL
称取8.5g氯化钠溶于1000mL蒸馏水中,121℃高压灭菌15min。5
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。