标准分类号
标准ICS号:
03.120.00
中标分类号:综合>>标准化管理与一般规定>>A00标准化、质量管理
关联标准
采标情况:ISO/TS 19036:2006,MOD
出版信息
出版社:中国标准出版社
页数:24页
标准价格:24.0
出版日期:2017-04-01
相关单位信息
起草人:马维兴、林超、王曼霞、雷质文
起草单位:中华人民共和国山东出入境检验检疫局
提出单位:国家认证认可监督委员会
发布部门:国家认证认可监督管理委员会
标准简介
RB/T 151-2016 食品微生物定量检测的测量不确定度评估指南
RB/T151-2016
本标准规定了食品微生物定量检测的测量不确定度的评定和表示方法。
本标准适用于食品,以及用于监测加工和贮藏食品的环境样品的定量分析的测量不确定度评估活动,也适用于可替代微生物常规菌落计数方法的仪器定量分析法。
本标准不适用于最可能值计数方法以及低含量微生物的分析方法。
动物饲料产品定量分析的测量不确定度评估也参考本标准。
标准内容
ICS03.120.00
中华人民共和国认证认可行业标准RB/T151—2016
食品微生物定量检测的
测量不确定度评估指南
Guidelines for the estimation of measurement uncertainty offoodmicrobiologicalquantitativedetection(ISO/TS 19036:2006 Microbiology of food and animal fceding stuffs-Guidelines for theestimation of measurementuncertainty forquantitativedeterminations,MOD)2016-09-22发布
国家认证认可监督管理委员会
2017-04-01实施
本标准按照GB/T1.1—2009的规则起草。RB/T151—2016
本标准使用重新起草法修改采用ISO/TS19036:2006《食品与动物饲料微生物学定量检测不确定度的评估指南》(英文版)。本标准与ISO/TS19036:2006《食品与动物饲料微生物学定量检测不确定度的评估指南》(英文版)存在的技术性差异如下:
将ISO/TS19036:2006中与动物饲料相关的所有内容删除,只保留与食品相关的内容;加入规范性引用文件章节;
用\GB/T270252008\替换ISO/TS19036:2006中的ISO/IEC17025:2005”;将ISO/TS19036:2006中2.1“注3”,修改为正文内容;将ISO/TS19036:2006中4.2和5\实验室内再现性标准偏差(intralaboratorystandarddevia-tionof reproducibility)”作出解释,并注明使用“实验室内再现性标准偏差”这一名称进行表述的原因,
将ISO/TS19036:2006中5.2.2“注1”和“注2”修改为正文内容;将ISO/TS19036:2006表A.1~表A.5中“sR”与\ss”“sm”和“sr”三者之间的数值关系和“scnnd”“sea”的计算方法做了表述。本标准还做了下列编辑性修改:用\a”“b”“c”“d”依次代替英文版ISO/TS19036:2006附录表A.1~表A.5中“分类(category)”一栏中的\i\\ii\\ii\\iv”,使之与A.2.2基质的分类所用符号一致;删除国际标准的序言和前言。
本标准由国家认证认可监督委员会提出并归口。本标准起草单位:中华人民共和国山东出人境检验检疫局。本标准主要起草人:马维兴、林超、王曼霞、雷质文。1范围
食品微生物定量检测的
测量不确定度评估指南bzxZ.net
本标准规定了食品微生物定量检测的测量不确定度的评定和表示方法RB/T151—2016
本标准适用于食品,以及用于监测加工和贮藏食品的环境样品的定量分析的测量不确定度评估活动,也适用于可替代微生物常规菌落计数方法的仪器定量分析法。本标准不适用于最可能值计数方法以及低含量微生物的分析方法。动物饲料产品定量分析的测量不确定度评估也参考本标准。2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注口期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB/Z22553—2010利用重复性、再现性和正确度的估计值评估测量不确定度的指南GB/T270252008检测和校准实验室能力的通用要求ISO16140:2003食品和动物饲料微生物学替代方法验证协议(Microbiologyoffoodandanimal feeding stuffsProtocol for the validation of alternative mcthods)ISO/IECGuide98-3:2008测量的不确定度第3部分:测量中不确定度的表示指南(GUM:1995,Guide to the expression of uncertainty in measurement)3术语和定义
下列术语和定义适用于本文件。3.1
测量不确定度
uncertainty (of measurement)与测量结果相关联的参数,用以表征合理赋予被测量值的分散性。注1:此参数可以是标准偏差或其倍数,也可以是给定置信概率的置信区间的半宽度注2:测量不确定度一般由许多分量组成,其中一些分量可以用测量结果的统计分布来进行测算,并且以实验标准偏差表征;而另些分量可以根据经验或其他信息的假定概率分布来进行测算,并且也以标准偏差表征。测量结果为被测量值的最佳估计。所有不确定度的分量都与分散性有关,包括那些由系统影响产生的分量(如与修正值和参考测量标准相关的)。3.2
standarduncertainty
标准不确定度
以标准偏差表示的测量不确定度。3.3
combined standard uncertainty合成标准不确定度
当测量结果是由若干个其他量的值求得时,按其他的各量的方差和协方差计算出的标准不确定度。1
RB/T151—2016
扩展不确定度expandeduncertaintyU
确定测量结果区间的量,合理赋予被测量的值大多数在此区间。注:此区间也被称为覆盖概率或置信区间概率(置信概率)。扩展不确定度一定要有一个明确的扩展区间。要将一个特定置信概率与扩展不确定度所规定的区间结合起来,需要对测量结果及其标准不确定度所表示的概率分布进行外在或隐含假设,这个区间可能的置信概率只有在这些假设验证成立的范围内有效。扩展不确定度U是由合成标准不确定度u((3.3)和包含因子k(3.5)计算出的:U一ku(y)。3.5
包含因子
coverage faetnr
包含因子的值通常作为合成标准不确定度的倍数,两者的乘积即为扩展不确定度。注:包含因子
范围内。
结果的期望值与可接受的参考值之间的差注:与随机误差相比,偏倚是指点的系统差,它商可接受的参考值之间的案就识美4原理
4.1整体法评估测量不确定度
,也可能是市多个系统误差组成,偏倚值越大,说明本标准来用整体法评估测量不确定度它是以影响测试结果分析程序的总变量为基础进行评估的,这个总变量包括精密度(任意成分)和偏倚(系统成分)。在食品微生物领域的实际应用中,通常不考虑偏倚(4.2)。
本标准中测量不确定度的整体法评估,是对全部测量程序最终结果可再现性的标准偏差进行实验性评估得到的。该标准偏差相当于合成标准不确定度(5.1)。整体法可看作是一个黑原了”系统(如图1所示),食品微生物不确定度的主要来源都被标识出来了。该图有助于识别不确定度米源,不论其是否包括在实验方案中2
实验室
培养基
随机误差
次级取样/
初级稀释
操作员/时间
RB/T151—2016
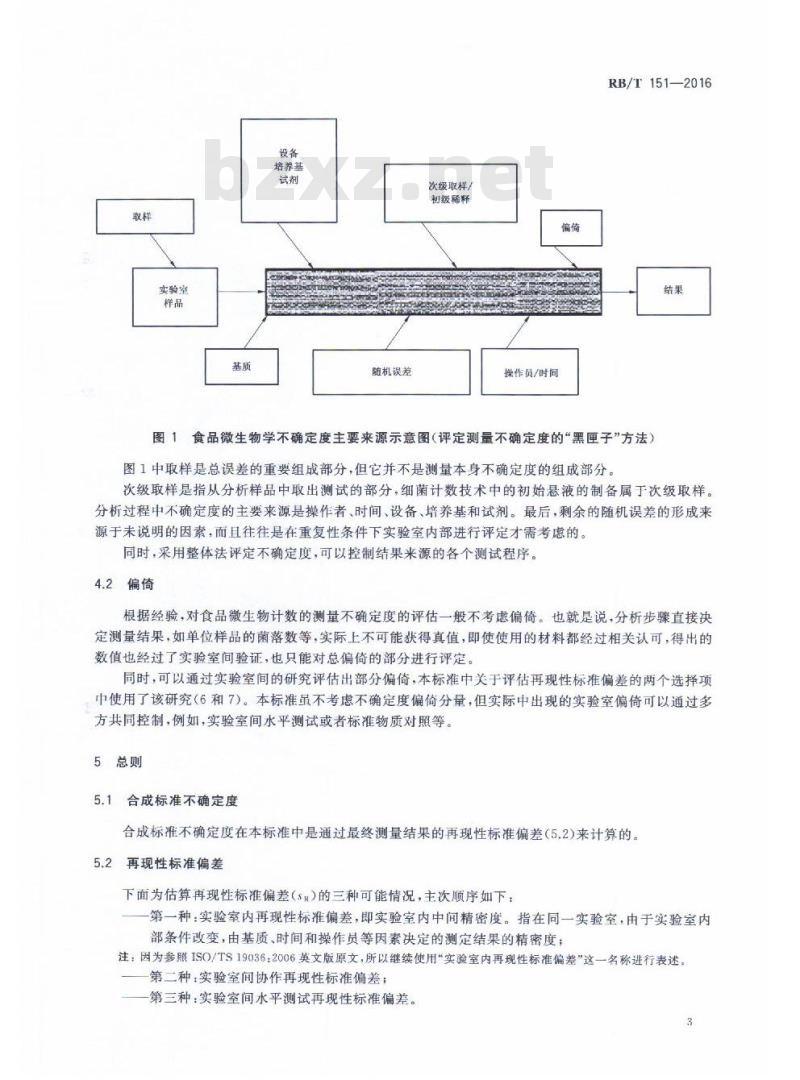
图1食品微生物学不确定度主要来源示意图(评定测量不确定度的“黑匣子”方法)图1中取样是总误差的重要组成部分,但它并不是测量本身不确定度的组成部分。次级取样是指从分析样品中取出测试的部分,细菌计数技术中的初始悬液的制备属于次级取样。分析过程中不确定度的主要来源是操作者、时间、设备、培养基和试剂。最后,剩余的随机误差的形成来源于未说明的因素,而且往往是在重复性条件下实验室内部进行评定才需考虑的。同时,采用整体法评定不确定度,可以控制结果米源的各个测试程序。4.2偏倚
根据经验,对食品微生物计数的测量不确定度的评估一般不考虑偏倚。也就是说,分析步骤直接决定测量结果,如单位样品的菌落数等,实际上不可能获得真值,即使使用的材料都经过相关认可,得出的数值也经过了实验室间验证,也只能对总偏倚的部分进行评定。同时,可以通过实验室间的研究评估出部分偏倚,本标准中关于评估再现性标准偏差的两个选择项中使用了该研究(6和7)。本标准虽不考虑不确定度偏分量,但实际中出现的实验室偏倚可以通过多方共同控制,例如,实验室间水平测试或者标准物质对照等。5总则
5.1合成标准不确定度
合成标准不确定度在本标准中是通过最终测量结果的再现性标准偏差(5.2)来计算的。5.2再现性标准偏差
下面为估算再现性标准偏差(s)的三种可能情况,主次顺序如下:第一种:实验室内再现性标准偏差,即实验室内中间精密度。指在同一实验室,由于实验室内部条件改变,由基质、时间和操作员等因素决定的测定结果的精密度;注:因为参照ISO/TS19036:2006英文版原文,所以继续使用“实验室内再现性标准偏差”这一名称进行表述。第二种:实验室间协作再现性标准偏差;第三种:实验室间水平测试再现性标准偏差。3
RB/T151—2016
第一种情况最为主要。
在5.4中列出了估算再现性标准偏差的基本原则。以上三种情况将在第6章~第8章中详细说明。
5.3扩展不确定度
按照ISO/IECGuide98-3:2008,扩展不确定度U为合成标准不确定度u(y)(3.3)和包含因了表(3.5)的乘积,本标准中k值为2(大约对应95%的置信水平),按式(1)计算:U=ku.(y)=2u.(y)=2sR
式中:
包含因子;
扩展不确定度
u(y)
合成标准不确定度
再现性标准偏美
估算再现性标准偏差的基本原则·(1)
本标准引用的黑更了理念,其实就是提倡要尽可能多地考虑图1中不确定度来源,特别是实验室要了解测试的基质里的微生物分布,并将其考虑到测算不确是度的次级取样分量中(1.1)再现性标准偏差要针对每种日标微生物(或与自标微生物一致的群体)佳对每种基质(或与基质一,通过
致的群体)
注1:
个获得常规测试结果的指定的实验车方法进行估算致”是指对测量不确定度有同价值的撤量物、方法或基质的群你注2:影响测生不确定度评估的主更因素是实验室自身的情祝特定的检侧条件(如不同的操作员,操作过程、仪个种定的测量不确定度值。实验空分析方法对测量不试剂等)下将得到
确定度评估的影响并
不特定的检测结果会得到一
按照B/127025一2008的准如确定来自方法或实验室方前的可能影响测量结果的美键因素,如培养基或其他试剂的来源、种类计算方法(人工或自动操作者等,并证明这些关键因素受到有效控制。为了保证估算能反映实际情况,测试结果能得到有效控制,对测量不确定度的估算工作要进行必要的过程监控。
上任何关键因素发生变化时,测量不确定度都需要重新估算。6实验室内再现性标准偏差
6.1概述
实验室内再现性标准偏差,是获取测量不确定度的首选。实验室可以据此在检测报告中给出测量不确定度值。此方法的理论缺陷是无法考虑到偏倚在食品微生物学中,基质对测量不确定度的影响是不可避免的,因此实验方案需要考虑从样品(如测试的食物样品)中选取测试部分所进行的次级取样对测量不确定度的影响。对于每一种目标微生物(或与目标微生物一致的群体)和一种指定的基质,实验方案(6.2)的实施要在同样基质中至少10个样品上进行。为了尽可能覆盖不同时间所引起的操作条件的变化,重复实验需在不同的日期进行,这样就可获得一段时间内累积的数据。检测的基质种类数取决于实验室常规分析的基质的多样性。选定的基质要在对不确定度值的影响方面以及以往实验室分析所用基质类型方面都具有一定的代表性,还要适合于所测试的微生物。附录A通过列举大量具有国际水准实验室的实验结果为我们提供了基质选择指南。其目的是评价来自实验室样品测试部分的次级取样和准备初始悬浮液相关的测量不确定度分量。更多的指导信息请按照ISO16140:2003市附录B。
RB/T151—2016
在不考虑低水平污染的情况下,将数据转换成对数形式再计算标准偏差,这样可以稳定不同污染程度下标准偏差的再现性变化。因此,不需要对每种污染水平的再现性标准偏差一一进行估算,但是选取的样品和(或)稀释浓度仍要尽可能地涵盖常规检测的浓度范围。选择样品时要尽可能多地使用白然污染的样品,以便能够给出更为真实的测量不确定度的估值,这样才能更好地定性自然污染样品的实验结果。若需要接种目标菌,一定要严格控制,防止对结果造成其他影响。接种需要尽可能设计模仿真正的污染物。
6.2实验方案
实验方案的描述如图2所示。
食品样品
操作员1(情况A)
初级最浮液
人造污染物
(如果需要)
不同情况
操作员2(情况B)
初级悬浮液
图2测算实验室内再现性标准偏差的实验方案对于每种样品,每个操作员取一次试验的剂量,用其制备一份初级悬浮液,进行一次分析。分析按常规测验(如进行一系列10倍梯度稀释,每个稀释度接种到12个平血)进行。在测试时,“操作员”可以为一组人员(技术人员),每人负责指定的部分。在这种情况下,整组人员要被看成一个操作员。成员的任务分配发生变化时,则该组成员将被视为另一个操作员。本方案来源于4.1中提到的黑匣子法。不同的不确定度来源,如次级取样、基质的性质、残留的随机误差、操作员、时间等,同时加以考虑。情况A和情况B要尽量不同,也要尽可能多地包含实验室不同检测日期内遇到的不同情况,如技术人员,各批次的培养基和试剂、漩涡混合器、PH计、培养箱、分析时间等。如果食品样品的污染情况相对稳定(这种情况在食品微生物学中比较少见),情况A和情况B要包含不同的分析日期。6.3应用
图3给出了本方案中不确定度的主要来源,以及排除的项目(取样和偏倚)。5
RB/T151—2016
注:排除的来源用叉号表示。
培养基
次级取样/
初级稀粹
随机误差
操作员/时间
图3实验室内再现性实验中涵盖和排除的主要不确定度来源结果
本方案将测试部分样品取样的影响并入到总不确定度评估中了。另外在食品微生物学中,食品的自然污染水平(尤其是加工,熟制后的固体食物等)通常差异很大。因此,本方案考虑到了由这种不均勾性导致的结果差异,这对评定样品分析结果超山范围的情况时(如微生物标准规定)是非常重要的注:如果对人工污染初始悬浮液(图2)估算其不确定度时,基质差异对不确定度的影响可不予考虑但是,这种方案在某些情况下可行性很低。因为自然污染物的分布和基质的种类紧密相联,这就是为什么实验方案要使用每种基质(或一致的基质群体)反复进行常规分析的原因。当然实验室分析基质越多,所带来的工作量也就越大。本方案不包括偏差对测量不确定度可能的影响。6.4计算
按照惯例,在计算之前,数据(微生物计数结果)单位从CFU/g或CFU/mL转换为log1(CFU/g)或log1e(CFU/mL)
注:按照ISO,十进制对数的符号为“1g”。但在本标准中,推荐使用在食品微生物学实验室领域中广为使用的符号\logio\
计算n个给定基质样品的再现性标准偏差5R的方法,按式(2)计算:SR
式中:
再现性标准偏差;
(yiA-YB)
对数转换值,单位为log1。(CFU/g)或logh(CFU/mL);给定基质样品数量;
样品的序号,i=1~n(n≥10);再现性条件的编号,j=A或j=B。表1中列举了混合家禽肉中好氧嗜中温菌群的示例。6
-(2)
再现性标准偏差的计算
RB/T151—2016
混合家禽肉中好氧嗜中温性菌群的计数示例YiAlogIo(TA)
对y;数值取对数,则再现性标准偏差为:SR
(Yi—y)\/2
实验室间协作再现性标准偏差
7.1概述
0.0064+0.0017+.+0.0453
yBloglo(rB)
(YiA-B)\
V0.02191-0.15(log1o)CFU/g
若实验室内常规测试的方法已提交到实验室间进行确认,在以下前提条件下(见下文),该实验室可使用此再现性标准偏差计算方法测算测量不确定度。来自实验室间再现性研究的标准偏差仅与方法有关,与报告不确定度结果的实验室无关。这些前提条件为:
实验室偏差要与实验室间协作研究预期要得到的重复性和再现性一致;实验室内测量得出的精密度要与实验室间协作研究预期要得到的重复性和再现性一致;实验室间协作研究要正确地包含了各种不确定度的来源(特别是样品制备和均质)。GB/Z225532010中对这些情况都进行了详细说明。7.2在食品微生物学中的应用
图4标出了本方案中包含的和已排除的(取样)不确定度的主要来源。7
RB/T151—2016
注:排除的来源用叉号标出。
培养基
次级取样/韧级稀释
重复性标准偏差
操作员/时间
图4跨实验室协作研究包含和排除的不确定度主要来源次级取样,初始悬液的制备以及基质这些因素对不确定度的影响依赖于实验的设计情况。结果
这种方法能够使参与实验室间协作研究的某一实验室对其实验偏倚,测量不确定度的部分偏倚分量进行评估,本标准对该方面内容不做详细介绍。计算方法见第6章。但是在食品微生物学中,本方法有一定的局限性,以下会列出。这也是为什么在5.2中按主次顺序将其列为第二种情况的原因。
除了需要检查实验室间的精密度和偏倚值与采用本方法的实验室间研究所得的相应值一致外,实际上只有很少的再现性参数是通过实验室间标准化参考方法研究得出的。而且,根据特殊样品分析米概括常规样品分析会有一定的难度。实验室间研究得出的精密度是在正好符合某些限制条件下得出的,该条件整合了基质、微生物种类、污染水平以及给定的背景微生物群落(如果出现)等。而且,由于要满足协作研究中对样品均匀性的要求,所以与实际情况相比,在送往实验空过程中样品的均勾性和稳定性使得样品污染的机会减少,这样就导致对不确定度的估计不足。8实验室间水平测试再现性标准偏差如果实验室参加了一项实验室间的水平测试,在以下情况下,可以用从该测试中得出的再现性标准偏差来推算其测量不确定度:
在实验室间测试中,该实验室使用的方法为常规分析中所使用的方法;在测试中使用的样品(在基质和污染水平方面)和常规分析的样品类似;参试实验室没有使用不同的测试方法,或者有足够数量的参试者使用同样方法,从而确保正确估计再现性标准偏差。
图4说明了本方案中不确定度的主要来源和一个排除的因素:取样。该方法的目的之一是使参与实验室间水平测试的实验室能够评估部分测量不确定度偏倚分量,本标准方法对该方面不做详细说明。计算方法见第6章。9测试报告中测量不确定度的表示依照上述方法得出测量不确定度之后,如果需要,可在报告中与测试结果一起表述,表述方法可以为log1.为单位的区间、白然值(每克或每毫升的CFU值)或百分比。下面给出相关示例。报告的结果9
或不确定度的区间的值不超过两位有效数字RB/T151—2016
测试结果以y=log10表示,再现性标准偏差以sR表示,在包含因子k一2(置信水平95%)时,则扩展不确定度U等于25R。
测试结果可按照以下的形式进行报告:y±2sr(logio);
y·logioLy-2sR·y+2s;
xCFU/g或CFU/mL[10%-2R,10+2k],%,10%+10%+2起
αCFU/g或CFU/mL10%_
10%-2R
示例:再现性标准偏差8k为土0.151og19,这样包含因子为2(置信水平95%)的扩展不确定度U即为0.15×2-0.3log10:测试结果为5.0log1oCFU/g。测试结果可以用下列形式进行报告:-5.0log1o±0.3logie
5.0logio[4.7,5.3];
10°CFU/g[5X10/,2X105]
-10CFU/g[10550%,105+100%
RB/T151—2016
附录A
(资料性附录)
与次级取样试验和初始悬浮液制备相关的不确定度分量的试验结果A.1简介和实验方案
试验由AFSSA(法国)组织,代表ISO/TC34/SC9秘书处,在2003年和2004年进行。目的是测定不同产品基质中关于次级取样和初始悬液制备部分对测量不确定度的影响。一个样品在不同的条件下可以得出8组计数结果,在图A.1中详细列出。实验室()
初始悬液(A)
条件(1)
说明:
初始悬液(A)、初始悬液(B)
条件(1)、条件(2)
编号A11、A12等
条件(2)
条件(1)
初始悬液(B)
条件(2)
分别制备的两组初始悬液,两组悬浮液的情况尽可能不同(如不同的操作员、不同的平衡程度、不同的稀释液批次等);两组尽量不同的条件(不同的操作员、不同批次的培养基、不同的培养箱等);在重复条件下的两次操作(例如,每一种条件下,对初始悬浮液的两组稀释)。注:图2(6.2)的实验方案为图A.1的简化版,在图2中只列举出了图A.1中的A11和B21。图A.1
实验方案
A.2结果
A.2.1概述
共有79个实验室参加了此次测试,实验室按1~79号依次编号,每个实验室使用了一种或多种方法对一类或多类基质进行试验,因此共搜集到了122个数据文件(一个实验室、一种方法和一种基质)。其中,有28个数据文件由于不符合试验标准而未采用。这样就获得了94个再现性标准偏差(sR),每个都来自一个实验室、一种方法和一种基质。另外,依据变化分量理论,每个再现性标准偏差都能够通过以下3种不确定度来源进行识别:a)与基质、试验部分次级取样和初始稀释相关的;b)
与再现性情况(操作员/时间)相关的;c
与重复性条件下随机误差相关的。
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。






 ✕
✕