基本信息
标准号:
GB 31660.6-2019
中文名称:动物性食品中5种α2-受体激动剂残留量的测定 液相色谱-串联质谱法
标准类别:国家标准(GB)
标准状态:现行
出版语种:简体中文
下载格式:.zip .pdf
下载大小:401.13 KB
相关标签:
食品
受体
激动剂
残留量
测定
色谱
串联
质谱法

标准分类号
关联标准
出版信息
相关单位信息
标准简介
标准号:GB 31660.6-2019
标准名称:动物性食品中5种α2-受体激动剂残留量的测定 液相色谱-串联质谱法
英文名称:Determination of five kinds of alpha-ago ists residues in animal
derived food by liquid chromatography- tandem mass spectrometry method
标准格式:PDF
发布时间:2019-09-06
实施时间:2020-04-01
标准大小:314K
标准介绍:食品安全国家标准
本标准规定了动物性食品中5种2-受体激动剂的制样和液相色谱串联质谱测定方法。
本标准适用于猪肌肉、肝脏和肾脏组织及鸡肌肉和肝脏组织中替扎尼定、赛拉嗪、溴莫
尼定、安普乐定和可乐定残留量的测定。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅所注日期的版本
适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件
GBT6682分析实验室用水规格和试验方法
试样中残留的α受体激动剂,用碳酸钠缓冲溶液、乙酸乙酯提取,固相萃取柱净
液相色谱串联质谱测定,外标法定量
除另有规定外,所有试剂均为分析纯,水为符合GBT6682规定的一级水
4.1试剂
41.1乙腈(CHCN):色谱纯
4.1.2甲酸( HCOOH):色谱纯
4.1.3甲醇(CH3OH)
414氨水(NHOH)
41.5无水碳酸钠(Na2CO3)。
41.6碳酸氢钠( Nahco3)
41.7乙酸乙酯(CH3 COOC,H)
4.2溶液配制
42.1碳酸钠溶液:取无水碳酸钠10.6g,用水溶解并稀释至100mL
42.2碳酸氢钠溶液:取碳酸氢钠84g,用水溶解并稀释至100mL
42.3碳酸钠缓冲溶液:取碳酸钠溶液90mL、碳酸氢钠溶液10mL,混匀,现用现配。
42.4甲酸溶液(0.2%):取甲酸1mL,用水溶解并稀释至500mL。4.2.5甲酸-乙腈溶液:取02%甲酸溶液80mL,加乙腈20m,混匀4.2.6氨水甲醇溶液(5%):取氨水5mL,用甲醇溶解并稀释至100mL。
标准内容
中华人民共和国国家标准
GB31660.62019
食品安全国家标准
动物性食品中5种α2-受体激动剂残留量的测定
液相色谱-串联质谱法
National food safety standard-Determination of five kinds of alpha-agonists residues in animaderivedfoodby Iiquid chromatography-tandemmass spectrometrymethod2019-09-06发布
中华人民共和国农业农村部
中华人民共和国国家卫生健康委员会国家市场监督管理总局
2020-04-01实施
本标准系首次发布。
GB31660.62019
1范围
食品安全国家标准
GB31660.62019
动物性食品中5种α2-受体激动剂残留量的测定液相色谱-串联质谱法
本标准规定了动物性食品中5种2-受体激动剂的制样和液相色谱-串联质谱测定方法本标准适用于猪肌肉、肝脏和肾脏组织及鸡肌肉和肝脏组织中替扎尼定、赛拉嗪、溴莫尼定、安普乐定和可乐定残留量的测定规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅所注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB/T6682分析实验室用水规格和试验方法3原理
试样中残留的α2-受体激动剂,用碳酸钠缓冲溶液、乙酸乙酯提取,固相萃取柱净化,液相色谱-串联质谱测定,外标法定量。4试剂和材料
除另有规定外,所有试剂均为分析纯,水为符合GB/T6682规定的一级水。4.1试剂
4.1.1乙(CHCN):色谱纯。
4.1.2甲酸(HCOOH):色谱纯
4.1.3甲醇(CH,OH)。
氨水(NHOH)。
无水碳酸钠(Na2CO3)。
碳酸氢钠(NaHCO,)。
乙酸乙酯(CHCOOCH)。
4.2溶液配制
碳酸钠溶液:取无水碳酸钠10.6g,用水溶解并稀释至100mL。碳酸氢钠溶液:取碳酸氢钠8.4g,用水溶解并稀释至100mL。碳酸钠缓冲溶液:取碳酸钠溶液90mL、碳酸氢钠溶液10mL,混匀,现用现配。甲酸溶液(0.2%):取甲酸1mL,用水溶解并稀释至500mL。4.2.4
甲酸-乙晴溶液:取0.2%甲酸溶液80mL,加乙睛20mL,混匀。4.2.5
4.2.6氨水甲醇溶液(5%):取氨水5mL,用甲醇溶解并稀释至100mL。4.3标准品
盐酸替扎尼定(Tizanidinehydrochloride,C,H.CIN,S·HCl,CAS:64461-82-1)、盐酸赛拉嗪(XylazineHydrochloride,Cr2HiN,S,CAS:7361-61-7)、溴莫尼定(Brimonidine,C1HoBrNsCAS:59803-98-4)、盐酸安普乐定(Apraclonidinehydrochloride,C,HioN4Cl2·HCl1
GB31660.62019
CAS:73218-79-8)和盐酸可乐定(Clonidinehydrochloride,CHioClN3,CAS:4205-91-8):含量均≥98%。
4.4标准溶液制备
4.4.1标准贮备液:取盐酸替扎尼定、盐酸赛拉嗪、溴莫尼定、盐酸安普乐定和盐酸可乐定标准品各约10mg,精密称定,分别于10mL量瓶中,用甲醇溶解并稀释至刻度,配制成浓度均为1mg/mL的盐酸替扎尼定、盐酸赛拉嗪、溴莫尼定、盐酸安普乐定和盐酸可乐定标准贮备液。2~8℃保存,有效期6个月。4.4.2混合标准工作液:分别精密量取上述标准购备液各1mL,手100mL量瓶中,用甲醇溶解并稀释至刻度,配制成浓度为10μg/mL的混合标准工作液。于2~8℃保存,有效期1个月。
4.4.3标准曲线制备:分别精密量取混合标准工作液适量,用甲酸-乙溶液稀释配制成浓度为0.5、1、10、50和100ug/L系列混合标准工作液,临用现配4.5材料
4.5.1固相萃取MCX柱:60mg/3mL,或相当者。4.5.2滤膜:有机相,0.22μm。5仪器和设备
5.1液相色谱-串联质谱仪:配电喷雾电离源。5.2分析天平:感量0.00001g和0.01g。5.3均质机。
5.4离心机。
5.5涡旋振荡器。
5.6旋转蒸发仪。
固相萃取装置。
5.8鸡心瓶。
5.9离心管:50mL。
试料的制备与保存
6.1试料的制备
取适量新鲜或解冻的空白或供试组织,绞碎并使均质。取均质的供试样品,作为供试试料。取均质的空白样品,作为空白试料。一取均质的空白样品,添加适宜浓度的标准工作液,作为空白添加试料。6.2样品的保存
-20℃以下保存。
测定步骤
7.1提取
GB31660.62019
取试料2g(准确至土20mg),于50mL离心管中,加碳酸钠缓冲液5mL,振荡混匀,加乙酸乙酯10mL,充分振荡,于8000r/min离心5min,取上清液于鸡心瓶中,下层溶液中加乙酸乙酯10mL重复提取一次,合并两次上清液。于55℃旋转蒸发至干,加甲酸-乙睛溶液4.0mL溶解残余物,备用。
7.2净化
MCX柱依次用甲醇、水各3mL活化。取备用液过柱,用水3mL、甲醇3mL分别淋洗,挤干,氨水甲醇溶液6mL洗脱,收集洗脱液,于60℃旋转蒸发至干,用甲酸-乙睛溶液1.0mL溶解残余物,滤过,液相色谱-串联质谱测定。7.3测定
7.3.1色谱条件
a)色谱柱:Ci8(100mmx3.0mm,粒径1.8jμm),或相当者:b)柱温:30℃;
c)进样量:10μL;
d)流速:0.3mL/min;
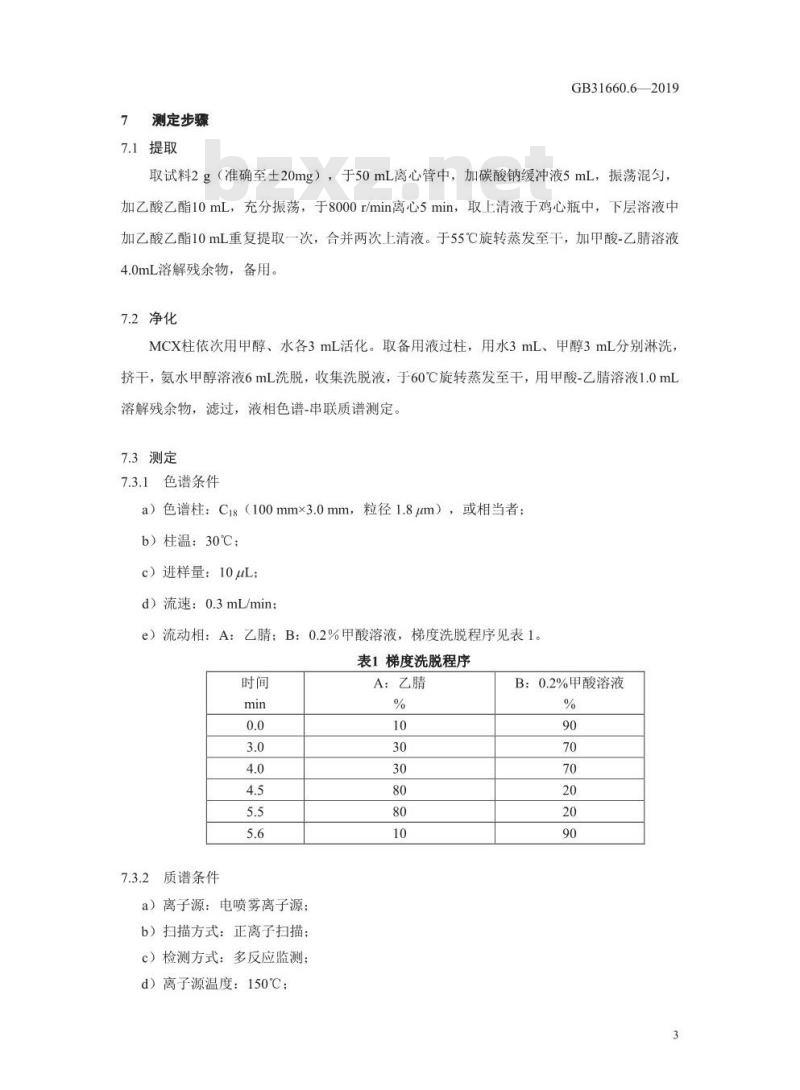
e)流动相:A:乙睛:B:0.2%甲酸溶液,梯度洗脱程序见表1。表1梯度洗脱程序
7.3.2质谱条件
a)离子源:电喷雾离子源;
b)扫描方式:正离子扫描;
c)检测方式:多反应监测;
d)离子源温度:150℃:
A:乙腈bzxZ.net
B:0.2%甲酸溶液
e)脱溶剂温度:500℃;
f)毛细管电压:3.0V;
g)定性离子对、定量离子对及锥孔电压和碰撞能量见表2。表25种α2受体激动剂类药物的质谱参数被测物名称
替扎尼定
赛拉嗪
溴莫尼定
安普乐定
可乐定
7.4测定法
7.4.1定性测定
定性离子对
254.1>44.1
254.1>210.0
221.1>90.0
221.1>164.0
292.2>170.2
292.2>212.3
245.2>174.2
245.2>209.2
230.0>160.0
230.0>213.0
定量离子对
254.1>44.1
221.1>90.0
292.2>212.3
245.2>174.2
230.0>213.0
锥孔电
GB31660.62019
碰撞能量
在同样测试条件下,试样液中α2-受体激动剂的保留时间与标准工作液中相应α2-受体激动剂的保留时间之比,偏差在±5%以内,且检测到离子的相对丰度,应当与浓度相当的校正标准溶液相对丰度一致,其允许偏差应符合表3要求。表3定性确证时相对离子丰度的最大允许误差相对离子丰度%
允许的最大偏差%
7.4.2定量测定
取试样溶液和相应的标准工作液,按外标法以峰面积定量,标准工作液及试样溶液中的α2受体激动剂类响应值均应在仪器检测的线性范围内。在上述条件下,αz受体激动剂标准溶液特征离子质量色谱图见附录A。7.5空自试验
除不加试料外,采用完全相同的步骤进行平行操作。结果计算和表述
试料中待测药物的残留量按式(1)计算:4
式中:
C,×A×V
GB31660.62019
(1)
-供试试料中相应的α2受体激动剂类药物残留量,单位为微克每千克(ug/kg):-标准溶液中相应的α2受体激动剂类药物浓度,单位为微克每升(μug/L);-试样溶液中相应的α2受体激动剂类药物的色谱峰面积:As—标准溶液中相应的α2受体激动剂类药物色谱峰面积:V溶解残余物所用的溶液体积,单位为毫升(mL);m供试试料质量,单位为克(g);计算结果需扣除空白值,测定结果用平行测定的算术平均值表示,保留两位有效数字9
检测方法灵敏度、准确度和精密度灵敏度
本方法的检测限为0.5μg/kg,定量限为1μg/kg。9.2准确度
本方法在1~100μg/kg添加浓度水平上的回收率为60%~100%。9.3精密度
本方法批内相对标准偏差≤15%,批间相对标准偏差≤20%。5
附录A
(资料性附录)
特征离子质量色谱图
GB31660.62019
3: MRM of 2 Channels ES+
245.2 :174.2(Apraconidine)
5: MRM of 2 Channels Es+
292.2 ≥ 212.3 (Brmoni cine)5.34e5
4: MRM of 2 Channels ES+
254.051 = 44.1 (Tizani cline)3.89e5
2: MRM of2 Channels ES+
230 > 213 (Cloni dine)
1: MRM of 2 Channels ES+
221.1 ≥ 90 (Xyezine)
++++++++++ Tirne
110ug/La,受体激动剂类药物标准溶液特征离子质量色谱图图A.1
1-赛拉嗪特征离子质量色谱图(221.1>90.0)2-可乐定特征离子质量色谱图(230.0>213.0)3-替扎尼定特征离子质量色谱图(254.1>44.1)4-溴莫尼定特征离子质量色谱图(292.2>212.3)5-安普乐定特征离子质量色谱图(245.2>174.2)6
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。






 ✕
✕