GB 8368-1998
基本信息
标准号: GB 8368-1998
中文名称:一次性使用输液器
标准类别:国家标准(GB)
英文名称: Disposable infusion sets
标准状态:已作废
发布日期:1998-01-01
实施日期:1999-02-01
作废日期:2006-07-01
出版语种:简体中文
下载格式:.rar.pdf
下载大小:430632

标准分类号
标准ICS号:医药卫生技术>>医疗设备>>11.040.20输血、输液和注射设备
中标分类号:医药、卫生、劳动保护>>医疗器械>>C31一般与显微外科器械
出版信息
出版社:中国标准出版社
书号:155066.1-15510
标准价格:13.0 元
出版日期:2004-04-05
相关单位信息
复审日期:2004-10-14
起草单位:国家医药管理局医用高分子产品质量检测中心
标准简介
本标准规定了一次性使用、重力输液式输液器的要求,以保证与输液容器和静脉器具相适应。本标准为输液器所用材料的性能及其质量规范提供了指南,并给出输液器组件的标记。 GB 8368-1998 一次性使用输液器 GB8368-1998 标准下载解压密码:www.bzxz.net
标准图片预览



标准内容
GB8368--1998
本标准等效采用IS)8536-4:1998《医用输液器具第4部分:一次性使用输液器重力输液式》。同时也是GB8368--93的修订版,本标准与IS08536-4:1998的主要技术差异如下:本标准增加了空气过滤器的滤除率、软管壁厚与外径、流量调节器调节行程、环氧乙烷残留量等技术指标;化学要求中酸碱度检验国际标准是采用滴定法,而本标准是采用酸度计法;本标准微粒含量的测定方法以及软管长度指标与国际标准有差异,增加子附录H检验规则。本标准与GB8368.---93的主要技术差异如下:物理要求方面,对微粒污染、密封性、瓶塞穿刺器、空气过滤器、软管尺寸、滴斗、流量调节器、注射件、保护套.外圆锥接头等要求都有所改变;化学要求方面,试验方法由参照采用改为等效采用国际标准,因此技术指标相应有了很大的改变,试验项目取消了氯化物,增加了镉含量的测定和紫外吸光度等。在包装标志方面也做了一定的改动。本标准的这次修订,将YY0002一90《一次性使用输液器用药液过滤器》、YY/T0142一94《一次性使用输液、输血器具用空气过滤器》的有关内容并人到本标准中。本标准自实施之日起代替GB8368--93。YY0002—90和YYT0142-94同时废止。本标准的附录A、附录B、附录C、附录D、附录E、附录F、附录G和附录H都是标准的附录本标准附录」是提示的附录。
本标摊由国家药品监督管理局提出。本标准由全国医用输液器具标准化技术委员会归口。本标准起草单位:国家医药管理局医用高分子产品质量检测中心。本标准主要起草人:吴平、王延伟、秦冬立、张强、骆红宇。本标准于1987年首次发布。
GB 8368- 1998
ISO前言
IS()(国际标准化组织)是由各国标准化团体(IS()成员团体)组成的世界性的联合会,制定国际标准的工作通常由IS)的技术委员会完成,各成员团体若对某技术委员会已确立的标准项目感兴趣,均有权参加该委员会的工作。与IS)保持联系的各国际组织(官方的或非官方的)也可参加有关工.作。在电工技术标准化方面IS())与国际电王委员会(IEC)保持密切合作关系由技术委员会正式通过的国际标准草案提交各成员团体表决,国际标准需取得至少75%参加表决的成员团体的同意才能正武通过。国际标准IS()8536.4是由IS)/TC76国际标准化组织医用输血、输液和注射器具技术委员会制定的。
ISO)8536的总题目是医用输液器具,由下列部分组成:第1部分:玻璃输液瓶
第2部分:输液瓶塞
第3部分:输液瓶铝盖
第4部分:--次性使用输液器
重力输液式
第5部分:滴定管式输液器
第6部分:输液瓶冷冻干燥瓶塞
第7部分:铝塑组合输液瓶盖
附录A、附录B、附录C、附录D、附录E和附录F是标准的组成部分、附录G、附录H和附录J仅供参考。
1范围
中华人民共和国国家标准
一次性使用输液器
Infusion sets for singleuse
GB83681998
eqv 1s0 8536-4:1998
代替(1 836893
本标准规定了,·次性使用、重力输液式输液器的要求,以保证与输液容器和静脉器具相适应本标湘为输液器所用材料的性能及其质量规范提供了指南.并给出输液器组件的标记、2引用标准
下列标准所包含的条义,通过在本标准中引用而构成为本标准的条文。本标准出版时,所示版本均为有效。所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。G131962~1995注射器、注射针及其他医疗器械6:100例锥接头(cqVIS()594-1:1996)(B2828.87逐批检查计数抽样程序及抽样表(适用于连续批的检查)GB/T14233.11998医用输液、输血、注射器具检验方法第部分:化学分析方法GB/T14233.2·93医用输液、输血、注射器具检验方法第二部分:生物试验方法G3T14437---93品质量计数次监督抽样检验程序(适用于总体量较大的情形)GB 15811 1995
次性使用无菌注射针(ne4IS0)7864:1993)(GB3/T16886.1·1997医疗器械生物学评价第1部分:试验选择指南(idtIS()10993-1:1992)-次性使用静脉输液针
YY(0028-.90
YY/03131998医用高分子产品包装、标志、运输和购存IS)594.2:1991注射器、注射针及其他医疗器械6%(鲁尔)圆锥接头3通用要求
第二部分:锁定锥头
3.1输液器组件和分离式进气器件组件的名称如图1、图2和图3所示,江:【冬1、图2和图3列举了输液器和进气器件的结构.只要能达到相同的效果,出可采用其他结构3.2图2所示的输液器适用于塑料折式输液容器。3.3图】所示输液器,或带有图3所示分离式进气器件的图2所示的输液器适用于硬质输液器,国家质量技术监督局199811-26批准1999-02-01实施
GB 8368-- 1998
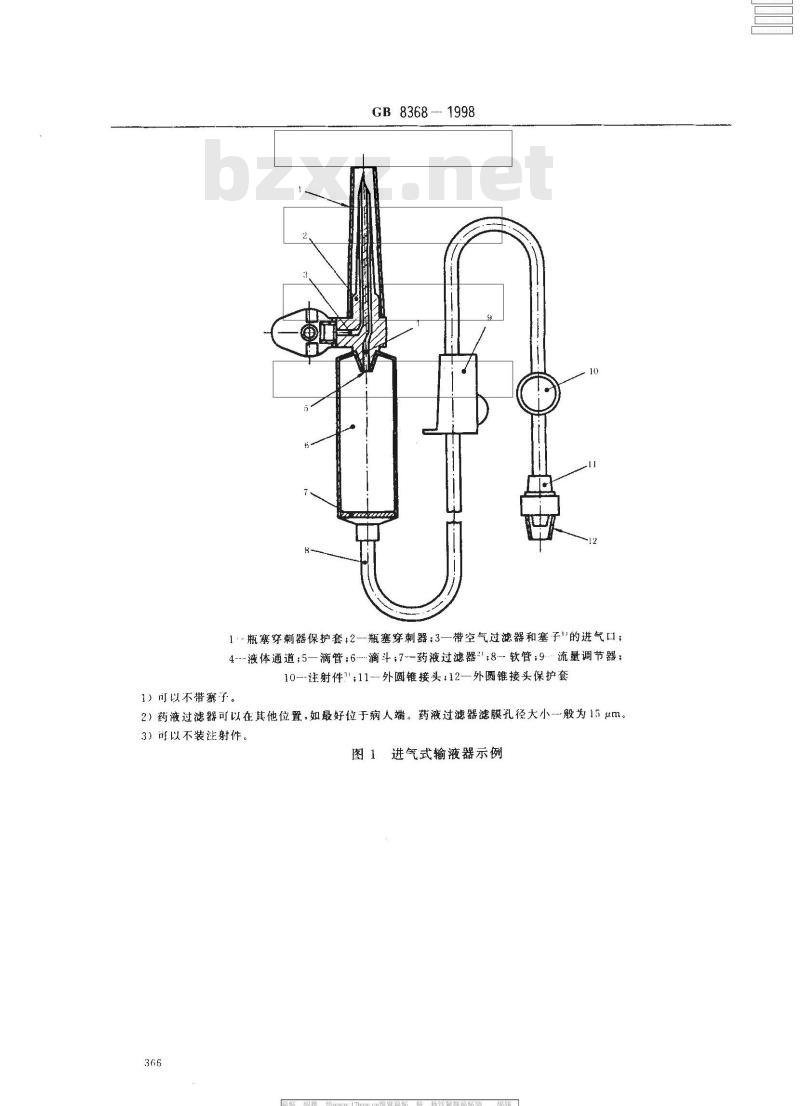
!·瓶塞穿刺器保护套;2--瓶塞穿刺器3一带空气过滤器和塞子\的进气口;4-液体通道;5—滴管:6-滴斗·-药液过滤器””,8.-软管;9.流量调节器;10--注射件3\;11-外圆锥接头:12—外圆锥接头保护套1)可以不带塞子。
2)药液过滤器可以在其他位置,如最好位于病人端。药液过滤器滤膜孔径大小-般为15um。3)可以不装注射件。
图1进气式输液器示例
GB8368--1998
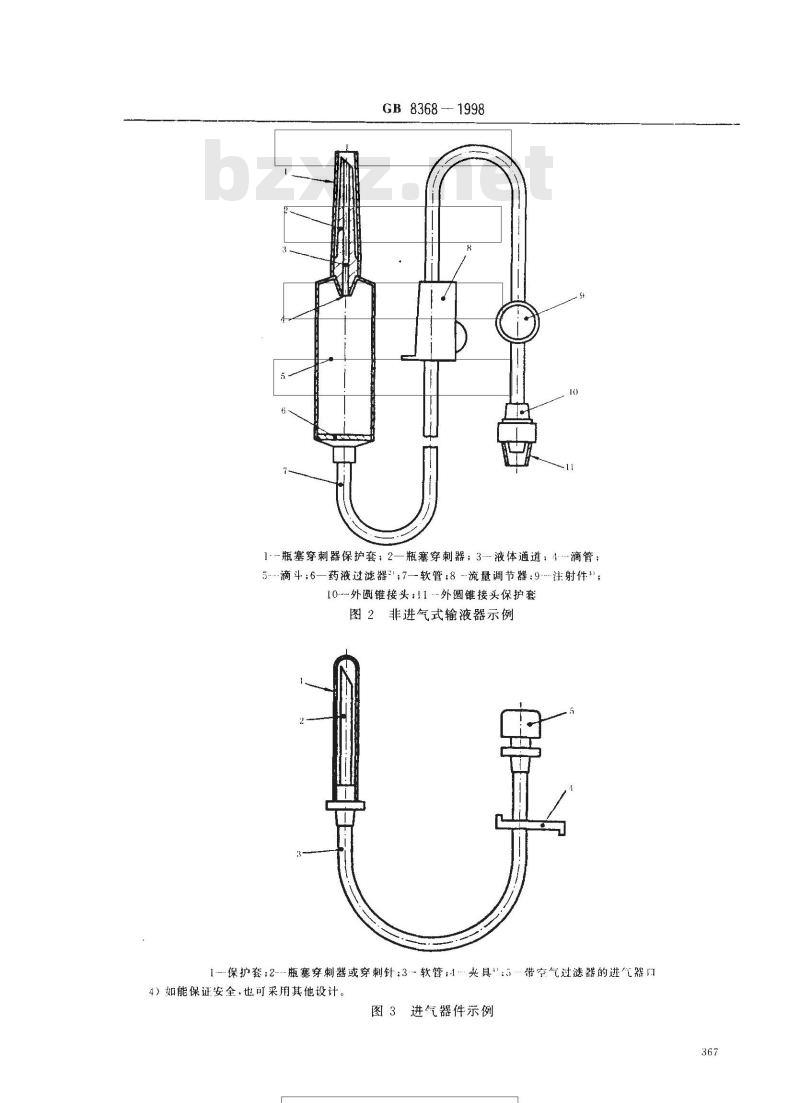
1--瓶塞穿刺器保护套;2—瓶塞穿刺器;3液体通道;4滴管:5-滴斗;6—药液过滤器”;7—软管;8-流量调节器.9.-注射件”,10---外圆锥接头:1-外圆锥接头保护套图2非进气式输液器示例
1--保护套;2--瓶塞穿刺器或穿刺针3软管:4夹具”·5带空气过滤器的进气器门4)如能保证安全,也可采用其他设计。图3进气器件示例
GB 8368 - 1998
3.4输液器应有保护套,使输液器内腔在使用前保持无菌。进气器件的瓶塞穿刺器或穿刺针也应有保护套
4标记示例
4.1输液器
符合本标准要求的进气式输液器的标记示例为:“输液器”学样加本标准号册产净IS,对进气式输液器加字母V.对非进气式输液器加字母NV:示例:
输液器GB8368IS-V
输液器GB8368IS-NV
4.2气器件
符合本标准要求的进气器件的标记示例为:“进气器件\字样加本标准号加宇母AD):例:
进气器件GB8368-AD
5材料
制造第3章给出的输液器及组件的材料应满足第6章的要求。输液器与溶液接触的组件,还应符合第7简和第8章规定的要求。
注:输液器用聚氮乙烯原材料的标准免GB15593。6物理要求
6.1微粒污染
按附F或其他等效方法测定.200ml洗脱液中.15μm~25μm的微粒数不得超过1个/ml.大于25um的微粒数不得超过0.5个/ml。6.2密封性
按照附录A试验时,应无气体泄漏现象。6.3连接强度
输液器液体通道各组件间的连接,不包括保护套,应能承受不小于【5V的静拉力持续15.6.4瓶寒穿刺器
6.4.1瓶寒穿刺器的尺寸应符合图4所示。尺寸:mm
注:金属穿刺器不受图4尺寸限制。采用说明:
1:6.1与1S85361:1998非等效
图4瓶塞穿刺器尺寸
GB 8368— 1998
6.4.2瓶塞穿刺器应能刺透未穿刺过的液体容器的瓶塞.在穿刺过程中应不引起落6.5进气器件
6.5.1进气器件应符食3.4和8.2要求6.5.2进气器件应有:空气过滤器,以防止微生物进大它所插入的容器。当按附录B进行试验时,空气过滤器对空气中0.5μm以上微粒的滤除率应不小于90%。6.5.3进气器件可以与输液器的瓶塞穿刺器为-体,也可以与之分离。6.5.4当进气器件插人硬质容器时,进人容器的空气应不进人到流出液中。6.5.5空气汽过滤器的安装应使所有进人硬质容器的空气都通过它。按附录B试验时,相对于自由进气容器的流出液的流量应不降低20%。6.6软管
6.6.1由软质材料制成的管子应塑化均勾,并透明或足够透明。当有气泡通过时,用正常或矫正视力可以发现水和空气的分界面。
6.6.2未端至滴斗的软管[包括注射件(如果有)和外圆锥接头}的长度应不小于1250)mm26.6.3:软管壁厚应不小于0.4mm,外径应不小于3.5mm。6.7药液过滤器
输液器应有药液过滤器。
当按附录(试验时,过滤器滤除率应不小于80%。6.8滴斗马滴管
6.8.1滴斗应可以连续观察液滴。液体应经过一插人滴斗的滴管进人滴斗。滴管端部至滴斗出的距离应不小于40mm,滴管和药液过滤器间的距离应不小于20mm。滴斗内壁与滴管终端的外壁距离应不小于5mm。在23(土2(,流速为50滴/min±10滴/min的条件下,滴管滴下20滴或60滴蒸馏水应为1 ml.±(. 1 ml(l g±0. 1 g)
6.8.2滴斗应能借助其弹性将输液容器中药液引入输液器,其外体积应不小于10cm,壁厚平均不小于0.7 nim。
6.9流量调节器
流量调节器应能调节液流从零至最大,其调节行程应不小于30mm。注:流量调节器应能在次输液中持续使用而不损伤软管。流量调节器和软管接触在起贮存时应不产生有害反应。
6.10输液流速
输液器在1m静压头下,对于滴管为20滴/ml.的输液器,10min内输出氟化钠溶液[质量浓度((NaCl)=9g/I]应不少于1000mL;对于滴管为60滴/mL的输液器,40min内输出氯化钠溶液[质量浓度(NacCl)==9g/LJ应不少于1000ml。6.11注射件
如有注射件.按附录ID试验时,水的泄漏量应不超过一滴。注:注射件宜位于外圆锥接头附近。6.12外圆锥接头
软律的末端应有-符合GB1962或ISO594-2的外圆锥接头。注:(/T1962.1中规定的锥头分离力指标为推荐性的。各类检验报告应包含该项性能的检验信息和结论,以利促进产品质量的提商,
采用说明:
21、3、5)、6:IS0)8536-4:1998无此项技术指标。31[s0 8536-4:1998 是1500 mm
6.13保护餐
GB 8368--1998
输液器终端的保护套应保持瓶塞穿刺器、外圆锥接头和输液器内表面无菌。保护套不应自然脱落并易于拆除。7化学要求
7.1还原物质(易氧化物)
按附录F试验时,检验液和空白液消耗高锰酸钾溶液Lc(KMnO,)=0.002mol/L]的体积之差应不超过2.0ml.。
7.2金属离子
当按E3.1用原子吸收分光光度计法(AAS)或相当的方法进行测定时,检验液中钡、铬、铜、铅、锡的总含量应不超过1μg/ml。辐的含量应不超过0.1μg/ml当按E3.2试验时,试验液呈现的颜色应不超过质量浓度o(Pb)=1ug/mL的标准对照液。
7.3酸碱度?
按附录E试验时.检验液与空白液pH值之差应不超过1.5。7.4蒸发残渣
按附录E试验时、蒸发残渣的总量应不超过2mg。7.5紫外吸光度
按附录E试验时,检验液的吸光度应不大于0.1。7.6环氧乙烷残留量”
按GB/T14233.1试验时,每套输液器环氧乙烷残留量应不大于0.5mg。8生物要求
8.1总则
输液器应不释放出任何对患者产生副作用的物质。应用适宜的试验来评价输液器材料的毒性,试验结果应表明无毒性。GB/T16886.1给出了毒性试验指南。8.2无菌
单包装内的输液器和/或进气器件应经过一有效的灭菌过程使产品无菌。附录G给出了无菌试验方法。
8.3热原
应用适当的试验来评价输液器和/或进气器件的致热性,结果应表明输液器无热原。附录(给出了热原试验方法。
8.4溶血
应评价输液器无溶血成分,试验结果应表明输液器无溶血反应。GB/T14233.2给出了溶血试验方法。
8.5急性全身毒性
应评价输液器急性全身毒性作用,试验结果应表明输液器无急性全身毒性。GB/T14233.2给出了急性企身毒性试验方法。
采用说明:
7:IS03536-4:998是用滴定法
811S03536-4:1998是5 mg
9)IS0)3536-4:.998无此项技术指标370
9标志
9.1单包装
单包装上应至少标有下列信息:GB8368 -1998
a)文字说明内装物,包括\只能重力输液”字样;b)用YY/T0313中给出的图形符号,标明输液器无菌:)输液器无热原;
d)输液器仅供-一次性使用,或同等说明;注:叫另外给出符合YY/9313中的“-次性使用\图形符号。e)使用说明,包括检查包装密封完整性和有关保护套脱落情况的警示;注:使用说明也可采用插页形式。1)批号、以\批”字开头:
&)失效年月(必须能清晰识别):h)制造商和/或经销商名称和地址;i)滴管滴20滴或60滴蒸馏水相当于1ml.±0.1ml.(1g士0.1g)的说明;j)如配静脉针,应注明规格。
9.2中包装
中包装上应至少有下列信息:
a)文字说明内装物,包括“只能重力输液”字样;b)输液器数量:
C)用YY/T0313中给出的图形符号标明输液器无菌;d)批号以“批”字开头;
e)失效年月:
f)制造商和/或经销商名称和地址;多)推荐的忙存条件(如果有),9.3外包装
外包装上信息应符含YY/T0313。10包装
10.1输液器和/或进气器件应单件包装,以使其在贮存期内保持无菌单包装打开后应留下打开过的迹象。10.2输液器和/或进气器件的包装和灭菌应使其在备用时无扁嬉或打折。10.3单包装内不应有肉眼可见异物$71
GB 8368 --- 1998
附录A
(标准的附录)
密封性试验
输液器--端封叫,浸人20E30的水申,通人高于大气压强20kPa的气压10s。检查输液器漏气的迹象。
附录B
(标准的附录)
空气过滤器滤除率、流量降低率试验方法B1滤除率试验
B1.1试验仪器
尘埃粒子计数器:采样管长度为1m,采样次数为1次/min。转子流量计:量程为80ml./min或100ml./min。B1.2试验步骤
在静态环境条件下,将尘埃粒子计数器与流量计相连,在空气流量为50ml./min下,测定1min内采集的空气中0.5pm以上的微粒数.连续读取五个数据。另取空气过滤器按使用方向使其与流量计进气口相连,在相同空气流量下,测定1mi内流经空气过滤器后的空气中0.5μm以上的微粒数。连续读取五个数据。将五个数据中的最大值和最小值去掉,取其余三个值的平均值B1.3结巢表示
式(B1)给出过滤器滤除率.以百分数表示:/×100bzxz.net
式中:n.空气中0.5μm以上的微粒数;流经空气过滤器后的空气中0.5um以上的微粒数。n
B2流量降低率试验
·(B1)
B2.1用-只玻璃输液瓶装入23C土2C的蒸馏水,盖上瓶塞。把支外径为0.8mm针装到输液器的外圆锥接头上。进气器件通过瓶塞插人瓶中,然后调节流量调节器,使输液器处于关闭状态,使瓶子有1m的静水头。流量调节器调至最大,测量水的流量。从进气器件上取下过滤器、重复上述步骤。B2.2对于瓶塞穿刺器与进气器件为一体的输液器.按B2.1步骤,但无分离进气器件插入这--步骤372
显微镜法(仲裁法)
C1.1试验液制备
GB 8368 -- 1998
附录C
(标准的附录)
药液过滤器滤除率试验
用直径20um!!mm胶乳粒子悬浮液,100ml试验液中含有粒子1000个。C1.2张骤
在图(1所示的试验装置中安装药液过滤器,使其与实际使用状态一致,在药液过滤器下端约10cm处剪断输液器软管
用5ml.则液瓶中的试验液冲洗药液过滤器,弃去滤出液。将100ml.试验液通过药液过滤器,在抽真空条件下,使流出液全部通过--个孔径为5um~8μm、直径47mm的黑色格栅滤膜,将留有胶乳粒子的滤膜放在适当的显微镜的载玻片或托盘上,在50至100倍的放大倍数下对不小于50%的网格面积中的胶乳粒子进行计数,明显的非胶乳粒子不计。试验进行两次。
如达不到所需的80%滤除率,重复试验。注:该试验的全部过程应在洁净的环境中进行,如可能可在层流条件下进行。C1.3结果表示
式(C1)给出过滤器的滤除率,以百分数表示:11-
j× 100
武中:”…过滤膜上滞留(通过药液过滤器)的粒子数;所用试验液中的粒子数。
C2粒子计数器法
C2.1试验仪器
电阻式粒子计数器.--次取样量为100ml。C2.2试验液
((1)
试验液为直径20um士1μm胶乳粒子悬浮液,每100ml试验液(质量浓度为9g/1.的氯化钠溶液)中含有3(000)个胶乳粒子的标准物质。C2.3步骤
取150n1l.试验液,使其在1m静压头下流过药液过滤器,使滤过液流人洁净的计数器的样品池中、对样品池中100ml滤过液中直径为20um士1μm的粒子计数。C2.4结表示
按式(C1)计算药液过滤器的滤除率。采用说明:
10![S8536-4:1998未规楚粒于计数器法。373
GB8368
1贮液瓶;2--输送管;3流量调节器;4--连接器件;5穿刺器;6—药液过滤器;7—滤膜图C1药液过滤器效率试验装置
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
本标准等效采用IS)8536-4:1998《医用输液器具第4部分:一次性使用输液器重力输液式》。同时也是GB8368--93的修订版,本标准与IS08536-4:1998的主要技术差异如下:本标准增加了空气过滤器的滤除率、软管壁厚与外径、流量调节器调节行程、环氧乙烷残留量等技术指标;化学要求中酸碱度检验国际标准是采用滴定法,而本标准是采用酸度计法;本标准微粒含量的测定方法以及软管长度指标与国际标准有差异,增加子附录H检验规则。本标准与GB8368.---93的主要技术差异如下:物理要求方面,对微粒污染、密封性、瓶塞穿刺器、空气过滤器、软管尺寸、滴斗、流量调节器、注射件、保护套.外圆锥接头等要求都有所改变;化学要求方面,试验方法由参照采用改为等效采用国际标准,因此技术指标相应有了很大的改变,试验项目取消了氯化物,增加了镉含量的测定和紫外吸光度等。在包装标志方面也做了一定的改动。本标准的这次修订,将YY0002一90《一次性使用输液器用药液过滤器》、YY/T0142一94《一次性使用输液、输血器具用空气过滤器》的有关内容并人到本标准中。本标准自实施之日起代替GB8368--93。YY0002—90和YYT0142-94同时废止。本标准的附录A、附录B、附录C、附录D、附录E、附录F、附录G和附录H都是标准的附录本标准附录」是提示的附录。
本标摊由国家药品监督管理局提出。本标准由全国医用输液器具标准化技术委员会归口。本标准起草单位:国家医药管理局医用高分子产品质量检测中心。本标准主要起草人:吴平、王延伟、秦冬立、张强、骆红宇。本标准于1987年首次发布。
GB 8368- 1998
ISO前言
IS()(国际标准化组织)是由各国标准化团体(IS()成员团体)组成的世界性的联合会,制定国际标准的工作通常由IS)的技术委员会完成,各成员团体若对某技术委员会已确立的标准项目感兴趣,均有权参加该委员会的工作。与IS)保持联系的各国际组织(官方的或非官方的)也可参加有关工.作。在电工技术标准化方面IS())与国际电王委员会(IEC)保持密切合作关系由技术委员会正式通过的国际标准草案提交各成员团体表决,国际标准需取得至少75%参加表决的成员团体的同意才能正武通过。国际标准IS()8536.4是由IS)/TC76国际标准化组织医用输血、输液和注射器具技术委员会制定的。
ISO)8536的总题目是医用输液器具,由下列部分组成:第1部分:玻璃输液瓶
第2部分:输液瓶塞
第3部分:输液瓶铝盖
第4部分:--次性使用输液器
重力输液式
第5部分:滴定管式输液器
第6部分:输液瓶冷冻干燥瓶塞
第7部分:铝塑组合输液瓶盖
附录A、附录B、附录C、附录D、附录E和附录F是标准的组成部分、附录G、附录H和附录J仅供参考。
1范围
中华人民共和国国家标准
一次性使用输液器
Infusion sets for singleuse
GB83681998
eqv 1s0 8536-4:1998
代替(1 836893
本标准规定了,·次性使用、重力输液式输液器的要求,以保证与输液容器和静脉器具相适应本标湘为输液器所用材料的性能及其质量规范提供了指南.并给出输液器组件的标记、2引用标准
下列标准所包含的条义,通过在本标准中引用而构成为本标准的条文。本标准出版时,所示版本均为有效。所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。G131962~1995注射器、注射针及其他医疗器械6:100例锥接头(cqVIS()594-1:1996)(B2828.87逐批检查计数抽样程序及抽样表(适用于连续批的检查)GB/T14233.11998医用输液、输血、注射器具检验方法第部分:化学分析方法GB/T14233.2·93医用输液、输血、注射器具检验方法第二部分:生物试验方法G3T14437---93品质量计数次监督抽样检验程序(适用于总体量较大的情形)GB 15811 1995
次性使用无菌注射针(ne4IS0)7864:1993)(GB3/T16886.1·1997医疗器械生物学评价第1部分:试验选择指南(idtIS()10993-1:1992)-次性使用静脉输液针
YY(0028-.90
YY/03131998医用高分子产品包装、标志、运输和购存IS)594.2:1991注射器、注射针及其他医疗器械6%(鲁尔)圆锥接头3通用要求
第二部分:锁定锥头
3.1输液器组件和分离式进气器件组件的名称如图1、图2和图3所示,江:【冬1、图2和图3列举了输液器和进气器件的结构.只要能达到相同的效果,出可采用其他结构3.2图2所示的输液器适用于塑料折式输液容器。3.3图】所示输液器,或带有图3所示分离式进气器件的图2所示的输液器适用于硬质输液器,国家质量技术监督局199811-26批准1999-02-01实施
GB 8368-- 1998
!·瓶塞穿刺器保护套;2--瓶塞穿刺器3一带空气过滤器和塞子\的进气口;4-液体通道;5—滴管:6-滴斗·-药液过滤器””,8.-软管;9.流量调节器;10--注射件3\;11-外圆锥接头:12—外圆锥接头保护套1)可以不带塞子。
2)药液过滤器可以在其他位置,如最好位于病人端。药液过滤器滤膜孔径大小-般为15um。3)可以不装注射件。
图1进气式输液器示例
GB8368--1998
1--瓶塞穿刺器保护套;2—瓶塞穿刺器;3液体通道;4滴管:5-滴斗;6—药液过滤器”;7—软管;8-流量调节器.9.-注射件”,10---外圆锥接头:1-外圆锥接头保护套图2非进气式输液器示例
1--保护套;2--瓶塞穿刺器或穿刺针3软管:4夹具”·5带空气过滤器的进气器门4)如能保证安全,也可采用其他设计。图3进气器件示例
GB 8368 - 1998
3.4输液器应有保护套,使输液器内腔在使用前保持无菌。进气器件的瓶塞穿刺器或穿刺针也应有保护套
4标记示例
4.1输液器
符合本标准要求的进气式输液器的标记示例为:“输液器”学样加本标准号册产净IS,对进气式输液器加字母V.对非进气式输液器加字母NV:示例:
输液器GB8368IS-V
输液器GB8368IS-NV
4.2气器件
符合本标准要求的进气器件的标记示例为:“进气器件\字样加本标准号加宇母AD):例:
进气器件GB8368-AD
5材料
制造第3章给出的输液器及组件的材料应满足第6章的要求。输液器与溶液接触的组件,还应符合第7简和第8章规定的要求。
注:输液器用聚氮乙烯原材料的标准免GB15593。6物理要求
6.1微粒污染
按附F或其他等效方法测定.200ml洗脱液中.15μm~25μm的微粒数不得超过1个/ml.大于25um的微粒数不得超过0.5个/ml。6.2密封性
按照附录A试验时,应无气体泄漏现象。6.3连接强度
输液器液体通道各组件间的连接,不包括保护套,应能承受不小于【5V的静拉力持续15.6.4瓶寒穿刺器
6.4.1瓶寒穿刺器的尺寸应符合图4所示。尺寸:mm
注:金属穿刺器不受图4尺寸限制。采用说明:
1:6.1与1S85361:1998非等效
图4瓶塞穿刺器尺寸
GB 8368— 1998
6.4.2瓶塞穿刺器应能刺透未穿刺过的液体容器的瓶塞.在穿刺过程中应不引起落6.5进气器件
6.5.1进气器件应符食3.4和8.2要求6.5.2进气器件应有:空气过滤器,以防止微生物进大它所插入的容器。当按附录B进行试验时,空气过滤器对空气中0.5μm以上微粒的滤除率应不小于90%。6.5.3进气器件可以与输液器的瓶塞穿刺器为-体,也可以与之分离。6.5.4当进气器件插人硬质容器时,进人容器的空气应不进人到流出液中。6.5.5空气汽过滤器的安装应使所有进人硬质容器的空气都通过它。按附录B试验时,相对于自由进气容器的流出液的流量应不降低20%。6.6软管
6.6.1由软质材料制成的管子应塑化均勾,并透明或足够透明。当有气泡通过时,用正常或矫正视力可以发现水和空气的分界面。
6.6.2未端至滴斗的软管[包括注射件(如果有)和外圆锥接头}的长度应不小于1250)mm26.6.3:软管壁厚应不小于0.4mm,外径应不小于3.5mm。6.7药液过滤器
输液器应有药液过滤器。
当按附录(试验时,过滤器滤除率应不小于80%。6.8滴斗马滴管
6.8.1滴斗应可以连续观察液滴。液体应经过一插人滴斗的滴管进人滴斗。滴管端部至滴斗出的距离应不小于40mm,滴管和药液过滤器间的距离应不小于20mm。滴斗内壁与滴管终端的外壁距离应不小于5mm。在23(土2(,流速为50滴/min±10滴/min的条件下,滴管滴下20滴或60滴蒸馏水应为1 ml.±(. 1 ml(l g±0. 1 g)
6.8.2滴斗应能借助其弹性将输液容器中药液引入输液器,其外体积应不小于10cm,壁厚平均不小于0.7 nim。
6.9流量调节器
流量调节器应能调节液流从零至最大,其调节行程应不小于30mm。注:流量调节器应能在次输液中持续使用而不损伤软管。流量调节器和软管接触在起贮存时应不产生有害反应。
6.10输液流速
输液器在1m静压头下,对于滴管为20滴/ml.的输液器,10min内输出氟化钠溶液[质量浓度((NaCl)=9g/I]应不少于1000mL;对于滴管为60滴/mL的输液器,40min内输出氯化钠溶液[质量浓度(NacCl)==9g/LJ应不少于1000ml。6.11注射件
如有注射件.按附录ID试验时,水的泄漏量应不超过一滴。注:注射件宜位于外圆锥接头附近。6.12外圆锥接头
软律的末端应有-符合GB1962或ISO594-2的外圆锥接头。注:(/T1962.1中规定的锥头分离力指标为推荐性的。各类检验报告应包含该项性能的检验信息和结论,以利促进产品质量的提商,
采用说明:
21、3、5)、6:IS0)8536-4:1998无此项技术指标。31[s0 8536-4:1998 是1500 mm
6.13保护餐
GB 8368--1998
输液器终端的保护套应保持瓶塞穿刺器、外圆锥接头和输液器内表面无菌。保护套不应自然脱落并易于拆除。7化学要求
7.1还原物质(易氧化物)
按附录F试验时,检验液和空白液消耗高锰酸钾溶液Lc(KMnO,)=0.002mol/L]的体积之差应不超过2.0ml.。
7.2金属离子
当按E3.1用原子吸收分光光度计法(AAS)或相当的方法进行测定时,检验液中钡、铬、铜、铅、锡的总含量应不超过1μg/ml。辐的含量应不超过0.1μg/ml当按E3.2试验时,试验液呈现的颜色应不超过质量浓度o(Pb)=1ug/mL的标准对照液。
7.3酸碱度?
按附录E试验时.检验液与空白液pH值之差应不超过1.5。7.4蒸发残渣
按附录E试验时、蒸发残渣的总量应不超过2mg。7.5紫外吸光度
按附录E试验时,检验液的吸光度应不大于0.1。7.6环氧乙烷残留量”
按GB/T14233.1试验时,每套输液器环氧乙烷残留量应不大于0.5mg。8生物要求
8.1总则
输液器应不释放出任何对患者产生副作用的物质。应用适宜的试验来评价输液器材料的毒性,试验结果应表明无毒性。GB/T16886.1给出了毒性试验指南。8.2无菌
单包装内的输液器和/或进气器件应经过一有效的灭菌过程使产品无菌。附录G给出了无菌试验方法。
8.3热原
应用适当的试验来评价输液器和/或进气器件的致热性,结果应表明输液器无热原。附录(给出了热原试验方法。
8.4溶血
应评价输液器无溶血成分,试验结果应表明输液器无溶血反应。GB/T14233.2给出了溶血试验方法。
8.5急性全身毒性
应评价输液器急性全身毒性作用,试验结果应表明输液器无急性全身毒性。GB/T14233.2给出了急性企身毒性试验方法。
采用说明:
7:IS03536-4:998是用滴定法
811S03536-4:1998是5 mg
9)IS0)3536-4:.998无此项技术指标370
9标志
9.1单包装
单包装上应至少标有下列信息:GB8368 -1998
a)文字说明内装物,包括\只能重力输液”字样;b)用YY/T0313中给出的图形符号,标明输液器无菌:)输液器无热原;
d)输液器仅供-一次性使用,或同等说明;注:叫另外给出符合YY/9313中的“-次性使用\图形符号。e)使用说明,包括检查包装密封完整性和有关保护套脱落情况的警示;注:使用说明也可采用插页形式。1)批号、以\批”字开头:
&)失效年月(必须能清晰识别):h)制造商和/或经销商名称和地址;i)滴管滴20滴或60滴蒸馏水相当于1ml.±0.1ml.(1g士0.1g)的说明;j)如配静脉针,应注明规格。
9.2中包装
中包装上应至少有下列信息:
a)文字说明内装物,包括“只能重力输液”字样;b)输液器数量:
C)用YY/T0313中给出的图形符号标明输液器无菌;d)批号以“批”字开头;
e)失效年月:
f)制造商和/或经销商名称和地址;多)推荐的忙存条件(如果有),9.3外包装
外包装上信息应符含YY/T0313。10包装
10.1输液器和/或进气器件应单件包装,以使其在贮存期内保持无菌单包装打开后应留下打开过的迹象。10.2输液器和/或进气器件的包装和灭菌应使其在备用时无扁嬉或打折。10.3单包装内不应有肉眼可见异物$71
GB 8368 --- 1998
附录A
(标准的附录)
密封性试验
输液器--端封叫,浸人20E30的水申,通人高于大气压强20kPa的气压10s。检查输液器漏气的迹象。
附录B
(标准的附录)
空气过滤器滤除率、流量降低率试验方法B1滤除率试验
B1.1试验仪器
尘埃粒子计数器:采样管长度为1m,采样次数为1次/min。转子流量计:量程为80ml./min或100ml./min。B1.2试验步骤
在静态环境条件下,将尘埃粒子计数器与流量计相连,在空气流量为50ml./min下,测定1min内采集的空气中0.5pm以上的微粒数.连续读取五个数据。另取空气过滤器按使用方向使其与流量计进气口相连,在相同空气流量下,测定1mi内流经空气过滤器后的空气中0.5μm以上的微粒数。连续读取五个数据。将五个数据中的最大值和最小值去掉,取其余三个值的平均值B1.3结巢表示
式(B1)给出过滤器滤除率.以百分数表示:/×100bzxz.net
式中:n.空气中0.5μm以上的微粒数;流经空气过滤器后的空气中0.5um以上的微粒数。n
B2流量降低率试验
·(B1)
B2.1用-只玻璃输液瓶装入23C土2C的蒸馏水,盖上瓶塞。把支外径为0.8mm针装到输液器的外圆锥接头上。进气器件通过瓶塞插人瓶中,然后调节流量调节器,使输液器处于关闭状态,使瓶子有1m的静水头。流量调节器调至最大,测量水的流量。从进气器件上取下过滤器、重复上述步骤。B2.2对于瓶塞穿刺器与进气器件为一体的输液器.按B2.1步骤,但无分离进气器件插入这--步骤372
显微镜法(仲裁法)
C1.1试验液制备
GB 8368 -- 1998
附录C
(标准的附录)
药液过滤器滤除率试验
用直径20um!!mm胶乳粒子悬浮液,100ml试验液中含有粒子1000个。C1.2张骤
在图(1所示的试验装置中安装药液过滤器,使其与实际使用状态一致,在药液过滤器下端约10cm处剪断输液器软管
用5ml.则液瓶中的试验液冲洗药液过滤器,弃去滤出液。将100ml.试验液通过药液过滤器,在抽真空条件下,使流出液全部通过--个孔径为5um~8μm、直径47mm的黑色格栅滤膜,将留有胶乳粒子的滤膜放在适当的显微镜的载玻片或托盘上,在50至100倍的放大倍数下对不小于50%的网格面积中的胶乳粒子进行计数,明显的非胶乳粒子不计。试验进行两次。
如达不到所需的80%滤除率,重复试验。注:该试验的全部过程应在洁净的环境中进行,如可能可在层流条件下进行。C1.3结果表示
式(C1)给出过滤器的滤除率,以百分数表示:11-
j× 100
武中:”…过滤膜上滞留(通过药液过滤器)的粒子数;所用试验液中的粒子数。
C2粒子计数器法
C2.1试验仪器
电阻式粒子计数器.--次取样量为100ml。C2.2试验液
((1)
试验液为直径20um士1μm胶乳粒子悬浮液,每100ml试验液(质量浓度为9g/1.的氯化钠溶液)中含有3(000)个胶乳粒子的标准物质。C2.3步骤
取150n1l.试验液,使其在1m静压头下流过药液过滤器,使滤过液流人洁净的计数器的样品池中、对样品池中100ml滤过液中直径为20um士1μm的粒子计数。C2.4结表示
按式(C1)计算药液过滤器的滤除率。采用说明:
10![S8536-4:1998未规楚粒于计数器法。373
GB8368
1贮液瓶;2--输送管;3流量调节器;4--连接器件;5穿刺器;6—药液过滤器;7—滤膜图C1药液过滤器效率试验装置
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。