中华人民共和国国家标准
GB4789.4—2016
食品安全国家标准
食品微生物学检验
2016-12-23发布
沙门氏菌检验
2017-06-23实施
中华人民共和国国家卫生和计划生育委员会国家食品药品监督管理总局
GB4789.4—2016
本标准代替GB4789.4一2010《食品安全国家标准食品微生物学检验沙门氏菌检验》、
SN0170—1992《出口食品沙门氏菌属(包括亚利桑那菌)检验方法》、SN/T2552.52010《乳及乳制品卫生微生物学检验方法第5部分:沙门氏菌检验》。整合后的标准与GB4789.4—2010相比,主要变化如下:—一修改了检测流程和血清学检测操作程序;—修改了附录A和附录B。
1范围
食品安全国家标准
食品微生物学检验
沙门氏菌检验
本标准规定了食品中沙门氏菌(Salmonella)的检验方法本标准适用于食品中沙门氏菌的检验设备和材料
除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:冰箱:2℃~5℃。
恒温培养箱:36℃1℃,42℃士1℃。均质器。
振荡器。wwW.bzxz.Net
电子天平:感量0.1g。
无菌锥形瓶:容量500mL,250mL。GB 4789.4—2016
无菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)或微量移液器及吸头无菌培养皿:直径60mm,90mm。无菌试管:3mm×50mm10mm×75mm。pH计或pH比色管或精密pH试纸
全自动微生物生化鉴定系统。
无菌毛细管。
培养基和试剂
缓冲蛋白陈水(BPW):见A.1。
四硫磺酸钠煌绿(TTB)增菌液:见A.2。亚硒酸盐胱氨酸(SC)增菌液:见A.3。亚硫酸铋(BS)琼脂:见A.4。
HE琼脂:见A.5。
木糖赖氨酸脱氧胆盐(XLD)琼脂:见A.6。沙门氏菌属显色培养基。
三糖铁(TSI)琼脂:见A.7。
蛋白陈水、靛基质试剂:见A.8。尿素琼脂(pH7.2):见A.9。
氰化钾(KCN)培养基:见A.10。赖氨酸脱羧酶试验培养基:见A.11。糖发酵管:见A.12。
邻硝基酚3-D半乳糖苷(ONPG培养基:见A.13。半固体琼脂:见A.14。
丙二酸钠培养基:见A.15。
沙门氏菌O、H和Vi诊断血清。
生化鉴定试剂盒。
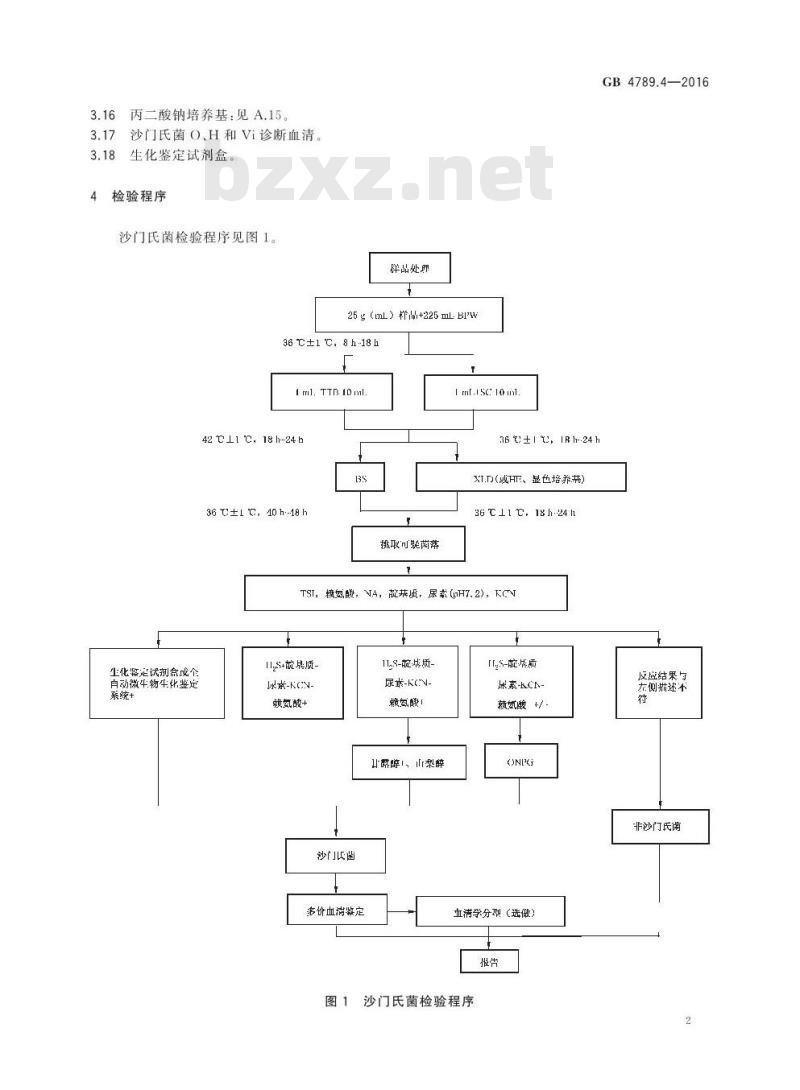
4检验程序
沙门氏菌检验程序见图1。
群品处师
25g(ml)样品+225mLBPW
36 C±1 C, 8 h-18 h
I rnl. TTB 10 ml.
42 11 C, 18 h-24 h
36 ±1 ,40 h.-18 h
挑联n凝菌落
+ t.15c: 10m.
36 t±I , IR h-24 h
XT.T)(或HF、显色培养带)
36 ℃ 11 , 18 h-24 l
TSI,忽酸,NA,莱质,尿素(H7.2),KCN生化鉴定试剂盒或个
自动微牛物牛化鉴定
系统+
,s+蔬转质-
康素-KCN-
顿氨酸+
沙门抵菌
多价血消婺定
11.S-靛成质-
尿紫-KN-
赖氨酸!
醇、梨醇
[,S-靛造质
素-KcCn-
羧效酸+7
血清学分型(选做)
沙门氏菌检验程序
GB4789.4—2016
疫应结果与
在侧描述不
非沙门氏菌
5操作步骤
5.1预增菌
GB4789.4—2016
无菌操作称取25g(mL)样品,置于盛有225mLBPW的无菌均质杯或合适容器内,以8000r/min10000r/min均质1min~2min,或置于盛有225mLBPW的无菌均质袋中,用拍击式均质器拍打1min~2min。若样品为液态,不需要均质,振荡混匀。如需调整pH,用1mol/mL无菌NaOH或HC1调pH至6.8土0.2。无菌操作将样品转至500mL锥形瓶或其他合适容器内(如均质杯本身具有无孔盖,可不转移样品),如使用均质袋,可直接进行培养,于36℃土1℃培养8h~18h。如为冷冻产品,应在45℃以下不超过15min,或2℃~5℃不超过18h解冻。5.2增菌
轻轻摇动培养过的样品混合物,移取1mL转种于10mLTTB内,于42℃1℃培养18h~24h。同时,另取1mL,转种于10mLSC内,于36℃±1℃培养18h~24h。5.3分离
分别用直径3mm的接种环取增菌液1环,划线接种于二个BS琼脂平板和一个XLD琼脂平板(或HE琼脂平板或沙门氏菌属显色培养基平板),于36℃土1℃分别培养40h~48h(BS琼脂平板)或18h~24h(XLD琼脂平板、HE琼脂平板、沙门氏菌属显色培养基平板),观察各个平板上生长的菌落,各个平板上的菌落特征见表1。
表1沙门氏菌属在不同选择性琼脂平板上的菌落特征选择性琼脂平板
BS琼脂
HE琼脂
XLD琼脂
沙门氏菌属显色培
5.4生化试验
沙门氏菌
菌落为黑色有金属光泽、棕褐色或灰色,菌落周围培养基可呈黑色或棕色:有些菌株形成灰绿色的菌落,周围培养基不变
蓝绿色或蓝色,多数菌落中心黑色或几乎全黑色有些菌株为黄色,中心黑色或几乎全黑色菌落呈粉红色,带或不带黑色中心,有些菌株可呈现大的带光泽的黑色中心,或呈现全部黑色的菌落;有些菌株为黄色菌落,带或不带黑色中心按照显色培养基的说明进行判定5.4.1自选择性琼脂平板上分别挑取2个以上典型或可疑菌落,接种三糖铁琼脂,先在斜面划线,再于底层穿刺;接种针不要灭菌,直接接种赖氨酸脱羧酶试验培养基和营养琼脂平板,于36℃土1℃C培养18h~24h,必要时可延长至48h。在三糖铁琼脂和赖氨酸脱羧酶试验培养基内,沙门氏菌属的反应结果见表2。
GB4789.4—2016
表2沙门氏菌属在三糖铁琼脂和赖氨酸脱羧酶试验培养基内的反应结果三糖铁琼脂
硫化氢
赖氨酸脱羧酶试验培养基
初步判断
可疑沙门氏菌属
可疑沙门氏菌属
可疑沙门氏菌属
非沙门氏菌
非沙门氏菌
注:K:产碱,A:产酸;十:阳性,一:阴性;十(-):多数阳性,少数阴性;十/一:阳性或阴性5.4.2接种三糖铁琼脂和赖氨酸脱羧酶试验培养基的同时,可直接接种蛋白陈水(供做靛基质试验)尿素琼脂(pH7.2)、氰化钾(KCN)培养基,也可在初步判断结果后从营养琼脂平板上挑取可疑菌落接种。于36℃士1℃培养18h~24h,必要时可延长至48h,按表3判定结果。将已挑菌落的平板储存于2℃~5℃或室温至少保留24h,以备必要时复查。表3沙门氏菌属生化反应初步鉴别表反应序号
硫化氢(H,S)
靛基质
注:十阳性;一阴性;十/一阳性或阴性。5.4.2.1
PH7.2尿素
氰化钾(KCN)
赖氨酸脱羧酶
反应序号A1:典型反应判定为沙门氏菌属。如尿素、KCN和赖氨酸脱羧酶3项中有1项异常,按表4可判定为沙门氏菌。如有2项异常为非沙门氏菌。表4沙门氏菌属生化反应初步鉴别表pH7.2尿素
注:十表示阳性;一表示阴性、氰化钾(KCN)
赖氨酸脱羧酶
判定结果
甲型副伤寒沙门氏菌(要
求血清学鉴定结果)
沙门氏菌IV或V(要求符
合本群生化特性)
沙门氏菌个别变体(要求
血清学鉴定结果)
5.4.2.2反应序号A2:补做甘露醇和山梨醇试验,沙门氏菌靛基质阳性变体两项试验结果均为阳性,但需要结合血清学鉴定结果进行判定5.4.2.3反应序号A3:补做ONPG。ONPG阴性为沙门氏菌,同时赖氨酸脱羧酶阳性,甲型副伤寒沙门氏菌为赖氨酸脱羧酶阴性、
5.4.2.4必要时按表5进行沙门氏菌生化群的鉴别。4
卫矛醇
山梨醇
水杨苷
丙二酸盐
注:十表示阳性;一表示阴性
表5沙门氏菌属各生化群的鉴别
GB4789.4—2016
5.4.3如选择生化鉴定试剂盒或全自动微生物生化鉴定系统,可根据5.4.1的初步判断结果,从营养琼脂平板上挑取可疑菌落,用生理盐水制备成浊度适当的菌悬液,使用生化鉴定试剂盒或全自动微生物生化鉴定系统进行鉴定。
5.5血清学鉴定
5.5.1检查培养物有无自凝性
一般采用1.2%~1.5%琼脂培养物作为玻片凝集试验用的抗原。首先排除自凝集反应,在洁净的玻片上滴加一滴生理盐水,将待试培养物混合于生理盐水滴内,使成为均一性的混浊悬液,将玻片轻轻摇动30s~60s,在黑色背景下观察反应(必要时用放大镜观察),若出现可见的菌体凝集,即认为有自凝性,反之无自凝性。对无自凝的培养物参照下面方法进行血清学鉴定。5.5.2多价菌体抗原(0)鉴定
在玻片上划出2个约1cm×2cm的区域,挑取1环待测菌,各放1/2环于玻片上的每一区域上部,在其中一个区域下部加1滴多价菌体(O)抗血清,在另一区域下部加人1滴生理盐水,作为对照。再用无菌的接种环或针分别将两个区域内的菌苔研成乳状液。将玻片倾斜摇动混合1min,并对着黑暗背景进行观察,任何程度的凝集现象皆为阳性反应。0血清不凝集时,将菌株接种在琼脂量较高的(如2%~3%)培养基上再检查:如果是由于Vi抗原的存在而阻止了0凝集反应时,可挑取菌苔于1mL生理盐水中做成浓菌液,于酒精灯火焰上煮沸后再检查。5.5.3多价鞭毛抗原(H)鉴定
操作同5.5.2。H抗原发育不良时,将菌株接种在0.55%~0.65%半固体琼脂平板的中央,待菌落蔓延生长时,在其边缘部分取菌检查;或将菌株通过接种装有0.3%0.4%半固体琼脂的小玻管1次~2次,自远端取菌培养后再检查。5.6血清学分型(选做项目)
5.6.10抗原的鉴定
用A~F多价○血清做玻片凝集试验,同时用生理盐水做对照。在生理盐水中自凝者为粗糙型菌株,不能分型。
被A~F多价0血清凝集者,依次用04;03、010;07;08;09;02和O11因子血清做凝集试验根据试验结果,判定0群。被03、010血清凝集的菌株,再用010、015、034、019单因子血清做凝集5
GB4789.4—2016
试验,判定E1、E4各亚群,每一个O抗原成分的最后确定均应根据〇单因子血清的检查结果,没有O单因子血清的要用两个○复合因子血清进行核对。不被A~F多价O血清凝集者,先用9种多价O血清检查,如有其中一种血清凝集,则用这种血清所包括的O群血清逐一检查,以确定O群。每种多价O血清所包括的O因子如下:O多价1A,B.C,D.E,F群(并包括6,14群)13.16,17,18,21群
0多价2
0多价3
0多价4
0多价5
0多价6
0多价7
0多价8
0多价9
28.30,35.38,39群
40,41,42.43群
44.45,4748群
50.51.52,53群
55,56,57.58群
59.60,61,62群
63.65,66.67群
5.6.2H抗原的鉴定
属于A~F各O群的常见菌型,依次用表6所述H因子血清检查第1相和第2相的H抗原。表6A~F群常见菌型
H抗原表
D(不产气的)
D(产气的)
第1相
第2相
不常见的菌型,先用8种多价H血清检查,如有其中一种或两种血清凝集,则再用这一种或两种血清所包括的各种H因子血清逐一检查,以第1相和第2项的H抗原。8种多价H血清所包括的H因子如下:
H多价1a,b.c,d.i
ehenx,enzs,fg.gms.gpu.gp.gq.mt,gzsH多价2
H多价3
k.r.y.z.zro.lv.lw,lzia.lzs.lz4oH多价412:1.5;1.6;1.7;z6
H多价5z4Z23,Z4Z24,Z4Zs2,Z29+Zs5,Z36+Z38H多价6
H多价7
H多价8
Z3g,Z41+Z42Zt4
Z52-Z53-Z54Z55
Z56,Z57,Z60Z61-Z62
每一个H抗原成分的最后确定均应根据H单因子血清的检查结果,没有H单因子血清的要用两个H复合因子血清进行核对。
检出第1相H抗原而未检出第2相H抗原的或检出第2相H抗原而未检出第1相H抗原的,可6
GB4789.4—2016
在琼脂斜面上移种1代~2代后再检查。如仍只检出一个相的H抗原,要用位相变异的方法检查其另二个相。单相菌不必做位相变异检查。位相变异试验方法如下:
简易平板法:将0.35%~0.4%半固体琼脂平板烘干表面水分,挑取因子血清1环,滴在半固体平板表面,放置片刻,待血清吸收到琼脂内,在血清部位的中央点种待检菌株,培养后,在形成蔓延生长的菌苔边缘取菌检查。
小玻管法:将半固体管(每管约1mL~2mL)在酒精灯上溶化并冷至50℃,取已知相的H因子血清0.05mL~0.1mL,加人于溶化的半固体内,混勾后,用毛细吸管吸取分装于供位相变异试验的小玻管内,待凝固后,用接种针挑取待检菌,接种于一端。将小玻管平放在平血内,并在其旁放一团湿棉花,以防琼脂中水分蒸发而干缩,每天检查结果,待另一相细菌解离后,可以从另一端挑取细菌进行检查。培养基内血清的浓度应有适当的比例,过高时细菌不能生长,过低时同一相细菌的动力不能抑制。一般按原血清1:200~1:800的量加人。小倒管法:将两端开口的小玻管(下端开口要留一个缺口,不要平齐)放在半固体管内,小玻管的上端应高出于培养基的表面,灭菌后备用。临用时在酒精灯上加热溶化,冷至50℃,挑取因子血清1环,加人小套管中的半固体内,略加搅动,使其混匀,待凝固后,将待检菌株接种于小套管中的半固体表层内,每天检查结果,待另一相细菌解离后,可从套管外的半固体表面取菌检查,或转种1%软琼脂斜面,于36℃培养后再做凝集试验。
5.6.3Vi抗原的鉴定
用Vi因子血清检查。已知具有Vi抗原的菌型有:伤寒沙门氏菌,丙型副伤寒沙门氏菌,都柏林沙门氏菌。
5.6.4菌型的判定
根据血清学分型鉴定的结果,按照附录B或有关沙门氏菌属抗原表判定菌型。6结果与报告
综合以上生化试验和血清学鉴定的结果,报告25g(mL)样品中检出或未检出沙门氏菌。A.1缓冲蛋白陈水(BPW)
A.1.1成分
蛋白陈
氯化钠
磷酸氢二钠(含12个结晶水)
磷酸二氢钾
蒸馏水
附录A
培养基和试剂
1000mL
GB4789.4—2016
将各成分加人蒸馏水中,搅混均匀,静置约10min,煮沸溶解,调节pH至7.2土0.2.高压灭菌121℃,15min。
四硫磺酸钠煌绿(TTB)增菌液
基础液
蛋白陈
牛肉膏
氯化钠
碳酸钙
蒸馏水
1000mL
除碳酸钙外,将各成分加入蒸馏水中,煮沸溶解,再加入碳酸钙,调节pH至7.0士0.2.高压灭菌121℃,20min。
硫代硫酸钠溶液
硫代硫酸钠(含5个结晶水)
蒸馏水
高压灭菌121℃,20min。
碘溶液
碘化钾
蒸馏水
加至100mL
加至100mL
将碘化钾充分溶解于少量的蒸馏水中,再投人碘片,振摇玻瓶至碘片全部溶解为止,然后加蒸馏水至规定的总量,贮存于棕色瓶内,塞紧瓶盖备用。A.2.4
0.5%煌绿水溶液
蒸馏水
溶解后,存放暗处,不少于1d,使其自然灭菌。A.2.5
牛胆盐溶液
牛胆盐
蒸馏水
加热煮沸至完全溶解,高压灭菌121℃,20minA.2.6
基础液
硫代硫酸钠溶液
碘溶液
煌绿水溶液
牛胆盐溶液
GB4789.4—2016
临用前,按上列顺序,以无菌操作依次加入基础液中,每加入一种成分,均应摇匀后再加入另一种成分。
A.3亚硒酸盐胱氨酸(SC)增菌液
蛋白陈
磷酸氢二钠
亚硒酸氢钠
L-胱氨酸
蒸馏水
1000ml
除亚硒酸氢钠和L-胱氨酸外,将各成分加入蒸馏水中,煮沸溶解,冷至55℃以下,以无菌操作加入亚硒酸氢钠和1g/LL-胱氨酸溶液10mL(称取0.1gL-胱氨酸.加1mol/L氢氧化钠溶液15mL,使溶解,再加无菌蒸馏水至100mL即成,如为DL-胱氨酸,用量应加倍)。摇匀,调节pH至7.0土0.2。A.4
亚硫酸铋(BS)琼脂
蛋白陈
牛肉膏
葡萄糖
硫酸亚铁
磷酸氢二钠
柠檬酸铋铵
0.025g或5.0g/L水溶液5.0mL
亚硫酸钠
蒸馏水
2制法
18.0g~20.0g
1000ml
GB4789.4—2016
将前三种成分加入300mL蒸馏水(制作基础液)硫酸亚铁和磷酸氢二钠分别加入20mL和30mL蒸馅水中,柠檬酸铋铵和亚硫酸钠分别加入另一20mL和30mL蒸馏水中,琼脂加人600mL蒸馏水中。然后分别搅拌均匀,煮沸溶解。冷至80℃左右时,先将硫酸亚铁和磷酸氢二钠混匀.倒入基础液中,混匀。将柠檬酸铋铵和亚硫酸钠混匀.倒人基础液中,再混。调节pH至7.5士0.2.随即倾人琼脂液中,混合均匀,冷至50℃~55℃。加人煌绿溶液,充分混匀后立即倾注平皿。注:本培养基不需要高压灭菌.在制备过程中不宜过分加热,避免降低其选择性,贮于室温暗处,超过48h会降低其选择性,本培养基宜于当天制备,第二天使用。A.5HE琼脂(HektoenEntericAgar)A.5.1成分
蛋白陈
牛肉膏
水杨素
氯化钠
蒸馏水
0.4%溴麝香草酚蓝溶液
Andrade指示剂
2制法
18.0g~20.0g
1000ml
将前面七种成分溶解于400mL蒸馏水内作为基础液:将琼脂加人于600mL蒸馏水内。然后分别搅拌均匀,煮沸溶解。加人甲液和乙液于基础液内,调节pH至7.5士0.2。再加入指示剂,并与琼脂液合并,待冷至50℃~55℃倾注平血。注:①本培养基不需要高压灭菌,在制备过程中不宜过分加热避免降低其选择性。②甲液的配制
硫代硫酸钠
柠檬酸铁铵
蒸馏水
③乙液的配制
去氧胆酸钠
蒸馏水
①Andrade
酸性复红
指示剂
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。






 ✕
✕