基本信息
标准号:
HG/T 5567-2019
中文名称:水处理剂用氢氧化铝
标准类别:化工行业标准(HG)
标准状态:现行
出版语种:简体中文
下载格式:.zip .pdf
下载大小:8.09 MB
相关标签:
处理剂
氢氧化铝

标准分类号
关联标准
出版信息
相关单位信息
标准简介
HG/T 5567-2019.Aluminium hydroxide for water treatment chemicals.
1范围
HG/T 5567规定了水处理剂用氢氧化铝的产品分型、要求、试验方法、检验规则以及标志、标签、包装和运输。
HG/T 5567适用于水处理剂用氢氧化铝。该产品以铝土矿、石灰石、工业氢氧化钠或工业碳酸钠为主要原料,主要用作饮用水、工业用水和污水处理用聚氯化铝、硫酸铝和其他含铝水处理剂的生产原料。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文
件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 601化学试剂标准滴 定溶液的制备
GB/T 602化学试剂杂质测定用标准溶液的制备
GB/T 603化学试剂试验方法中所用制剂及制品的制备
GB/T 6682分析实验室用水规格和试验方法
GB/T 8170数值修约规则 与极限数值的表示和判定
GB/T 12573水泥取样方法
YS/T 534.1氢氧化铝化学分析方法 第1部分:水分的测定重量法
YS/T 534.4氢氧化铝化学分析方法 第4部分:三氧化二铁含量的测定邻二氮杂菲光度法
3产品分型
水处理剂用氢氧化铝产品按氧化铝溶出率分为I型和II型。
4要求
4.1外观: 白色、微黄色粉末或砂状晶体。
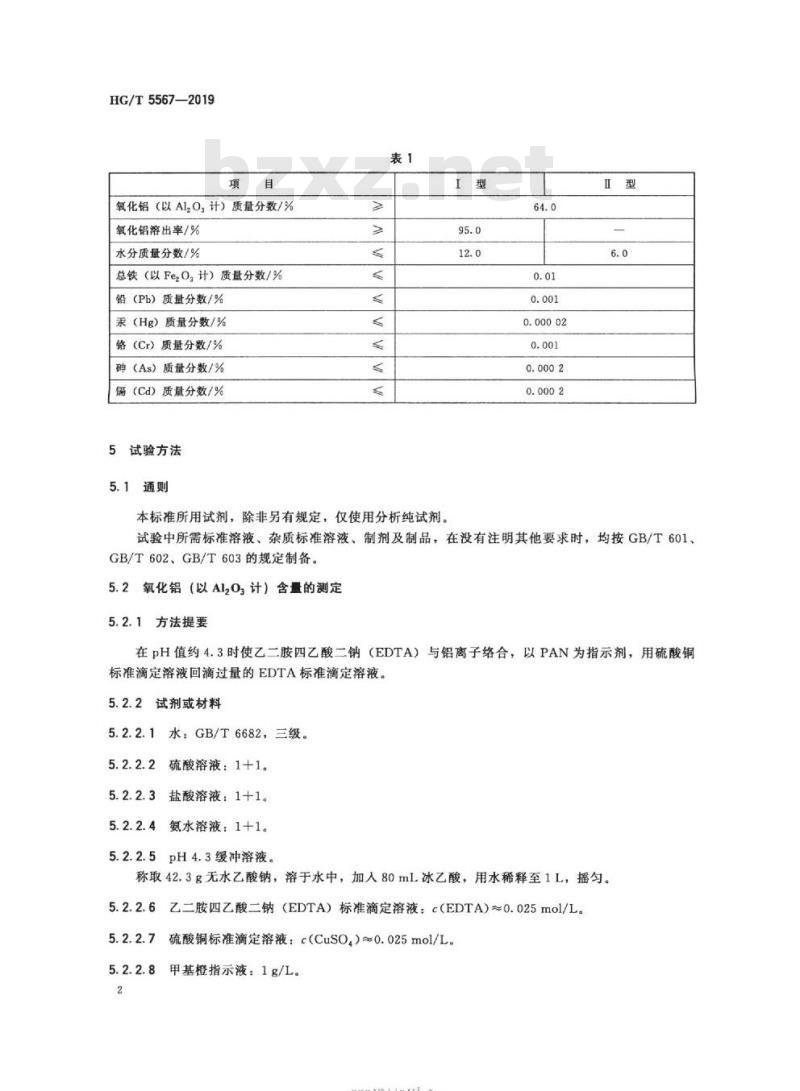
4.2水处理剂用氢氧化铝应符合表1的要求。
5试验方法
5.1 通则
本标准所用试剂,除非另有规定,仅使用分析纯试剂。
试验中所需标准溶液、杂质标准溶液、制剂及制品,在没有注明其他要求时,均按GB/T 601、GB/T 602、GB/T 603的规定制备。
标准内容
ICS13.060.99
中华人民共和国化工行业标准
HG/T5567—2019
水处理剂用氢氧化铝
Aluminiumhydroxidefor watertreatment chemicals2019-12-24发布
2020-07-01实施
中华人民共和国工业和信息化部发布rKaeerKca-
本标准按照GB/T1.12009给出的规则起草。本标准由中国石油和化学工业联合会提出,HG/T5567—2019
本标准由全国化学标准化技术委员会水处理剂分技术委员会(SAC/TC63/SC5)归口。本标准起草单位:深圳市中润水工业技术发展有限公司、中铝中州铝业有限公司、中铝山东有限公司、淄博正河净水剂有限公司、江苏省特种设备安全监督检验研究院常州分院、同济大学、蓝保(厦门)水处理科技有限公司、浙江水知音环保科技有限公司、中海油天津化工研究设计院有限公司。本标准主要起草人:李润生、李志刚、董晓辉、杨爱国、陈道琰、李风亭、陈嘉宾、俞明华、李琳、郡宏谦。
rrKaeeikAca
水处理剂用氢氧化铝
HG/T5567—2019
警示一一本标准所使用的强酸、强碱具有腐蚀性,使用时应注意。溅到身上时,用大量水冲洗,避免吸入或接触皮肤。
1范围
本标准规定了水处理剂用氢氧化铝的产品分型、要求、试验方法、检验规则以及标志、标签、包装和运输。
本标准适用于水处理剂用氢氧化铝。该产品以铝土矿、石灰石、工业氢氧化钠或工业碳酸钠为主要原料,主要用作饮用水、工业用水和污水处理用聚氯化铝、硫酸铝和其他含铝水处理剂的生产原料。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件GB/T601
GB/T602
GB/T603
GB/T6682
GB/T8170
化学试剂
化学试剂
化学试剂
标准滴定溶液的制备
杂质测定用标准溶液的制备
试验方法中所用制剂及制品的制备分析实验室用水规格和试验方法数值修约规则与极限数值的表示和判定GB/T12573
YS/T534.1
YS/T534.4
3产品分型
水泥取样方法
氢氧化铝化学分析方法
第1部分:水分的测定重量法
氢氧化铝化学分析方法
第4部分:三氧化二铁含量的测定水处理剂用氢氧化铝产品按氧化铝溶出率分为I型和Ⅱ型。4要求
4.1外观:白色、微黄色粉末或砂状晶体。2水处理剂用氢氧化铝应符合表1的要求。4.2
-KaeerKAca-
邻二氮杂菲光度法
HG/T5567—2019
氧化铝(以Al,0,计)质量分数/%氧化铝溶出率/%
水分质量分数/%
总铁(以Fe2O,计)质量分数/%
铅(Pb)质量分数/%
汞(Hg)质量分数/%
铬(Cr)质量分数/%
碑(As)质量分数/%
镉(Cd)质量分数/%
试验方法
5.1通则
本标准所用试剂,除非另有规定,仅使用分析纯试剂。型
试验中所需标准溶液、杂质标准溶液、制剂及制品,在没有注明其他要求时,均按GB/T601、GB/T602、GB/T603的规定制备。5.2氧化铝(以Al20计)含量的测定5.2.1方法提要
在pH值约4.3时使乙二胺四乙酸二钠(EDTA)与铝离子络合,以PAN为指示剂,用硫酸铜标准滴定溶液回滴过量的EDTA标准滴定溶液。5.2.2
2试剂或材料
水:GB/T6682,三级。
硫酸溶液:1十1。
盐酸溶液:1+1。
氨水溶液:1十1。
pH4.3缓冲溶液。
称取42.3g无水乙酸钠,溶于水中,加入80mL冰乙酸,用水稀释至1L,摇勺。5.2.2.6
乙二胺四乙酸二钠(EDTA)标准滴定溶液:c(EDTA)0.025mol/L。硫酸铜标准滴定溶液:c(CuSO,)α0.025mol/L。甲基橙指示液:1g/L。
-KaeerKAca-
5.2.2.91-(2-吡啶偶氮)-2-萘酚(PAN)指示剂。称取0.2gPAN,溶于100mL体积分数为95%的乙醇溶液中。5.2.3分析步骤
HG/T5567—2019
称取预先于110℃土5℃下烘2h后的试样1.0g(m),精确至0.2mg。放人锥形瓶中,加人10mL硫酸溶液,放在电炉上加热溶解至透明,加水稀释冷却后,移人500mL容量瓶中,定容,摇匀。此为试液A。
移取25.00mL试液A于250mL锥形瓶中,加人30.00mL乙二胺四乙酸二钠(EDTA)标准滴定溶液,加水至约100mL。将溶液加热至70℃~80℃,滴加2滴甲基橙指示液,用氨水溶液将试液颜色调至红色突变为黄色,加人2滴盐酸溶液,再加人15mLpH4.3缓冲溶液,煮沸2min。取下,稍冷,加人5滴~6滴PAN指示剂,以硫酸铜标准滴定溶液滴定至亮紫色或紫红色。5.2.4结果计算
氧化铝(Al,O,)含量以质量分数w计,数值以%表示,按公式(1)计算:wi
式中:
(V1c/1000—Vc/1000)M/2
mX(25/500)
移取乙二胺四乙酸二钠(EDTA)标准滴定溶液的体积的数值,单位为毫升(mL)(V,=30);Vi种
乙二胺四乙酸二钠(EDTA)标准滴定溶液的浓度的准确数值,单位为摩尔每升(mol/L);-滴定时试液消耗硫酸铜标准滴定溶液的体积的数值,单位为毫升(mL);V
一硫酸铜标准滴定溶液的浓度的准确数值,单位为摩尔每升(mol/L);M——三氧化二铝的摩尔质量的数值,单位为克每摩尔(g/mol)(M=101.96);m—试料的质量的数值,单位为克(g)。5.2.5允许差
取平行测定结果的算术平均值为测定结果,平行测定结果的绝对差值不大于0.1%。5.3氧化铝溶出率的测定
5.3.1方法提要
根据盐酸与氢氧化铝溶出反应滤液体积和含量以及氢氧化铝的加量,计算氢氧化铝中氧化铝溶出率。
5.3.2试剂或材料
5.3.2.1水:GB/T6682,三级。
5.3.2.2盐酸溶液:1+1。
5.3.2.3氨水溶液:1+1。
5.3.2.4pH4.3缓冲溶液。
称取42.3g无水乙酸钠,溶于水中,加人80mL冰乙酸,用水稀释至1L,摇勾。5.3.2.5乙二胺四乙酸二钠(EDTA)标准滴定溶液:c(EDTA)~0.025mol/L。5.3.2.6硫酸铜标准滴定溶液:c(CuSO,)~0.025mol/L。3
rKacerkAca-
HG/T5567—2019
5.3.2.7甲基橙指示液:1g/L。
5.3.2.81-(2-吡啶偶氮)-2-萘酚(PAN)指示液。称取0.2gPAN,溶于100mL体积分数为95%的乙醇溶液中。5.3.3仪器设备
5.3.3.1可控加热搅拌反应器:带45mm橄榄型聚四氟搅拌子。5.3.3.2玻璃冷凝回流装置:带250mL磨口三角烧瓶和磨口球型冷凝管。5.3.3.3玻璃抽滤装置:带250mL抽滤瓶和直径80mm的布氏漏斗。5.3.4分析步骤
移取100mL盐酸溶液于250mL磨口三角烧瓶中,放人聚四氟搅拌子。称取试料(干基)16.0g,精确至0.01g(m,)。在搅拌下放人磨口三角烧瓶内,套上磨口球型冷凝管,加热回流反应,自100℃开始计时,保持沸腾反应2h。取下,热用布氏漏斗以中速定性滤纸真空抽滤。用水洗涤磨口三角烧瓶,并用水洗涤滤渣,反复洗滤,每次用水不超过20mL。滤液移人500mL容量瓶中,用水稀释至刻度,摇匀。此为试液B。移取20.00mL试液B于250mL容量瓶中,加水至刻度,摇匀。移取20.00mL稀释液于250mL锥形瓶中,加人30.00mL乙二胺四乙酸二钠(EDTA)标准滴定溶液,加水至约100mL,加热至70℃~80℃。滴加2滴甲基橙指示液,用氨水溶液调至红色突变为黄色。加入2滴盐酸溶液,再加入15mLpH4.3缓冲溶液,煮沸2min。取下,稍冷,加人5滴~6滴PAN指示液,以硫酸铜标准滴定溶液滴定至亮紫色或紫红色。5.3.5结果计算
可溶性氧化铝含量以质量分数w,计,数值以%表示,按公式(2)计算:(Vic1/1000-Ve/1000)M/2
w2=mx(20/500)x(20/250)
式中:
Vi一—移取乙二胺四乙酸二钠(EDTA)标准滴定溶液的体积的数值,单位为毫升(mL)(V,=30);
乙二胺四乙酸二钠(EDTA)标准滴定溶液的浓度的准确数值,单位为摩尔每升(mol/L);滴定时试样消耗硫酸铜标准滴定溶液的体积的数值,单位为毫升(mL);-硫酸铜标准滴定溶液的浓度的准确数值,单位为摩尔每升(mol/L);三氧化二铝的摩尔质量的数值,单位为克每摩尔(g/mol)(M=101.96);试料的质量的数值,单位为克(g)。氧化铝溶出率以百分数X计,数值以%表示,按公式(3)计算:x-W2x100
式中:
w2——可溶性氧化铝含量,以%表示;w1———按5.2求出的氧化铝含量,以%表示。5.3.6允许差
取平行测定结果的算术平均值为测定结果,平行测定结果的绝对差值不大于0.1%。4
-rrKaeerKca-
5.4水分含量的测定
按YS/T534.1的规定进行水分含量的测定5.5总铁(以Fe203计)含量的测定按YS/T534.4的规定进行总铁(以Fe,O,计)含量的测定。5.6铅含量的测定
5.6.1方法提要
采用电加热原子吸收光谱法,在波长283.3nm处测定吸光度,求出铅含量。5.6.2试剂或材料
5.6.2.1硝酸溶液:1+1。
5.6.2.2铅标准贮备溶液:0.1mg/mL。5.6.2.3铅标准溶液:1mL含有1μgPb。HG/T5567—2019
移取1.00mL铅标准贮备溶液,置于100mL容量瓶中,加人2mL硝酸溶液,用水稀释至刻度,摇匀。
5.6.3仪器设备
5.6.3.1微量进液装置:装有按钮式5μL~500μL微量液体流量计或自动进样器。5.6.3.2电加热原子吸收分析装置:带电加热方式,可进行反向接地补偿。5.6.3.3发热炉:石墨或耐高温金属制。5.6.3.4铅空心阴极灯。
5.6.4分析步骤
分别移取0.00mL(空白)、1.00mL、2.00mL、3.00mL铅标准溶液于4个50mL容量瓶中,各加入1mL硝酸溶液,用水稀释至刻度,摇匀。用微量进液装置将配好的试样注入发热炉,经干燥、灰化、原子化后,在波长283.3nm处测其吸光度。以铅标准溶液的质量浓度(μg/L)为横坐标、相应的吸光度为纵坐标绘制校准曲线或计算回归方程。移取适量体积的试液A,按上述步骤操作,测定。由校准曲线或回归方程得出铅的质量浓度。5.6.5
结果计算
铅含量以质量分数w,计,数值以%表示,按公式(4)计算:—pVx10-9
mV,/VA
式中:
p—试样中铅的质量浓度的数值,单位为微克每升(μg/L);V—测定时试样溶液的总体积的数值,单位为毫升(mL)(V=50);m——试料的质量的数值,单位为克(g);Vi—一移取试液A的体积的数值,单位为毫升(mL);-KaeerKAca-bzxZ.net
HG/T5567—2019
VA——试液A的总体积的数值,单位为毫升(mL)(VA=500)。5.6.6充许差
取平行测定结果的算术平均值为测定结果,平行测定结果的绝对差值不大于0.0002%。5.7汞含量的测定
5.7.1方法提要
试样经酸加热消解后,在酸性介质中,试样中的汞被硼氢化钾(KBH)还原成原子态汞,由载气(氩气)带入原子化器中,在特制汞空心阴极灯照射下基态汞原子被激发至高能态,在去活化到基态时发射出特征波长的荧光,其荧光强度与汞含量成正比,与标准系列比较定量。5.7.2试剂或材料
5.7.2.1硝酸:优级纯。
5.7.2.2盐酸:优级纯。
5.7.2.3硫酸溶液:1+1。
5.7.2.4硝酸溶液:1+4。
5.7.2.5盐酸溶液:1+19。
5.7.2.6硼氢化钾-氢氧化钠溶液。称取2.5g氢氧化钠和10.0g硼氢化钾于聚乙烯烧杯中,用水溶解,稀释至1000mL。此溶液现用现配。
5.7.2.7汞标准贮备溶液:0.1mg/mL。5.7.2.8汞标准溶液(I):5μg/mL。移取5mL汞标准贮备溶液,置于100mL容量瓶中,加入0.05g重铬酸钾、5mL硝酸,用水稀释至刻度。此溶液现用现配。
9汞标准溶液(II):0.05μg/mL。5.7.2.9
移取1mL汞标准溶液(I),置于100mL容量瓶中,加人0.05g重铬酸钾、5mL盐酸,用水稀释至刻度。此溶液现用现配。5.7.3仪器设备
5.7.3.1原子荧光光度计。
5.7.3.2汞空心阴极灯.
5.7.4校准曲线的绘制
分别取0.00mL(空白)、2.00mL、4.00mL、6.00mL、8.00mL、10.00mL汞标准溶液()于6个100mL容量瓶中,各加入5mL盐酸,稀释至刻度,摇匀。此系列溶液中汞含量分别为0μg/L、1μg/L、2μg/L、3μg/L、4μg/L、5μg/L。仪器稳定后,以硼氢化钾-氢氧化钠溶液为还原剂,以盐酸溶液为载流溶液,在仪器最佳工作条件下测定其荧光值。以测得的荧光值为纵坐标、相对应的汞的质量浓度(ug/L)为横坐标绘制校准6
rrKaeerKAca-
曲线或计算回归方程。
HG/T5567—2019
注:使用原子荧光光谱仪测定时,所需的硼氢化钾溶液浓度、载流溶液浓度以及各种元素校准曲线线性范围、样品溶液的pH值等会因仪器的型号不同而有差异,使用者可根据仪器型号选择最佳测试条件。5.7.5分析步骤
5.7.5.1玻璃仪器的预清洗
实验所用玻璃器血使用前应使用硝酸溶液(1十4)浸泡24h,然后用水冲洗干净,备用。5.7.5.2样品的测定
称取预先于110℃士5℃下烘2h后的试样1.0g(m),精确至0.2mg。放人锥形瓶中,加人10mL硫酸溶液,放在电炉上加热溶解至透明,加水稀释冷却后,移人100mL容量瓶中,加入5mL盐酸,稀释至刻度,摇匀。再按5.7.4的步骤进行测定(如有浑浊,使用中速定量滤纸干过滤后测定),由校准曲线或回归方程得出汞的质量浓度。5.7.6结果计算
汞含量以质量分数w。计,数值以%表示,按公式(5)计算:pVx10-
式中:
p———由校准曲线查得或由回归方程计算出的试样中汞的质量浓度的数值,单位为微克每升(μg/L);
V—试样溶液的总体积的数值,单位为毫升(mL)(V=100);m——试料的质量的数值,单位为克(g)。5.7.7允许差
取平行测定结果的算术平均值为测定结果,平行测定结果的绝对差值不大于0.000005%。5.8铬含量的测定
5.8.1方法提要
采用电加热原子吸收光谱法,在波长429.0nm处测定铬原子的吸光度,求出铬含量。5.8.2试剂或材料
5.8.2.1硝酸溶液:1+1。
5.8.2.2铬标准贮备溶液:0.1mg/mL。5.8.2.3铬标准溶液:1mL含有1μgCr。移取1.00mL铬标准贮备溶液于100mL容量瓶中,加入2mL硝酸溶液,用水稀释至刻度摇匀。
5.8.3仪器设备
5.8.3.1微量进液装置:装有按钮式5μL~500μL微量液体流量计或自动进样器。7
-KaeerKAca-
HG/T5567—2019
5.8.3.2电加热原子吸收分析装置:带电加热方式,可进行反向接地补偿。5.8.3.3发热炉:石墨或耐高温金属制。5.8.3.4铬空心阴极灯。
5.8.4分析步骤
分别移取0.00mL(空白)、1.00mL、2.00mL、3.00mL铬标准溶液于4个50mL容量瓶中,各加入1mL硝酸溶液,用水稀释至刻度,播匀。用微量进液装置将配好的试样注人发热炉,经干燥、灰化、原子化后,在波长429.0nm处测其吸光度。以铬标准溶液的质量浓度(μg/L)为横坐标、相应的吸光度为纵坐标绘制校准曲线或计算回归方程。移取适量体积的试液A,按上述步骤从“各加人1mL硝酸溶液,…...”操作,测定,由校准曲线或回归方程得出铬的质量浓度。5.8.5结果计算
铬含量以质量分数ws计,数值以%表示,按公式(6)计算:pvx10-9
式中:
P—试样中铬的质量浓度的数值,单位为微克每升(μg/L);V——测定时试样溶液的总体积的数值,单位为毫升(mL)(V=50);m—试料的质量的数值,单位为克(g);Vi一—移取试液A的体积的数值,单位为毫升(mL);VA——试液A的总体积的数值,单位为毫升(mL)(VA=500)。5.8.6允许差
取平行测定结果的算术平均值为测定结果,平行测定结果的绝对差值不大于0.0002%。5.9
9砷含量的测定
5.9.1方法提要
试样经加酸处理后,加入硫脲使5价砷预还原为3价砷,再加人硼氢化钠或硼氢化钾使还原生成砷化氢,由氩气载人石英原子化器中分解为原子态砷,在砷空心阴极灯的发射光激发下产生原子荧光,其荧光强度在固定条件下与被测溶液中的砷的浓度成正比,与标准系列比较定量。5.9.2试剂或材料
5.9.2.1盐酸:优级纯。
5.9.2.2硝酸:优级纯。
5.9.2.3盐酸溶液:1+19。
5.9.2.4硝酸溶液:1+4。
5.9.2.5硫脲溶液:50g/L。
硼氢化钾-氢氧化钠溶液。
-nKaerkAca-
HG/T5567-2019
称取5.0g氢氧化钠和20.0g硼氢化钾于聚乙烯烧杯中,用水溶解,稀释至1000mL,贮存于聚乙烯瓶中。
5.9.2.7砷标准贮备溶液:0.1mg/mL。5.9.2.8砷标准溶液:0.2μg/mL。移取10.00mL砷标准贮备溶液于100mL容量瓶中,加入5.0mL盐酸,用水稀释至刻度,混匀。临用时移取2.00mL此溶液,置于100mL容量瓶中,加入5.0mL盐酸,用水稀释至刻度,混匀。
5.9.3仪器设备
5.9.3.1原子荧光光度计。
5.9.3.2砷空心阴极灯。
5.9.4校准曲线的绘制
分别移取0.00mL(空白)、2.00mL、4.00mL、6.00mL、8.00mL碑标准溶液于5个100mL容量瓶中,各加人5.0mL盐酸、20mL硫豚溶液,用水稀释至刻度,摇匀,放置30min。此系列溶液中砷的质量浓度分别为0μg/L、4μg/L、8μg/L、12μg/L、16μg/L。仪器稳定后,以硼氢化钾-氢氧化钠溶液为还原剂,以盐酸溶液为载流溶液,在仪器最佳工作条件下测定其荧光值。以测得的荧光值为纵坐标、相对应的砷的质量浓度(μg/L)为横坐标绘制校准曲线或计算回归方程。
注:使用原子荧光光谱仪测定时,所需的硼氢化钾溶液浓度、载流溶液浓度以及各种元素校准曲线线性范围、样品溶液的pH值等会因仪器的型号不同而有差异,使用者可根据仪器型号选择最佳测试条件。5.9.5分析步骤
5.9.5.1玻璃仪器的预清洗
实验所用玻璃器血使用前应使用硝酸溶液(1十4)浸泡24h,然后用水冲洗干净,备用。5.9.5.2样品的测定
移取适量体积试液A,置于100mL容量瓶中,按5.9.4的步骤进行测定(如有浑浊,使用中速定量滤纸干过滤后测定),由校准曲线或回归方程得出碑含量。5.9.6结果计算
砷含量以质量分数w。计,数值以%表示,按公式(7)计算:evx10-9
mV.V-×100
式中:
·(7)
p——由校准曲线查得或由回归方程计算出的砷的质量浓度的数值,单位为微克每升(μg/L);V一试样溶液的总体积的数值,单位为毫升(mL)(V=100);m——试料的质量的数值,单位为克(g);V1一移取试液A的体积的数值,单位为毫升(mL);VA——试液A的总体积的数值,单位为毫升(mL)(V^=500)。9
-KaeerKAca-
HG/T5567—2019
5.9.7允许差
取平行测定结果的算术平均值为测定结果,平行测定结果的绝对差值不大于0.00005%。5.10镉含量的测定
5.10.1方法提要
采用电加热原子吸收光谱法,在波长228.8nm处测定吸光度,求出镉含量。5.10.2试剂或材料
5.10.2.1硝酸溶液:1+1。
5.10.2.2镉标准贮备溶液:0.1mg/1mL。5.10.2.3镉标准溶液:此溶液1mL含0.1μgCd。移取1.00mL镉标准贮备溶液,置于100mL容量瓶中,加人2mL硝酸溶液,用水稀释至刻度,摇勾。再取10.00mL该溶液于100mL容量瓶中,加入2mL硝酸溶液,用水稀释至刻度,摇匀。此溶液现用现配。
5.10.3仪器设备
5.10.3.1微量进液装置:装有按钮式5μL~500μL微量液体流量计或自动进样器。5.10.3.2电加热原子吸收分析装置:带电加热方式,可进行反向接地补偿。5.10.3.3发热炉:石墨或耐高温金属制。5.10.3.4锅空心阴极灯。
5.10.4分析步骤
分别移取0.00mL(空白)、0.50mL、1.00mL、1.50mL标准溶液于4个50mL容量瓶中,各加入1mL硝酸溶液,用水稀释至刻度,摇匀。用微量进液装置将配好的试样注人发热炉,经干燥、灰化、原子化后,在波长228.8nm处测其吸光度。以镉标准溶液的质量浓度(μg/L)为横坐标、相应的吸光度为纵坐标绘制校准曲线或计算回归方程。移取适量体积的试液A,按上述步骤操作,测定。由校准曲线或回归方程得出辐的质量浓度,5.10.5结果计算
镉含量以质量分数w,计,数值以%表示,按公式(8)计算:evx10-9
mVi/VA
由校准曲线或回归方程得出的试样中镉的质量浓度的数值,单位为微克每升(μg/L);V—测定时试样溶液的总体积的数值,单位为毫升(mL)(V=50);-试料的质量的数值,单位为克(g);m
Vi——移取试液A的体积的数值,单位为毫升(mL);VA一—试液A的总体积的数值,单位为毫升(mL)(Va=500)。10
rrKaeerKAca-
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。






 ✕
✕