基本信息
标准号:
HG/T 2323-2019
中文名称:代替 HG/T 2323-2012 工业氯化锌
标准类别:化工行业标准(HG)
标准状态:现行
出版语种:简体中文
下载格式:.zip .pdf
下载大小:9.35 MB
相关标签:
2012
工业
氯化锌

标准分类号
关联标准
出版信息
相关单位信息
标准简介
HG/T 2323-2019.Zinc chloride for industrial use.
1范围
HG/T 2323规定了工业氯化锌的分类、要求、试验方法、检验规则、标志、标签、包装、运输和
贮存。
HG/T 2323适用于固体氯化锌和氯化锌溶液。该产品主要用于电池、活性炭、焊药、造纸、钛白粉等工业,也可用作有机合成的脱水剂、缩合剂,木材防腐剂,橡胶助剂,水处理剂等。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文
件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB 190危险货物包装标志
GB/T 191-2008包装储运图示标志
GB/T 6678化工产品采样总则
GB/T 6680液体化工产 品采样通则
GB/T 6682-2008分析实验室用水规格和试验方法
GB/T 8170数值修约规则与极限数值的表示和判定
GB 12268-2012 危险货物品名表
GB/T 23768-2009 无机化工产品火焰原子吸收光谱法通则
HG/T 3696.1无机化工产品 化学分析用标准溶液、制剂及制品的制备第1部分:标准滴定溶液的制备
HG/T 3696.2无机化工产品化学分析用标准溶液、制剂及制品的制备第2部分:杂质标准溶液的制备
HG/T 3696.3无机化工产品化学分析用标准溶液、制剂及制品的制备第3部分:制剂及制品的制备
YS/T 565电池用锌板和锌带
标准内容
ICS71.060.50
中华人民共和国化工行业标准
HG/T2323—2019
代替HG/T2323—2012
工业氯化锌
Zincchlorideforindustrialuse2019-12-24发布
2020-07-01实施
中华人民共和国工业和信息化部发布rKaeerKca-
本标准按照GB/T1.1—2009给出的规则起草。HG/T2323—2019
本标准代替HG/T2323—2012《工业氯化锌》。与HG/T2323—2012相比,除编辑性修改外主要技术变化如下:
修改了产品分类(见4,2012年版的4);修改了产品技术要求(见5.2,2012年版的5.2);修改了锌片腐蚀试验方法(见6.13,2012年版的6.11);修改了产品检验规则(见7,2012年版的7);修改了产品包装、运输要求(见9,2012年版的9);删除了碱和碱土金属指标(见2012年版的5.2);删除了碱和碱土金属测定方法(见2012年版的6.10);删除了产品保质期要求(见2012年版的9.4);删除了附录A(见2012年版的附录A);-增加了氯化锌含量测定方法,原方法作为仲裁法(见6.3.2);增加了、钙、水分指标(见5.2);一增加了、钙、水分测定方法(见6.9、6.10、6.11)。本标准由中国石油和化学工业联合会提出。本标准由全国化学标准化技术委员会无机化工分技术委员会(SAC/TC63/SC1)归口。本标准起草单位:中海油天津化工研究设计院有限公司、国家无机盐产品质量监督检验中心、潍坊恒丰化工有限公司、深圳市中润水工业技术发展有限公司、潍坊门捷化工有限公司、嘉善绿野环保材料厂。
本标准主要起草人:安晓英、梁媛、王正利、李润生、刘泉军、俞明华、张天壤、庄爱娟、丁灵、弓创周。
本标准的历次版本发布情况为:HG/T2323—1979;HG/T2323—1992;HG/T2323—2004;HG/T2323-—2012。I
-KaeerKAca-
工业氯化锌
HG/T2323—2019
警示一—按GB12268一2012第6章的规定,本产品属第8类腐蚀性物质,操作时应小心谨慎。本试验方法中使用的部分试剂具有毒性或腐蚀性,操作时须小心谨慎!如溅到皮肤或眼睛上应立即用水冲洗,严重者应立即就医。
1范围
本标准规定了工业氯化锌的分类、要求、试验方法、检验规则、标志、标签、包装、运输和贮存。
本标准适用于固体氯化锌和氯化锌溶液。该产品主要用于电池、活性炭、焊药、造纸、钛白粉等工业,也可用作有机合成的脱水剂、缩合剂,木材防腐剂,橡胶助剂,水处理剂等。2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB190危险货物包装标志
GB/T191—2008包装储运图示标志GB/T6678化工产品采样总则
GB/T6680液体化工产品采样通则GB/T6682—2008分析实验室用水规格和试验方法GB/T8170数值修约规则与极限数值的表示和判定GB12268—2012危险货物品名表
GB/T23768—2009无机化工产品
火焰原子吸收光谱法通则
HG/T3696.1
无机化工产品化学分析用标准溶液、制剂及制品的制备第1部分:标准滴定溶液的制备
第2部分:杂质标
无机化工产品化学分析用标准溶液、制剂及制品的制备HG/T3696.2
准溶液的制备
HG/T3696.3
无机化工产品化学分析用标准溶液、制剂及制品的制备第3部分:制剂及制品的制备
YS/T565电池用锌板和锌带
3分子式和相对分子质量
分子式:ZnClz
相对分子质量:136.28(按2016年国际相对原子质量)4分类
工业氯化锌分为固体和液体两类,每个类别分型:1
-KaeerKAca-
HG/T2323—2019
固体I型主要用于有机合成、电池工业等,Ⅱ型主要用于电池工业及一般工业;液体I型主要用于有机合成、钛白粉生产等,Ⅱ型主要用于电池工业,Ⅲ型主要用于一般工业。
5要求
外观:固体应为白色粉末或小颗粒;液体应为无色透明溶液。5.2
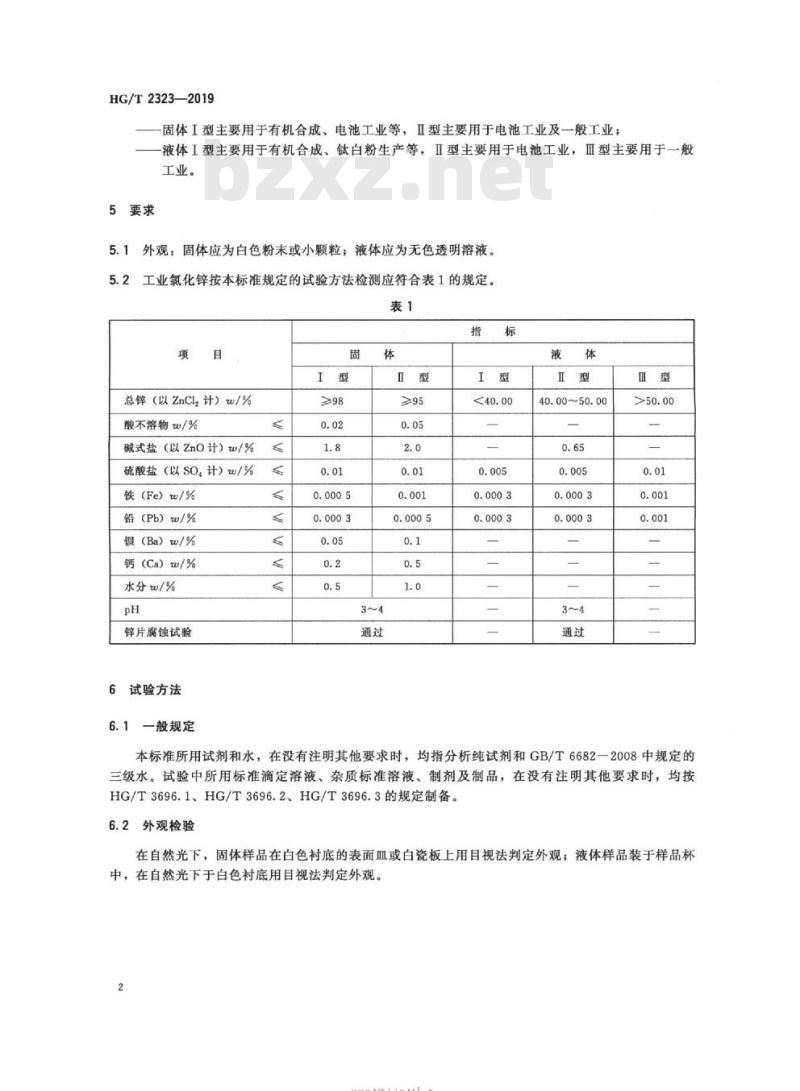
工业氯化锌按本标准规定的试验方法检测应符合表1的规定。表1
总锌(以ZnClz计)w/%
酸不溶物w/%
碱式盐(以Zno计)w/%
硫酸盐(以SO,计)w/%
铁(Fe)w/%
铅(Pb)w/%
(Ba)w/%
钙(Ca)w/%
水分w/%
锌片腐蚀试验
试验方法
6.1一般规定
40.00~50.00
本标准所用试剂和水,在没有注明其他要求时,均指分析纯试剂和GB/T6682一2008中规定的三级水。试验中所用标准滴定溶液、杂质标准溶液、制剂及制品,在没有注明其他要求时,均按HG/T3696.1、HG/T3696.2、HG/T3696.3的规定制备。6.2外观检验
在自然光下,固体样品在白色衬底的表面皿或白瓷板上用目视法判定外观;液体样品装于样品杯中,在自然光下于白色衬底用目视法判定外观。2
-KaeerKAca-
6.3总锌含量的测定
6.3.1亚铁氰化钾法(仲裁法)
6.3.1.1原理
HG/T2323—2019
在酸性条件下,以二苯胺为指示液,用亚铁氰化钾标准滴定溶液滴定至溶液由蓝紫色变为黄绿色为终点。
6.3.1.2试剂或材料
6.3.1.2.1基准氧化锌。
6.3.1.2.2
2盐酸溶液:1十1。
3硫酸溶液:1十3。
6.3.1.2.3
6.3.1.2.4氨水溶液:1+1。
硫酸铵溶液:250g/L。
6.3.1.2.5
6.3.1.2.6
6二苯胺指示液:10g/L。
称取1.0g二苯胺,在搅拌下溶解于100mL浓硫酸中。6.3.1.2.7亚铁氰化钾标准滴定溶液:c[K,Fe(CN),]~0.05mol/L。按照下列步骤制备(保存时间不超过2个月):a)配制:称取21.6g亚铁氰化钾、0.6g铁氰化钾及0.2g无水碳酸钠于400mL烧杯中,加水溶解后,用水稀释至1000mL,置于棕色瓶中,放置1周后,用玻璃砂埚(滤板孔径为5μm~15μm)过滤,保存于棕色瓶中。如溶液中有沉淀产生,应重新过滤。b)标定:称取约1.7g于800℃灼烧至质量恒定的基准氧化锌,精确至0.0002g。用少许水湿润,加盐酸溶液溶解,移人250mL容量瓶中,用水稀释至刻度,摇匀。移取25mL上述溶液,置于250mL锥形瓶中,加入70mL水。滴加氨水溶液至白色胶状沉淀刚好产生,加入20mL硫酸铵溶液及20mL硫酸溶液,加热至75℃~80℃,用亚铁氰化钾标准滴定溶液滴定。近终点时加入2滴3滴二苯胺指示液。当滴定至溶液的蓝紫色突变至黄绿色,并在30s内不再反复蓝紫色时,即为终点,终点时溶液温度不得低于60℃,试验数据处理:亚铁氰化钾标准滴定溶液的浓度c,数值以mol/L表示,按公式(1)计算:c
mX(25/250)
c=(V/1000)XM
式中:
m一—称取基准氧化锌的质量的数值,单位为克(g);V一滴定时消耗亚铁氰化钾标准滴定溶液的体积的数值,单位为毫升(mL);M氧化锌(号2
ZnO)的摩尔质量的数值,单位为克每摩尔(g/mol)(M=122.07)。6.3.1.3试验步骤
试验溶液A的制备
6.3.1.3.1
在有盖的称量瓶中,迅速称取约3.5g固体试样,或称取适量液体试样(其中所含氯化锌质量约3
-KaeerKAca-
HG/T2323—2019
3.5g),精确至0.0002g。置于250mL烧杯中,加人50mL水及数滴盐酸溶液至溶液清亮,再过量3滴盐酸溶液,移人250mL容量瓶中,用水稀释室刻度,摇匀。此为试验溶液A,用于总锌含量的测定。
6.3.1.3.2试验
移取25mL试验溶液A,置于250mL锥形瓶中,加人70mL水,以下操作按6.3.1.2.7b)所述,从“滴加氨水溶液至白色胶状沉淀刚好产生…….”开始,到“……终点时溶液温度不得低于60℃”为止。
6.3.1.4试验数据处理
总锌含量以氯化锌(ZnCl2)的质量分数wi计,按公式(2)计算:VeMX10-3
mX(25/250)
式中:
V一滴定试验溶液消耗亚铁氰化钾标准滴定溶液的体积的数值,单位为毫升(mL);c——亚铁氰化钾标准滴定溶液的浓度的准确数值,单位为摩尔每升(mol/L);....(2)
ZnCl2)的摩尔质量的数值,单位为克每摩尔(g/mol)(M=204.42);M-氯化锌
¥(2
m—试料的质量的数值,单位为克(g)。取平行测定结果的算术平均值为测定结果,两次平行测定结果的绝对差值不大于0.2%。6.3.2EDTA滴定法
6.3.2.1原理
在弱碱性条件下,以铬黑T为指示液,用乙二胺四乙酸二钠(EDTA)标准滴定溶液滴定至溶液由紫红色变为蓝色即为终点。6.3.2.2试剂或材料
6.3.2.2.1四水合酒石酸钾钠。
2氨水溶液:1+1。
6.3.2.2.2
6.3.2.2.3氨-氯化铵缓冲溶液:pH~106.3.2.2.4乙二胺四乙酸二钠(EDTA)标准滴定溶液:c(EDTA)~0.1mol/L。6.3.2.2.5铬黑T指示液:5g/L。6.3.2.3试验步骤
移取25mL试验溶液A(见6.3.1.3.1),置于250mL锥形瓶中,加人70mL水,再加人3g四水合酒石酸钾钠,溶解混匀。滴加氨水溶液至白色胶状沉淀刚好产生,加入15mL氨-氯化铵缓冲溶液,滴加3滴7滴铬黑T指示液,用乙二胺四乙酸二钠(EDTA)标准滴定溶液滴定至溶液由紫红色变为蓝色即为终点。
6.3.2.4试验数据处理
总锌含量以氯化锌(ZnClz)的质量分数wi计,按公式(3)计算:4
rKacerkAca-
式中:
VeMX10-3
mX(25/250)×100%
HG/T2323—2019
V—一滴定试验溶液消耗乙二胺四乙酸二钠(EDTA)标准滴定溶液的体积的数值,单位为毫升(mL);
乙二胺四乙酸二钠(EDTA)标准滴定溶液的浓度的准确数值,单位为摩尔每升(mol/L);M——氯化锌(ZnClz)的摩尔质量的数值,单位为克每摩尔(g/mol)(M=136.28);m—试料(见6.3.1.3.1)的质量的数值,单位为克(g)。取平行测定结果的算术平均值为测定结果,两次平行测定结果的绝对差值不大于0.2%。6.4酸不溶物含量的测定
6.4.1原理
固体试样在酸性条件下用水溶解,过滤、洗涤,不溶物在105℃~110℃下烘干至质量恒定。6.4.2试剂或材料
6.4.2.1盐酸溶液:2十1。
6.4.2.2硝酸银溶液:17g/L。
6.4.3仪器设备
6.4.3.1电热恒温干燥箱:温度能控制在105℃~110℃。6.4.3.2玻璃砂甘埚:滤板孔径5μm~15μm。6.4.4试验步骤
称取约20g固体试样,精确至0.01g。置于400mL烧杯中,加入200mL水及2mL盐酸溶液溶解,用已在105℃~110℃下烘于至质量恒定的玻璃砂地埚过滤。用热水洗涤至滤液中不含氯离子(用硝酸银溶液检查)为止。将玻璃砂埚连同不溶物一并移入电热恒温干燥箱中,在105℃~110℃下烘于至质量恒定。
6.4.5试验数据处理
酸不溶物含量的质量分数W2,按公式(4)计算:mi-m2×100%
式中:
玻璃砂埚和不溶物的质量的数值,单位为克(g);玻璃砂埚的质量的数值,单位为克(g);mo
m-—试料的质量的数值,单位为克(g)。取平行测定结果的算术平均值为测定结果,两次平行测定结果的绝对差值不大于0.005%6.5碱式盐含量的测定
6.5.1原理
以甲基橙作指示剂,用盐酸标准滴定溶液滴定。-nKaerKAca-
(4)
HG/T2323—2019
6.5.2试剂或材料
6.5.2.1盐酸标准滴定溶液:c(HCI)~0.5mol/L。6.5.2.2甲基橙指示液:1g/L。
6.5.3试验步骤
在有盖的称量瓶中,迅速称取约20g试样,或称取适量液体试样(其中所含氯化锌质量约20g),精确至0.01g。置于250mL锥形瓶中,加入50mL水和2滴甲基橙指示液,用盐酸标准滴定溶液滴定至溶液呈橙红色透明液体即为终点。6.5.4试验数据处理
碱式盐含量以氧化锌(ZnO)的质量分数w3计,按公式(5)计算:VeM×10-3
式中:
V—滴定试验溶液消耗盐酸标准滴定溶液的体积的数值,单位为毫升(mL);盐酸标准滴定溶液的浓度的准确数值,单位为摩尔每升(mol/L);1
ZnO)的摩尔质量的数值,单位为克每摩尔(g/mol)(M=40.69);M—氧化锌
试料的质量的数值,单位为克(g)。m
(5)
取平行测定结果的算术平均值为测定结果,两次平行测定结果的绝对差值固体试样不大于0.1%、液体试样不大于0.05%。
硫酸盐含量的测定
6.6.1原理
在酸性条件下,用氯化钡与硫酸根离子反应形成悬浊液,与硫酸标准比浊溶液目视比浊。试剂或材料
6.6.2.195%乙醇。
6.6.2.2盐酸溶液:1+1。
6.6.2.3氯化钡溶液:100g/L
6.6.2.4硫酸盐标准溶液:1mL溶液含硫酸盐(以SO,计)0.1mg。移取10.00mL按HG/T3696.2配制的硫酸盐(以SO4计)标准溶液,置于100mL容量瓶中,用水稀释至刻度,摇匀。
6.6.3试验步骤
6.6.3.1试验溶液B的制备
在有盖称量瓶中,迅速称取试样10.00g士0.01g,置于100mL烧杯中,加入40mL水及数滴盐酸溶液至溶液清亮,再过量3滴盐酸溶液,移人100mL容量瓶中,用水稀释至刻度,摇匀,备用。6
-KaeerKAca-
此溶液为试验溶液B,用于硫酸盐含量、铁含量、钡含量的测定,6.6.3.2试验
HG/T2323—2019
移取20mL试验溶液B,置于50mL比色管中,加入1mL盐酸溶液和3mL95%乙醇,再加人5mL氯化钡溶液,用水稀释至刻度,摇匀,放置30min。所呈浊度不得深于标准比浊溶液。标准比浊溶液的制备:移取表2规定体积的硫酸盐标准溶液,与试验溶液B同时同样处理。表2
6.7铁含量的测定
6.7.1原理
I型、I型
I型、Ⅱ型
移取硫酸盐标准溶液体积/mL
在酸性介质中,用过硫酸铵氧化2价铁,加人硫氰酸钾-正丁醇溶液萃取并显色,与标准比色溶液进行目视比色。
6.7.2试剂或材料
6.7.2.1过硫酸铵。
6.7.2.2盐酸溶液:1+1。
6.7.2.3硫氰酸钾-正丁醇溶液:10g/L。称取10g硫氰酸钾,用10mL水溶解,加热至25℃~30℃,加正丁醇稀释至1000mL,充分振摇至澄清。
6.7.2.4铁标准溶液:1mL溶液含铁(Fe)0.01mg。移取1.00mL按HG/T3696.2配制的铁标准溶液,置于100mL容量瓶中,用水稀释至刻度,摇勾。此溶液现用现配。
6.7.3试验步骤
移取20mL试验溶液B(见6.6.3.1),置于50mL比色管中,加人10mL水、1mL盐酸溶液、0.03g过硫酸铵,摇匀。加入15mL硫氰酸钾-正丁醇溶液,振摇30s。醇层所呈现的红色不得深于标准比色溶液。
标准比色溶液的制备:移取表3规定体积的铁标准溶液,与试验溶液B同时同样处理。7
-KaeerKAca-
HG/T2323—2019
铅含量的测定
6.8.1原理
I型、Ⅱ型
按GB/T23768—2009第4章。
6.8.2试剂或材料
6.8.2.1三氯甲烷。
6.8.2.2盐酸。
6.8.2.3硝酸。
6.8.2.4氢氧化钠溶液:250g/L。表3
6.8.2.5吡略烷二硫代甲酸铵溶液(APDC):20g/L。移取铁标准溶液体积/mL
溶解2.0g吡咯烷二硫代甲酸铵(APDC)于100mL水中,用前过滤沉淀物。6.8.2.6铅标准溶液:1mL溶液含铅(Pb)0.01mg。移取1.00mL按HG/T3696.2配制的铅标准溶液,置于100mL容量瓶中,用水稀释至刻度,摇匀。此溶液现用现配。
6.8.2.7二级水:符合GB/T6682—2008的规定。6.8.3仪器设备
原子吸收分光光度计:配有铅空心阴极灯。6.8.4试验步骤
6.8.4.1工作曲线的绘制
分别移取0.00mL、0.50mL、1.00mL、1.50mL铅标准溶液(相当0.0μg、5.0μg、10.0μg、15.0μg铅)于250mL分液漏斗中,分别加人1mL盐酸,盖上表面皿,加热煮沸5min。冷却,用二级水稀释至100mL。用氢氧化钠液调节溶液pH值为1.0~1.5(用精密pH试纸检验)。将此溶液转移至500mL分液漏斗中,用二级水稀释至约200mL。加入2mL吡咯烷二硫代氨基甲酸铵(APDC)溶液,混合。用三氯甲烷萃取2次,每次加入20mL,收集萃取液(即有机相)于50mL烧杯中,在蒸汽浴上蒸发至干(此操作必须在通风橱中进行)。于残渣中加人3mL硝酸,继续蒸发至近干。加入0.5mL硝酸和10mL二级水,加热直至溶液体积为3mL~5mL。转移至10mL容量瓶中,用二级水稀释至刻度,播匀。选用空气-乙炔火焰,于波长283.3nm处,以空白试验溶液调8
rrKaeerKAca-
HG/T2323—2019
零,测定各萃取后的铅标准溶液的吸光度。以铅的质量为横坐标、对应的吸光度为纵坐标,绘制工作曲线。免费标准下载网bzxz
6.8.4.2试验
称取约3g(固体、液体I型、Ⅱ型)试样或1g(液体Ⅲ型)试样,精确至0.0002g。置于150mL烧杯中,加人30mL二级水,再加人1mL盐酸。以下操作同6.8.4.1中“盖上表面血,加热煮沸5min,冷却,用二级水稀释至100mL…转移至10mL容量瓶中,用二级水稀释至刻度,摇匀”。在相同仪器条件下测定萃取后的试验溶液的吸光度,从工作曲线上查出试验溶液中铅的质量。同时进行空白试验。空白试验溶液除不加试样外,其他加入试剂的种类和量与试验溶液相同。6.8.5试验数据处理
铅含量以铅(Pb)的质量分数w4计,按公式(6)计算:@×(10×10-)
×100%
式中:
-从工作曲线上查出的试验溶液中铅的质量的数值,单位为微克每毫升(μg/mL);p
试料的质量的数值,单位为克(g))。m
取平行测定结果的算术平均值为测定结果,在重复性条件下两次独立测定结果铅含量的绝对差值不大于算数平均值的10%。
6.9钡含量的测定
6.9.1原理
在酸性条件下,用硫酸根与钡离子反应形成悬浊液,与硫酸钡标准比浊溶液目视比浊。6.9.2试剂或材料
6.9.2.195%乙醇。
6.9.2.2硫酸溶液:1+3。
6.9.2.3锁标准溶液:1mL溶液含锁(Ba)0.1mg。移取10.00mL按HG/T3696.2配制的锁标准溶液,置于100mL容量瓶中,用水稀释至刻度,摇匀。
6.9.3试验步骤
用移液管移取5mL试验溶液B(见6.6.3.1)于50mL比色管中,加入3mL95%乙醇和1mL硫酸溶液,用水稀释至刻度,摇勾,放置30min。所呈浊度不得深于标准比浊溶液。标准比浊溶液的制备:移取表4规定体积的钡标准溶液,与试验溶液B同时同样处理。表4
-KaeerKAca-
移取锁标准溶液体积/mL
HG/T2323—2019
6.10钙含量的测定
6.10.1原理
试样用水溶解,在原子吸收分光光度计上,于波长422.7nm处测定试样中钙含量。6.10.2试剂或材料
6.10.2.1氟化锶:100g/L。
6.10.2.2盐酸溶液:1十99。
6.10.2.3钙标准溶液:1mL溶液含钙(Ca)0.01mg。用移液管移取1.00mL按HG/T3696.2配制的钙标准溶液,置于100mL容量瓶中,用二级水稀释至刻度,摇匀。
6.10.2.4二级水:符合GB/T6682—2008中的规定。6.10.3仪器设备
原子吸收分光光度计:配有钙空心阴极灯。6.10.4试验步骤
6.10.4.1工作曲线的绘制
在4个100mL容量瓶中,分别加入0.0mL、5.0mL、10.0mL、15.0mL钙标准溶液,再加入1mL氯化锶溶液,用盐酸溶液稀释至刻度,摇匀。在原子吸收分光光度计上,于波长422.7nm处,用空气-乙炔火焰,选择最佳仪器工作条件,以二级水调零,测定其吸光度。以钙的质量(mg)为横坐标、对应的吸光度为纵坐标,绘制工作曲线。6.10.4.2测定
称取约3g试样,精确至0.0002g。置于100mL烧杯中,加入20mL盐酸溶液溶解后,用慢速滤纸过滤,滤液全部转移至100mL容量瓶中,用盐酸溶液定容。移取1mL该溶液至100mL容量瓶中,加人1mL氯化锶溶液,用盐酸溶液稀释至刻度,摇勾。在原子吸收分光光度计上,于波长422.7nm处,用空气-乙火焰,测定试验溶液的吸光度,根据吸光度从工作曲线上查得相应的钙的质量。
同时同样做空白试验。空白试验溶液除不加试样外,其他加入试剂的种类和量与试验溶液相同。6.10.5试验数据处理
钙含量以钙(Ca)的质量分数ws计,按公式(7)计算:(m-m。)X10-3
-×100%
m×(1/100)
式中:
m1—一从工作曲线上查出的试验溶液中钙的质量的数值,单位为毫克(mg);从工作曲线上查出的空白试验溶液中钙的质量的数值,单位为毫克(mg);mo
试料的质量的数值,单位为克(g)。-KaeerKAca-
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。






 ✕
✕