HG 3621-1999
基本信息
标准号: HG 3621-1999
中文名称:克百威原药
标准类别:化工行业标准(HG)
标准状态:现行
出版语种:简体中文
下载格式:.zip .pdf
下载大小:213804
相关标签: 百威

标准分类号
关联标准
出版信息
相关单位信息
标准简介
HG 3621-1999.Carbofuran Technical.
1范圈
HG 3621规定了克百威原药的要求、试验方法以及标志、标签、包装、贮运。
HG 3621适用于克百威及其生产中产生的杂质组成的克百威原药。
2引用标准
下列标准所包含的条文,通过在本标准中引用而构成为本标准的条文。本标准出版时,所示版本均为有效。所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。
GB 190-1990危险货物包装标志
GB/T 601-1988化学试剂滴定分析(容量分析)用标准溶液的制备
GB/T 1250-1989极限数值的表示法和判定方法
GB/T 1600-1979(1989)农药水分测定方法
GB/T 1604-1995商品农药验收规则
GB/T 1605-1979(1989)商品农药采样方法
GB 3796-1983农药包装通则
3要求
3.1外观:白色或灰白、浅黄色结晶,无可见外来杂质。
3.2克百威原药应符合表1要求。
4试验方法
4.1抽样
按照GB/T 1605-1979(1989)中“原药采样”方法进行,用随机数表法确定抽样包装件数。最终抽样量应不少于250g。
4.2鉴别试验
本鉴别试验可与克百威含量的测定同时进行。在相同的高效液相色谱(HPLC)操作条件下,试样溶液某一色谱峰保留时间与标样溶液克百威色谱峰的保留时间的相对差值应在1.5%以内。
4.3克百威含量测定
4.3.1方法提要
试样用含有苯乙酮作为内标物的甲醇溶解,以甲醇十水为流动相,使用以C18键合固定相为填充物的不锈钢柱和紫外检测器,对试样中克百威进行高效液相色谱分离和测定。
4.3.2试剂和溶液
甲醇:液相色谱纯,经0.5μm滤膜过滤。
水:二次重蒸水,经0.5μm滤膜过滤。
1范圈
HG 3621规定了克百威原药的要求、试验方法以及标志、标签、包装、贮运。
HG 3621适用于克百威及其生产中产生的杂质组成的克百威原药。
2引用标准
下列标准所包含的条文,通过在本标准中引用而构成为本标准的条文。本标准出版时,所示版本均为有效。所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。
GB 190-1990危险货物包装标志
GB/T 601-1988化学试剂滴定分析(容量分析)用标准溶液的制备
GB/T 1250-1989极限数值的表示法和判定方法
GB/T 1600-1979(1989)农药水分测定方法
GB/T 1604-1995商品农药验收规则
GB/T 1605-1979(1989)商品农药采样方法
GB 3796-1983农药包装通则
3要求
3.1外观:白色或灰白、浅黄色结晶,无可见外来杂质。
3.2克百威原药应符合表1要求。
4试验方法
4.1抽样
按照GB/T 1605-1979(1989)中“原药采样”方法进行,用随机数表法确定抽样包装件数。最终抽样量应不少于250g。
4.2鉴别试验
本鉴别试验可与克百威含量的测定同时进行。在相同的高效液相色谱(HPLC)操作条件下,试样溶液某一色谱峰保留时间与标样溶液克百威色谱峰的保留时间的相对差值应在1.5%以内。
4.3克百威含量测定
4.3.1方法提要
试样用含有苯乙酮作为内标物的甲醇溶解,以甲醇十水为流动相,使用以C18键合固定相为填充物的不锈钢柱和紫外检测器,对试样中克百威进行高效液相色谱分离和测定。
4.3.2试剂和溶液
甲醇:液相色谱纯,经0.5μm滤膜过滤。
水:二次重蒸水,经0.5μm滤膜过滤。
标准图片预览



标准内容
HG 3621—1999
本标准的产品质量控制项目是以中华人民共和国化工行业标准HG/T2467.11996《农药原药产品标准编写规范》为依据确定的。本标准有效成分的试验方法等同采用国际农药分析合作理事会(CIPAC)方法一高效液相色谱
本标准由中华人民共和国原化学工业部技术监督司提出。本标准由化学工业部沈阳化工研究院归口。本标准主要起草单位:湖南化工研究院。本标准参加起草单位:湖南海利化工股份有限公司试验工场、山东华阳农药化工集团公司、江苏铜山农药总厂。
本标准主要起草人:黄湘云、周志纯、刘志娟、刘自友、郑静宇、邵珠民。1198
中华人民共和国化工行业标准
克百威原药
Carbofuran Technical
克百威其他名称、结构式和基本物化参数如下:ISO通用名称:Carbofuran
CIPAC数字代号:276
化学名称:2,3-二氨-2,2-二甲基苯并呋喃-7-基N-甲基氨基甲酸酯结构式:
CO—NH—CH3
实验式:C12H1sNO3
相对分子质量:221.3(按1993年国际相对原子质量计)生物活性:杀虫
熔点(℃):151~152
蒸气压(33℃):2.7MPa
HG 3621-1999
溶解度(g/L,25℃):水中0.7;丙酮中150,二甲基甲酰氨中270;乙腈中140;环己酮中90,苯中40;乙醇中40;微溶于石油醚和二甲苯。稳定性:180℃开始分解,在酸性介质中较稳定,碱性中不稳定,温度和碱性对水解速度的影响较大。1范圈
本标准规定了克百威原药的要求、试验方法以及标志、标签、包装、贮运。本标推适用于克百威及其生产中产生的杂质组成的克百威原药。2引用标准
下列标准所包含的条文,通过在本标准中引用而构成为本标准的条文。本标准出版时,所示版本均为有效。所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。GB190—1990危险货物包装标志
GB/T601一1988化学试剂滴定分析(容量分析)用标准溶液的制备GB/T1250-1989极限数值的表示法和判定方法GB/T1600-1979(1989)农药水分测定方法GB/T1604-1995商品农药验收规则GB/T1605—1979(1989)商品农药采样方法GB3796-1983农药包装通则
国家石油和化学工业局1999-06-16批准2000-06-01实施
3要求
HG 3621---1999
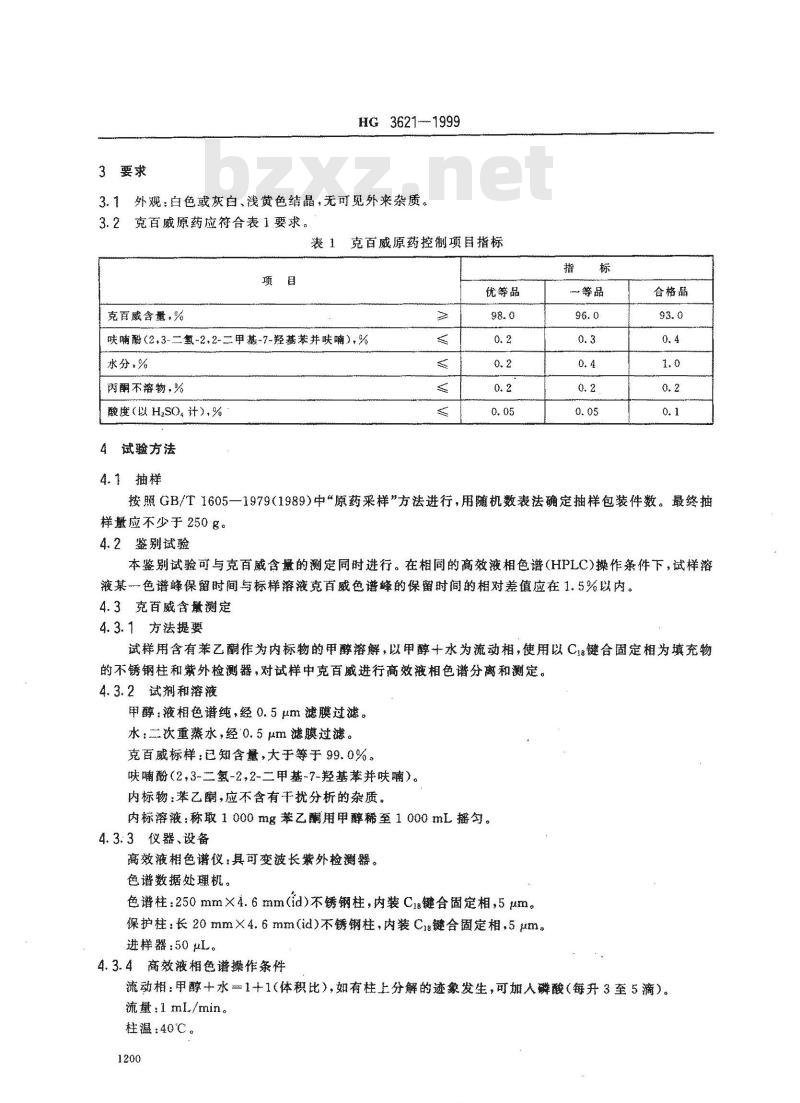
3.1外观:白色或灰白、浅黄色结晶,无可见外来杂质。3.2克百威原药应符合表1要求。表1克百威原药控制项目指标
优等品
克百威含量,%
呋哺酚(2,3-二氢-2,2-二甲基-7-羟基苯并呋哺),%水分,%
丙酮不溶物,%
酸度(以H,SO4计),%
4试验方法
4.1抽样
合格品
按照GB/T1605一1979(1989)中“原药采样*方法进行,用随机数表法确定抽样包装件数。最终抽样量应不少于250g。
4.2鉴别试验
本鉴别试验可与克百威含量的测定同时进行。在相同的高效液相色谱(HPLC)操作条件下,试样溶液某色谱蜂保留时间与标样溶液克百威色谱蜂的保留时间的相对差值应在1.5%以内。4.3克百威含测定
4.3.1方法提要
试样用含有苯艺酮作为内标物的甲醇溶解,以甲醇十水为流动相,使用以C键合固庭相为填充物的不锈钢柱和紫外检测器,对试样中克百威进行高效液相色谱分离和测定。4.3.2试剂和浴液
甲醇:液相色谱纯,经0.5um滤膜过滤。水二次重蒸水,经0.5μm滤膜过滤。克百威标样:已知含量,大于等于99.0%。峡喃酚(2,3-二氢-2,2-二甲基-7-羟基苯并呋喃)。内标物:苯乙酮,应不含有干扰分析的杂质。内标溶液:称取1000mg苯乙酮用甲醇稀至1000mL摇匀。4.3.3仪器、设备
高效液相色谱仪:具可变波长紫外检测器。色谱数据处理机。
色谱柱:250mm×4.6mm(id)不锈钢柱,内装Crs键合固定相,5μum。保护柱:长20mm×4.6mm(id)不锈钢柱,内装C键合固定相,5um进样器:50u。
4.3.4高效液样色谱操作条件
流动相:甲醇十水一1十1(体积比),如有柱上分解的迹象发生,可加人磷酸(每并3至5滴)。流:1 mL/min。
桂溢:40℃。
检测波长:280nm。
进样体积:10 μL。
检测器灵敏度:满刻度0.2吸光度。HG 3621—1999
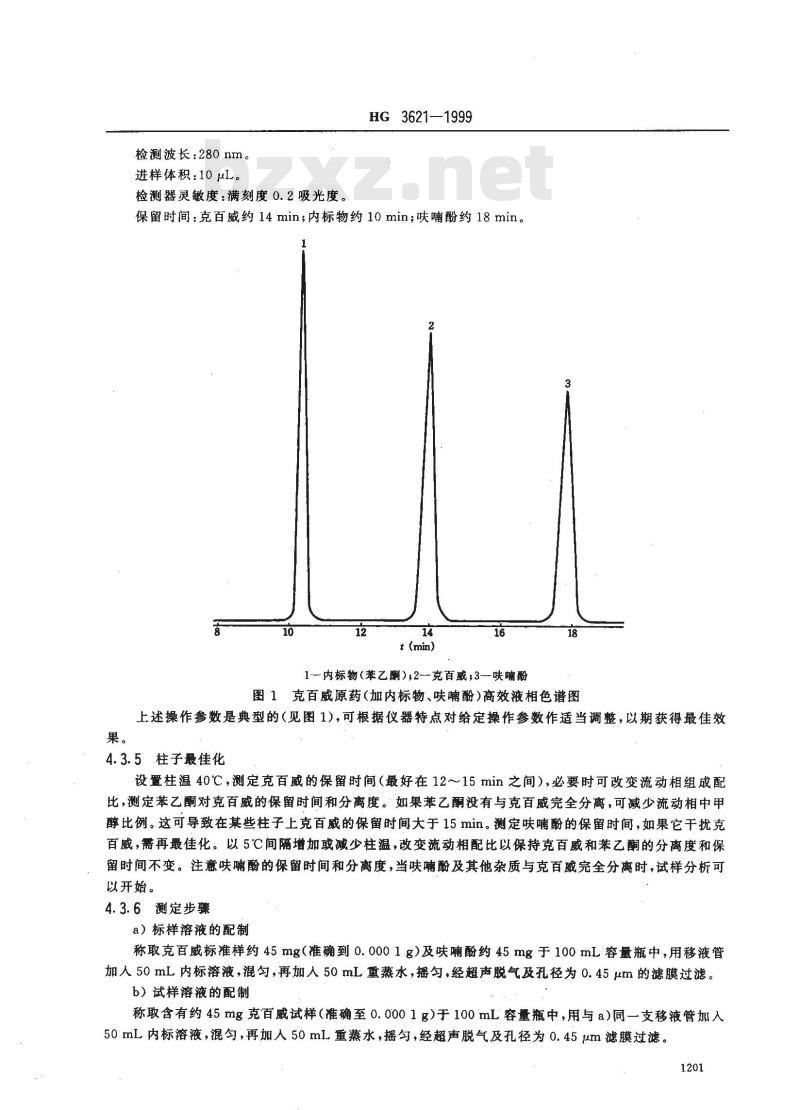
保留时间:克百威约14min;内标物约10min;呋酚约18min。2
t (min)
1——内标物(苯乙酮),2-克百威;3-呋嘀酚3
图1克百威原药(加内标物、呋喃酚)高效液相色谱图上述操作参数是典型的(见图1),可根据仪器特点对给定操作参数作适当调整,以期获得最佳效4.3.5柱子最佳化
设置柱温40℃,测定克百威的保留时间(最好在12~15min之间),必要时可改变流动相组成配比,测定苯乙酮对克百威的保留时间和分离度。如果苯乙酮没有与克百威完全分离,可减少流动相中甲醇比例。这可导致在某些柱子上克百威的保留时间大于15min。测定呋嘀酚的保留时间,如果它干扰克百威,需再最佳化。以5℃间隔增加或减少柱温,改变流动相配比以保持克百威和苯乙酮的分离度和保留时间不变。注意呋酚的保留时间和分离度,当呋酚及其他杂质与克百威完全分离时,试样分析可以开始。
4.3.6测定步骤
a)标样溶液的配制
称取克百威标准样约 45mg(准确到0.0001g)及呋喃酚约45mg于100mL容量瓶中,用移液管加人50mL内标溶液,混匀,再加人50mL重蒸水,摇匀,经超声脱气及孔径为0.45μm的滤膜过滤。b)试样溶液的配制
称取含有约45mg克百威试样(准确至0.0001g)于100mL容量瓶中,用与a)同一支移液管加入50mL内标溶液,混勾,再加人50mL重蒸水,摇匀,经超声脱气及孔径为0.45μm滤膜过滤。1201
c)测定
HG 3621--1999
在上述操作条件下,待仪器基线稳定后,重复注入标准溶液,计算每次进样的相对响应值,待相邻两针的相对响应值变化小于1%,按照标样溶液、样品溶液,样品溶液、标样溶液的顺序进行测定。4.3.7计算
将测得的两针试样溶液以及试样前后两针标样溶液中克百威与内标物峰面积之比,分别进行平均。以质量百分数表示的克百威含量(X,)按式(1)计算:ram,P
一标样溶液中,克百威与内标物峰面积比的平均值;式中:ri—
试样溶液中,克百威与内标物蜂面积比的平均值;m1———克百威标样的质量,g;
一试样的质量,g;
标样中克百威的质量百分含量。4.3.8允许差
两次平行测定结果之差,应不大于1.2%。4.4呋哺酚含量的测定
4.4.1方法提要
呋喃酚在酸性条件下与亚硝酸钠进行反应生成亚硝基呋喃酚,加人甲胺溶液后形成黄色的醌型结构化合物,于波长436nm处进行分光光度测定。4.4.2试剂和溶液
盐酸。
亚硝酸钠。下载标准就来标准下载网
丙酮。
甲胺水溶液:化学纯(也可用气态甲胺经蒸馏水吸收后,测定含量后使用)。盐酸溶液:c(HCI)=0. 1 mol/L。甲胺水溶液:25g/L,用盐酸标准溶液滴定测其精确浓度。亚硝酸钠水溶液:1.0mol/L,称取1.7g亚硝酸钠置于25mL容量瓶中,用蒸馏水稀至刻度摇匀(当天使用)。
呋喃酚标准溶液:称取含量大于等于98.0%呋喃酚约40mg(准至0.0002g)于50mL容量瓶中,加丙酮定容,摇勾,取此液2.5mL于25mL容量瓶中,加丙酮定容,摇匀,此液呋酚浓度约为0.08mg/mL。
4.4.3仪器、设备
分光光度计。
恒温水溶:控制精度土0.5℃。
刻度比色管:25mL。
容量瓶:25、50、250mL。
移液管:1、2 mL刻度移液管。
4.4.4测定步骤
称取克百威原药0.01~0.02g(准确至0.0002g),置于25mL刻度比色管中,加人2mL丙酮使之溶解。准确加人0.1mol/L盐酸溶液1.5mL,摇匀,沿比色管壁加人1.0moL亚硝酸钠2mL,准确振摇1min后置于40℃恒温水浴中加热20min,取出比色管,冷却至室温,再用1mL移液管加人25g/L甲胺水溶液0.5mL,加水稀释至10mL,摇匀。溶液置于1cm比色血中,在波长436nm处测其吸光度。同时,准确吸收呋喃酚标准溶液1mL,置于25mL比色管中,补加1mL丙酮。以下操作与试样相同。1202
4.4.5计算
HG 3621—1999
以质量百分数表示的游离酚(以呋喃酚计)含量(X,)按式(2)计算。X,
式中:mi-
标准溶液呋喃酚的质量,mg;
样品溶液的质量,mg
A-标样溶液的吸光度;
A试样溶液的吸光度。
4.4.6允许差
两次平行测定的差值不应大于0.02%。4.5水分测定
按GB/T1600-1979(1989)中的卡尔·费休永停电位终点法进行。4.6丙酮中固体不溶物的测定
4.6.1试剂和溶液
丙酮:经无水硫酸钠干燥。
4.6.2仪器、设备
锥形烧瓶:具玻璃磨口接头,250mL。回流冷凝器:与锥形烧瓶配套。砂芯坦埚;3#
烘箱。
4.6.3试验步骤
(2)
称取约10g试样(精确至0.01g),放入锥形瓶中,加人50mL丙酮,加热回流至所有可溶物溶解。用已质量恒定的埚过滤溶液,再用60mL丙酮分数次洗涤锥形瓶、埚,以确保固形物全部移人增埚,壁等处可溶物全部洗净。将埚置于110℃烘箱中干燥30min,取出于干燥器中冷却至室温,称量至质量恒定。
以质百分数表示的两酮中固体不溶物的含量(X3)按式(3)计算:m - mo × 100
式中:mi-
质量恒定后砂芯地埚与不溶物的质量,名;砂芯埚质量,g
m——试样质量,g。
4.7酸度的测定
4.7.1试剂和溶液
丙酮。
氢氧化钠标准滴定溶液:c(NaOH)0.02mol/L,按GB/T601中规定方法配制。配合指示液::2g/L甲基红乙醇液2 mL与2g/L溴甲酚绿乙醇溶液10 mL混合。4.7.2测定步骤
·(3)
称取8g试样(准确至0.0001g)置于250mL锥形瓶中,加入100mL丙酮,振摇使试样溶解,滴加0.6mL指示液,用氧氧化钠标准滴定溶液滴定至由黄色变为蓝绿色为终点。同时作空白测定。
以质量百分数表示的试样的酸度(X)(以H2SO4计)按式(4)计算:c(V/- Vo) × 0. 049 × 100*
(4)
HG36211999
一氢化钠标溶液的实际浓度,mol/,式中:
V,滴定试样溶液消耗氢氧化钠标准溶液的体积,mL,V。滴定空白溶液消耗氢氧化钠标准溶液的体积,mLm
—一试样的质量·,
0.049---与1.00mL氢氧化钠标准溶液[c(NaOH)=1.000mol/L]相当的以克表示的硫酸的质量。4.8产品检验与验收
产品的检验与验收应符合GB/T1604的有关规定,并在到货之日起三个月内验收。极限数值的处理采用修约值比较法。
5标惠、标签、包装、购运
5.1克百威原药的标志、标签和包装应符合GB3796中的有关规定。作为商品流通的原药,还应有商标和生产许可证号。
5.2克百威原药内用一层塑料薄膜袋包装,外套用業丙烯编织袋,然后封袋置于铁桶中,每桶净含量(100±0.2)kg。
5.3根据用户要求或订货协议,可以采用其他形式的包装,但要符合GB3796中有关规定。5.4包装件应存放在通风、干燥的库房中。5.5贮运时,严防潮湿和日,不得与食物、种子、饲料混放,避免与皮肤、眼睛接触,防止由口吸人。5.6安全
克百威属高毒氨基甲酸酯类杀盅剂,吞磁或吸人均有毒,还可通过皮肤渗入,故使用本品应穿防护服、带防护手套,皮肤或身体裸露部位接触本品后,应及时用肥和水洗净。如发生中毒现象,轻者可肌肉注射阿托品解毒,必要时应请医生诊治。1204
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
本标准的产品质量控制项目是以中华人民共和国化工行业标准HG/T2467.11996《农药原药产品标准编写规范》为依据确定的。本标准有效成分的试验方法等同采用国际农药分析合作理事会(CIPAC)方法一高效液相色谱
本标准由中华人民共和国原化学工业部技术监督司提出。本标准由化学工业部沈阳化工研究院归口。本标准主要起草单位:湖南化工研究院。本标准参加起草单位:湖南海利化工股份有限公司试验工场、山东华阳农药化工集团公司、江苏铜山农药总厂。
本标准主要起草人:黄湘云、周志纯、刘志娟、刘自友、郑静宇、邵珠民。1198
中华人民共和国化工行业标准
克百威原药
Carbofuran Technical
克百威其他名称、结构式和基本物化参数如下:ISO通用名称:Carbofuran
CIPAC数字代号:276
化学名称:2,3-二氨-2,2-二甲基苯并呋喃-7-基N-甲基氨基甲酸酯结构式:
CO—NH—CH3
实验式:C12H1sNO3
相对分子质量:221.3(按1993年国际相对原子质量计)生物活性:杀虫
熔点(℃):151~152
蒸气压(33℃):2.7MPa
HG 3621-1999
溶解度(g/L,25℃):水中0.7;丙酮中150,二甲基甲酰氨中270;乙腈中140;环己酮中90,苯中40;乙醇中40;微溶于石油醚和二甲苯。稳定性:180℃开始分解,在酸性介质中较稳定,碱性中不稳定,温度和碱性对水解速度的影响较大。1范圈
本标准规定了克百威原药的要求、试验方法以及标志、标签、包装、贮运。本标推适用于克百威及其生产中产生的杂质组成的克百威原药。2引用标准
下列标准所包含的条文,通过在本标准中引用而构成为本标准的条文。本标准出版时,所示版本均为有效。所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。GB190—1990危险货物包装标志
GB/T601一1988化学试剂滴定分析(容量分析)用标准溶液的制备GB/T1250-1989极限数值的表示法和判定方法GB/T1600-1979(1989)农药水分测定方法GB/T1604-1995商品农药验收规则GB/T1605—1979(1989)商品农药采样方法GB3796-1983农药包装通则
国家石油和化学工业局1999-06-16批准2000-06-01实施
3要求
HG 3621---1999
3.1外观:白色或灰白、浅黄色结晶,无可见外来杂质。3.2克百威原药应符合表1要求。表1克百威原药控制项目指标
优等品
克百威含量,%
呋哺酚(2,3-二氢-2,2-二甲基-7-羟基苯并呋哺),%水分,%
丙酮不溶物,%
酸度(以H,SO4计),%
4试验方法
4.1抽样
合格品
按照GB/T1605一1979(1989)中“原药采样*方法进行,用随机数表法确定抽样包装件数。最终抽样量应不少于250g。
4.2鉴别试验
本鉴别试验可与克百威含量的测定同时进行。在相同的高效液相色谱(HPLC)操作条件下,试样溶液某色谱蜂保留时间与标样溶液克百威色谱蜂的保留时间的相对差值应在1.5%以内。4.3克百威含测定
4.3.1方法提要
试样用含有苯艺酮作为内标物的甲醇溶解,以甲醇十水为流动相,使用以C键合固庭相为填充物的不锈钢柱和紫外检测器,对试样中克百威进行高效液相色谱分离和测定。4.3.2试剂和浴液
甲醇:液相色谱纯,经0.5um滤膜过滤。水二次重蒸水,经0.5μm滤膜过滤。克百威标样:已知含量,大于等于99.0%。峡喃酚(2,3-二氢-2,2-二甲基-7-羟基苯并呋喃)。内标物:苯乙酮,应不含有干扰分析的杂质。内标溶液:称取1000mg苯乙酮用甲醇稀至1000mL摇匀。4.3.3仪器、设备
高效液相色谱仪:具可变波长紫外检测器。色谱数据处理机。
色谱柱:250mm×4.6mm(id)不锈钢柱,内装Crs键合固定相,5μum。保护柱:长20mm×4.6mm(id)不锈钢柱,内装C键合固定相,5um进样器:50u。
4.3.4高效液样色谱操作条件
流动相:甲醇十水一1十1(体积比),如有柱上分解的迹象发生,可加人磷酸(每并3至5滴)。流:1 mL/min。
桂溢:40℃。
检测波长:280nm。
进样体积:10 μL。
检测器灵敏度:满刻度0.2吸光度。HG 3621—1999
保留时间:克百威约14min;内标物约10min;呋酚约18min。2
t (min)
1——内标物(苯乙酮),2-克百威;3-呋嘀酚3
图1克百威原药(加内标物、呋喃酚)高效液相色谱图上述操作参数是典型的(见图1),可根据仪器特点对给定操作参数作适当调整,以期获得最佳效4.3.5柱子最佳化
设置柱温40℃,测定克百威的保留时间(最好在12~15min之间),必要时可改变流动相组成配比,测定苯乙酮对克百威的保留时间和分离度。如果苯乙酮没有与克百威完全分离,可减少流动相中甲醇比例。这可导致在某些柱子上克百威的保留时间大于15min。测定呋嘀酚的保留时间,如果它干扰克百威,需再最佳化。以5℃间隔增加或减少柱温,改变流动相配比以保持克百威和苯乙酮的分离度和保留时间不变。注意呋酚的保留时间和分离度,当呋酚及其他杂质与克百威完全分离时,试样分析可以开始。
4.3.6测定步骤
a)标样溶液的配制
称取克百威标准样约 45mg(准确到0.0001g)及呋喃酚约45mg于100mL容量瓶中,用移液管加人50mL内标溶液,混匀,再加人50mL重蒸水,摇匀,经超声脱气及孔径为0.45μm的滤膜过滤。b)试样溶液的配制
称取含有约45mg克百威试样(准确至0.0001g)于100mL容量瓶中,用与a)同一支移液管加入50mL内标溶液,混勾,再加人50mL重蒸水,摇匀,经超声脱气及孔径为0.45μm滤膜过滤。1201
c)测定
HG 3621--1999
在上述操作条件下,待仪器基线稳定后,重复注入标准溶液,计算每次进样的相对响应值,待相邻两针的相对响应值变化小于1%,按照标样溶液、样品溶液,样品溶液、标样溶液的顺序进行测定。4.3.7计算
将测得的两针试样溶液以及试样前后两针标样溶液中克百威与内标物峰面积之比,分别进行平均。以质量百分数表示的克百威含量(X,)按式(1)计算:ram,P
一标样溶液中,克百威与内标物峰面积比的平均值;式中:ri—
试样溶液中,克百威与内标物蜂面积比的平均值;m1———克百威标样的质量,g;
一试样的质量,g;
标样中克百威的质量百分含量。4.3.8允许差
两次平行测定结果之差,应不大于1.2%。4.4呋哺酚含量的测定
4.4.1方法提要
呋喃酚在酸性条件下与亚硝酸钠进行反应生成亚硝基呋喃酚,加人甲胺溶液后形成黄色的醌型结构化合物,于波长436nm处进行分光光度测定。4.4.2试剂和溶液
盐酸。
亚硝酸钠。下载标准就来标准下载网
丙酮。
甲胺水溶液:化学纯(也可用气态甲胺经蒸馏水吸收后,测定含量后使用)。盐酸溶液:c(HCI)=0. 1 mol/L。甲胺水溶液:25g/L,用盐酸标准溶液滴定测其精确浓度。亚硝酸钠水溶液:1.0mol/L,称取1.7g亚硝酸钠置于25mL容量瓶中,用蒸馏水稀至刻度摇匀(当天使用)。
呋喃酚标准溶液:称取含量大于等于98.0%呋喃酚约40mg(准至0.0002g)于50mL容量瓶中,加丙酮定容,摇勾,取此液2.5mL于25mL容量瓶中,加丙酮定容,摇匀,此液呋酚浓度约为0.08mg/mL。
4.4.3仪器、设备
分光光度计。
恒温水溶:控制精度土0.5℃。
刻度比色管:25mL。
容量瓶:25、50、250mL。
移液管:1、2 mL刻度移液管。
4.4.4测定步骤
称取克百威原药0.01~0.02g(准确至0.0002g),置于25mL刻度比色管中,加人2mL丙酮使之溶解。准确加人0.1mol/L盐酸溶液1.5mL,摇匀,沿比色管壁加人1.0moL亚硝酸钠2mL,准确振摇1min后置于40℃恒温水浴中加热20min,取出比色管,冷却至室温,再用1mL移液管加人25g/L甲胺水溶液0.5mL,加水稀释至10mL,摇匀。溶液置于1cm比色血中,在波长436nm处测其吸光度。同时,准确吸收呋喃酚标准溶液1mL,置于25mL比色管中,补加1mL丙酮。以下操作与试样相同。1202
4.4.5计算
HG 3621—1999
以质量百分数表示的游离酚(以呋喃酚计)含量(X,)按式(2)计算。X,
式中:mi-
标准溶液呋喃酚的质量,mg;
样品溶液的质量,mg
A-标样溶液的吸光度;
A试样溶液的吸光度。
4.4.6允许差
两次平行测定的差值不应大于0.02%。4.5水分测定
按GB/T1600-1979(1989)中的卡尔·费休永停电位终点法进行。4.6丙酮中固体不溶物的测定
4.6.1试剂和溶液
丙酮:经无水硫酸钠干燥。
4.6.2仪器、设备
锥形烧瓶:具玻璃磨口接头,250mL。回流冷凝器:与锥形烧瓶配套。砂芯坦埚;3#
烘箱。
4.6.3试验步骤
(2)
称取约10g试样(精确至0.01g),放入锥形瓶中,加人50mL丙酮,加热回流至所有可溶物溶解。用已质量恒定的埚过滤溶液,再用60mL丙酮分数次洗涤锥形瓶、埚,以确保固形物全部移人增埚,壁等处可溶物全部洗净。将埚置于110℃烘箱中干燥30min,取出于干燥器中冷却至室温,称量至质量恒定。
以质百分数表示的两酮中固体不溶物的含量(X3)按式(3)计算:m - mo × 100
式中:mi-
质量恒定后砂芯地埚与不溶物的质量,名;砂芯埚质量,g
m——试样质量,g。
4.7酸度的测定
4.7.1试剂和溶液
丙酮。
氢氧化钠标准滴定溶液:c(NaOH)0.02mol/L,按GB/T601中规定方法配制。配合指示液::2g/L甲基红乙醇液2 mL与2g/L溴甲酚绿乙醇溶液10 mL混合。4.7.2测定步骤
·(3)
称取8g试样(准确至0.0001g)置于250mL锥形瓶中,加入100mL丙酮,振摇使试样溶解,滴加0.6mL指示液,用氧氧化钠标准滴定溶液滴定至由黄色变为蓝绿色为终点。同时作空白测定。
以质量百分数表示的试样的酸度(X)(以H2SO4计)按式(4)计算:c(V/- Vo) × 0. 049 × 100*
(4)
HG36211999
一氢化钠标溶液的实际浓度,mol/,式中:
V,滴定试样溶液消耗氢氧化钠标准溶液的体积,mL,V。滴定空白溶液消耗氢氧化钠标准溶液的体积,mLm
—一试样的质量·,
0.049---与1.00mL氢氧化钠标准溶液[c(NaOH)=1.000mol/L]相当的以克表示的硫酸的质量。4.8产品检验与验收
产品的检验与验收应符合GB/T1604的有关规定,并在到货之日起三个月内验收。极限数值的处理采用修约值比较法。
5标惠、标签、包装、购运
5.1克百威原药的标志、标签和包装应符合GB3796中的有关规定。作为商品流通的原药,还应有商标和生产许可证号。
5.2克百威原药内用一层塑料薄膜袋包装,外套用業丙烯编织袋,然后封袋置于铁桶中,每桶净含量(100±0.2)kg。
5.3根据用户要求或订货协议,可以采用其他形式的包装,但要符合GB3796中有关规定。5.4包装件应存放在通风、干燥的库房中。5.5贮运时,严防潮湿和日,不得与食物、种子、饲料混放,避免与皮肤、眼睛接触,防止由口吸人。5.6安全
克百威属高毒氨基甲酸酯类杀盅剂,吞磁或吸人均有毒,还可通过皮肤渗入,故使用本品应穿防护服、带防护手套,皮肤或身体裸露部位接触本品后,应及时用肥和水洗净。如发生中毒现象,轻者可肌肉注射阿托品解毒,必要时应请医生诊治。1204
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。