GA/T 934-2011
基本信息
标准号: GA/T 934-2011
中文名称:生物样品中次乌头碱、乌头碱、中乌头碱的液相色谱-串联质谱检验方法
标准类别:公共安全行业标准(GA)
标准状态:现行
出版语种:简体中文
下载格式:.zip .pdf
下载大小:1172721

标准分类号
关联标准
出版信息
相关单位信息
标准简介
GA/T 934-2011.LC-MS-MS examination method for hypaconitine aconitine and mesaconitine in biological samples.
1范围
GA/T 934规定了生物样品中次乌头碱、乌头碱、中乌头碱的液相色谱串联质谱(LC-MSMS)检验方法。
GA/T 934适用于生物样品(如血、尿、组织脏器等)中次乌头碱、乌头碱、中乌头碱的定性分析和定量分析。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注8期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GA/T 122毒物分析名词术语
3术语和定义
GA/T 122界定的术语和定义适用于本文件。
4原理
检材用盐酸酸化,经阳离子交换固相萃取净化后,用液相色谱串联质谱法(LC-MS-MS)分析,根据MSMS特征离子对定性,外标法定量。
5试剂和材料
本法试验用水为去离子水,除非另有说明所用试剂均为色谱纯:
a)甲醇;
b)乙腈;
c) 0.1 mol/L,6.0 mol/L的盐酸;
d)甲酸;
e)碳酸氢铵 ;
f)氨水(分析纯) ;
g)微孔滤膜,0. 22 μm;
h)混合 型阳离子交换固相萃取柱(30 mg,1 mL):
1)基 质为苯磺酸化的聚苯乙烯-二乙烯苯高聚物;
2)使用前依次用1 mL甲醇,1 mL水活化。
i)标准品溶液:
1) 次乌头碱、乌头碱、中乌头碱标准品,纯度大于99.0% ;
1范围
GA/T 934规定了生物样品中次乌头碱、乌头碱、中乌头碱的液相色谱串联质谱(LC-MSMS)检验方法。
GA/T 934适用于生物样品(如血、尿、组织脏器等)中次乌头碱、乌头碱、中乌头碱的定性分析和定量分析。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注8期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GA/T 122毒物分析名词术语
3术语和定义
GA/T 122界定的术语和定义适用于本文件。
4原理
检材用盐酸酸化,经阳离子交换固相萃取净化后,用液相色谱串联质谱法(LC-MS-MS)分析,根据MSMS特征离子对定性,外标法定量。
5试剂和材料
本法试验用水为去离子水,除非另有说明所用试剂均为色谱纯:
a)甲醇;
b)乙腈;
c) 0.1 mol/L,6.0 mol/L的盐酸;
d)甲酸;
e)碳酸氢铵 ;
f)氨水(分析纯) ;
g)微孔滤膜,0. 22 μm;
h)混合 型阳离子交换固相萃取柱(30 mg,1 mL):
1)基 质为苯磺酸化的聚苯乙烯-二乙烯苯高聚物;
2)使用前依次用1 mL甲醇,1 mL水活化。
i)标准品溶液:
1) 次乌头碱、乌头碱、中乌头碱标准品,纯度大于99.0% ;
标准图片预览




标准内容
ICS13.310
中华人民共和国公共安全行业标准GA/T934—2011bzxz.net
生物样品中次乌头碱、乌头碱、中乌头碱的液相色谱-串联质谱检验方法
LC-MS-MS examination method for hypaconitine,aconitine andmesaconitineinbiologicalsamples2011-04-06发布
中华人民共和国公安部
2011-05-01实施
本标准按照GB/T1.1—2009给出的规则起草。GA/T934—2011
请注意本文件的某些内容可能涉及专利,本文件的发布机构不承担识别这些专利的责任。本标准由公安部物证鉴定中心提出。本标准由全国刑事技术标准化技术委员会毒物分析标准化分技术委员会(SAC/TC179/SC1)归口。
本标准起草单位:公安部物证鉴定中心毒物检验鉴定处。本标准主要起草人:王朝虹、何毅、王志萍。1范围
生物样品中次乌头碱、乌头碱、中乌头碱的液相色谱-串联质谱检验方法
GA/T934—2011
本标准规定了生物样品中次乌头碱、乌头碱、中乌头碱的液相色谱申联质谱(LC-MS-MS)检验方法。
本标准适用于生物样品(如血、尿、组织脏器等)中次乌头碱、乌头碱、中乌头碱的定性分析和定量分析。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GA/T122毒物分析名词术语
3术语和定义
GA/T122界定的术语和定义适用于本文件。4原理
检材用盐酸酸化,经阳离子交换固相萃取净化后,用液相色谱联质谱法(LC-MS-MS)分析,根据MS-MS特征离子对定性,外标法定量。5试剂和材料
本法试验用水为去离子水,除非另有说明所用试剂均为色谱纯:a)甲醇;
b)乙腈,
0.1mol/L,6.0mol/L的盐酸;
甲酸;
碳酸氢铵;
氨水(分析纯));
微孔滤膜,0.22μm;
混合型阳离子交换固相萃取柱(30mg,1mL):1)基质为苯磺酸化的聚苯乙烯-二乙烯苯高聚物;2)使用前依次用1mL甲醇,1mL水活化,i)
标准品溶液:
1)次乌头碱、乌头碱、中乌头碱标准品,纯度大于99.0%:1
GA/T934--2011
2)次乌头碱、乌头碱、中乌头碱标准储备液:分别准确称取次乌头碱、乌头碱和中乌头碱25mg(精确到0.1mg)于25mL容量瓶中,加入乙腈少量溶解并定容至刻度,混匀,配制成浓度为1.0mg/mL的标准储备液。置于冰箱中冷冻保存,可使用12个月;次乌头碱,乌头碱,中乌头碱标准工作液:吸取0.1mL标准储备液放入10mL容量瓶中,3)
用乙稀释至刻度,混勾,配制成浓度为10μg/mL的标准工作液。置于冰箱中4℃保存,可使用6个月。
6仪器
6.1LC-MS-MS:配有电喷雾离子源(ESI)6.2电子分析天平:感量为0.01mg和0.01g。6.3高速离心机。
6.4涡旋混合器。
6.5固相萃取装置。
6.6微量移液器5μl~100μ,100μ~1000μ。6.7
具塞塑料离心管。
7操作方法
7.1提取
检材的取材量可根据实际情况进行调整,按以下方法进行提取:a)取4mL尿,添加6mol/L500L盐酸,经微孔滤膜过滤,转移至固相萃取柱中,控制流速为1mL/min,依次以1mL0.1mol/L盐酸和1mL甲醇淋洗,抽至近干后,以1mL含5%氨水的70%甲醇溶液洗脱,洗脱液低于40℃蒸于,残留物用0.1mol/L甲酸溶液定容至1mL,泻旋混合1min,过微孔滤膜后,供LC-MS-MS测定b)取1mL血,肺、肝,肾、心、脑、胃组织、肌肉或呕吐物等检材取1g,以0.1mol/L5mL的盐酸匀浆,以不低于8000r/min离心20min,取上清液至固相萃取柱中,控制流速为1mL/min,依次以1mL0.1mol/L盐酸和1mL甲醇淋洗,抽至近干后,以1mL含5%氨水的70%甲醇溶液洗脱,洗脱液低于40℃蒸干,残留物用0.1mol/L甲酸溶液定容至1ml,涡旋混合1min,过微孔滤膜后,供LC-MS-MS测定。空白实验:取相应空白检材,均按上述步骤进行。c)
基质标准工作溶液:吸取不同体积标准工作溶液,用空白样品提取液配成1ng/g(mL)、10ng/d)
g(mL)、100ng/g(mL).200ng/g(mL).500ng/g(mL)不同浓度的基质标准工作溶液。当天配制。
7.2LC-MS-MS测定
7.2.1LC参考条件
以下条件作为参考,可根据不同仪器和不同检材实际进行调整:a)色谱柱:ACQUITYUPLCBEHSHIELDRP柱(50mmX2.1mm1.7μm),或相当者;b)流动相:乙腈:10mmol/L乙酸铵水溶液(氨水调pH9.5),比例为50:50;c)进样量:2μL;
d)柱温:30℃;
e)流速:0.4mL/min
质谱参考条件
以下条件作为参考,可根据不同仪器和不同检材实际进行调整:离子化模式:ESI+,MRM模式:
毛细管电压:3.0kV;
源温度:150℃;
雾化气流速:1000L/Hr;
雾化气温度:450℃;
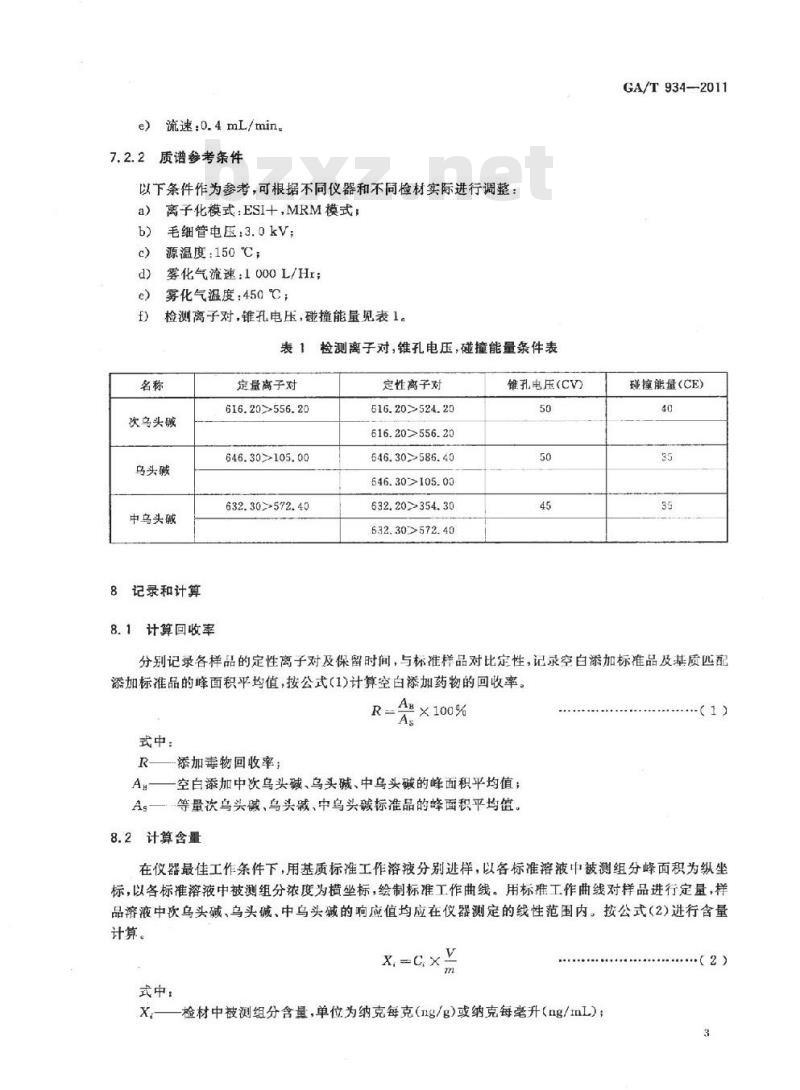
检测离子对,锥孔电压,碰撞能量见表1。表1检测离子对,锥孔电压,碰撞能量条件表名称
次乌头碱
乌头碱
中乌头碱
8记录和计算
8.1计算回收率
定量离子对
616.20>556.20
646.30>105.00
632.30>572.40
定性高子对
616.20>524.20
616.20>556.20
646.30>586.40
646.30>105.00
632.20>354.30
632.30>572.40
锥孔电压(CV)
GA/T934—2011
班撞能量(CE)
分别记录各样品的定性离子对及保留时间,与标准样品对比定性,记录空白添加标准品及基质匹配添加标准品的峰面积平均值,按公式(1)计算空白添加药物的回收率。R
式中:
R—添加毒物回收率;
A—空白添加中次乌头碱、乌头碱、中乌头碱的峰面积平均值;As—等量次乌头碱,乌头敲、中乌头碱标准品的峰面积平均值。8.2计算含量
在仪器最佳工作条件下,用基质标准工作溶液分别进样,以各标准溶液中被测组分峰面积为纵坐标,以各标准溶液中被测组分浓度为横坐标,绘制标准工作曲线。用标准工作曲线对样品进行定量,样品溶液中次乌头碱、乌头碱、中乌头碱的响应值均应在仪器测定的线性范围内。按公式(2)进行含量计算。
X,=C X
式中:
X,检材中被测组分含量,单位为纳克每克(ng/g)或纳克每毫升(ng/mL);..(2)
GA/T934-2011
从标准曲线上得到的被测组分溶液浓度,单位为纳克每毫升(ng/mL);C--
-样品溶液的体积,单位为毫升(mL):检材质量或体积,单位为克(g)或毫升(mL)。8.3相对相差
记录两份平行操作的检材含量,按照公式(3)计算相对相差。RD=1x=.1×100%
式中:
9结果评价
相对相差;
两个样品平行定量测定的含量数值;一两个样品平行定量测定含量的平均值。9.1定性结果评价
(3)
9.1.11mL血样或1g空白组织中添加100ng次乌头碱,乌头碱、中乌头碱的回收率在60%以上,空白无干扰,检材出现阴性结果可信:如次乌头碱、乌头碱、中乌头碱的回收率低于60%,检材出现阴性时,不能作未检出结论,应重新操作。9.1.2应用LC-MS-MS对次乌头碱、乌头碱、中乌头碱进行检验,在生物检材中的检出限应高于0.1ng/g(mL)。相关总离子流图和提取离子流图参见图A.1,图A.2。按照上述条件测定,被测组分选择一个母离子,两个以上子离子,在相同的试验条件下,检材提取液中待测组分的保留时间与标准溶液中对应组分的保留时间偏差在士2.5%之内;且检材提取液中各组分定性离子对的相对丰度与浓度接近的标准溶液中对应的定性离子对的相对丰度进行比较,若偏差不超过表规定的范围(见表2),可判断检材中存在次乌头碱、乌头碱、中乌头碱。表2定性确证时相对离子丰度的最大允许偏差相对离子丰度
允许的相对偏差
9.2定量结果评价
>20%~50%
>10%~20%
两份检材在相同条件下所得的次乌头碱、乌头碱、中乌头碱的含量相对相差不超过20%,说明定量数据可靠,否则说明操作有误,应重新定量。9.3中毒参考资料
附录B提供的乌头碱类生物碱中毒参考资料有助于缩小检验范围,印证定性定量结果。附录A
(资料性附录)
乌头类生物碱的相关色谱图
GA/T934—2011
A.1乌头类生物碱按照以上方法获得的总离子流图和提取离子流图,见图A.1、图A.2IQpph乌头碱
IOpph乌头戚
3:MRMof2ChannelsES+
TIC (Aconitine)
2:MRMof 2 Channels ES-1
TIC (Mesueonitine)
1:MRM of 2 Chenncls ES+
TIC (Hypaconitine)
乌头碱、中乌头碱、次乌头碱的MRM总离子流图2.75
3:MRMof2ChannelsES+
646.3>586.4(Aconitine)
乌头碱、中乌头碱、次乌头碱的提取离子流图2.50
3:MRMof2Channels ES+
646.3>105(Acomtine)
2:MRMof2ChennelsES+
G32.3>572.4(Mesaconitine)
2: MRMofa Channels ES-
632.3>354.5(Mesaconitine)
l:MRMof2ChannelsES+
616.2>556.2 (Hygaconitine)
1: MRM of 2 Charncis ES+
616.2>524. 2(Hypaconitinc)
GA/T934—2011
B.1中毒症状
附录B
(资料性附录)
乌头类生物碱中毒诊断参考资料多在服药后10min至2h内出现症状,首先感到唇舌辛辣、灼热、发痒麻木,从指间始至四肢及全身,痛觉减弱或消失、感到头昏、恶心、呕吐、流涎,腹痛腹泻、肠鸣音亢进、耳鸣复视、瞳孔先缩小后放大、呼吸急促、咳嗽血痰、紫结、急性肺水肿、心气急、心动过缓、心律失常、血压下降、房室脱节、完全性房室传导阻滞、心室颤动、此时可能肌肉强直、肌体发硬、阵发性抽搐、牙关紧闭、大小便失禁、呼吸困难,痊李室息而致死亡。
B.2中毒死亡机理
乌头碱主要作用于神经系统,使之先兴奋后抑制甚至麻痹。乌头碱选择性兴奋中枢神经系统,对迷走神经有强烈兴奋作用,可引起窦房结抑制,房室传导阻滞,从而导致心律绥慢或心律失常;也可直接作用于心肌,增高心肌应激性,引起过早搏动、室性心动过速,室额、严重心率失常,至呼吸麻痹而死。乌头类生物碱半数致死量(LDs。)B.3
乌头类生物碱的小鼠LD%见表B.1。表B.1乌头类生物碱的小鼠LDs
生物碱
乌头碱
中鸟头碱”
次乌头碱”
苯甲酰乌头碱*
苯甲酰中乌头碱
苯甲酰次乌头碱?
乌头原碱
去氧乌头碱”
3-乙酰乌头碱
soaconitine(HNO,)
Bullatined(HCI)
Delavaconitine\
皮下注射
腹腔注射
单位为毫克每千克
静脉注射
生物碱
滇乌碱
北草乌碱
.单醋生物碱。
。双酯生物碱。
。三酯生物碱。
。原碱。
表B.1(续)
皮下注射
腹腔注射
GA/T 934—2011
单位为毫克每千克
静脉注射
0.05(大鼠)
GA/T 934-2011
打印日期:2011年6月13日F008A00中华人民共和国公共安全
行业标准
生物样品中次乌头碱、乌头碱、中乌头碱的液相色谱-串联质谱检验方法
GA/T934—2011
中国标准出版社出版发行
北京复兴门外三里河北街16号
邮政编码:100045
网址spc.net.cn
电话:6852394668517548
中国标准出版社秦皇岛印剧厂印刷各地新华书店经销
开本880×12301/16印张0.75字数15千字2011年5月第一版2011年5月第一次印刷书号:155066·2-21980定价16.00元如有印装差错由本社发行中心调换版权专有侵权必究
举报电话:(010)68533533
110226/
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
中华人民共和国公共安全行业标准GA/T934—2011bzxz.net
生物样品中次乌头碱、乌头碱、中乌头碱的液相色谱-串联质谱检验方法
LC-MS-MS examination method for hypaconitine,aconitine andmesaconitineinbiologicalsamples2011-04-06发布
中华人民共和国公安部
2011-05-01实施
本标准按照GB/T1.1—2009给出的规则起草。GA/T934—2011
请注意本文件的某些内容可能涉及专利,本文件的发布机构不承担识别这些专利的责任。本标准由公安部物证鉴定中心提出。本标准由全国刑事技术标准化技术委员会毒物分析标准化分技术委员会(SAC/TC179/SC1)归口。
本标准起草单位:公安部物证鉴定中心毒物检验鉴定处。本标准主要起草人:王朝虹、何毅、王志萍。1范围
生物样品中次乌头碱、乌头碱、中乌头碱的液相色谱-串联质谱检验方法
GA/T934—2011
本标准规定了生物样品中次乌头碱、乌头碱、中乌头碱的液相色谱申联质谱(LC-MS-MS)检验方法。
本标准适用于生物样品(如血、尿、组织脏器等)中次乌头碱、乌头碱、中乌头碱的定性分析和定量分析。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GA/T122毒物分析名词术语
3术语和定义
GA/T122界定的术语和定义适用于本文件。4原理
检材用盐酸酸化,经阳离子交换固相萃取净化后,用液相色谱联质谱法(LC-MS-MS)分析,根据MS-MS特征离子对定性,外标法定量。5试剂和材料
本法试验用水为去离子水,除非另有说明所用试剂均为色谱纯:a)甲醇;
b)乙腈,
0.1mol/L,6.0mol/L的盐酸;
甲酸;
碳酸氢铵;
氨水(分析纯));
微孔滤膜,0.22μm;
混合型阳离子交换固相萃取柱(30mg,1mL):1)基质为苯磺酸化的聚苯乙烯-二乙烯苯高聚物;2)使用前依次用1mL甲醇,1mL水活化,i)
标准品溶液:
1)次乌头碱、乌头碱、中乌头碱标准品,纯度大于99.0%:1
GA/T934--2011
2)次乌头碱、乌头碱、中乌头碱标准储备液:分别准确称取次乌头碱、乌头碱和中乌头碱25mg(精确到0.1mg)于25mL容量瓶中,加入乙腈少量溶解并定容至刻度,混匀,配制成浓度为1.0mg/mL的标准储备液。置于冰箱中冷冻保存,可使用12个月;次乌头碱,乌头碱,中乌头碱标准工作液:吸取0.1mL标准储备液放入10mL容量瓶中,3)
用乙稀释至刻度,混勾,配制成浓度为10μg/mL的标准工作液。置于冰箱中4℃保存,可使用6个月。
6仪器
6.1LC-MS-MS:配有电喷雾离子源(ESI)6.2电子分析天平:感量为0.01mg和0.01g。6.3高速离心机。
6.4涡旋混合器。
6.5固相萃取装置。
6.6微量移液器5μl~100μ,100μ~1000μ。6.7
具塞塑料离心管。
7操作方法
7.1提取
检材的取材量可根据实际情况进行调整,按以下方法进行提取:a)取4mL尿,添加6mol/L500L盐酸,经微孔滤膜过滤,转移至固相萃取柱中,控制流速为1mL/min,依次以1mL0.1mol/L盐酸和1mL甲醇淋洗,抽至近干后,以1mL含5%氨水的70%甲醇溶液洗脱,洗脱液低于40℃蒸于,残留物用0.1mol/L甲酸溶液定容至1mL,泻旋混合1min,过微孔滤膜后,供LC-MS-MS测定b)取1mL血,肺、肝,肾、心、脑、胃组织、肌肉或呕吐物等检材取1g,以0.1mol/L5mL的盐酸匀浆,以不低于8000r/min离心20min,取上清液至固相萃取柱中,控制流速为1mL/min,依次以1mL0.1mol/L盐酸和1mL甲醇淋洗,抽至近干后,以1mL含5%氨水的70%甲醇溶液洗脱,洗脱液低于40℃蒸干,残留物用0.1mol/L甲酸溶液定容至1ml,涡旋混合1min,过微孔滤膜后,供LC-MS-MS测定。空白实验:取相应空白检材,均按上述步骤进行。c)
基质标准工作溶液:吸取不同体积标准工作溶液,用空白样品提取液配成1ng/g(mL)、10ng/d)
g(mL)、100ng/g(mL).200ng/g(mL).500ng/g(mL)不同浓度的基质标准工作溶液。当天配制。
7.2LC-MS-MS测定
7.2.1LC参考条件
以下条件作为参考,可根据不同仪器和不同检材实际进行调整:a)色谱柱:ACQUITYUPLCBEHSHIELDRP柱(50mmX2.1mm1.7μm),或相当者;b)流动相:乙腈:10mmol/L乙酸铵水溶液(氨水调pH9.5),比例为50:50;c)进样量:2μL;
d)柱温:30℃;
e)流速:0.4mL/min
质谱参考条件
以下条件作为参考,可根据不同仪器和不同检材实际进行调整:离子化模式:ESI+,MRM模式:
毛细管电压:3.0kV;
源温度:150℃;
雾化气流速:1000L/Hr;
雾化气温度:450℃;
检测离子对,锥孔电压,碰撞能量见表1。表1检测离子对,锥孔电压,碰撞能量条件表名称
次乌头碱
乌头碱
中乌头碱
8记录和计算
8.1计算回收率
定量离子对
616.20>556.20
646.30>105.00
632.30>572.40
定性高子对
616.20>524.20
616.20>556.20
646.30>586.40
646.30>105.00
632.20>354.30
632.30>572.40
锥孔电压(CV)
GA/T934—2011
班撞能量(CE)
分别记录各样品的定性离子对及保留时间,与标准样品对比定性,记录空白添加标准品及基质匹配添加标准品的峰面积平均值,按公式(1)计算空白添加药物的回收率。R
式中:
R—添加毒物回收率;
A—空白添加中次乌头碱、乌头碱、中乌头碱的峰面积平均值;As—等量次乌头碱,乌头敲、中乌头碱标准品的峰面积平均值。8.2计算含量
在仪器最佳工作条件下,用基质标准工作溶液分别进样,以各标准溶液中被测组分峰面积为纵坐标,以各标准溶液中被测组分浓度为横坐标,绘制标准工作曲线。用标准工作曲线对样品进行定量,样品溶液中次乌头碱、乌头碱、中乌头碱的响应值均应在仪器测定的线性范围内。按公式(2)进行含量计算。
X,=C X
式中:
X,检材中被测组分含量,单位为纳克每克(ng/g)或纳克每毫升(ng/mL);..(2)
GA/T934-2011
从标准曲线上得到的被测组分溶液浓度,单位为纳克每毫升(ng/mL);C--
-样品溶液的体积,单位为毫升(mL):检材质量或体积,单位为克(g)或毫升(mL)。8.3相对相差
记录两份平行操作的检材含量,按照公式(3)计算相对相差。RD=1x=.1×100%
式中:
9结果评价
相对相差;
两个样品平行定量测定的含量数值;一两个样品平行定量测定含量的平均值。9.1定性结果评价
(3)
9.1.11mL血样或1g空白组织中添加100ng次乌头碱,乌头碱、中乌头碱的回收率在60%以上,空白无干扰,检材出现阴性结果可信:如次乌头碱、乌头碱、中乌头碱的回收率低于60%,检材出现阴性时,不能作未检出结论,应重新操作。9.1.2应用LC-MS-MS对次乌头碱、乌头碱、中乌头碱进行检验,在生物检材中的检出限应高于0.1ng/g(mL)。相关总离子流图和提取离子流图参见图A.1,图A.2。按照上述条件测定,被测组分选择一个母离子,两个以上子离子,在相同的试验条件下,检材提取液中待测组分的保留时间与标准溶液中对应组分的保留时间偏差在士2.5%之内;且检材提取液中各组分定性离子对的相对丰度与浓度接近的标准溶液中对应的定性离子对的相对丰度进行比较,若偏差不超过表规定的范围(见表2),可判断检材中存在次乌头碱、乌头碱、中乌头碱。表2定性确证时相对离子丰度的最大允许偏差相对离子丰度
允许的相对偏差
9.2定量结果评价
>20%~50%
>10%~20%
两份检材在相同条件下所得的次乌头碱、乌头碱、中乌头碱的含量相对相差不超过20%,说明定量数据可靠,否则说明操作有误,应重新定量。9.3中毒参考资料
附录B提供的乌头碱类生物碱中毒参考资料有助于缩小检验范围,印证定性定量结果。附录A
(资料性附录)
乌头类生物碱的相关色谱图
GA/T934—2011
A.1乌头类生物碱按照以上方法获得的总离子流图和提取离子流图,见图A.1、图A.2IQpph乌头碱
IOpph乌头戚
3:MRMof2ChannelsES+
TIC (Aconitine)
2:MRMof 2 Channels ES-1
TIC (Mesueonitine)
1:MRM of 2 Chenncls ES+
TIC (Hypaconitine)
乌头碱、中乌头碱、次乌头碱的MRM总离子流图2.75
3:MRMof2ChannelsES+
646.3>586.4(Aconitine)
乌头碱、中乌头碱、次乌头碱的提取离子流图2.50
3:MRMof2Channels ES+
646.3>105(Acomtine)
2:MRMof2ChennelsES+
G32.3>572.4(Mesaconitine)
2: MRMofa Channels ES-
632.3>354.5(Mesaconitine)
l:MRMof2ChannelsES+
616.2>556.2 (Hygaconitine)
1: MRM of 2 Charncis ES+
616.2>524. 2(Hypaconitinc)
GA/T934—2011
B.1中毒症状
附录B
(资料性附录)
乌头类生物碱中毒诊断参考资料多在服药后10min至2h内出现症状,首先感到唇舌辛辣、灼热、发痒麻木,从指间始至四肢及全身,痛觉减弱或消失、感到头昏、恶心、呕吐、流涎,腹痛腹泻、肠鸣音亢进、耳鸣复视、瞳孔先缩小后放大、呼吸急促、咳嗽血痰、紫结、急性肺水肿、心气急、心动过缓、心律失常、血压下降、房室脱节、完全性房室传导阻滞、心室颤动、此时可能肌肉强直、肌体发硬、阵发性抽搐、牙关紧闭、大小便失禁、呼吸困难,痊李室息而致死亡。
B.2中毒死亡机理
乌头碱主要作用于神经系统,使之先兴奋后抑制甚至麻痹。乌头碱选择性兴奋中枢神经系统,对迷走神经有强烈兴奋作用,可引起窦房结抑制,房室传导阻滞,从而导致心律绥慢或心律失常;也可直接作用于心肌,增高心肌应激性,引起过早搏动、室性心动过速,室额、严重心率失常,至呼吸麻痹而死。乌头类生物碱半数致死量(LDs。)B.3
乌头类生物碱的小鼠LD%见表B.1。表B.1乌头类生物碱的小鼠LDs
生物碱
乌头碱
中鸟头碱”
次乌头碱”
苯甲酰乌头碱*
苯甲酰中乌头碱
苯甲酰次乌头碱?
乌头原碱
去氧乌头碱”
3-乙酰乌头碱
soaconitine(HNO,)
Bullatined(HCI)
Delavaconitine\
皮下注射
腹腔注射
单位为毫克每千克
静脉注射
生物碱
滇乌碱
北草乌碱
.单醋生物碱。
。双酯生物碱。
。三酯生物碱。
。原碱。
表B.1(续)
皮下注射
腹腔注射
GA/T 934—2011
单位为毫克每千克
静脉注射
0.05(大鼠)
GA/T 934-2011
打印日期:2011年6月13日F008A00中华人民共和国公共安全
行业标准
生物样品中次乌头碱、乌头碱、中乌头碱的液相色谱-串联质谱检验方法
GA/T934—2011
中国标准出版社出版发行
北京复兴门外三里河北街16号
邮政编码:100045
网址spc.net.cn
电话:6852394668517548
中国标准出版社秦皇岛印剧厂印刷各地新华书店经销
开本880×12301/16印张0.75字数15千字2011年5月第一版2011年5月第一次印刷书号:155066·2-21980定价16.00元如有印装差错由本社发行中心调换版权专有侵权必究
举报电话:(010)68533533
110226/
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。