基本信息
标准号:
HG 2351-1992
中文名称:镉红颜料
标准类别:化工行业标准(HG)
英文名称: Cadmium Red Pigment
标准状态:现行
发布日期:1992-07-14
实施日期:1993-05-01
出版语种:简体中文
下载格式:.rar.pdf
下载大小:638.53 KB
相关标签:
颜料

标准分类号
标准ICS号:涂料和颜料工业>>涂料配料>>87.060.10颜料和填充剂
中标分类号:化工>>涂料、颜料、染料>>G54颜料
关联标准
采标情况:ISO 4620-86 NEQ
相关单位信息
标准简介
HG 2351-1992 镉红颜料 HG2351-1992
标准内容
中华人民共和国化工行业标准
HG2351—92
镉红颜料
1992-07-14发布
中华人民共和国化学工业部
3发布
1993-05-01实施
中华人民共和国化工行业标准
镉红颜料
本标准参照采用国际标准ISO4620—1986《镉颜料规格和试验方法》。1主题内容和适用范围
HG235192
本标准规定了适合于一般用途的镉红颜料的技术要求、试验方法、检验规则以及包装、标志、运输和购存。
本标准适用于以可溶性镉盐、硫化钠和硒粉等为原料制得的镉红颜料。该产品主要用于塘瓷、玻璃、色漆、塑料和橡胶等。
2引用标准
GB1711
颜料在烘干型漆料中热稳定性的比较颜料水悬浮液pH值的测定
GB1717
GB1864
颜料颜色的比较
GB5211.15
GB5211.18
GB5211.19
GB6682
GB9760
GB7686
GB9285
GB9287
颜料水溶物测定冷萃取法
颜料在105℃挥发物的测定
颜料吸油量的测定
颜料筛余物的测定水法手工操作着色颜料相对着色力和冲淡色的测定目视比较法实验室用水规格
色漆和清漆液体或粉末状色漆中酸萃取物的制备化工产品中砷含量测定的通用方法色漆和清漆用原材料取样
颜料易分散程度的比较振荡法
色漆和清漆“可溶性”金属含量的测定第一部分:铅含量的测定火焰原子吸收光谱法和双硫腺分光光度法
色漆和清漆“可溶性”金属含量的测定第二部分,锑含量的测定火焰原子吸收光谱法和若丹明B分光光度法
色漆和清漆“可溶性”金属含量的测定第三部分:钡含量的测定火焰原子发射光谱法
色漆和清漆“可溶性”金属含量的测定第四部分:镉含量的测定火焰原子吸收光谱法和极谱法
色漆和清漆“可溶性”金属含量的测定第六部分:色漆的液体部分中铬总含量的测GB9758.6
定火焰原子吸收光谱法
色漆和清漆“可溶性”金属含量的测定第七部分:色漆的颜料部分和水可稀释漆的液体部分的汞含量的测定无焰原子吸收光谱法中华人民共和国化学工业部1992-07-14批准1993-05-01实施
产品分型
根据用途镉红颜料分为如下三种类型:HG2351—92
I型:浓缩品种。为调整其相对着色力,这类颜料所含体质颜料不得大于30%(m/m)。I型:淡质品种。为便于加工,这类颜料所含体质颜料不得大于70%(m/m)。I型:纯粹品种。这种颜料基本上是纯的,且不含任何体质颜料。技术要求
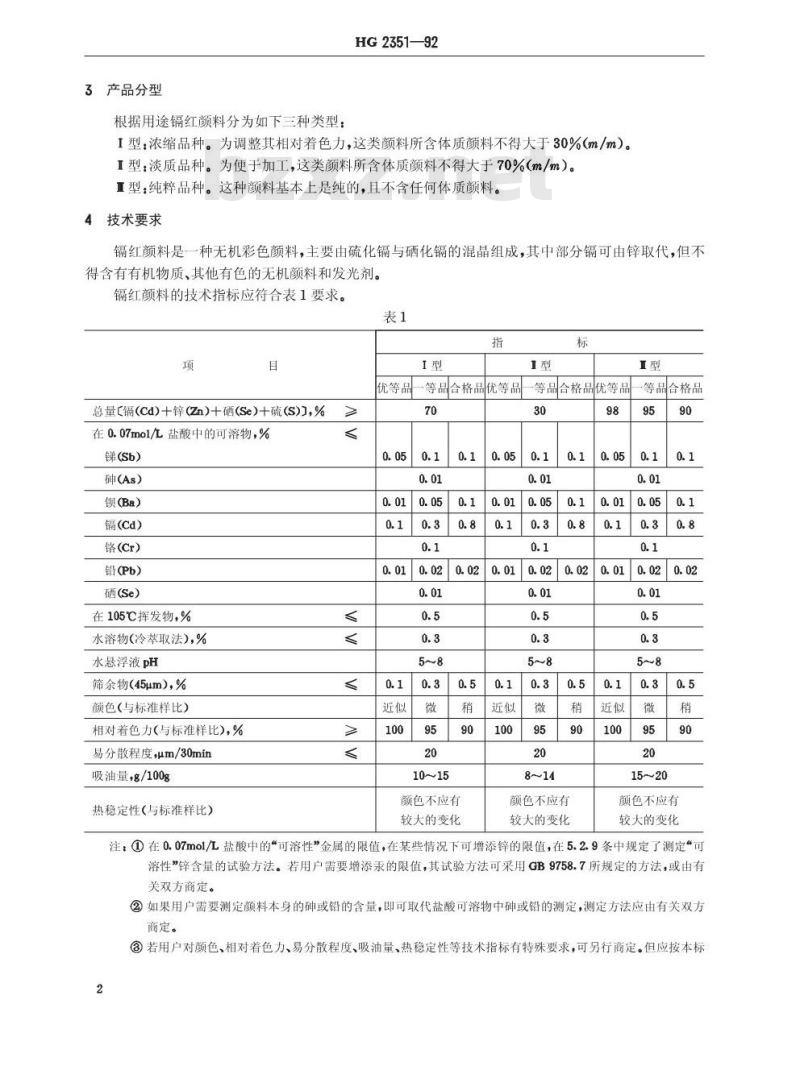
镉红颜料是一种无机彩色颜料,主要由硫化镉与硒化镉的混晶组成,其中部分镉可由锌取代,但不得含有有机物质、其他有色的无机颜料和发光剂。镉红颜料的技术指标应符合表1要求。表1
总量(镉(Cd)士锌(Zn)十硒(Se)士硫(S)J,%在0.07mo1/L盐酸中的可溶物,%锑(Sb)
砷(As)
镉(ca)
铬(Cr)
铅(Pb)
硒(Se)
在105℃挥发物,%
水溶物(冷萃取法),%
水悬浮液pH
筛余物(45μm),%
颜色(与标准样比)
相对着色力(与标准样比),%
易分散程度μm/30min
吸油量+g/100g
热稳定性(与标准样比)
优等品一等品合格品优等品
一等品合格品优等品
颜色不应有
较大的变化
颜色不应有
较大的变化
等品合格品
颜色不应有
较大的变化
注:①在0.07mo1/L盐酸中的*可溶性”金属的限值,在某些情况下可增添锌的限值,在5.2.9条中规定了测定“可溶性”锌含量的试验方法。若用户需要增添汞的限值,其试验方法可采用GB9758.7所规定的方法,或由有关双方商定。
②如果用户需要测定颜料本身的砷或铅的含量,即可取代盐酸可溶物中砷或铅的测定,测定方法应由有关双方商定。
③若用户对颜色、相对着色力、易分散程度、吸油量、热稳定性等技术指标有特殊要求,可另行商定。但应按本标2
准规定的试验方法进行检验。
HG2351—92
④“颜色”“相对着色力”的标准样:I型,湘潭市化工研究设计院:1型,湘潭市染料化工总厂:I型,湘潭市化工研究设计院、上海玻糖化工厂。5试验方法
在分析过程中,所用试剂均应采用分析纯试剂,使用GB6682规定的三级水或相应纯度的水。5.1总量[镉(Cd)十锌(Zn)十硒(Se)士硫(S)的测定5.1.1和锌含量的测定
5.1.1.1原理
将试样溶于盐酸和硝酸中,中和后,加入鼠化钾,并用EDTA标准滴定溶液滴定碱土金属。加入甲醛溶液以破环氰化镉和氰化锌络合物,用EDTA标准滴定溶液滴定镉离子和锌离子总量。在滴定溶液里用二乙基二硫代氨基甲酸钠破坏镉一EDTA络合物,并用氨水沉淀镉,用硫酸镁标准溶液滴定原先与镉络合的EDTA。
5.1.1.2试剂
5.1.1.2.1盐酸:1.18g/mL。
5.1.1.2.2盐酸溶液:用1.18g/mL盐酸稀释,1+115。5.1.1.2.3
硝酸:1.40g/mL。
5.1.1.2.4
氢氧化钠溶液:100g/L。
5.1.1.2.5
氨水:0.91g/mL。
甲醛溶液:30%(m/m)。
5.1.1.2.6
5. 1. 1. 2. 7
5.1.1.2.8
5.1.1.2.9
氯化铵溶液:107g/L。
二乙基二硫代氨基甲酸钠。
氰化钾。
加倍注意:氰化钾是一种致死的毒品。5.1.1.2.10
EDTA标准滴定溶液:c(EDTA)三0.01molL。准确称取乙二胺四乙酸二钠(C1oH14N20gNaz·2H20)3.7223g溶于水,移入1000mL容量瓶中,并稀释至刻度,摇匀。5.1.1.2.11硫酸镁标准溶液:c(MgSO4)=0.01mol/L。准确称取硫酸镁(MgSO4·7H20)2.4637g溶于盐酸溶液(0.5+999.5),移入1000mL容量瓶中,用同一盐酸溶液稀释至刻度,摇匀。2甲基橙溶液:0.1g/L。
5. 1. 1.2. 12
3铬黑T指示剂。将1g铬黑T与100g氯化铵混和并研磨均匀。5. 1. 1. 2. 13
5.1.1.2.14缓冲溶液。将70g氯化铵溶于774mL氨水中,并用水稀释至1000mL。5.1.1.3仪器
一般实验室仪器和
5.1.1.3.1容量瓶:250mL、1000mL。5.1.1.3.2移液管25mL。
5.1.1.3.3滴定管:50mL。
5.1.1.4操作步骤
进行两份样品的平行测定。
称取试样0.3~0.4g(精确至0.0001g)置于250mL烧杯中,用少量水润湿试样,加入约10mL盐酸(5.1.1.2.1),小心加热,直至盐酸蒸干,向残余物中加2mL硝酸(5.1.1.2.3),烧杯上盖以表面血,在电炉上加热10min或直至溶液清晰。加100mL水,煮沸2~3min。若有不溶物,用致密滤纸过滤。先用盐酸溶液(5.1.1.2.2)洗涤,而后用水洗涤,将滤液和洗涤液收集在250mL容量瓶中,稀释至刻度并充分混匀。
HG2351—92
用移液管吸取上述溶液25mL,置于250mL烧杯中,用水稀释至100mL,加1~2滴甲基橙溶液(5.1.1.2.12),用氢氧化钠溶液(5.1.1.2.4)中和,加2~3mL缓冲溶液(5.1.1.2.14),0.25g络黑T指示剂(5.1.1.2.13)及约2g氰化钾(5.1.1.2.9)。用EDTA标准滴定溶液(5.1.1.2.10)滴定至溶液由红色变为蓝色。
向得到的溶液中加入约20mL甲醛溶液(5.1.1.2.6),滴加氯化铵溶液(5.1.1.2.7)至pH为10~10.5。用EDTA标准滴定溶液(5.1.1.2.10)滴定至溶液由红色变为蓝色。记录滴定用EDTA标准滴定溶液的体积。
向已滴定的溶液中加入约1g二乙基二硫代氨基甲酸钠(5.1.1.2.8)和2~3滴氨水(5.1.1.2.5),用硫酸镁标准溶液(5.1.1.2.11)滴定至溶液由蓝色变为红色。记录滴定用硫酸镁溶液的体积。5.1.1.5结果的表示
镉的质量百分数以Wc表示,按式(1)计算:Vicix0.1124×100
锌的质量百分数以W盈表示,按式(2)计算:(V。V)X0. 065 4×100
_(V。-V)X0.654
式中.V。
-EDTA标准滴定溶液的体积,mL;V1—硫酸镁标准溶液的体积,mL;c1——硫酸镁标准溶液的浓度,mol/L;C2
一EDTA标准滴定溶液的浓度,mol/L;一试样的质量,g;
0.1124—与1.00mL硫酸镁标准溶液[c(MgS04)=1.000mo1/LJ相当的,以克表示的镉的质量0.0654-
一与1.00mLEDTA标准滴定溶液[c(EDTA)=1.000mol/LJ相当的,以克表示的锌的质量。平行测定结果的差值不大于0.4%。取算样平均值为测定结果。5.1.2硒含量的测定
5.1.2.1原理
将试样溶于溴水,待溴驱尽之后,用二盐酸联胺将硒还原、沉淀,而后称量。5.1.2.2试剂和材料
5.1.2.2.1盐酸:1.18g/mL。
5.1.2.2.2盐酸溶液:用1.18g/mL盐酸稀释,1+115。5.1.2.2.3溴。
二盐酸联胺(H2N·NH2·2HCI)。5.1.2.2.4
加倍注意:二盐酸联胺是一种剧毒品。二氧化碳或氮气:压缩气体。
5.1.2.2.5
5.1.2.3仪器
般实验室仪器和
HG2351—92
5.1.2.3.1锥形瓶:100mL,磨口塞规格18.8mm/19mm。5.1.2.3.2直形冷凝管:长度为400mm,上、下口内直径为13mm,下端为磨塞型,规格18.8mm/19mm。
5.1.2.3.3安全移液管:1mL。
5.1.2.3.4水浴:能保持在98士2℃。5.1.2.3.5玻璃滤器:孔径为7~8um。5.1.2.3.6电热干燥箱:能保持105土2℃。5.1.2.3.7干燥器:内装有效干燥剂。5.1.2.4操作步骤
加倍注意:凡进行溴的操作,都应在通风厨里进行,并使用安全手套。进行两份样品的平行测定。
称取试样约0.5g(精确至0.0001g),置于带磨口玻璃塞的100mL锥形瓶内,使其悬浮在10mL水中,用安全移液管加入1mL溴(5.1.2.2.3),盖上瓶塞,让其静置至少3h或放置过夜。用约20mL水稀释溶液,在锥形瓶上装以直形冷凝管。将一根拉成尖咀的玻璃管通过冷凝管插到靠近锥形瓶的底部,使玻璃管与二氧化碳或氮气(5.1.2.2.5)的气源连接。在缓慢加热下,将二氧化碳或氮气通入溶液,直至将溴完全驱尽。在冷凝管的上口用碘化钾-淀粉试纸检验溴。向无漠的溶液中加入5mL盐酸(5.1.2.2.1),者有不溶物,则用致密滤纸过滤。先用盐酸溶液(5.1.2.2.2)洗涤,而后用热水洗涤至无氯化物。向每100mL滤液和洗涤液里加入20~30mL盐酸(5.1.2.2.1),溶液冷却后,加入约5g二盐酸联胺(5.1.2.2.4),在水浴上加热。当红色沉淀物完全转变成黑色状态时,用已称量过的玻璃滤器过滤,并用热水洗涤之。合并滤液和洗涤液,供测定硫含量(见5.1.3条)用。将玻璃滤器和滤渣置于电热干燥箱内,在105℃干燥1h。置于干燥器内,冷却至室温后,称量(精确至0.0001g)。重复进行干燥、冷却和称量操作,直至恒重。5.1.2.5结果的表示
硒的质量百分数以Ws表示,按式(3)计算:Wse
式中m1——试样的质量,;
m2—硒的质量,g。
m2×100
平行测定结果的差值不大于0.4%。取算术平均值为测定结果。5.1.3硫含量的测定
用本方法测定的硫含量既有硫化物中的硫又有硫酸盐中的硫,但不溶性的硫酸盐,如硫酸钡中的硫除外。
5.1.3.1试剂
5.1.3.1.1氨水0.91g/mL。
5.1.3.1.2盐酸溶液:用1.18g/mL盐酸稀释,1+12。5.1.3.1.3氯化锁溶液:100g/L。5.1.3.1.4甲基橙溶液:0.1g/L。5.1.3.2仪器
一般实验室仪器和
5.1.3.2.1瓷:30mL。
HG2351—92
5.1.3.2.2箱形电阻炉:能保持在800士25℃。5.1.3.2.3干燥器:内装有效干燥剂。5.1.3.3操作步骤
进行两份样品的平行测定。
向第5.1.2.4条所述测定硒含量时所得的滤液和洗涤液中加5~6滴甲基橙溶液(5.1.3.1.4),用氨水(5.1.3.1.1)中和,每100mL溶液中加3~5mL盐酸溶液(5.1.3.1.2),加热至沸,在搅拌下逐滴加入约15mL氯化钡溶液(5.1.3.1.3),并再次煮沸。待沉淀析出后(如有必要,可静置过夜。)用致密滤纸过滤,先用盐酸溶液(5.1.3.1.2)洗涤沉淀,而后再用热水洗涤之。将滤纸和沉淀置于已称量过的瓷珀里,通入空气,加热,使滤纸缓慢灰化。将瓷增埚和残余物置于箱形电阻炉内,加热至约800℃,灼烧30min,置于干燥器内,冷却至室温后,称量。5.1.3.4结果的表示
硫的质量百分数以Ws表示,按式(4)计算:Ws-maX13.74
式中:m1——试样的质量,g;
m3—硫酸钡的质量,g;
13.74——BaSO4换算为S之系数乘以100。平行测定结果的差值不大于0.4%。取算术平均值为测定结果。5.1.4、锌、硒和硫总含量的计算颜料的Cd、Zn,Se和S的总含量,以质量百分数W总表示,按式(5)计算:W急Wca+Wz十Wse+Ws
式中:Wca——按5.1.1条测定的额料镉含量;Wz——按5.1.1条测定的颜料锌含量;Wse——按5.1.2条测定的颜料硒含量,Ws—按5.1.3条测定的颜料硫含量。5.2在0.07mol/L盐酸中的可溶物一一锑、砷、钡、镉、铬、铅、硒和锌的测定5.2.1盐酸萃取溶液的制备
.(4)
(5)
按GB9760第8.2.3条所述的操作步骤制备镉红颜料样品中,包含铅在内的所有金属的盐酸萃取溶液。同时按GB6760第8.4条所述的操作步骤,制备空白试验溶液。5.2.2“可溶性”锑含量的测定
按GB9758.2第3章所述的方法(火焰原子吸收光谱法)测定颜料样品的“可溶性”锑含量,并用GB9758.2第3.6.1.1条的公式(1)计算盐酸萃取溶液中“可溶性锑的质量m。乘以10/m,(m为制备盐酸萃取溶液所用试样的质量,采用的是5.00士0.01g),计算颜料的“可溶性”锑含量。5.2.3“可溶性”砷含量的测定
按GB7686所述的方法测定颜料样品的“可溶性”含量,并用GB7686第6章测定的盐酸萃取溶液中“可溶性”砷的质量mo乘以10°/m(m4为制备盐酸萃取溶液所用试样的质量,采用的是5.00士0.01g),计算颜料的“可溶性”砷含量。5.2.4“可溶性”钡含量的测定
5.2.4.1火焰原子发射光谱法(仲裁法)按GB9758.3所述的方法测定颜料样品的“可溶性”锁含量,并用GB9758.3第7.1.1条的公式(1)计算盐酸萃取溶液中\可溶性”锁的质量m。乘以10°/m(m为制备盐酸萃取溶液所用试样的质量,采用的是5.00士0.01g),计算颜料的*可溶性锁含量。5.2.4.2硫酸钡浊度法
5.2.4.2.1试剂
盐酸:c(HCI)=0.07mol/L
硫酸:c(H,So,)约为1mol/L;
HG2351—92
锁标准溶液:每升含100mg(Ba)。在1000mL容量瓶中,将0.1779g二水合氯化(BaCl2·2H20)溶于水,稀释至刻度并充分混匀,此标准溶液1mL含100ug(Ba)。5.2.4.2.2仪器
般实验室仪器和
滴定管:10mL;
移液管:10mL;
比色管:10mL;
容量瓶:1000mL。
5.2.4.2.3操作步骤
标准浊度溶液的制备
用滴定管向5支比色管中,分别加入5mL盐酸及表2所示的锁标准溶液和水的体积。表2钡的标准浊度溶液
标准浊度溶液
锁标准溶液(5.2.4.2.1c)的体积mL
向每一溶液中加入0.5mL硫酸并充分混匀。b。测定
进行两份样品的平行测定。
标准浊度溶液中含有钡的质量
用移液管量取按第5.2.1条所述操作步骤制备的盐酸萃取溶液1mL,或2mL、或10mL,置于比色管中,用盐酸稀释至10mL加0.5mL硫酸(5.2.4.2.1b),并充分混匀。15min后与标准比较。5.2.4.2.4结果的表示
钡的质量百分数以W·s表示,按式(6)计算:Wa·s
式中.a-
由钡的标准浊度溶液系列测得所用盐酸萃取溶液中钡的质量,ug;V1—一由第5.2.1条所述萃取用盐酸与乙醇的体积之和(采用的是77mL),mL;Vz——测定用盐酸萃取溶液的体积(采用的是1mL、或2mL、或10mL),mL;一由第5.2.1条所述制备盐酸萃取溶液所用试样的质量(采用的是5.00士0.01g),g。m
5.2.5“可溶性”镉含量的测定
5.2.5.1火焰原子吸收光谱法(仲裁法)(6)
按GB9758.4第3章所述的方法(火焰原子吸收光谱法)测定颜料样品的“可溶性”镉含量,并用GB9758.4中3.5.1.1条公式(1)计算盐酸萃取溶液中“可溶性”的质量mo乘以10°/m(m4为制备盐酸萃取溶液所用试样的质量,采用的是5.00土0.01g),计算颜料的“可溶性”镉含量。5.2.5.2络合滴定法
5.2.5.2.1原理
HG2351—92
用EDTA标准滴定溶液滴定和锌离子的总量,以二乙基二硫代氨基甲酸钠破坏滴定溶液中的镉-EDTA络合物,用硫酸镁标准溶液滴定原先与镉络合的EDTA。为滴定锌,需要用EDTA标准滴定溶液滴定另一份试验溶液中的碱土金属,用所耗EDTA标准滴定溶液体积之差计算锌含量。
5.2.5.2.2试剂
氨水:0.91g/mL;
b.二乙基二硫代氨基甲酸钠;
氰化钾溶液:65g/L;
加倍注意:氰化钾是一种致死的毒品。EDTA标准滴定溶液:c(EDTA)=0.01mol/L;d.
硫酸镁标准溶液:c(MgSO,)=0.01mol/L,制备方法见本标准第5.1.1.2.11条;e.
f.铬黑T指示剂:制备方法见本标准第5.1.1.2.13条;甲基橙溶液:0.1g/L。
5.2.5.2.3仪器
通常使用二等实验玻璃仪器,但在有争议时,应采用一等仪器。一般实验室仪器和
a.移液管:20mL;
b.滴定管:10mL。
5.2.5.2.4操作步骤
进行两份样品的平行测定。
用移液管量取按5.2.1条所述的操作步骤制备的盐酸萃取溶液20mL,置于锥形瓶中,用水稀释至50mL,加入1~2滴甲基橙溶液(5.2.5.2.2g),用氨水(5.2.5.2.2a)中和,再多加1mL氨水,而后加0.25g铬黑T指示剂(5.2.5.2.2f)。用EDTA标准滴定溶液(5.2.5.2.2d)滴定至颜色由红变蓝,再准确加入3mLEDTA标准滴定溶液,摇匀。记录加入EDTA标准滴定溶液的总体积。再用硫酸镁标准溶液(5.2.5.2.2e)回滴至稳定的红色,记录所用硫酸镁标准溶液的体积。加入约1g二乙基二硫代氨基甲酸钠(5.2.5.2.2b),摇匀。用硫酸镁标准溶液(5.2.5.2.2e)滴定释放出的EDTA,直至颜色改变。记录所用硫酸镁标准溶液的体积。用移液管量取上述用的盐酸萃取溶液(5.2.1)20mL,用水稀释至50mL,加入1~2滴甲基橙溶液(5.2.5.2.2g),用氨水(5.2.5.2.2a)中和,再多加1mL氨水,并加入10mL氰化钾溶液(5.2.5.2.2c)及0.25g铬黑T指示剂(5.2.5.2.2f)。用EDTA标准滴定溶液滴定至颜色改变,记录所用EDTA标准滴定溶液的体积。
5.2.5.2.5结果的表示
镉的质量百分数以Wcas表示,按式(7)计算:VcX0.1124×100
V1V.X0.1124
颜料的“可溶性”锌含量W益·s,以锌质量百分数表示,按式(8)计算:(7)
Wz·s-
HG2351—92
s+Vs+Ve)) ·c×0. 065 4×100Vama
V, (Vs-(V++Ve+Ve))X0. 065 4
式中:V1一一由第5.2.1条所述萃取用盐酸与乙醇的体积之和(采用的是77mL),mL;V2——测定用盐酸与乙醇萃取溶液的体积(采用的是20mL),mL;V:滴加到试验溶液中的EDTA标准滴定溶液的总体积,mL;V4一一加入二乙基二硫代氨基甲酸钠之前,滴定用硫酸镁标准溶液的体积,mL;Vs一一加入二乙基二硫代氨基甲酸钠之后,滴定用硫酸镁标准溶液的体积,mL;Ve—一滴定用氰化钾处理的溶液所用EDTA标准滴定溶液的体积,mL;ci——硫酸镁标准溶液的浓度,mol/L;C2——EDTA标准滴定溶液的浓度,mol/L;m—一由第5.2.1条所述制备盐酸萃取溶液所用试样的质量(采用的是5.00土0.01g),g;(8)
0.1124—与1.00mL硫酸镁标准溶液Cc(MgSO,)=1.000mol/L)相当的,以克表示的镉的质量;一与1.00mLEDTA标准滴定溶液[c(EDTA)=1.000mol/LJ相当的,以克表示的锌的质量。0.0654-
5.2.6“可溶性”铬含量的测定
按GB9758.6所述的方法测定颜料样品的*可溶性”铬含量。并用GB9758.6中7.1条的公式(1计算盐酸萃取溶液中“可溶性”铬的质量m。乘以10/m(m为制备盐酸萃取溶液所用试样的质量,采用的是5.00士0.01g),计算颜料的“可溶性”铬含量。5.2.7“可溶性”铅含量的测定
按GB9758.1第3章所述的方法(火焰原子吸收光谱法)测定颜料样品的“可溶性”铅含量。并用GB9758.1中3.5.1.1条公式(1)计算盐酸萃取溶液中可溶性”铅的质量m。乘以10/m4(m4为制备盐酸萃取溶液所用试样的质量,采用的是5.00士0.01g),计算颜料的可溶性”铅含量。5.2.8“可溶性”硒含量的测定
5.2.8.1原理
硒与3,3'-二氨基联苯胺盐酸盐形成的有色络合物用甲苯萃取之后,在波长420nm处,用分光光度计测定有机相的吸光度。
5.2.8.2试剂
5.2.8.2.1甲酸溶液:100g/L。
氨水:0.91g/mL。
5.2.8.2.2
5.2.8.2.3EDTA溶液:120g/L。
5.2.8.2.4高氯酸:p约为1.67g/mL。硝酸:p约为1.40g/mL。
5.2.8.2.5
5.2.8.2.6间甲酚紫溶液,1g/L:取0.1g间甲酚紫和一粒氢氧化钠,加10mL水,微热溶解,冷却至室温后,稀释至100mL。5.2.8.2.73,3'-二氨基联苯胺盐酸盐溶液:5g/L。5.2.8.2.8甲苯。
5.2.8.2.9硫酸钠:400℃锻烧1~2h。5.2.8.2.10硒标准贮备溶液,每升含1g硒(Se):将1.0000g纯硒粉用最少量的硝酸溶解,置于水浴上蒸干。加水溶解,移入到1000mL容量瓶中,稀释至刻度并充分混匀。
此标准贮备溶液1mL含1mg硒(Se)。HG2351—92
5.2.8.2.11硒标准溶液,每升含10mg(Se):此溶液应在使用的当天制备。
移取10mL硒标准贮备溶液于1000mL容量瓶中,稀释至刻度并充分混勾。此标准溶液1mL含10ug硒(Se)。
5.2.8.3仪器
一般实验室仪器和
5.2.8.3.1分光光度计:适于在波长420m处测量,配有厚度为50mm的吸收池。5.2.8.3.2水浴:能保持在100℃。5.2.8.3.3移液管:10mL。
5.2.8.3.4滴定管:10mL。
5.2.8.3.5容量瓶:50mL和1000mL。5.2.8.3.6分液漏斗:100mL。
5.2.8.4操作步骤
5.2.8.4.1标准比对溶液的制备
用滴定管向5只250mL锥形瓶中分别加入表3所示体积的晒标准溶液(5.2.8.2.11)。表3硒的标准比对溶液
标准比对溶液
注:1)空白溶液。
硒标准溶液(5.2.8.2.11)的体积mL
标准比对溶液中硒的相应浓度Www.bzxZ.net
μg/mL
向每份溶液中加入3mL高氯酸(5.2.8.2.4),加热蒸发至体积为2mL,冷却至室温。加50mL水5mLEDTA溶液(5.2.8.2.3)及2滴间甲酚紫溶液(5.2.8.2.6),滴加氨水(5.2.8.2.2)直至颜色变黄。而后加2mL甲酸溶液(5.2.8.2.1)和2mL3,3-二氨基联苯胺盐酸盐溶液5.2.8.2.7),混匀。置于沸水浴中加热5min,取出,冷却至室温。滴加氨水(5.2.8.2.2)直至颜色变紫。将溶液移入分液漏斗中,用20mL甲苯(5.2.8.2.8)萃取30s。将有机相移入50mL容量瓶中,用3g硫酸钠(5.2.8.2.9)进行干燥。
5.2.8.4.2分光光度法测量
用分光光度计在波长420nm处,以参比池中的甲苯(5.2.8.2.8)为参照,测量各标准比对溶液的吸光度。每次测量之前,要用标准比对溶液冲洗吸收池,分别将各标准比对溶液的吸光度值减去空白溶液的吸光度值。
5.2.8.4.3标准曲线绘制
以标准比对溶液中硒的浓度(以g/mL计)为横坐标,相应的吸光度值为纵坐标,绘制标准曲线。如果准确地按操作步骤进行,则此标准曲线应为一条直线。5.2.8.4.4测定
进行两份样品的平行测定。
用移液管量取一定体积的按5.2.1条所述的操作步骤制备的盐酸萃取溶液和空白试验溶液,置于10
HG2351—92
250mL锥形瓶中。所取盐酸萃取溶液的体积数应能使其吸光度值处于标准曲线的范围之内。加10mL硝酸(5.2.8.2.5)和4mL高氯酸(5.2.8.2.4),加热蒸发至体积为2mL。按5.2.8.4.1条的操作步骤处理溶液。而后按5.2.8.4.2条的操作步骤测量吸光度值。5.2.8.5结果的表示
硒的质量百分数以Ws·s表示,按式(9)计算:20(a1-ao)X10-6
_20(a1-ao)·V1×10-4
V2·m4
式中:ao——由标准曲线上测得的空白比对溶液中硒的浓度,g/mL;a
一由标准曲线上测得的试样比对溶液中硒的浓度,g/mL;V1—一由5.2.1条所述萃取用盐酸与乙醇的体积之和(采用的是77mL),mL;V2——测定用盐酸和乙醇萃取溶液的体积,mL;20一一测定中萃取有机相用甲苯的体积(采用的是20mL),mL;m——由5.2.1条所述制备盐酸萃取溶液所用试样的质量(采用的是5.00士0.01g),g。5.2.9“可溶性”锌含量的测定
5.2.9.1火焰原子吸收光谱法(仲裁法)(9)
将试验溶液吸入到乙炔-空气火焰中,测量由锌空心阴极灯或锌无极放电灯发射的选择谱线波长在213.9nm处的吸收。
5.2.9.1.1试剂和材料
盐酸:c(HCI)=0.07mol/L;
乙炔:工业用,装在钢瓶中;
c.压缩空气;
d锌标准贮备溶液:每升含1g锌(Zn),在1000mL容量瓶中,将4.3980g七水合硫酸锌(ZnSO,·7H2O)溶于盐酸,用同一盐酸稀释至刻度并充分混匀。此标准贮备溶液1mL含1mg锌(Zn);e。锌标准溶液:每升含10mg锌(Zn),此溶液应在使用的当天制备。移取10mL锌标准贮备溶液于1000mL容量瓶中,用盐酸稀释至刻度并充分混勾。此标准溶液1mL含10ug锌(Zn)。5.2.9.1.2仪器
通常使用二等实验玻璃仪器,但在有争议时,应采用一等仪器。一般实验室仪器和
火焰原子吸收光谱仪:适合于波长在213.9nm处测量,并装有一个可通入乙炔和空气的燃烧a.
锌空心阴极灯或锌无极放电灯;b.
移液管:10mL;
滴定管:10mL;
e.容量瓶:100mL和1000mL。
5.2.9.1.3操作步骤
a.标准参比溶液的制备
用滴定管向7只100mL容量瓶中分别加入表3所示体积的锌标准溶液(5.2.9.1.1e),用盐酸(5.2.9.1.1a)稀释至刻度并充分混匀。b。光谱测量
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。






 ✕
✕