JB/T 10053-1999
基本信息
标准号: JB/T 10053-1999
中文名称:铅酸蓄电池用水
标准类别:机械行业标准(JB)
英文名称: Water for lead-acid batteries
标准状态:现行
发布日期:1999-08-06
实施日期:2000-01-01
出版语种:简体中文
下载格式:.rar.pdf
下载大小:423849
标准分类号
中标分类号:电工>>电源>>K84蓄电能装置
关联标准
替代情况:ZB K84004-1989
出版信息
出版社:机械工业出版社
页数:12页
标准价格:16.0 元
出版日期:2000-01-01
相关单位信息
起草人:庄雅静
起草单位:沈阳蓄电池研究所
提出单位:全国铅酸蓄电池标准化技术委员会
发布部门:中华人民共和国机械工业部
标准简介
本标准规定了铅酸蓄电池用水的要求试验方法、检验原则、标志、包装、运输、贮存和使用。本标准适用于铅酸蓄电池用水。本标准不适用于密封式铅酸蓄电池用水。 JB/T 10053-1999 铅酸蓄电池用水 JB/T10053-1999 标准下载解压密码:www.bzxz.net
标准图片预览




标准内容
JB/T 10053-1999
本标准是对ZBK84004一89《铅酸蓄电池用水》进行的修订。本标准编写格式和规则采用GB/T1.1一1993,以保证标准编写的统-~,尽可能与国际一致。本标准与ZBK84004一89标准比较主要在下列部分有变化:一增加前言;
一章、条按照内容的变化重新编排;-4.1(增加抽样);
—4.2(增加外观检验);
-4.9.3试剂和溶液中增加硫酸亚铁铵溶液;——4.9.4增加比值的校正。
本标准自实施之日起,同时代替ZBK84004—89。本标准由全国铅酸蓄电池标准化技术委员会归口。本标准由沈阳蓄电池研究所负责起草。本标主要起草人:庄雅静。
本标准于1989年3月首次发布,1998年第一次修订。108
1范围
中华人民共和国机械行业标准
铅酸蓄电池用水
Water For Lead Acid Storage BatteriesJB/T 10053—1999
代替ZBK84004—89
本标准规定了铅酸蓄电池用水的要求,试验方法、检验原则、标志、包装、运输、贮存和使用。本标准适用于铅酸蓄电池用水。本标准不适用于密封式铅酸蓄电池用水。2引用标准
下列标准所包含的条文,通过在本标准中引用而构成为本标准的条文。在标准出版时,所示版本均为有效。所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。GB/T 1. 4--1988
GB/T 622--1989
GB/T 625—1989
GB/T 626-1989
GB/T 629--1981
GB/T 631—1989
GB/T 643—1988
GB/T 647--1993
GB/T 655--1994
GB/T 661--1992
GB 1254—1990
GB/T 1266—1986
GB/T 1272-1988
GB/T 1288—1992
GB/T 1293—1989
GB/T 1401—1985
GB/T 6685—1986
GB/T 10729--1989
GB 12595—1990
HG 3-918—1976
HG 3—1067—1977
HG 2306--1980
标准化工作导则化学分析方法标推编写规定化学试剂盐酸
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
氢氧化钠
高锰酸钾
硝酸钾
过硫酸铵
硫酸亚铁铵
工作基准试剂草酸钠
氯化钠
碘化钾
酒石酸钾钠
1,10—菲罗啉
乙二胺四乙酸二钠
盐酸羟胺
工作基准试剂(容量)
硝酸银
化学试剂
化学试剂
化学试剂
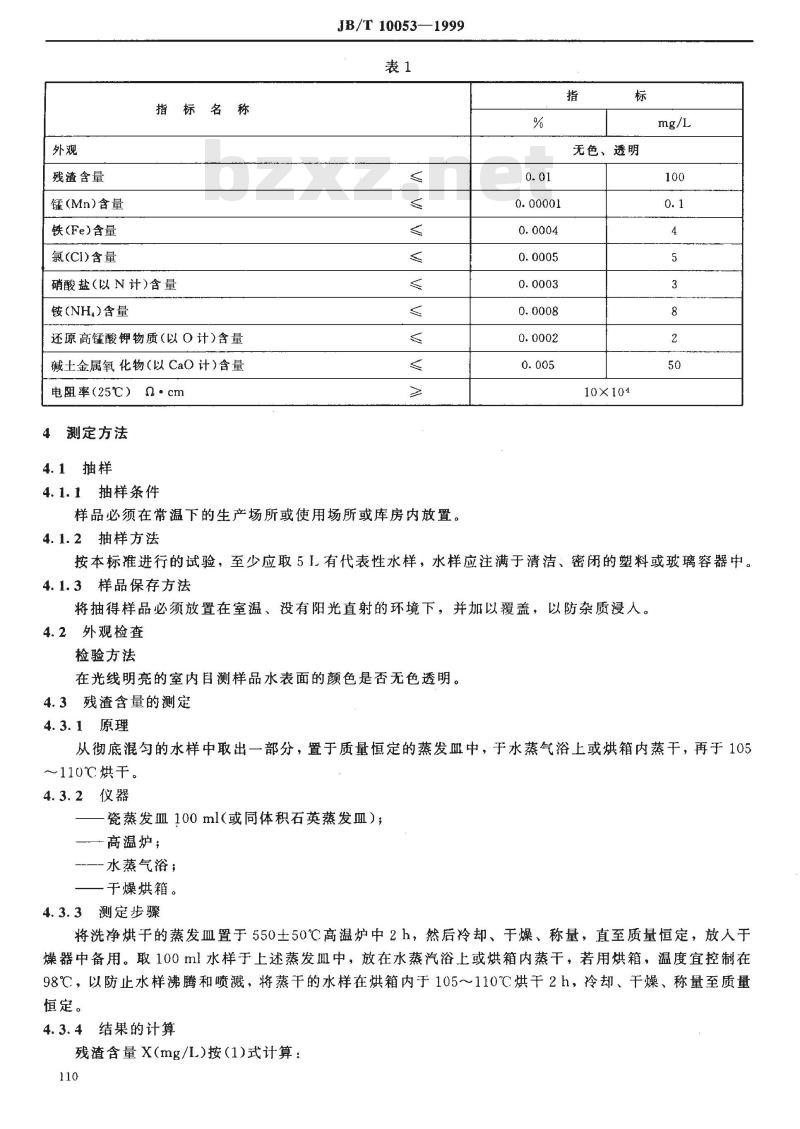
铅酸蓄电池用水应符合表1要求。国家机械工业局1999-08—06批准铬酸钾
氯化汞
氢氧化钾
2000—01-01实施
残渣含量
锰(Mn)含量
铁(Fe)含量
氯(CI)含量
指标名称
硝酸盐(以N计)含量
铵(NH)含量
还原高锰酸钾物质(以O计)含量碱土金属氧化物(以CaO计)含量电阻率(25℃)α·cm
测定方法
4.1抽样
4.1.1抽样条件
JB/T10053—1999
样品必须在常温下的生产场所或使用场所或库房内放置。4.1.2抽样方法
无色、透明
10×104
按本标准进行的试验,至少应取5L有代表性水样,水样应注满于清洁、密闭的塑料或玻璃容器中。4.1.3样品保存方法
将抽得样品必须放置在室温、没有阳光直射的环境下,并加以覆盖,以防杂质浸人。4.2外观检查
检验方法
在光线明亮的室内目测样品水表面的颜色是否无色透明。4.3残渣含量的测定
4.3.1原理
从彻底混匀的水样中取出一部分,置于质量恒定的蒸发Ⅲ中,于水蒸气浴上或烘箱内蒸干,再于105~110℃烘干。
4.3.2仪器
-瓷蒸发血100ml(或同体积石英蒸发血);-高温炉;
水蒸气浴;
-干燥烘箱。
4.3.3测定步骤
将洗净烘于的蒸发血置于550土50℃高温炉中2h,然后冷却、于燥、称量,直至质量恒定,放入于燥器中备用。取100ml水样于上述蒸发Ⅲ中,放在水蒸汽浴上或烘箱内蒸干,若用烘箱,温度宜控制在98℃,以防止水样沸腾和喷溅,将蒸干的水样在烘箱内于105~110℃烘干2h,冷却、干燥、称量至质量恒定。
4.3.4结果的计算
残渣含量X(mg/L)按(1)式计算:110
式中: m2
残渣及蒸发血质量,g;
mi-—发皿质量,g;
V-水样体积,ml。
4.4锰含量的测定
4.4.1原理
JB/T 10053—1999
(m2-m)X1000
在硝酸银存在下,以过硫酸铵将可溶性亚锰化合物氧化高锰酸盐,与标准色列比色测定。4.4.2仪器
分光光度计;
—一实验室一般仪器。
4.4.3试剂和溶液
—硝酸(GB/T626)分析纯,1+1溶液;一硝酸银(GB/T670)分析纯,5%溶液;--过硫酸铵(GB/T655)分析纯;锰标准溶液0.010mg/ml。
称取金属锰(99.99%)0.1000g于200ml烧杯中,加人1十110ml硝酸溶液,加热溶解,冷却后用水移入1000ml容量瓶中,并稀释至刻度,摇匀。作为锰标准贮备液(0.100mg/ml),每次使用时,吸取10ml贮备液准确稀释至100ml,作为锰标准溶液。4.4.4测定步骤
4.4.4.1标准曲线的绘制
分别吸取锰标准溶液0.00,0.50,1.50,2.50,4.00,5.00ml于50ml比色管中,加水至40ml左右,各加人1十1硝酸溶液1.5ml,摇匀。5%硝酸银溶液1ml,摇匀。过硫酸铵0.5g,置于沸水浴上10min,冷却后以水稀至刻度,混匀,于525nm波长处,以试剂空白为参比,测定吸光度值。4.4.4.2水样测定
吸取50.0ml水样于锥形瓶中,加1十1硝酸溶液1.5ml,加热蒸发至约40ml,加5%硝酸银溶液1ml,过硫酸铵0.5g,于沸水浴上10min,冷却后移人50ml比色管中,以水稀释至刻度,混匀,下同标准曲线操作步骤,也可用目视比色。4.4.5结果的计算
从标准曲线上查出吸光度所对应的锰含量水样中锰含量X(mg/L)按(2)式计算:m-mX1000
式中:m—由标准曲线上查出的水样中的锰含量,mg;V水样体积,ml。
4.5铁含量的测定
4.5.1原理
二价铁离子与邻菲罗琳在水溶液中反应生成橙红色铬合物,吸收峰在510nm处,有色溶液的吸光度与二价铁离子的浓度成正比。颜色强度在pH3~9间不变,长时间稳定。4.5.2仪器
一分光光度计;
—实验室一般仪器。
4.5.3试剂和溶液
JB/T 10053-—1999
盐酸(GB/T622)分析纯,1+9溶液;硝酸(GB/T626)分析纯,1+1溶液;氮水(GB/T631)分析纯;
邻菲罗啉(GB/T1293)分析纯,0.12%溶液;盐酸羟胺(HG3-967)分析纯,10%溶液:铁标准溶液0.010mg/ml。
称取金属铁(99.99%)0.1000g于200ml烧杯中,加人1+1硝酸溶液10ml,加热使其溶解,煮沸去除氮氧化物,冷却,移人1000ml容量瓶中,用水稀至刻度,混匀,作为铁标准贮备液,每次使用时,吸取10ml贮备液准确稀释至100ml,作为铁标准溶液。4.5.4测定步骤
4.5.4.1标准曲线的绘制
分别吸取铁标准溶液0.00,0.25,0.50,0.75,1.00,1.50ml于50ml比色管中,用水稀至刻度,各管加人1十9盐酸溶液1ml,混匀,加10%盐酸羟胺溶液1ml,摇匀,0.12%邻菲罗啉溶液1ml,摇匀,再加人氨水0.2ml,摇匀,用分光光度计,于510nm波长下测定吸光度。4.5.4.2水样测定
吸取50.0ml水样于50ml比色管中,加人1+9盐酸溶液1ml,下同制标准曲线操作步骤,也可用目视比色。
4.5.5结果的计算
从标准曲线上查出吸光度所对应的铁含量。水样中铁含量X(mg/I)按(3)式计算:=m×1000
式中:m—由标准曲线上查出的水样中的铁含量,mg;V一水样体积,ml。
4.6氯含量的测量
4.6.1原理
(3)
硝酸银与氯化物生成氯化银沉淀,用铬酸钾作指示剂,当水样中的氯化物与硝酸银全部作用后,多加人的硝酸银即与铬酸钾生成红色的铬酸银。因为氯化银的溶解度小于铬酸银,所以铬酸银的出现表示溶液中的氯化物已沉淀完全,反应已达到终点。4.6.2仪器
一实验室一般仪器。
4.6.3试剂和溶液
—氯化钠(GB/T1266)分析纯,标准溶液C1-1=1mg/ml。取分析纯氯化钠于清洁的中,加热至500~600℃,冷却后称取1.6480g,溶于水中,移人1000ml容量瓶中,以水稀至刻度。此溶液1ml含氯离子 1 mg。
硝酸银(GB/T670)分析纯,标准溶液。取分析纯硝酸银于105~110℃烘箱内1h,取出放人干燥器冷却后称取2.3950g放人烧杯中加水使其溶解,倾人1000ml容量瓶中,用水稀至刻度。此溶液1ml约相当于0.50mg的氯化物。硝酸银标准溶液的标定:
吸取氯化钠标准溶液10.0ml于瓷蒸发Ⅲ中,加10.0ml水,于另一蒸发皿中加20.0ml水作为滴定时比较终点颜色的空白。
各皿中加人铬酸钾溶液1ml,分别用滴定管滴人硝酸银标准溶液,用玻璃棒不断搅拌至生成淡砖红色为止。
JB/T 10053—1999
X为1ml硝酸银溶液所相当的氯化物量(mg)。V
X=V-V,=V,-V
式中:V-氯化钠标准溶液用量,ml;V,一一水对硝酸银标准溶液用量,ml;V2-—标定氯化钠溶液时硝酸银标准溶液用量,ml;校正硝酸银溶液浓度,使1.00ml相当于0.50mg的氯化物。铬酸钾(HG3一918)分析纯,5%溶液;(4)
称取5g铬酸钾,溶于少量水中,加人硝酸银标准溶液至红色沉淀不褪,搅拌均匀后,放置过夜,用滤纸过滤,滤液用水稀释至100ml。酚酸(HGB3039)分析纯,0.5%溶液;称取0.5g酚酞,溶于50mi95%的乙醇中,加50ml水;硫酸(GB/T625)分析纯,0.025mol/I.溶液;一一氢氧化钠(GB/T629)分析纯,0.025mol/L溶液。4.6.4测定步骤
吸取100ml水样水蒸发血中,加人酚溶液4滴,用0.025mo1/1.的硫酸或0.025mol/l的氢氧化钠溶液调节水样的pH值,使红色刚变为无色,另取100ml离子交换水于另一蒸Ⅲ中,各中加人1ml铬酸钾溶液用滴定管滴入硝酸银标准溶液,用玻璃棒不断搅拌,直至产生淡砖红色为止。4.6.5结果的计算
水样中的氯含量X(mg/L)按(5)式计算:(Vz-V1)×0.50X1000
式中:V2——水样滴定用去硝酸银标准液用量,ml;V,—一离子交换水滴定用硝酸银标准液用量,ml;V—一水样体积,ml。
4.7硝酸盐含量的测定
4.7.1原理
(5)
马钱子碱在硫酸溶液中和硝酸盐生成黄色化合物,其颜色强度和硝酸盐浓度成比例关系,此法测定条件较严,标准色列和水样应严格保持同一条件下进行。本法采用目视比色,也可在410nm波长下分光测定。
4.7.2仪器
实验室一般仪器。
4.7.3试剂和溶液
-硫酸(GB/T625)分析纯,溶液500+75;一盐酸(GB/T622)分析纯;
马钱子碱(危规32003)分析纯—一对氨基苯磺酸(HG3--992)分析纯溶液。称取1.0g马钱子碱硫酸盐或0.78g马钱子碱和0.10g对氨基苯碘酸,溶于水中,溶于70ml热水中,加入3ml盐酸,冷却后,稀至100ml。(此液可使用数月,最好贮于棕色瓶中在5℃下保存,马钱子碱是剧毒药,倍加小心使用)。-—硝酸钾(GB/T 647)标准溶液,NOs—N0.010 mg/ml。称取0.7216g硝酸钾溶于水中,在容量瓶中稀释至1000ml,此液为硝酸钾贮备液,NO3-N的浓度为0.100mg/ml,每星期新配制硝酸钾标准液,吸取10.0ml贮备液准确稀释至100ml。4.7.4测定步骤
4.7.4.1标准色列的配制
JB/T 10053-1999
分别吸取硝酸钾标准溶波0.00,0.10,0.30,0.50,0.70,1.00,1.50,2.00ml.于50ml烧杯中(不足2ml的以水补足至2ml)加入1ml马钱子碱一一对氨基苯磺酸溶液然后小心地加人硫酸溶液10ml,充分混匀,在暗处放置10min,各杯中加人水10ml,为充分混合,可另备50ml烧杯来回倒几次,再在暗处放置10min转入50ml比色管中,即成标准色列。4.7.4.2水样测定
在配制标准色列的同时,吸取2.0ml水样于50ml烧杯中,加人马钱子碱一一对氨基苯溶液1ml。以下测定步骤同标准色列配制步骤。用目视比色法测定。
4.7.5结果的计算
从对应的标准色列得出NO;一N的含量水样中硝酸盐氮(NO;一N)X(mg/L)按(6)式计算:m_m×1000
式中:m——相对应的标准色列中 NO:-N的含量,mg;V—一水样体积,ml。
4.8铵(NH+)含量的测量
4.8.1原理
铵盐中的 NH+与OH-生成 NH~和 H2O。氨与碘化汞钾在碱性溶液中反应,能形成淡黄色到褐色的络合物,其色度与氮含量成正比。氮的含量在0.05~5mg/.范围内,比色法可得到良好的结果。4.8.2仪器
——分光光度计。
4.8.3试剂和溶液
一无氨水在每升离子交换水中加25ml5%氢氧化钠溶液,并煮沸1h;一氢氧化钠(GB/T629)分析纯,5%溶液;一碘化钾(GB/T1272)分析纯;
—氯化汞(HG3—1068)分析纯;氢氧化钾(HGB一3006)分析纯,50%溶液;一酒石酸钾钠(GB/T1288)分析纯,50%溶液;一碱性碘化汞试剂。
溶解50g碘化钾于50ml无氨水中,另将35g氯化汞溶于150ml煮沸过的无氨水中,将热的氯化汞溶液在不断搅拌下徐徐注人碘化钾溶液中,直到生成的红色沉淀不再溶解时为止。用玻璃丝过滤,在滤液中加人氢氧化钾溶液300ml,氯化汞溶液5ml,再用无氨水稀释至1L。溶液保存在棕色瓶中,若再有沉淀产生,可待沉淀沉降后,取上层清液应用。一氯化铵标准溶液0.010mg/ml。称取0.2970g在90℃干燥过的氯化铵(GB/T658)分析纯溶于无氨水中,在容量瓶中稀释至100ml,作为铵标准贮备液(NH+)0.100mg/ml,在每次使用时,吸取10ml铵标准贮备液,准确稀释至100ml,作为铵标准溶液。
4.8.4测定步骤
4.8.4.1标准曲线的绘制
吸取铵标准溶液0.00,0.25,0.50,1.00,1.50,2.00,2.50,3.00,4.00,5.00ml于50ml比色管中,用无氨水稀至50ml,加人酒石酸钾钠溶液0.5ml,碱性碘化汞试剂1ml,混匀放置10min。114
JB/T 10053-1999
在分光光度计上,于450nm波长处,以试剂空白为参比,测定吸光度值。以标推溶液中铵的毫克数为横坐标,对应吸光度为纵坐标绘制标准曲线。4.8.4.2水样测定
取50ml水样于50ml比色管中,加人酒石酸钾钠溶液0.5ml,下同标准曲线分析步骤。4.8.5结果的计算
从标准曲线上查出吸光度所对应的铵(NH+)含量。水样中铵(NH4)含量X(mg/L)按(7)式计算xw
m_mX1000
式中:m——由标准曲线上查出的水样中的铵含量,mg;V一水样体积,ml。
4.9还原高锰酸钾物质(O)含量测定4.9.1原理
将过量的高锰酸钾溶液注入试样,以充分氧化还原性物质,用硫酸亚铁铵溶液反滴定,求还原高锰酸钾物质含量。
4.9.2仪器
—实验室一般仪器。
4.9.3试剂和溶液
硫酸(GB/T625)分析纯;
-草酸钠(GB/T1254):基准试剂;硫酸亚铁铵(GB/T661):分析纯,C[(NH4),Fc(SO),]=0.01mol/I.的溶液,称取4g(NH,),Fe(S0)2·6H20溶解于100mL1+1的硫酸溶液中,用水稀释至1000mL;高锰酸钾(GB/T643):分析纯,C1/5KMn)4)=0.1mol/I.的标准溶液:(此标准溶液用以配制C(1/5KMO)=0.01mol/I.的标准溶液a)配制
称取3.3g高锰酸钾,溶于1050ml水中,缓和煮沸20~30min,于暗处放置一周,用玻璃棉过滤,滤液保存于棕色具磨口塞瓶中。b)标定
称取于105~110℃干燥2h的基准草酸钠0.2g,准确至0.0001g,溶于50ml.水中,加8mL浓硫酸,用C(1/5KMnO)=0.1mol/l.的高锰酸钾溶液滴定近终点时,加热至70~80℃,继续滴定至溶液所呈粉红色保持30s,同时做空白试验。c)计算
高锰酸钾的浓度C(1/5KMnO4)按(8)式计算:C(1/5 KMnO)=
式中:m——称取草酸钠的质量,g;V一高锰酸钾溶液的用量,ml.;m
M(1/2Na2C,04)
M(1/2Na2C20,)-—草酸钠的摩尔质量,g/mol。(8)
使用时将C(1/5KMnO)=0.1mol/I的高锰酸钾标准溶液用水准确稀释为C(1/5KMnO)=0. 01 mol/L.
4.9.4测定步骤
4.9.4.1·比值的校正
JB/T10053—-1999
C(1/5 KMnO)=0.01 mol/L的高锰酸钾标准溶液的用量(mI)对C[(NH),Fe(SO),}-0.01mol/L的硫酸亚铁铵溶液的用量(ml.)的比值,以K表示,按以下方法校正和计算:量取化验室分析用水100ml,于250ml锥形瓶中,加入硫酸8ml,用滴定管准确加人C(1/5KMnO4)一0.01mol/l.的高锰酸钾标准溶液10ml.,加热70~80℃,冷却至室温,准确加人C[(NH)2Fe(SO4)2J=0.01mol/I.的硫酸亚铁铵溶液10ml,立即用C(1/5KMnO,)=0.01mol/L高锰酸钾标准溶液滴至淡紫红色为终点。K=
式中:V一高锰酸钾标推溶液用量,mI,Vi-硫酸亚铁铵溶液用量,ml。
4.9.4.2试样测定
...(9)
取100ml水样注人250ml锥形瓶中,加人硫酸8ml,准确加人高锰酸钾溶液10ml,加热至70~80C,冷却至室温,准确加人C[(NH4),Fe(SO)2]=0.01mol/L的硫酸亚铁铵溶液10ml,立即用C(1/5KMnO)=0.01mol/L高锰酸钾标准溶液滴至淡紫红色为终点。4.9.5结果的计算
还原高锰酸钾物质的含量以耗氧量X(mg/1.)表示,按(10)式计算:X=(Vi-KV.)×C(/5 KMnO,)×0. 08×100Vx0.01
式中:Vi—一滴定中消耗的高锰酸钾溶液的体积,ml;Vz-滴定10ml硫酸亚铁铵溶液所消耗的高锰酸钾溶液体积,ml;C(1/5KMnO,)——高锰酸钾溶液浓度,moi/L;V--一水样体积,ml;
0.08——相当于1ml0.01mol/l.高锰酸钾标准溶液的氧())的质量,mg;K——1mlC[(NH),Fe(S),)]=0.01mol/L.的硫酸亚铁铵溶液相当C(1/5KMnO,)=0.01mol/I.高锰酸钾标准溶液的毫升数。4.10碱土金属氧化物含量的测定4.10.1原理
当水样中有铬黑T指示剂时,与水样中的钙、镁离子形成酒红色的络合物,这些络合物的不稳定常数大于EDTA(乙二胺四乙酸二钠,下同)与钙、镁离子形成的络合物的不稳定常数,所以在加人EDTA后,钙、镁离子就从指示剂形成的络合物中被夺取出来而游离出指示剂,当pH为10时,EDTA先与钙离子形成络合物,然后再与镁离子络合,滴定终点时溶液呈现铬黑T指示剂的兰色。4.10.2仪器
实验室一般仪器。
4.10.3试剂和溶液
—EDTA(GB/T 1401)分析纯标准溶液。称取3.72gEDTA溶于水中,稀释至1000ml,贮于塑料瓶或硬质玻璃瓶中,此溶液浓度约为0.01mol/L,用下法标定其准确浓度:称取金属锌(99.99%)0.6538g溶于少量盐酸中,用水在容量瓶中稀释至1000ml,摇匀。此液为0.0100mol/1锌基准溶液。吸取25.00ml锌基准溶液于250ml锥形瓶中,加25ml水,用氮水调整溶液的pH值至微碱性,加5ml缓冲液,加铬黑T指示剂5滴,用EDTA标准溶液滴定至溶液转变为兰色为终点,由(11)式计算EDTA标准溶液的浓度。
(11)
JB/T10053—-1999
式中:Ci—一为锌基准溶液的浓度,mol/l;V,—一为锌基准溶液的体积,mlV-一为滴定用的 EDTA标准溶液的体积,ml。盐酸(GB/T622)分析纯,1+1溶液;—氮水(GB/T631)分析纯,1十1溶液;氮一氯化铵缓冲溶液。
称取20g氯化铵(GB/T658)分析纯溶于500ml水中,加人浓氮水100ml,用水稀释至1000ml。铬黑T(HGB3086)分析纯,0.5%溶液。称取0.5g铬黑T,溶于10ml缓冲液中,并用无水乙醇稀至100ml,此液有效大约一个月。用下法配制的指示剂可较长期有效;称取10g铬黑T,加氯化钠(GB/T1266)100g,研磨均勾,紧塞备用。
4.10.4测定步骤
取100ml水样于锥形瓶中,用氨水调节水样至微碱性,加缓冲溶液10ml,加0.5%铬黑T指示剂5滴或加固体指示剂一小勺,立即用EDTA标准溶液滴定,滴至溶液由酒红色转变为兰色时,即到达终点。
4.10.5结果的计算
结果以氧化钙的含量X(mg/L)表示,按(12)式计算:x=cxV×100×56.08
式中:C-—EDTA标准溶液浓度,mol/I;Vi—一EDTA标准溶液用量,ml;V一一水样体积,ml;
56.08——氧化钙的摩尔质量,g。4.11电阻率的测定
4.11.1原理
电阻率的倒数是电导率。用电导仪,在同温下,测定水样电阻和已知电导率的氯化钾溶液的电阻。4.11.2仪器
—电导率仪;
电导电极。
4.11.3测定步骤
按所用的电导仪的说明,本仪器大体按下列步骤:预热、调零、校正、预热和测量(由大电导率逐挡下降测定)。
4.11.4结果的计算
直接由仪器读出电导率,单位为μS/cm。其倒数为电阻率,单位为Q·cm。5检验规则
5.1检验分类Www.bzxZ.net
5.1.1鉴定检验
5.1.1.1制造铅酸蓄电池用水投产时,必须附有鉴定检验凭单,其技术条件应符合第3章要求。试验方法应符合第4章要求。允许用其它仪器检测蓄电池用水杂质,但仲裁时采用本标准规定的方法。5.1.1.2当制造铅酸蓄电池用水的主要设计、工艺、材料及零部件(元器件)变更后或停产后恢复生产时,应进行鉴定检验。
5.1.2质量致性检验
5.1.2.1A组检验(逐批)
JB/T10053-1999
当制造铅酸蓄电池用水经鉴定检验并投人正常生产时,可选用电阻率为代表性检测项目。以此检验与控制水质的一致性,当电阻率不合格时,则必须按本标准第3章技术要求进行其他项的检验。5.1.2.2B组检验(逐批)
经长期贮存的铅酸蓄电池用水,使用前如对质量产生怀疑,应进行下列检验。对于非铁质和非聚氯乙稀容器贮存的水,应进行电阻率测定,合格时,按本标准第3章技术要求,继续进行其他项检验,不合格时,允许复验,复验合格后,按本标准第3章技术要求继续进行其他项检验。对于铁质容器贮存的水,应进行电阻率和铁质含量的检验,合格时,按本标准第3章技术要求,继续进行其他项检验,不合格时,允许复验,复验合格后,按本标准第3章技术要求,继续进行其他项检验。
对于材质为聚氯乙稀容器贮存的水,应进行电阻率和氯含量的检验,合格时,按本标准第3章要求,继续进行其他项检验,不合格时,允许复验,复验合格后,按本标准第3章技术要求,继续进行其他项检验。
5.1.2.3C组检验(周期)
当铅酸蓄电池用水制作方法改变或水源发生变化时,应进行周期性的检验,直至水质符合第3章技术要求。
选用电阻率为代表性检测项目,合格时,按本标准第3章技术要求,继续进行其他项检验。5.2判定规则
5.2.1正常生产的水样检验,按本标准电阻率规范判别合格与否。5.2.2首批水样以及各种特殊情况下的水样的检验分两步进行。首先进行电阻测定,合格后,按本标准第3章要求进行其他项检验,判别合格与否。5.2.3对水样产生怀疑时,可重新取样检验,判定规则按5.2.1或5.2.2执行。5.2.4经检验合格的水,每个贮存容器上都应备有检查员签属的合格证。6标志、包装、运输、贮存和使用6.1标志
6.1.1铅酸蓄电池用水的贮存容器,应在明显可见的位置上附有标记。6.1.2产品标记
产品标记由下列三部分组成,并按表2顺序排列:表2
产品名称
铅酸蓄电池用水
6.1.3标记示例
蒸馏水
技术特性
离子交换水
电渗析水
反渗透水
电渗析一离子交换水
反渗透一离子交换水
用离子交换法制取的铅酸蓄电池用水。铅酸蓄电池用水离子交换水JB/T10053-1999。6.2包装
标准号
JB/T10053—1999
JB/T10053--1999
6.2.1铅酸蓄电池用水应装于塑料陶瓷或玻璃等专用密闭容器内,陶瓷坛或玻璃瓶容器可置于木箱中容器周围应衬草或刨花等防震隔离物。6.2.2每批铅酸蓄电池用水都应附有质量证明书,内容包括:制造厂名、产品名称、商标、产品出厂日期(或编号)或生产批号、分析结果,净重(毛重),检验单位印章和本标准编号。6.2.3包装箱的明显部位应标明制造厂名、产品名称、净重(毛重)和本标准编号的标记。6.3运输
运输条件:装卸时应轻拿轻放,运输过程中应尽量防止震动,以免贮存容器的破裂。6.4贮存
6.4.1贮存场所:专用库房或场地。6.4.2存条件:室温、没有阳光直射,无外界杂质沾污。6.4.3贮存期限:以使用前检验合格为极限。6.5使用
使用铅酸蓄电池用水时,可采用倾倒或导管排放法。119
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
本标准是对ZBK84004一89《铅酸蓄电池用水》进行的修订。本标准编写格式和规则采用GB/T1.1一1993,以保证标准编写的统-~,尽可能与国际一致。本标准与ZBK84004一89标准比较主要在下列部分有变化:一增加前言;
一章、条按照内容的变化重新编排;-4.1(增加抽样);
—4.2(增加外观检验);
-4.9.3试剂和溶液中增加硫酸亚铁铵溶液;——4.9.4增加比值的校正。
本标准自实施之日起,同时代替ZBK84004—89。本标准由全国铅酸蓄电池标准化技术委员会归口。本标准由沈阳蓄电池研究所负责起草。本标主要起草人:庄雅静。
本标准于1989年3月首次发布,1998年第一次修订。108
1范围
中华人民共和国机械行业标准
铅酸蓄电池用水
Water For Lead Acid Storage BatteriesJB/T 10053—1999
代替ZBK84004—89
本标准规定了铅酸蓄电池用水的要求,试验方法、检验原则、标志、包装、运输、贮存和使用。本标准适用于铅酸蓄电池用水。本标准不适用于密封式铅酸蓄电池用水。2引用标准
下列标准所包含的条文,通过在本标准中引用而构成为本标准的条文。在标准出版时,所示版本均为有效。所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。GB/T 1. 4--1988
GB/T 622--1989
GB/T 625—1989
GB/T 626-1989
GB/T 629--1981
GB/T 631—1989
GB/T 643—1988
GB/T 647--1993
GB/T 655--1994
GB/T 661--1992
GB 1254—1990
GB/T 1266—1986
GB/T 1272-1988
GB/T 1288—1992
GB/T 1293—1989
GB/T 1401—1985
GB/T 6685—1986
GB/T 10729--1989
GB 12595—1990
HG 3-918—1976
HG 3—1067—1977
HG 2306--1980
标准化工作导则化学分析方法标推编写规定化学试剂盐酸
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
化学试剂
氢氧化钠
高锰酸钾
硝酸钾
过硫酸铵
硫酸亚铁铵
工作基准试剂草酸钠
氯化钠
碘化钾
酒石酸钾钠
1,10—菲罗啉
乙二胺四乙酸二钠
盐酸羟胺
工作基准试剂(容量)
硝酸银
化学试剂
化学试剂
化学试剂
铅酸蓄电池用水应符合表1要求。国家机械工业局1999-08—06批准铬酸钾
氯化汞
氢氧化钾
2000—01-01实施
残渣含量
锰(Mn)含量
铁(Fe)含量
氯(CI)含量
指标名称
硝酸盐(以N计)含量
铵(NH)含量
还原高锰酸钾物质(以O计)含量碱土金属氧化物(以CaO计)含量电阻率(25℃)α·cm
测定方法
4.1抽样
4.1.1抽样条件
JB/T10053—1999
样品必须在常温下的生产场所或使用场所或库房内放置。4.1.2抽样方法
无色、透明
10×104
按本标准进行的试验,至少应取5L有代表性水样,水样应注满于清洁、密闭的塑料或玻璃容器中。4.1.3样品保存方法
将抽得样品必须放置在室温、没有阳光直射的环境下,并加以覆盖,以防杂质浸人。4.2外观检查
检验方法
在光线明亮的室内目测样品水表面的颜色是否无色透明。4.3残渣含量的测定
4.3.1原理
从彻底混匀的水样中取出一部分,置于质量恒定的蒸发Ⅲ中,于水蒸气浴上或烘箱内蒸干,再于105~110℃烘干。
4.3.2仪器
-瓷蒸发血100ml(或同体积石英蒸发血);-高温炉;
水蒸气浴;
-干燥烘箱。
4.3.3测定步骤
将洗净烘于的蒸发血置于550土50℃高温炉中2h,然后冷却、于燥、称量,直至质量恒定,放入于燥器中备用。取100ml水样于上述蒸发Ⅲ中,放在水蒸汽浴上或烘箱内蒸干,若用烘箱,温度宜控制在98℃,以防止水样沸腾和喷溅,将蒸干的水样在烘箱内于105~110℃烘干2h,冷却、干燥、称量至质量恒定。
4.3.4结果的计算
残渣含量X(mg/L)按(1)式计算:110
式中: m2
残渣及蒸发血质量,g;
mi-—发皿质量,g;
V-水样体积,ml。
4.4锰含量的测定
4.4.1原理
JB/T 10053—1999
(m2-m)X1000
在硝酸银存在下,以过硫酸铵将可溶性亚锰化合物氧化高锰酸盐,与标准色列比色测定。4.4.2仪器
分光光度计;
—一实验室一般仪器。
4.4.3试剂和溶液
—硝酸(GB/T626)分析纯,1+1溶液;一硝酸银(GB/T670)分析纯,5%溶液;--过硫酸铵(GB/T655)分析纯;锰标准溶液0.010mg/ml。
称取金属锰(99.99%)0.1000g于200ml烧杯中,加人1十110ml硝酸溶液,加热溶解,冷却后用水移入1000ml容量瓶中,并稀释至刻度,摇匀。作为锰标准贮备液(0.100mg/ml),每次使用时,吸取10ml贮备液准确稀释至100ml,作为锰标准溶液。4.4.4测定步骤
4.4.4.1标准曲线的绘制
分别吸取锰标准溶液0.00,0.50,1.50,2.50,4.00,5.00ml于50ml比色管中,加水至40ml左右,各加人1十1硝酸溶液1.5ml,摇匀。5%硝酸银溶液1ml,摇匀。过硫酸铵0.5g,置于沸水浴上10min,冷却后以水稀至刻度,混匀,于525nm波长处,以试剂空白为参比,测定吸光度值。4.4.4.2水样测定
吸取50.0ml水样于锥形瓶中,加1十1硝酸溶液1.5ml,加热蒸发至约40ml,加5%硝酸银溶液1ml,过硫酸铵0.5g,于沸水浴上10min,冷却后移人50ml比色管中,以水稀释至刻度,混匀,下同标准曲线操作步骤,也可用目视比色。4.4.5结果的计算
从标准曲线上查出吸光度所对应的锰含量水样中锰含量X(mg/L)按(2)式计算:m-mX1000
式中:m—由标准曲线上查出的水样中的锰含量,mg;V水样体积,ml。
4.5铁含量的测定
4.5.1原理
二价铁离子与邻菲罗琳在水溶液中反应生成橙红色铬合物,吸收峰在510nm处,有色溶液的吸光度与二价铁离子的浓度成正比。颜色强度在pH3~9间不变,长时间稳定。4.5.2仪器
一分光光度计;
—实验室一般仪器。
4.5.3试剂和溶液
JB/T 10053-—1999
盐酸(GB/T622)分析纯,1+9溶液;硝酸(GB/T626)分析纯,1+1溶液;氮水(GB/T631)分析纯;
邻菲罗啉(GB/T1293)分析纯,0.12%溶液;盐酸羟胺(HG3-967)分析纯,10%溶液:铁标准溶液0.010mg/ml。
称取金属铁(99.99%)0.1000g于200ml烧杯中,加人1+1硝酸溶液10ml,加热使其溶解,煮沸去除氮氧化物,冷却,移人1000ml容量瓶中,用水稀至刻度,混匀,作为铁标准贮备液,每次使用时,吸取10ml贮备液准确稀释至100ml,作为铁标准溶液。4.5.4测定步骤
4.5.4.1标准曲线的绘制
分别吸取铁标准溶液0.00,0.25,0.50,0.75,1.00,1.50ml于50ml比色管中,用水稀至刻度,各管加人1十9盐酸溶液1ml,混匀,加10%盐酸羟胺溶液1ml,摇匀,0.12%邻菲罗啉溶液1ml,摇匀,再加人氨水0.2ml,摇匀,用分光光度计,于510nm波长下测定吸光度。4.5.4.2水样测定
吸取50.0ml水样于50ml比色管中,加人1+9盐酸溶液1ml,下同制标准曲线操作步骤,也可用目视比色。
4.5.5结果的计算
从标准曲线上查出吸光度所对应的铁含量。水样中铁含量X(mg/I)按(3)式计算:=m×1000
式中:m—由标准曲线上查出的水样中的铁含量,mg;V一水样体积,ml。
4.6氯含量的测量
4.6.1原理
(3)
硝酸银与氯化物生成氯化银沉淀,用铬酸钾作指示剂,当水样中的氯化物与硝酸银全部作用后,多加人的硝酸银即与铬酸钾生成红色的铬酸银。因为氯化银的溶解度小于铬酸银,所以铬酸银的出现表示溶液中的氯化物已沉淀完全,反应已达到终点。4.6.2仪器
一实验室一般仪器。
4.6.3试剂和溶液
—氯化钠(GB/T1266)分析纯,标准溶液C1-1=1mg/ml。取分析纯氯化钠于清洁的中,加热至500~600℃,冷却后称取1.6480g,溶于水中,移人1000ml容量瓶中,以水稀至刻度。此溶液1ml含氯离子 1 mg。
硝酸银(GB/T670)分析纯,标准溶液。取分析纯硝酸银于105~110℃烘箱内1h,取出放人干燥器冷却后称取2.3950g放人烧杯中加水使其溶解,倾人1000ml容量瓶中,用水稀至刻度。此溶液1ml约相当于0.50mg的氯化物。硝酸银标准溶液的标定:
吸取氯化钠标准溶液10.0ml于瓷蒸发Ⅲ中,加10.0ml水,于另一蒸发皿中加20.0ml水作为滴定时比较终点颜色的空白。
各皿中加人铬酸钾溶液1ml,分别用滴定管滴人硝酸银标准溶液,用玻璃棒不断搅拌至生成淡砖红色为止。
JB/T 10053—1999
X为1ml硝酸银溶液所相当的氯化物量(mg)。V
X=V-V,=V,-V
式中:V-氯化钠标准溶液用量,ml;V,一一水对硝酸银标准溶液用量,ml;V2-—标定氯化钠溶液时硝酸银标准溶液用量,ml;校正硝酸银溶液浓度,使1.00ml相当于0.50mg的氯化物。铬酸钾(HG3一918)分析纯,5%溶液;(4)
称取5g铬酸钾,溶于少量水中,加人硝酸银标准溶液至红色沉淀不褪,搅拌均匀后,放置过夜,用滤纸过滤,滤液用水稀释至100ml。酚酸(HGB3039)分析纯,0.5%溶液;称取0.5g酚酞,溶于50mi95%的乙醇中,加50ml水;硫酸(GB/T625)分析纯,0.025mol/I.溶液;一一氢氧化钠(GB/T629)分析纯,0.025mol/L溶液。4.6.4测定步骤
吸取100ml水样水蒸发血中,加人酚溶液4滴,用0.025mo1/1.的硫酸或0.025mol/l的氢氧化钠溶液调节水样的pH值,使红色刚变为无色,另取100ml离子交换水于另一蒸Ⅲ中,各中加人1ml铬酸钾溶液用滴定管滴入硝酸银标准溶液,用玻璃棒不断搅拌,直至产生淡砖红色为止。4.6.5结果的计算
水样中的氯含量X(mg/L)按(5)式计算:(Vz-V1)×0.50X1000
式中:V2——水样滴定用去硝酸银标准液用量,ml;V,—一离子交换水滴定用硝酸银标准液用量,ml;V—一水样体积,ml。
4.7硝酸盐含量的测定
4.7.1原理
(5)
马钱子碱在硫酸溶液中和硝酸盐生成黄色化合物,其颜色强度和硝酸盐浓度成比例关系,此法测定条件较严,标准色列和水样应严格保持同一条件下进行。本法采用目视比色,也可在410nm波长下分光测定。
4.7.2仪器
实验室一般仪器。
4.7.3试剂和溶液
-硫酸(GB/T625)分析纯,溶液500+75;一盐酸(GB/T622)分析纯;
马钱子碱(危规32003)分析纯—一对氨基苯磺酸(HG3--992)分析纯溶液。称取1.0g马钱子碱硫酸盐或0.78g马钱子碱和0.10g对氨基苯碘酸,溶于水中,溶于70ml热水中,加入3ml盐酸,冷却后,稀至100ml。(此液可使用数月,最好贮于棕色瓶中在5℃下保存,马钱子碱是剧毒药,倍加小心使用)。-—硝酸钾(GB/T 647)标准溶液,NOs—N0.010 mg/ml。称取0.7216g硝酸钾溶于水中,在容量瓶中稀释至1000ml,此液为硝酸钾贮备液,NO3-N的浓度为0.100mg/ml,每星期新配制硝酸钾标准液,吸取10.0ml贮备液准确稀释至100ml。4.7.4测定步骤
4.7.4.1标准色列的配制
JB/T 10053-1999
分别吸取硝酸钾标准溶波0.00,0.10,0.30,0.50,0.70,1.00,1.50,2.00ml.于50ml烧杯中(不足2ml的以水补足至2ml)加入1ml马钱子碱一一对氨基苯磺酸溶液然后小心地加人硫酸溶液10ml,充分混匀,在暗处放置10min,各杯中加人水10ml,为充分混合,可另备50ml烧杯来回倒几次,再在暗处放置10min转入50ml比色管中,即成标准色列。4.7.4.2水样测定
在配制标准色列的同时,吸取2.0ml水样于50ml烧杯中,加人马钱子碱一一对氨基苯溶液1ml。以下测定步骤同标准色列配制步骤。用目视比色法测定。
4.7.5结果的计算
从对应的标准色列得出NO;一N的含量水样中硝酸盐氮(NO;一N)X(mg/L)按(6)式计算:m_m×1000
式中:m——相对应的标准色列中 NO:-N的含量,mg;V—一水样体积,ml。
4.8铵(NH+)含量的测量
4.8.1原理
铵盐中的 NH+与OH-生成 NH~和 H2O。氨与碘化汞钾在碱性溶液中反应,能形成淡黄色到褐色的络合物,其色度与氮含量成正比。氮的含量在0.05~5mg/.范围内,比色法可得到良好的结果。4.8.2仪器
——分光光度计。
4.8.3试剂和溶液
一无氨水在每升离子交换水中加25ml5%氢氧化钠溶液,并煮沸1h;一氢氧化钠(GB/T629)分析纯,5%溶液;一碘化钾(GB/T1272)分析纯;
—氯化汞(HG3—1068)分析纯;氢氧化钾(HGB一3006)分析纯,50%溶液;一酒石酸钾钠(GB/T1288)分析纯,50%溶液;一碱性碘化汞试剂。
溶解50g碘化钾于50ml无氨水中,另将35g氯化汞溶于150ml煮沸过的无氨水中,将热的氯化汞溶液在不断搅拌下徐徐注人碘化钾溶液中,直到生成的红色沉淀不再溶解时为止。用玻璃丝过滤,在滤液中加人氢氧化钾溶液300ml,氯化汞溶液5ml,再用无氨水稀释至1L。溶液保存在棕色瓶中,若再有沉淀产生,可待沉淀沉降后,取上层清液应用。一氯化铵标准溶液0.010mg/ml。称取0.2970g在90℃干燥过的氯化铵(GB/T658)分析纯溶于无氨水中,在容量瓶中稀释至100ml,作为铵标准贮备液(NH+)0.100mg/ml,在每次使用时,吸取10ml铵标准贮备液,准确稀释至100ml,作为铵标准溶液。
4.8.4测定步骤
4.8.4.1标准曲线的绘制
吸取铵标准溶液0.00,0.25,0.50,1.00,1.50,2.00,2.50,3.00,4.00,5.00ml于50ml比色管中,用无氨水稀至50ml,加人酒石酸钾钠溶液0.5ml,碱性碘化汞试剂1ml,混匀放置10min。114
JB/T 10053-1999
在分光光度计上,于450nm波长处,以试剂空白为参比,测定吸光度值。以标推溶液中铵的毫克数为横坐标,对应吸光度为纵坐标绘制标准曲线。4.8.4.2水样测定
取50ml水样于50ml比色管中,加人酒石酸钾钠溶液0.5ml,下同标准曲线分析步骤。4.8.5结果的计算
从标准曲线上查出吸光度所对应的铵(NH+)含量。水样中铵(NH4)含量X(mg/L)按(7)式计算xw
m_mX1000
式中:m——由标准曲线上查出的水样中的铵含量,mg;V一水样体积,ml。
4.9还原高锰酸钾物质(O)含量测定4.9.1原理
将过量的高锰酸钾溶液注入试样,以充分氧化还原性物质,用硫酸亚铁铵溶液反滴定,求还原高锰酸钾物质含量。
4.9.2仪器
—实验室一般仪器。
4.9.3试剂和溶液
硫酸(GB/T625)分析纯;
-草酸钠(GB/T1254):基准试剂;硫酸亚铁铵(GB/T661):分析纯,C[(NH4),Fc(SO),]=0.01mol/I.的溶液,称取4g(NH,),Fe(S0)2·6H20溶解于100mL1+1的硫酸溶液中,用水稀释至1000mL;高锰酸钾(GB/T643):分析纯,C1/5KMn)4)=0.1mol/I.的标准溶液:(此标准溶液用以配制C(1/5KMO)=0.01mol/I.的标准溶液a)配制
称取3.3g高锰酸钾,溶于1050ml水中,缓和煮沸20~30min,于暗处放置一周,用玻璃棉过滤,滤液保存于棕色具磨口塞瓶中。b)标定
称取于105~110℃干燥2h的基准草酸钠0.2g,准确至0.0001g,溶于50ml.水中,加8mL浓硫酸,用C(1/5KMnO)=0.1mol/l.的高锰酸钾溶液滴定近终点时,加热至70~80℃,继续滴定至溶液所呈粉红色保持30s,同时做空白试验。c)计算
高锰酸钾的浓度C(1/5KMnO4)按(8)式计算:C(1/5 KMnO)=
式中:m——称取草酸钠的质量,g;V一高锰酸钾溶液的用量,ml.;m
M(1/2Na2C,04)
M(1/2Na2C20,)-—草酸钠的摩尔质量,g/mol。(8)
使用时将C(1/5KMnO)=0.1mol/I的高锰酸钾标准溶液用水准确稀释为C(1/5KMnO)=0. 01 mol/L.
4.9.4测定步骤
4.9.4.1·比值的校正
JB/T10053—-1999
C(1/5 KMnO)=0.01 mol/L的高锰酸钾标准溶液的用量(mI)对C[(NH),Fe(SO),}-0.01mol/L的硫酸亚铁铵溶液的用量(ml.)的比值,以K表示,按以下方法校正和计算:量取化验室分析用水100ml,于250ml锥形瓶中,加入硫酸8ml,用滴定管准确加人C(1/5KMnO4)一0.01mol/l.的高锰酸钾标准溶液10ml.,加热70~80℃,冷却至室温,准确加人C[(NH)2Fe(SO4)2J=0.01mol/I.的硫酸亚铁铵溶液10ml,立即用C(1/5KMnO,)=0.01mol/L高锰酸钾标准溶液滴至淡紫红色为终点。K=
式中:V一高锰酸钾标推溶液用量,mI,Vi-硫酸亚铁铵溶液用量,ml。
4.9.4.2试样测定
...(9)
取100ml水样注人250ml锥形瓶中,加人硫酸8ml,准确加人高锰酸钾溶液10ml,加热至70~80C,冷却至室温,准确加人C[(NH4),Fe(SO)2]=0.01mol/L的硫酸亚铁铵溶液10ml,立即用C(1/5KMnO)=0.01mol/L高锰酸钾标准溶液滴至淡紫红色为终点。4.9.5结果的计算
还原高锰酸钾物质的含量以耗氧量X(mg/1.)表示,按(10)式计算:X=(Vi-KV.)×C(/5 KMnO,)×0. 08×100Vx0.01
式中:Vi—一滴定中消耗的高锰酸钾溶液的体积,ml;Vz-滴定10ml硫酸亚铁铵溶液所消耗的高锰酸钾溶液体积,ml;C(1/5KMnO,)——高锰酸钾溶液浓度,moi/L;V--一水样体积,ml;
0.08——相当于1ml0.01mol/l.高锰酸钾标准溶液的氧())的质量,mg;K——1mlC[(NH),Fe(S),)]=0.01mol/L.的硫酸亚铁铵溶液相当C(1/5KMnO,)=0.01mol/I.高锰酸钾标准溶液的毫升数。4.10碱土金属氧化物含量的测定4.10.1原理
当水样中有铬黑T指示剂时,与水样中的钙、镁离子形成酒红色的络合物,这些络合物的不稳定常数大于EDTA(乙二胺四乙酸二钠,下同)与钙、镁离子形成的络合物的不稳定常数,所以在加人EDTA后,钙、镁离子就从指示剂形成的络合物中被夺取出来而游离出指示剂,当pH为10时,EDTA先与钙离子形成络合物,然后再与镁离子络合,滴定终点时溶液呈现铬黑T指示剂的兰色。4.10.2仪器
实验室一般仪器。
4.10.3试剂和溶液
—EDTA(GB/T 1401)分析纯标准溶液。称取3.72gEDTA溶于水中,稀释至1000ml,贮于塑料瓶或硬质玻璃瓶中,此溶液浓度约为0.01mol/L,用下法标定其准确浓度:称取金属锌(99.99%)0.6538g溶于少量盐酸中,用水在容量瓶中稀释至1000ml,摇匀。此液为0.0100mol/1锌基准溶液。吸取25.00ml锌基准溶液于250ml锥形瓶中,加25ml水,用氮水调整溶液的pH值至微碱性,加5ml缓冲液,加铬黑T指示剂5滴,用EDTA标准溶液滴定至溶液转变为兰色为终点,由(11)式计算EDTA标准溶液的浓度。
(11)
JB/T10053—-1999
式中:Ci—一为锌基准溶液的浓度,mol/l;V,—一为锌基准溶液的体积,mlV-一为滴定用的 EDTA标准溶液的体积,ml。盐酸(GB/T622)分析纯,1+1溶液;—氮水(GB/T631)分析纯,1十1溶液;氮一氯化铵缓冲溶液。
称取20g氯化铵(GB/T658)分析纯溶于500ml水中,加人浓氮水100ml,用水稀释至1000ml。铬黑T(HGB3086)分析纯,0.5%溶液。称取0.5g铬黑T,溶于10ml缓冲液中,并用无水乙醇稀至100ml,此液有效大约一个月。用下法配制的指示剂可较长期有效;称取10g铬黑T,加氯化钠(GB/T1266)100g,研磨均勾,紧塞备用。
4.10.4测定步骤
取100ml水样于锥形瓶中,用氨水调节水样至微碱性,加缓冲溶液10ml,加0.5%铬黑T指示剂5滴或加固体指示剂一小勺,立即用EDTA标准溶液滴定,滴至溶液由酒红色转变为兰色时,即到达终点。
4.10.5结果的计算
结果以氧化钙的含量X(mg/L)表示,按(12)式计算:x=cxV×100×56.08
式中:C-—EDTA标准溶液浓度,mol/I;Vi—一EDTA标准溶液用量,ml;V一一水样体积,ml;
56.08——氧化钙的摩尔质量,g。4.11电阻率的测定
4.11.1原理
电阻率的倒数是电导率。用电导仪,在同温下,测定水样电阻和已知电导率的氯化钾溶液的电阻。4.11.2仪器
—电导率仪;
电导电极。
4.11.3测定步骤
按所用的电导仪的说明,本仪器大体按下列步骤:预热、调零、校正、预热和测量(由大电导率逐挡下降测定)。
4.11.4结果的计算
直接由仪器读出电导率,单位为μS/cm。其倒数为电阻率,单位为Q·cm。5检验规则
5.1检验分类Www.bzxZ.net
5.1.1鉴定检验
5.1.1.1制造铅酸蓄电池用水投产时,必须附有鉴定检验凭单,其技术条件应符合第3章要求。试验方法应符合第4章要求。允许用其它仪器检测蓄电池用水杂质,但仲裁时采用本标准规定的方法。5.1.1.2当制造铅酸蓄电池用水的主要设计、工艺、材料及零部件(元器件)变更后或停产后恢复生产时,应进行鉴定检验。
5.1.2质量致性检验
5.1.2.1A组检验(逐批)
JB/T10053-1999
当制造铅酸蓄电池用水经鉴定检验并投人正常生产时,可选用电阻率为代表性检测项目。以此检验与控制水质的一致性,当电阻率不合格时,则必须按本标准第3章技术要求进行其他项的检验。5.1.2.2B组检验(逐批)
经长期贮存的铅酸蓄电池用水,使用前如对质量产生怀疑,应进行下列检验。对于非铁质和非聚氯乙稀容器贮存的水,应进行电阻率测定,合格时,按本标准第3章技术要求,继续进行其他项检验,不合格时,允许复验,复验合格后,按本标准第3章技术要求继续进行其他项检验。对于铁质容器贮存的水,应进行电阻率和铁质含量的检验,合格时,按本标准第3章技术要求,继续进行其他项检验,不合格时,允许复验,复验合格后,按本标准第3章技术要求,继续进行其他项检验。
对于材质为聚氯乙稀容器贮存的水,应进行电阻率和氯含量的检验,合格时,按本标准第3章要求,继续进行其他项检验,不合格时,允许复验,复验合格后,按本标准第3章技术要求,继续进行其他项检验。
5.1.2.3C组检验(周期)
当铅酸蓄电池用水制作方法改变或水源发生变化时,应进行周期性的检验,直至水质符合第3章技术要求。
选用电阻率为代表性检测项目,合格时,按本标准第3章技术要求,继续进行其他项检验。5.2判定规则
5.2.1正常生产的水样检验,按本标准电阻率规范判别合格与否。5.2.2首批水样以及各种特殊情况下的水样的检验分两步进行。首先进行电阻测定,合格后,按本标准第3章要求进行其他项检验,判别合格与否。5.2.3对水样产生怀疑时,可重新取样检验,判定规则按5.2.1或5.2.2执行。5.2.4经检验合格的水,每个贮存容器上都应备有检查员签属的合格证。6标志、包装、运输、贮存和使用6.1标志
6.1.1铅酸蓄电池用水的贮存容器,应在明显可见的位置上附有标记。6.1.2产品标记
产品标记由下列三部分组成,并按表2顺序排列:表2
产品名称
铅酸蓄电池用水
6.1.3标记示例
蒸馏水
技术特性
离子交换水
电渗析水
反渗透水
电渗析一离子交换水
反渗透一离子交换水
用离子交换法制取的铅酸蓄电池用水。铅酸蓄电池用水离子交换水JB/T10053-1999。6.2包装
标准号
JB/T10053—1999
JB/T10053--1999
6.2.1铅酸蓄电池用水应装于塑料陶瓷或玻璃等专用密闭容器内,陶瓷坛或玻璃瓶容器可置于木箱中容器周围应衬草或刨花等防震隔离物。6.2.2每批铅酸蓄电池用水都应附有质量证明书,内容包括:制造厂名、产品名称、商标、产品出厂日期(或编号)或生产批号、分析结果,净重(毛重),检验单位印章和本标准编号。6.2.3包装箱的明显部位应标明制造厂名、产品名称、净重(毛重)和本标准编号的标记。6.3运输
运输条件:装卸时应轻拿轻放,运输过程中应尽量防止震动,以免贮存容器的破裂。6.4贮存
6.4.1贮存场所:专用库房或场地。6.4.2存条件:室温、没有阳光直射,无外界杂质沾污。6.4.3贮存期限:以使用前检验合格为极限。6.5使用
使用铅酸蓄电池用水时,可采用倾倒或导管排放法。119
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。