GB/T 4789.3-2008
基本信息
标准号: GB/T 4789.3-2008
中文名称:食品卫生微生物学检验 大肠菌群计数
标准类别:国家标准(GB)
标准状态:现行
发布日期:1984-12-25
实施日期:2009-03-01
出版语种:简体中文
下载格式:.rar.pdf
下载大小:588661

标准分类号
标准ICS号:数学、自然科学>>微生物学>>07.100.30
中标分类号:医药、卫生、劳动保护>>卫生>>C53食品卫生
关联标准
替代情况:替代GB/T 4789.3-2003
采标情况:MOD 美国食品药品管理局(FDA)《细菌学分析手册》第4章大肠杆菌和大肠菌群计数(2002年);国际分析家学会(AOAC INTERNATIONAL)AOAC 991.14《食品中大肠菌群和大肠杆菌计数Petrifilm测试片法》(1994年)
出版信息
出版社:中国标准出版社
书号:155066·1-36101
页数:10页
标准价格:14.0 元
计划单号:20061386-T-361
出版日期:2009-03-01
相关单位信息
首发日期:1984-12-25
起草人:刘秀梅、袁宝君、刘中学、刘弘、陈敏、卢行安、田静
起草单位:中国疾病预防控制中心营养与食品安全所、江苏省疾病预防控制中心等
归口单位:卫生部
提出单位:中华人民共和国卫生部
发布部门:中华人民共和国卫生部 中国国家标准化管理委员会
主管部门:卫生部
标准简介
本标准代替GB/T 4789.3-2003《食品卫生微生物学检验 大肠菌群测定》。本标准规定了食品中大肠菌群计数的方法。本标准适用于各类食品中大肠菌群的计数。本标准与GB/T 4789.3-2003相比主要修改如下:———将标准名称改为“食品卫生微生物学检验 大肠菌群计数”;———增加了大肠菌群的平板计数法和纸片检测方法;———大肠菌群的MPN(most probable number)法从以乳糖胆盐为主要培养基的MPN法,修改为以月桂基硫酸盐胰蛋白胨(lauryl sulfate tryptose,LST)肉汤为主要培养基的MPN法;———大肠菌群MPN法中原“报告每100mL(g)大肠菌群的MPN值”,修改为“报告每1mL(或1g)大肠菌群的MPN值”。 GB/T 4789.3-2008 食品卫生微生物学检验 大肠菌群计数 GB/T4789.3-2008 标准下载解压密码:www.bzxz.net
标准图片预览




标准内容
ICS 07. 100. 30
中华人民共和国国家标准
GB/T 4789.3—2008
代替 GB/T 4789.32003
食品卫生微生物学检验
大肠菌群计数
Microbiological examnination of food hygiene-Enumeration of coliforms
2008-11-21发布
中华人民共和国卫生部
中国国家标准化管理委员会
2009-03-01实施
中华人民共和
国家标准
食品卫生微生物学检验
大肠菌群计数
GB/T 4789, 3--2008
中国标准出版社出版发行
北京复兴门外三里河北街16号
邮政编码:100045
网址 www, spc, net. cn
电话:68523946
68517548
中国标准出版社案皇岛印剃厂印剧各地新华书店经销
印张0.75
开本 880×1230 1/16
字数17千学
2009年3月第一版2009年3月第一次印刷*
书号:155066·1-36101定价14.00元吉由本社发行中心调换
如有印装差错
版权专有侵权必究
举报电话:(010)68533533
http://foodmate.net前
GB/T4789.3—2008
本标准的第--法和第一法修改采用关国食品药品管理局(FDA)《细菌学分析于册》第4章大肠杆菌和人肠群计数(2002年)(BacteriologicalAnalyticalMantal,Chapler4:EnumcrationofEscherichiacoliandthecoliformbacteria,2002),第三法修改采用国际分析家学会(AOACINTERNATIONAL)AOAC991.14《食品中人肠菌群和大肠杆菌计数Pctriilm测试片法》(1994年)(AOACOfficial Method 99l, 14,Coliform and Escherichia coli counts in foods--Dry rchydratable film Petrifilt E. coli count platc: and Petrifiltn coliforfn count plate methods).本标谁与FDA和AOAC方法的主要区别是:将样品制备时样量50g(或50mL)修改为25g(或25mL);将培养温度由 35 ℃上1℃修改为 36 ℃士1 ℃。本标准代替GB/T4789.3·2003《食品卫生微牛物学检验大肠菌群测定》。本标准与GB/T4789.3—2003相比主要修改如下:-将标雅名称改为“食品卫生微生物学检验大肠菌群计数”;增加了大肠菌群的平板计数法和纸片检测方法;人肠菌群的MPN(mostprobablenumber)法从以乳糖胆盐为主要培养基的MPN法,修改为以月基硫酸盐膜蛋白(laurylsulfatetryptosc,IST)肉汤为牛要培养基的MPN法;大肠菌群MPN法中原\报告每10nmL(g)大肠菌群的MPN值”,修改为“报告每1mL(或1g)大肠菌群的MPN值”。
本标准的附录 A,附录 H为规范性附录。本标准由中华人民共和国卫牛部提出并归口,本标雅由中华人民共和国卫生部负责解释。本标准负责起草单位:中国疾病预防控制中心营养与食品安全所本标准参与起草单位:江苏省疾病预防控制中心、中华人民共和国内蒙占山人境检验检疫局、上海市疾病预防控制申心、中华人民共和国辽宁出人境检验检获局。本标准主要起草人:刘秀梅、衰宝君、刘中学、刘弘、陈敏、卢行安田静。本标准所代弊标推的历次版本发布情况为:GH 4789.3 : 1984,GB/T 4789.31994,GB/T 4789. 3--2003.1范围
食品卫生微生物学检验
大肠菌群计数
本标准规定了食品中大肠菌群计数的方法。本标准适用于各类食品中大肠菌群的计数。2术语和定义
下列术语和定义适用于本标准。2.1
大肠茵群coliforms
GB/T 4789.3—2008
-群在 36 ℃条件下培养18 h能发酵乳糖,心酸产气的需氧和兼性厌氧革兰氏阴性无芽肥杆托菌。该菌群主要米源于人畜粪便,作为粪便污染指标评价食品的卫生状说,推断食品中肠道致病菌污染的可能。
最可能数most probable number;MPN基于泊松分布的一种间接计数方法。3设备和材料
除徽生物实验室常规灭菌及培养设备外,其他设备和材料如下:3.1恒温培养箱;36℃±1℃。
3.2 冰箱:2 ℃~5 ℃
3.3恒温水浴箱:46℃11℃。
3.4天半,感量0.1g。
3.5均质器
3.6振药器。
3.7无菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)或微量移液器及吸头,3.8无菌锥形瓶:容量 500 ml。
3.9尤菌培养皿:直径90mm。
3.10pH计或 pH比色管或精密 pH试纸。3.11菌落计数器或PetririlmTmI白动判读仪。4培养基和试剂
4.1月桂基硫酸盐胰蛋白豚(lauryl sulFate1rypiose,I.ST)肉汤:见第A.1章。4.2煌绿乳糖朋盐(brilliantgreenlactosebile,BGLB)肉汤:见第A2章。4.3结晶紫中性红胆盐琼脂(violet red bile agar,VRBA),见第 A. 3 章。4.4磷酸盐缓冲液:见第A.4章。1)Petrifilm\M是由3M公司提供的产品的商品名。给出这一信息是为了方便本标准的使用者,并不表示对该产品的认可。如果其他等效产品具有相同的效果,则可使旧这些等效的产品。品成伴网h
GB/T 4789.3--2008
4.5无菌生理盐水:称取8.5g氯化钠溶于1000mL蒸馏水中,121℃离压灭菌15min。4.61 mol/1.氢氧化钠(NaQH):称 410 g氢氧化钠溶下 1 000 mL蒸馏水中。4.71mol/L.盐酸(HCl):移取浓盐酸90mL,用蒸馏水稀释至1000mL4.8PetrililmrTm人肠菌群检验测试片租压板。第法大肠菌群MPN计数
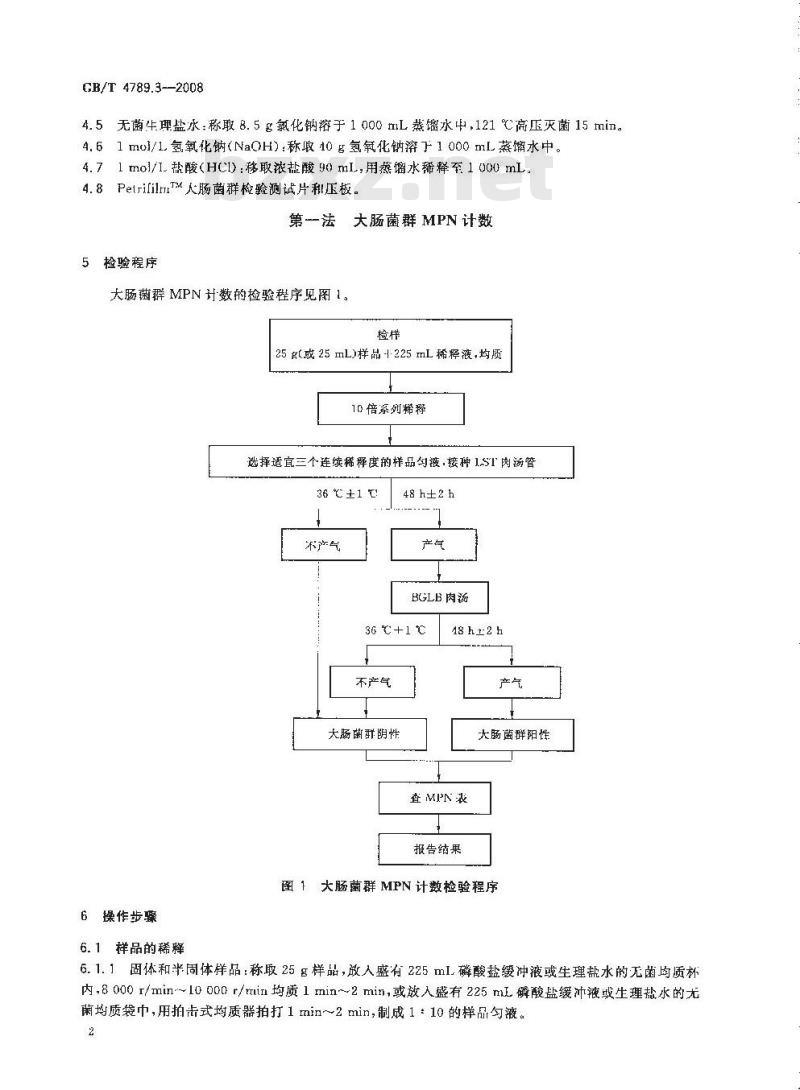
5检验程序
大肠菌群MPN计数的检验程序见图1检样
25g(或25mL)样品-225mL稀释液,均质10 倍系列稀释
选择适宜三个连续稀释度的样品勾液.接种1.ST肉汤管36 ℃±1 ℃
不产气
48 h±2 h
BGLB肉汤
不产气
大肠菌群阴性
48h±2h
大肠菌群阳性
查MPN表
报告结果
图1大肠菌群MPN计数检验程序
6操作步骤
6.1样品的稀释
6.1.1固体和半固体样品:称取25g样品,放入盛有225ml.磷酸盐缓冲液或生理盐水的无菌均质杯内,80001/min~10000r/rin均质1min~2min,或放人盛有225mL磷酸盐缓冲液或生理盐水的无菌均质袋中,用拍击式均质器拍打1min~2min,制成1=10的样品勾液。2
http:
GB/T 4789.3—2008
6.1.2液体样品:以无菌吸管吸取25mL样品,置盛有225mL磷酸盐缓冲液或生理盐水的无菌锥形瓶(瓶内预置适当数量的菌玻璃珠)中,充分混勾,制成1:10的样品匀液。6.1.3样品匀液的pH值应在6.5~7.5之间,必要时分别用1mol/L氢氧化钠(NaO)II)或1mol/L盐酸(HCI)调节。
6.1.4用1mL无菌吸管或微量移液器吸1:10样品勾液1ml,沿管缓缓注入9mL磷酸盐缓液或生理盐水的无菌试管中(注意吸管或吸头尖端不要触及稀释液面),振摇试管或换用I支!mL无菌吸管反复吹打,使其混合均匀,制成1:100的样品句液。6.1.5根据对样品污染状况的估计,按上述操作,依次制成10倍递增系列稀释样品句液。每递增稀释1次,换用1支1mL尤菌吸管或吸头。从制备样品勾液至样品接种完毕,全过程不得超过15min。6.?发酵试验
每个样品,选择3个适宜的连续稀释度的样品勾液(液体样品可以选择原液),每个稀释度接种3管月柱基硫酸盐胰蛋白陈(L.ST)肉汤,每管接种1mL(如接种量超过1mL,则用双料LST肉汤),36\C士1℃培养24h士2h,观察倒管内是否有气泡产生,如未产气则继续培养至48h土2h。记录在24h和48h内产气的LST肉汤管数。未产气者为大肠菌群阴性,产气者则进行复发醇酵试验。6.3复发酵试验
用接种环从所有18h土2h内发酵产气的LST肉汤管中分别取培养物1环,移种于熄绿乳糖胆盐(BGL13)肉汤管中,36℃上1℃培养18l土2h,观察产气情况。产气者,计为大肠菌群阳性管,6. 4大肠菌群最可能数(MPN)的报告根据大肠菌群阳性管数,检紫MPN表(见附录13),报告每克(或毫)样品中大肠菌群的MPN值。
第二法大肠菌群平板计数
7检验程序
人肠菌群平板计数的检验程序见图2。检样
25 g(或 25 mL)样品+225 1nL稀释液,均质+
10倍系列稀释
选择 2 个-~3 个适稀释度的样品勾被,接种 VRBA平板36 ℃±1 °
18 h~24 h
计数典型和可菌落
BGLB肉汤或复发酵试验
36 ±1 ℃
24 hb~~ 48 h
报告结果
图2大肠菌群平板计数检验程序
GB/T4789.3—2008
8操作步骤
8.1样品的稀释
按 6.1 逃行。
8.2平板计数
8.2.1选取2个~3个适宜的连续稀释度,每个稀释度接种两个无菌平匪,每1ml.。同时分别取1 ml. 生理盐水加人两个无菌平血作空白对照。8.2.2及时将15mL-20mL冷至46℃的结晶紫中性红胆盐琼脂(VR3A)约倾注于每个平Ⅲ中。小心旋转平血,将培养基与样液充分混勾,待琼脂凝固后,再加3mL~4mLVRBA覆盖平板表层。翻转平板,置于36℃±1℃培养18h~24h。8.3苹板菌落数的选择
选取菌落数在30~150之间的平板,分别计数平板上出现的典型和可疑人肠菌群菌落,典型菌落为紫红色,菌落周围有红色的朋盐沉淀环,菌落直径为0.5mm或更大。8.4证实试验
从VRBA平板上挑瑕10个不同类型的典型和可疑菌落,分别移种于BGLB肉荡管内,36℃上1℃培养24h-~48h,观察产气情况:凡BGLB肉汤管产:气,即可报告为大肠菌群阳性,8.5大肠菌群平板计数的报告
经最后证实为大肠菌群阳性的试管比例乘以8.3中计数的平板菌数,再乘以释倍数,即为每克(或毫升)样品中人肠菌群数。例:10-4样品稀释液1mL,在VRBA平板上右100个典型和可菌落,挑圾其中10个接种BGLB肉汤管,证实有6个阳性臂,则该样品的大肠菌群数为:100×6/10×10°/g(mL)--6.0X10° CFU/g(CFU/mL),第三法大肠菌群PetrifilmTM测试片法9检验程序
大肠菌群Petriilin\\测试片法的检验程序见图3。检样
25 g(或25 mL3样品+225 mL稀释,均质10倍系列稀释
选择2个~.3个适宜稀释度的样品勾液,接种 Petrifilmr*测试片36 ℃上1
24hl2h
计数红色带气泡的菌藩
报告结果
图 3 大肠菌群 PetrifilmTM测试片计数法程序图L此内容来自标准下载网
10操作步骤
10.1样品的稀释
按6.1进行。
10.2测定
10.2.1样品接种及培养
GB/F4789.3—2008
将待检样品选取2个~3个适宜的连续稀释度,每个稀释度接种两张测试片。将PctrifilmiTM大肠菌群测试片置于-坦实验台面,揭开上层膜,用吸管吸取1ml.样液垂直滴加在测试片的中央,将上层膜缓慢盖下,避免气泡产生和上层膜直接落下,把压板(平面底朝下)放置在上层膜中,轻轻地压下,使样液均勾覆盖于圆形的培养而积上,切勿扭转压板。掌起压板,静置至少1mi以使培养基凝固。将测试片的透明面朝上置于培养箱内,堆叠片数不超过20片,36℃士1℃培养24h土2h。10.2.2判读
培养24h士2h后应立即计数,可日测或用标准菌落计数器、放大镜或PctrifilmTX自动判读仪来计数。红色有气泡的菌落确认为大肠菌群。圆形培养区边缘上及边缘以外的菌落不作计数。当培养区域出现大量气泡,大量不明显小菌落或培养区呈暗红色三种情况,表明大肠菌群的浓度较高,需要进一步稀释样品以获得更准确的读数。10.3大肠菌群测试片计数的报告选取菌落数在15~150之间的测试片,计数具红色有气泡的菌落数,两个测试片的平均菌落数乘以稀释倍数即为每克或毫升)样品中的大肠菌群菌落形成单位(CFU)数。如果所有稀释度测试片上的菌落数都小于15,则计数稀释度最低的测试片.的平均菌落数乘以稀释倍数报告;如果所有稀释度的测试片上均无菌落生长,则以小于1乘以最低稀释倍数报告;如果最高稀释度的菌落数大于150,计数最高稀释度的测试片上的平均菌落数乘以释倍数报告。计数菌落数人于150的测试片时,可计数·个或两个具有代表性的方格内的菌落数,换算成单个方铬内的菌落数后乘以20即为测试片上估算的菌落数(圆形生长而积为20cm)。报岱单位以CFU/g(或CFU/mE)表示。5
GB/T 4789.3—2008
A.1月桂基硫酸盐胰蛋白陈(IST)肉汤A. 1. 1成分
胰蛋白豚或胰酪
氯化钠
磷酸氨二钾(K,HPO,)
磷酸二氢钾(KH,PO)
月桂基磺酸钠
蒸馏水
pH6.8±0.2
A.1.2制法
附录A
(规范性附录)
培养基和试剂
1 000 mL
将 [述成分溶解于蒸馏水中,调节 pH。分装到有玻璃小倒管的试管中,每管 10 ml.。121 ℃高压火菌15min.
A,2煌绿乳糖胆盐(BGLB)肉汤
A.2.1成分
蛋白炼
牛胆粉(oxgall或axbile)溶液
0.1%熄绿水溶液
蒸馏水
pH7.2±0.1
A. 2.2 制法
1000ml
将蛋白陈、乳糖溶于药 500 ml.蒸馏水中,加入牛胆粉溶液 200 tnL(将20.0 g脱水牛期粉溶于200 mL蒸馏水中,pH7.0~~7.5)用蒸馏水稀释到975mL,调节 pH至 7.4,再加入 0.1%煌绿水溶液13.3 mL.,用蒸馏水补足到1000mL,用棉花过滤后,分装到有玻璃小倒管的试管中,每管10mL。121℃高压灭菌 15 min。
A.3结晶紫中性红胆盐琼脂(VRBA)A.3.1成分
蛋白陈
酵母膏
氟化钠
胆盐或3号肥盐
中性红
结晶紫
http:
蒸馏水
pH7. 4±0. 1
A.3.2制法
15 g-~18 g
1 000 ml.
GB/T 4789.3--2008
将I述成分溶于蒸馏水中,静置几分钟,充分搅拌,调节pH。煮沸2mi,将培养基冷却至45℃~50℃倾注乎板,使用前临时制备,不得超过3h。A.4磷酸盐缓冲液
A,4.1成分
磷酸二氨钾(KH,PO,)
蒸馏水
A.4.2制法
存液:称取34.0名的磷酸二氢钾溶于500mL蒸馏水中,用大约175ml.的1mol/L氢氧化钠溶液调节pH至7.2,用蒸馏水稀释至1000ml.后贮存于冰箱,稀释液:取贮存液1.25mL,用蒸馏水稀释至1000nL,分装丁适宜容器中,121℃高压灭菌15min。
品成伴网httn:/
unfoodmate.nef
CB/T4789.3—2008
附录B
(规范性附录)
天肠菌群最可能数(MPN)检素表每克(或靠升)检样中大肠菌群最可能数(MPN)的检索见表B.1.表B.1大肠菌群最可能数(MPN)检索表阳性管数
95%可信限
陷性替数
95%可信限
注1:本表采用3个稀释度[0.1g(或0. 1ml)、0.01g(或0.01mL)和0.001g【或0. 001mL)],每个稀释度接种3營。
注2:表内所列检样量如改用1g(或1mL)、C.1g(或0.1ml.)和0.01g(或0.01ml.)时,表内数字应相应降低10借;如改用0.01g(或0.01mL),0.001g(或0.00)ml),0.0001g(或0.0001mL)时,则表内数学应相应增高10倍,其余类摊。
版权专有复权必究
书号:155066·1-36101
GB/T 4789. 3-2008
http:
rungfood
定价:
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
中华人民共和国国家标准
GB/T 4789.3—2008
代替 GB/T 4789.32003
食品卫生微生物学检验
大肠菌群计数
Microbiological examnination of food hygiene-Enumeration of coliforms
2008-11-21发布
中华人民共和国卫生部
中国国家标准化管理委员会
2009-03-01实施
中华人民共和
国家标准
食品卫生微生物学检验
大肠菌群计数
GB/T 4789, 3--2008
中国标准出版社出版发行
北京复兴门外三里河北街16号
邮政编码:100045
网址 www, spc, net. cn
电话:68523946
68517548
中国标准出版社案皇岛印剃厂印剧各地新华书店经销
印张0.75
开本 880×1230 1/16
字数17千学
2009年3月第一版2009年3月第一次印刷*
书号:155066·1-36101定价14.00元吉由本社发行中心调换
如有印装差错
版权专有侵权必究
举报电话:(010)68533533
http://foodmate.net前
GB/T4789.3—2008
本标准的第--法和第一法修改采用关国食品药品管理局(FDA)《细菌学分析于册》第4章大肠杆菌和人肠群计数(2002年)(BacteriologicalAnalyticalMantal,Chapler4:EnumcrationofEscherichiacoliandthecoliformbacteria,2002),第三法修改采用国际分析家学会(AOACINTERNATIONAL)AOAC991.14《食品中人肠菌群和大肠杆菌计数Pctriilm测试片法》(1994年)(AOACOfficial Method 99l, 14,Coliform and Escherichia coli counts in foods--Dry rchydratable film Petrifilt E. coli count platc: and Petrifiltn coliforfn count plate methods).本标谁与FDA和AOAC方法的主要区别是:将样品制备时样量50g(或50mL)修改为25g(或25mL);将培养温度由 35 ℃上1℃修改为 36 ℃士1 ℃。本标准代替GB/T4789.3·2003《食品卫生微牛物学检验大肠菌群测定》。本标准与GB/T4789.3—2003相比主要修改如下:-将标雅名称改为“食品卫生微生物学检验大肠菌群计数”;增加了大肠菌群的平板计数法和纸片检测方法;人肠菌群的MPN(mostprobablenumber)法从以乳糖胆盐为主要培养基的MPN法,修改为以月基硫酸盐膜蛋白(laurylsulfatetryptosc,IST)肉汤为牛要培养基的MPN法;大肠菌群MPN法中原\报告每10nmL(g)大肠菌群的MPN值”,修改为“报告每1mL(或1g)大肠菌群的MPN值”。
本标准的附录 A,附录 H为规范性附录。本标准由中华人民共和国卫牛部提出并归口,本标雅由中华人民共和国卫生部负责解释。本标准负责起草单位:中国疾病预防控制中心营养与食品安全所本标准参与起草单位:江苏省疾病预防控制中心、中华人民共和国内蒙占山人境检验检疫局、上海市疾病预防控制申心、中华人民共和国辽宁出人境检验检获局。本标准主要起草人:刘秀梅、衰宝君、刘中学、刘弘、陈敏、卢行安田静。本标准所代弊标推的历次版本发布情况为:GH 4789.3 : 1984,GB/T 4789.31994,GB/T 4789. 3--2003.1范围
食品卫生微生物学检验
大肠菌群计数
本标准规定了食品中大肠菌群计数的方法。本标准适用于各类食品中大肠菌群的计数。2术语和定义
下列术语和定义适用于本标准。2.1
大肠茵群coliforms
GB/T 4789.3—2008
-群在 36 ℃条件下培养18 h能发酵乳糖,心酸产气的需氧和兼性厌氧革兰氏阴性无芽肥杆托菌。该菌群主要米源于人畜粪便,作为粪便污染指标评价食品的卫生状说,推断食品中肠道致病菌污染的可能。
最可能数most probable number;MPN基于泊松分布的一种间接计数方法。3设备和材料
除徽生物实验室常规灭菌及培养设备外,其他设备和材料如下:3.1恒温培养箱;36℃±1℃。
3.2 冰箱:2 ℃~5 ℃
3.3恒温水浴箱:46℃11℃。
3.4天半,感量0.1g。
3.5均质器
3.6振药器。
3.7无菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)或微量移液器及吸头,3.8无菌锥形瓶:容量 500 ml。
3.9尤菌培养皿:直径90mm。
3.10pH计或 pH比色管或精密 pH试纸。3.11菌落计数器或PetririlmTmI白动判读仪。4培养基和试剂
4.1月桂基硫酸盐胰蛋白豚(lauryl sulFate1rypiose,I.ST)肉汤:见第A.1章。4.2煌绿乳糖朋盐(brilliantgreenlactosebile,BGLB)肉汤:见第A2章。4.3结晶紫中性红胆盐琼脂(violet red bile agar,VRBA),见第 A. 3 章。4.4磷酸盐缓冲液:见第A.4章。1)Petrifilm\M是由3M公司提供的产品的商品名。给出这一信息是为了方便本标准的使用者,并不表示对该产品的认可。如果其他等效产品具有相同的效果,则可使旧这些等效的产品。品成伴网h
GB/T 4789.3--2008
4.5无菌生理盐水:称取8.5g氯化钠溶于1000mL蒸馏水中,121℃离压灭菌15min。4.61 mol/1.氢氧化钠(NaQH):称 410 g氢氧化钠溶下 1 000 mL蒸馏水中。4.71mol/L.盐酸(HCl):移取浓盐酸90mL,用蒸馏水稀释至1000mL4.8PetrililmrTm人肠菌群检验测试片租压板。第法大肠菌群MPN计数
5检验程序
大肠菌群MPN计数的检验程序见图1检样
25g(或25mL)样品-225mL稀释液,均质10 倍系列稀释
选择适宜三个连续稀释度的样品勾液.接种1.ST肉汤管36 ℃±1 ℃
不产气
48 h±2 h
BGLB肉汤
不产气
大肠菌群阴性
48h±2h
大肠菌群阳性
查MPN表
报告结果
图1大肠菌群MPN计数检验程序
6操作步骤
6.1样品的稀释
6.1.1固体和半固体样品:称取25g样品,放入盛有225ml.磷酸盐缓冲液或生理盐水的无菌均质杯内,80001/min~10000r/rin均质1min~2min,或放人盛有225mL磷酸盐缓冲液或生理盐水的无菌均质袋中,用拍击式均质器拍打1min~2min,制成1=10的样品勾液。2
http:
GB/T 4789.3—2008
6.1.2液体样品:以无菌吸管吸取25mL样品,置盛有225mL磷酸盐缓冲液或生理盐水的无菌锥形瓶(瓶内预置适当数量的菌玻璃珠)中,充分混勾,制成1:10的样品匀液。6.1.3样品匀液的pH值应在6.5~7.5之间,必要时分别用1mol/L氢氧化钠(NaO)II)或1mol/L盐酸(HCI)调节。
6.1.4用1mL无菌吸管或微量移液器吸1:10样品勾液1ml,沿管缓缓注入9mL磷酸盐缓液或生理盐水的无菌试管中(注意吸管或吸头尖端不要触及稀释液面),振摇试管或换用I支!mL无菌吸管反复吹打,使其混合均匀,制成1:100的样品句液。6.1.5根据对样品污染状况的估计,按上述操作,依次制成10倍递增系列稀释样品句液。每递增稀释1次,换用1支1mL尤菌吸管或吸头。从制备样品勾液至样品接种完毕,全过程不得超过15min。6.?发酵试验
每个样品,选择3个适宜的连续稀释度的样品勾液(液体样品可以选择原液),每个稀释度接种3管月柱基硫酸盐胰蛋白陈(L.ST)肉汤,每管接种1mL(如接种量超过1mL,则用双料LST肉汤),36\C士1℃培养24h士2h,观察倒管内是否有气泡产生,如未产气则继续培养至48h土2h。记录在24h和48h内产气的LST肉汤管数。未产气者为大肠菌群阴性,产气者则进行复发醇酵试验。6.3复发酵试验
用接种环从所有18h土2h内发酵产气的LST肉汤管中分别取培养物1环,移种于熄绿乳糖胆盐(BGL13)肉汤管中,36℃上1℃培养18l土2h,观察产气情况。产气者,计为大肠菌群阳性管,6. 4大肠菌群最可能数(MPN)的报告根据大肠菌群阳性管数,检紫MPN表(见附录13),报告每克(或毫)样品中大肠菌群的MPN值。
第二法大肠菌群平板计数
7检验程序
人肠菌群平板计数的检验程序见图2。检样
25 g(或 25 mL)样品+225 1nL稀释液,均质+
10倍系列稀释
选择 2 个-~3 个适稀释度的样品勾被,接种 VRBA平板36 ℃±1 °
18 h~24 h
计数典型和可菌落
BGLB肉汤或复发酵试验
36 ±1 ℃
24 hb~~ 48 h
报告结果
图2大肠菌群平板计数检验程序
GB/T4789.3—2008
8操作步骤
8.1样品的稀释
按 6.1 逃行。
8.2平板计数
8.2.1选取2个~3个适宜的连续稀释度,每个稀释度接种两个无菌平匪,每1ml.。同时分别取1 ml. 生理盐水加人两个无菌平血作空白对照。8.2.2及时将15mL-20mL冷至46℃的结晶紫中性红胆盐琼脂(VR3A)约倾注于每个平Ⅲ中。小心旋转平血,将培养基与样液充分混勾,待琼脂凝固后,再加3mL~4mLVRBA覆盖平板表层。翻转平板,置于36℃±1℃培养18h~24h。8.3苹板菌落数的选择
选取菌落数在30~150之间的平板,分别计数平板上出现的典型和可疑人肠菌群菌落,典型菌落为紫红色,菌落周围有红色的朋盐沉淀环,菌落直径为0.5mm或更大。8.4证实试验
从VRBA平板上挑瑕10个不同类型的典型和可疑菌落,分别移种于BGLB肉荡管内,36℃上1℃培养24h-~48h,观察产气情况:凡BGLB肉汤管产:气,即可报告为大肠菌群阳性,8.5大肠菌群平板计数的报告
经最后证实为大肠菌群阳性的试管比例乘以8.3中计数的平板菌数,再乘以释倍数,即为每克(或毫升)样品中人肠菌群数。例:10-4样品稀释液1mL,在VRBA平板上右100个典型和可菌落,挑圾其中10个接种BGLB肉汤管,证实有6个阳性臂,则该样品的大肠菌群数为:100×6/10×10°/g(mL)--6.0X10° CFU/g(CFU/mL),第三法大肠菌群PetrifilmTM测试片法9检验程序
大肠菌群Petriilin\\测试片法的检验程序见图3。检样
25 g(或25 mL3样品+225 mL稀释,均质10倍系列稀释
选择2个~.3个适宜稀释度的样品勾液,接种 Petrifilmr*测试片36 ℃上1
24hl2h
计数红色带气泡的菌藩
报告结果
图 3 大肠菌群 PetrifilmTM测试片计数法程序图L此内容来自标准下载网
10操作步骤
10.1样品的稀释
按6.1进行。
10.2测定
10.2.1样品接种及培养
GB/F4789.3—2008
将待检样品选取2个~3个适宜的连续稀释度,每个稀释度接种两张测试片。将PctrifilmiTM大肠菌群测试片置于-坦实验台面,揭开上层膜,用吸管吸取1ml.样液垂直滴加在测试片的中央,将上层膜缓慢盖下,避免气泡产生和上层膜直接落下,把压板(平面底朝下)放置在上层膜中,轻轻地压下,使样液均勾覆盖于圆形的培养而积上,切勿扭转压板。掌起压板,静置至少1mi以使培养基凝固。将测试片的透明面朝上置于培养箱内,堆叠片数不超过20片,36℃士1℃培养24h土2h。10.2.2判读
培养24h士2h后应立即计数,可日测或用标准菌落计数器、放大镜或PctrifilmTX自动判读仪来计数。红色有气泡的菌落确认为大肠菌群。圆形培养区边缘上及边缘以外的菌落不作计数。当培养区域出现大量气泡,大量不明显小菌落或培养区呈暗红色三种情况,表明大肠菌群的浓度较高,需要进一步稀释样品以获得更准确的读数。10.3大肠菌群测试片计数的报告选取菌落数在15~150之间的测试片,计数具红色有气泡的菌落数,两个测试片的平均菌落数乘以稀释倍数即为每克或毫升)样品中的大肠菌群菌落形成单位(CFU)数。如果所有稀释度测试片上的菌落数都小于15,则计数稀释度最低的测试片.的平均菌落数乘以稀释倍数报告;如果所有稀释度的测试片上均无菌落生长,则以小于1乘以最低稀释倍数报告;如果最高稀释度的菌落数大于150,计数最高稀释度的测试片上的平均菌落数乘以释倍数报告。计数菌落数人于150的测试片时,可计数·个或两个具有代表性的方格内的菌落数,换算成单个方铬内的菌落数后乘以20即为测试片上估算的菌落数(圆形生长而积为20cm)。报岱单位以CFU/g(或CFU/mE)表示。5
GB/T 4789.3—2008
A.1月桂基硫酸盐胰蛋白陈(IST)肉汤A. 1. 1成分
胰蛋白豚或胰酪
氯化钠
磷酸氨二钾(K,HPO,)
磷酸二氢钾(KH,PO)
月桂基磺酸钠
蒸馏水
pH6.8±0.2
A.1.2制法
附录A
(规范性附录)
培养基和试剂
1 000 mL
将 [述成分溶解于蒸馏水中,调节 pH。分装到有玻璃小倒管的试管中,每管 10 ml.。121 ℃高压火菌15min.
A,2煌绿乳糖胆盐(BGLB)肉汤
A.2.1成分
蛋白炼
牛胆粉(oxgall或axbile)溶液
0.1%熄绿水溶液
蒸馏水
pH7.2±0.1
A. 2.2 制法
1000ml
将蛋白陈、乳糖溶于药 500 ml.蒸馏水中,加入牛胆粉溶液 200 tnL(将20.0 g脱水牛期粉溶于200 mL蒸馏水中,pH7.0~~7.5)用蒸馏水稀释到975mL,调节 pH至 7.4,再加入 0.1%煌绿水溶液13.3 mL.,用蒸馏水补足到1000mL,用棉花过滤后,分装到有玻璃小倒管的试管中,每管10mL。121℃高压灭菌 15 min。
A.3结晶紫中性红胆盐琼脂(VRBA)A.3.1成分
蛋白陈
酵母膏
氟化钠
胆盐或3号肥盐
中性红
结晶紫
http:
蒸馏水
pH7. 4±0. 1
A.3.2制法
15 g-~18 g
1 000 ml.
GB/T 4789.3--2008
将I述成分溶于蒸馏水中,静置几分钟,充分搅拌,调节pH。煮沸2mi,将培养基冷却至45℃~50℃倾注乎板,使用前临时制备,不得超过3h。A.4磷酸盐缓冲液
A,4.1成分
磷酸二氨钾(KH,PO,)
蒸馏水
A.4.2制法
存液:称取34.0名的磷酸二氢钾溶于500mL蒸馏水中,用大约175ml.的1mol/L氢氧化钠溶液调节pH至7.2,用蒸馏水稀释至1000ml.后贮存于冰箱,稀释液:取贮存液1.25mL,用蒸馏水稀释至1000nL,分装丁适宜容器中,121℃高压灭菌15min。
品成伴网httn:/
unfoodmate.nef
CB/T4789.3—2008
附录B
(规范性附录)
天肠菌群最可能数(MPN)检素表每克(或靠升)检样中大肠菌群最可能数(MPN)的检索见表B.1.表B.1大肠菌群最可能数(MPN)检索表阳性管数
95%可信限
陷性替数
95%可信限
注1:本表采用3个稀释度[0.1g(或0. 1ml)、0.01g(或0.01mL)和0.001g【或0. 001mL)],每个稀释度接种3營。
注2:表内所列检样量如改用1g(或1mL)、C.1g(或0.1ml.)和0.01g(或0.01ml.)时,表内数字应相应降低10借;如改用0.01g(或0.01mL),0.001g(或0.00)ml),0.0001g(或0.0001mL)时,则表内数学应相应增高10倍,其余类摊。
版权专有复权必究
书号:155066·1-36101
GB/T 4789. 3-2008
http:
rungfood
定价:
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。