GB 1445-2000
基本信息
标准号: GB 1445-2000
中文名称:绵白糖
标准类别:国家标准(GB)
英文名称: Softened sugar
标准状态:现行
发布日期:2000-01-01
实施日期:2001-10-01
出版语种:简体中文
下载格式:.rar.pdf
下载大小:427411

标准分类号
标准ICS号:食品技术>>糖、糖制品、淀粉>>67.180.10糖和糖制品
中标分类号:食品>>制糖与糖制品>>X31制糖
出版信息
出版社:中国标准出版社
书号:155066.1-17530
页数:平装16开/页数:/字数:
标准价格:12.0 元
出版日期:2004-07-19
相关单位信息
首发日期:1978-12-08
复审日期:2004-10-14
起草单位:中国轻工总会甜茶糖业研究所
发布部门:国家质量技术监督局
主管部门:国家标准化管理委员会
标准简介
本标准规定了绵白糖的技术要求、试验方法、检验规则及标志、包装、运输、贮存的要求。本标准适用于制糖工业中利用甜菜、粗糖为原料生产的绵白糖。 GB 1445-2000 绵白糖 GB1445-2000 标准下载解压密码:www.bzxz.net
标准图片预览



标准内容
GB1445—2000
本标准3.3条为强制性的,其余为推荐性的。本标准是根据GB1445.1—1991《绵白糖》、GB/T1445.2-1991《绵白糖试验方法》及QB1681—1993《精制绵白糖》进行修订的,在技术要求上非等效采用CODEXSTAN6—1981《白糖》和《国际糖品统一分析方法》,其他条款是严格按照我国有关标准和法规的要求编写的。在技术要求中,将QB/T16811993《精制绵白糖》并人《绵白糖》国家标准,即在绵白糖的等级中增加了“精制”级别,同时取消了“二级”品等级标谁。理化要求中的“水不溶杂质”及卫生要求中的“二氧化硫”指标有所提高。
在试验方法中,“色值的测定”以缓冲溶液法代替了以往的调pH法,同时还增加了“螨的检验”。在“检验规则”中,规定了新的抽样方法。对“标签、包装、运输、贮存”一章,也根据有关最新标准和法规进行了修订。
本标准自实施之日起,同时代替GB1445.1—1991、GB/T1445.2—1991和QB/T1681-1993。本标准由国家轻工业局提出。
本标准由全国甜菜糖业标准化中心归口。本标准起草单位:国家轻工业局甜菜糖业研究所。本标推主要起草人:张继峰、王茹菊、陈枫柏。120
1范围
中华人民共和国国家标准
绵白糖
White soft sugar
GB1445--2000
代替GB1445.1-1991
GB/T1445.2--.1991
本标准规定了绵白糖的技术要求、试验方法、检验规则及标签、包装、运输、贮存的要求。本标准适用于制糖工业中利用甜菜、粗糖为原料生产的绵白糖。2引用标准
下列标准所包含的条文,通过在本标准中引用而构成为本标准的条文。本标准出版时,所示版本均为有效。所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。微生物学部分
GB4789.1~4789.31—1994食品卫生检验方法GB/T5009.55-1996食糖卫生标准的分析方法GB7718-1994食品标签通用标准
白糖卫生标准
GB 13104—1991
3技术要求
绵白糖按技术要求的规定分为精制、优级、一一级。3.1感官要求
3.1.1晶粒细小、均勾,颜色洁白,质地绵软。3.1.2晶体或其水溶液味甜、无异味。3.1.3产品的水溶液清澈、透明。3.1.4精制级别每平方米表面积内长度大于0.2mm的黑点数量不多于12个,其他级别不多于16个。
3.2理化要求
绵白糖的各项理化指标见表1。
总糖分,%
还原糖分,%
干燥失重,%
电导灰分,%
色值,IU
粒度,mm
混浊度.度
不溶于水杂质,mg/kg
国家质量技术监督局2000-11-21批准精制
0.80~1.60
0.80~2.00
1.5~2.5
0.80~2.00
2001-10-01实施
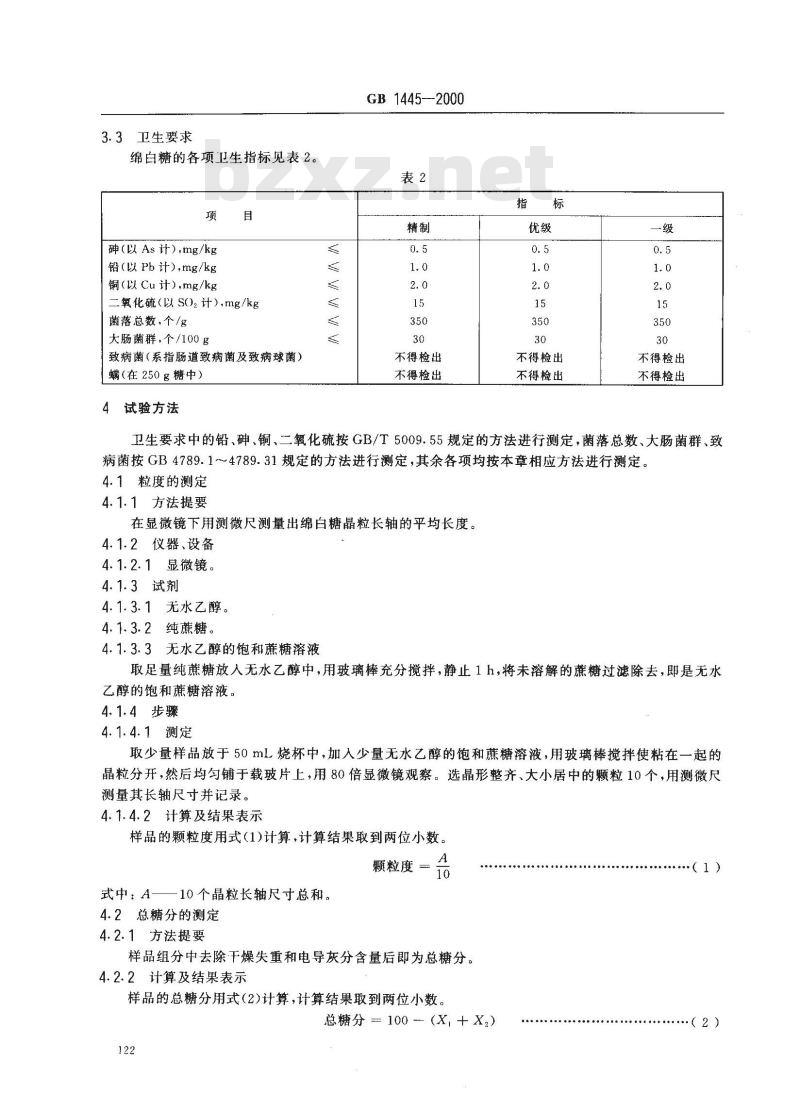
3.3卫生要求
绵白糖的各项卫生指标见表2。
砷(以As 计),mg/kg
铅(以 Pb计),mg/kg
铜(以Cu计),mg/kg
二氧化硫(以 S0),计),mg/kg
菌落总数,个/g
大肠菌群,个/100g
致病菌(系指肠道致病菌及致病球菌)螨(在250g糖中)
4试验方法
GB 1445--2000
不得检出
不得检出
不得检出
不得检出
不得检出
不得检出
卫生要求中的铅、砷、铜、二氧化硫按GB/T5009.55规定的方法进行测定,菌落总数、大肠菌群、致病菌按GB4789.1~4789.31规定的方法进行测定,其余各项均按本章相应方法进行测定。4.1粒度的测定
4.1.1方法提要
在显微镜下用测微尺测量出绵白糖晶粒长轴的平均长度。4.1.2仪器、设备
4.1.2.1显微镜。
4.1.3试剂
4.1.3.1无水乙醇。
4.1.3.2纯蔗糖。
4.1.3.3无水乙醇的饱和蔗糖溶液取足量纯蔗糖放入无水乙醇中,用玻璃棒充分搅拌,静止1h,将未溶解的燕糖过滤除去,即是无水乙醇的饱和蔗糖溶液。
4.1.4步骤
4.1.4.1测定
取少量样品放于50ml烧杯中,加入少量无水乙醇的饱和蔗糖溶液,用玻璃棒搅拌使粘在一起的晶粒分开,然后均勾铺于载玻片上,用80倍显微镜观察。选晶形整齐、大小居中的颗粒10个,用测微尺测量其长轴尺寸并记录。
4.1.4.2计算及结果表示
样品的颗粒度用式(1)计算,计算结果取到两位小数。颗粒度 一
式中:A-
-10个晶粒长轴尺寸总和。
4.2总糖分的测定
4.2.1方法提要
样品组分中去除·干燥失重和电导灰分含量后即为总糖分。4.2.2计算及结果表示
样品的总糖分用式(2)计算,计算结果取到两位小数总糖分100(X,+X)
(1)
GB 1445---2000
式中:X,—干燥失重以质量百分数表示);X2——电导灰分(以质量百分数表示)。4.3还原糖分的测定
4.3.1方法提要
在加热条件下,以四甲基蓝作指示剂,用配制好的糖溶液滴定标定过的费林氏液,根据消耗糖溶液的量,计算样品中还原糖的含量。4.3.2仪器、设备
4.3.2.1容量瓶:200ml.250mL,1000mL。4.3.2.2滴定管:50mL,刻度为0.1mL4.3.2.3吸液管:5mL。
4.3.2.4锥型管:250ml.。
4.3.2.5布氏斗及吸滤瓶。
4.3.3试剂
4.3.3.1费林氏甲液:取化学纯硫酸铜(CuSO.·5HzO)69.28g效人1000mL烧杯中,加蒸罐水约500mL后置于沸腾水浴中加热使其溶解,冷却后定容至1000mL。4.3.3.2费林氏乙液:取化学纯酒石酸钾钠(KNaC,H.O·4H,0)346g放入烧杯中,加人蒸馏水约500mL后加热使其溶解;用另一烧杯称取氢氧化钠100g,加人约500mL蒸馏水溶解;将两液混勾,冷却后定容至1000ml。
4.3.3.3纯蔗糖:取质量较好的白砂糖溶解于水中,在水浴上加热至70~80℃,继续加入白砂糖以玻璃棒搅拌,至不能溶解时为止。用少量脱脂梯作过滤介质,在保温漏斗中过滤。漏斗下放一杯无水乙醇,当热糖液滴下时不断搅拌,使自砂糖溶液在乙醇中生戒极细晶体。当杯中蔗糖晶体达到所需数量时,将部分结成小块的晶粒取出,用乳体研碎,然后一并在布氏漏斗中用真空吸滤法吸干。再将晶体溶解于70C~80℃水中至不能溶解为止。重复上述操作方法,将已经吸滤的蔗糖在乳钵中研碎,在50℃和一0.053MPa真空下于燥至恒重。4.3.3.4标准转化糖溶液(1转化糖/100mL):取9.500g纯蔗糖溶解于100mL蒸馏水中,缓慢加人分析纯浓盐酸(比重1.19)5ml,在20℃-~25C放置3天后于容量瓶中稀释至1000ml,倒人带有磨口的瓶中备用。此溶液是种稳定的储备液(可存放3~4个月),使用前随时稀释。4.3.3.5转化糖溶液(0.2g转化糖/100ml):吸取标准转化糖溶液50mL于250ml.容量瓶中,加入0.1mol氢氧化钠溶液中和后(氢氧化钠用量是以酚献为指示剂预先滴定计算雨得),加蒸罐水至标线。4.3.3.6四甲基蓝溶液(1g/100mL):称取分析纯四甲基蓝5g溶于蒸馏水中并稀释至500mL。4.3.4费林氏液的标定
吸取费林氏甲、乙液各5ml.于250mL锥形瓶中,用标准的滴定方法(见4.3.5.3)应耗用转化糖溶液(0.2g转化糖/100ml.)25.64mL。在需要进行少量调整时,可加人算好的硫铜量或水量后,随即充分摇勾。凡经调整后的溶液都应进行重新标定,直至恰好为25.64mL为止。4.3.5步骤
4.3.5.1样液的制备
称联20.00绵白糖样品,用蒸罐水溶解并定容至200ml.后装人50ml滴定管中备用。4.3.5.2预检
吸取费林氏甲、乙液各5mL手250mL维形瓶中,混匀。于滴定管中预加被检糖液15ml,在石棉网上用电炉加热至沸腾。溶液经煮沸10s~15后,如它的颜色显示费林氏液还没有还原完全,可再加糖液(一次10mL或5mL),每次沸腾后都要煮沸几秒钟直至铜离子变成橙色为止。记下滴定用去的被检糖液的总体积。
4.3.5.3标准的滴定方法
GB 1445—2000
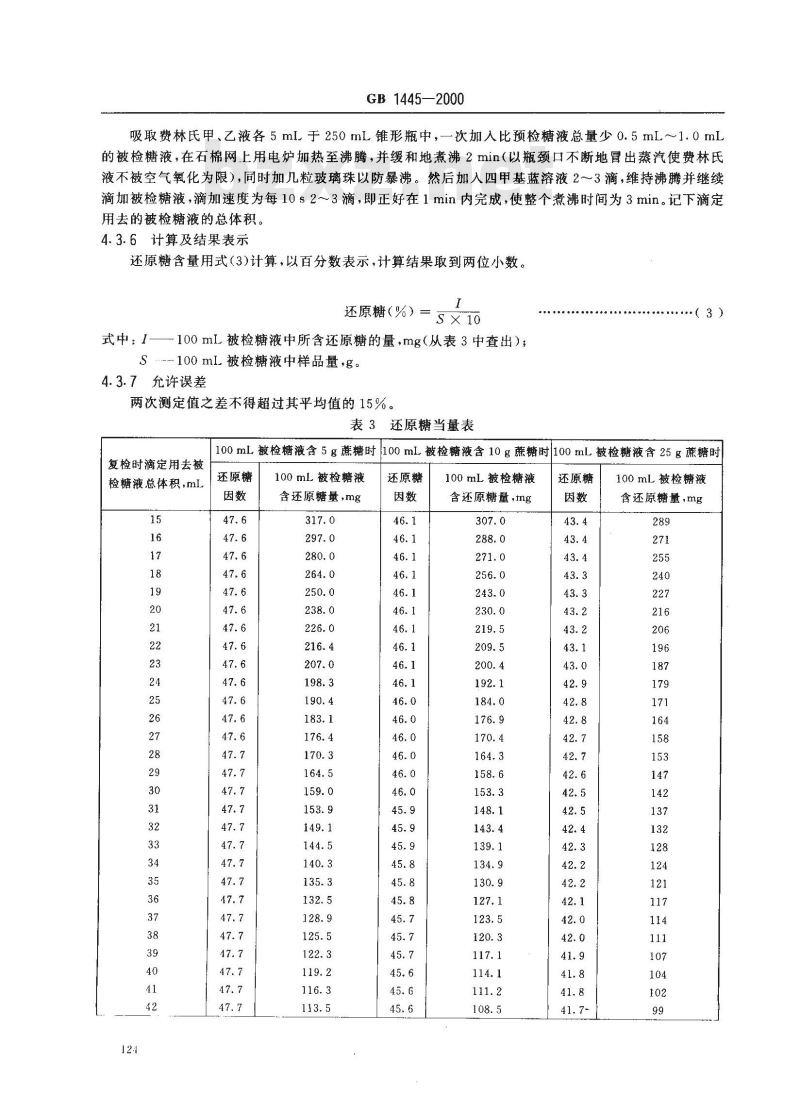
吸取费林氏甲、乙液各5mL于250mL锥形瓶中,一次加入比预检糖液总量少0.5mL~~1.0mL的被检糖液,在石棉网上用电炉加热至沸腾,并缓和地煮沸2min(以瓶颈口不断地冒出蒸汽使费林氏液不被空气氧化为限),同时加几粒玻璃珠以防暴沸。然后加入四甲基蓝溶液2~3滴,维持沸腾并继续滴加被检糖液,滴加速度为每10s2~~~3滴,即正好在1min内完成,使整个煮沸时间为3min。记下滴定用去的被检糖液的总体积。
4.3.6计算及结果表示
还原糖含量用式(3)计算,以百分数表示,计算结果取到两位小数。还原糖(%)=
100mL被检糖液中所含还原糖的量,mg(从表3中查出);式中:1
s.--100mL被检糖液中样品量,g。4.3.7允许误差
两次测定值之差不得超过其平均值的15%。表3还原糖当量表
复检时滴定用去被
检糖液总体积,mL
100mL被检糖液含5g蔗糖时100mL被检糖液含10g蔗糖时100ml被检糖液含25g蔗糖时还原糖
100mL被检糖液
含还原糖量,mg
还原糖
100 mL被检糖液
含还原糖量,mg
还原糖
100mL被检糖液
含还原糖量,mg
复检时滴定用去被
检糖液总体积,mL
GB 1445-2000
表3(完)
100mL被检糖液含5g蔗糖时100mL被检糖液含10g蔗糖时|100mL被检糖液含25g蔗糖时还原糖
4.4电导灰分的测定
4.4.1方法提要
100mL被检糖液
含还原糖量,mg
还原糖
100mL被检糖液
含还原糖量,mg
还原糖
100mL被检糖液
含还原糖量,mg
糖品中的灰分是由无机盐类和有机盐类组成,它们在水中大部分解离成带电荷的离子。电导率表示离子化水溶性盐类的浓度。测定糖液的电导率,然后应用转换系数即可算出电导灰分。4.4.2仪器、设备
电导率仪:DDS-11A型或DDS-11型。4.4.3试剂
4.4.3.1蒸馏水或去离子水:精制绵白糖、优级白砂糖必须用电导率低于2uS/cm的蒸馏水或去离子水。一级绵白糖充允许用电导率低于15 μuS/cm的蒸馏水。4.4.3.20.01mol/L氯化钾溶液:取分析纯氯化钾,加热至500℃(呈暗红炽热)脱水30min后,称取0.7455g,溶解于1000mL容量瓶中,并加水至标线。此溶液在20℃时电导率为1278μS/cm。4.4.3.30.0025mol/L氯化钾溶液:吸取0.01mol/L氯化钾溶液250mL移人1000mL容量瓶内,加水稀释至标线。此溶液在20℃时电导率为328μS/cm。4.4.4步骤
4.4.4.1测定
称取(31.7士0.1)g绵白糖样品于干洁烧杯中,加蒸馏水溶解并移人100mL容量瓶中,用蒸馏水多次冲洗烧杯及玻璃棒,洗水一并移人容量瓶中,加水至标线,摇匀。先用样液冲洗电导电极2~3次,然后将样液倒人小烧杯中,用电导率仪测定样液的电导率,记录读数及当时样液的温度。电导池常数应用0.0025mol/L氯化钾溶液校核计量。4.4.4.2计算及结果表示
电导灰分用式(4)计算,以百分数表示,计算结果取到两位小数。电导灰分(%)=6×10-4(C—0.35C2)式中:C,---
被测糖液在(20士0.2)℃时的电导率,μS/cm;-溶糖所用蒸馏水在(20士0.2)℃时的电导率,μS/cm。4.4.4.3温度校正
(4)
测定电导率的标准温度为(20士0.2)℃,如测定电导率时温度不在(20士0.2)℃时,则按式(5)校正,但测量温度范围一般不应超过(20士5)℃。溶糖用蒸馏水的电导率,因温度对其影响甚微,故可忽略不计,不需校正。
C = Ct[1 + 0. 026(20 — t)J
式中:Ci
被测糖液在t℃时的电导率,uS/cm;-测定糖液电导率时糖液的温度;℃。t
·(5)
4.4.4.4允许误差
GB 1445—2000
两次测定值之差不得超过其平均值的10%。4.5干燥失重的测定
4.5.1方法提要
将样品在一定温度及真空度的条件下进行干燥后称量,根据干燥前后样品失去的质量计算出样品的干燥失重。
4.5.2仪器、设备
4.5.2.1真空干燥箱:0~0.1MPa,温度范围0~100℃。4.5.2.2称量皿:直径50mm,单层盖。4.5.2.3天平:感量0.0001g。
4.5.3步骤
4.5.3.1测定
用恒重过的称量皿称取绵白糖样品约10.000g,开盖置于真空干燥箱内干燥60min(温度70℃~75C,真空度0.067MPa)。盖盖后将称量血取出置于干燥器内冷却至室温后称量。4.5.3.2计算及结果表示
干燥失重用式(6)计算,以百分数表示,计算结果取到两位小数。W-w×100
干燥失重(%)=
式中:W.——称量皿的质量,g;W2——称量血和干燥前样品的总质量,g;W3一—称量血和干燥后样品的总质量,g。4.5.3.3允许误差
两次测定值之差不得超过0.05%。4.6色值的测定
4.6.1方法提要
绵白糖样品用pH7.0士0.1缓冲溶液溶解后,经滤膜过滤,然后在420nm波长条件下以蒸馏水做参比溶液,测量溶液的吸光系数,将吸光系数的数值乘以1000,即为ICUMSA色值,单位(IU)。4.6.2仪器、设备
4.6.2.1分光光度计:测试范围0~2A,精度0.01A,波长精度(4201)nm;4.6.2.2比色血:1~5cm;用于测定与作参比的两只比色血,透光度不应超过0.2%(用蒸馏水检查)。4.6.2.3滤膜过滤器:带有孔径为0.45um滤膜和吸滤瓶。4.6.2.4阿贝折射仪:糖用。
4.6.2.5pH(酸度)计:分度值或最小显示值0.02pH。4.6.3试剂
4.6.3.10.1mol/l.盐酸溶液。
4.6.3.2三乙醇胺-盐酸缓冲溶液:称取三乙醇胺[(HOCH,CH,)NJ14.920g,用蒸馏水溶解并定容至1000mL,然后移人2000mL烧杯内,加人0.1mol/盐酸溶液约800mL,搅拌均匀并继续用0.1mol/L盐酸调到pH7.0(用酸度计的电极浸于此溶液中测量pH值),于棕色玻璃瓶中。4.6.4步骤
4.6.4.1测定
称取绵白糖样品100.0g,置于200ml烧杯中,加人三乙醇胺-盐酸缓冲溶液135ml,搅拌至完全溶解。倒人已预先铺好孔径为0.45μm滤膜的过滤器中在真空下抽滤,弃去最初50mL滤液,收集不少于50mI.的滤液后测其锤度,然后用比色皿装盛糖液,以三乙醇胺-盐酸缓冲溶液作参比,在分光光度126
计上于420nm波长下测其吸光度。GB1445—2000
蔗糖溶液折光锤度与每毫升含蔗糖克数(在空气中)对照表表4方
折光锤度
4.6.4.2计算及结果表示
折光锤度
色值用式(7)计算,以IU表示,计算结果取整数。国际糖色值:
式中:A420
折光锤度
在420nm波长下测得样液的吸光度;比色皿厚度,cm;
× 1 000
折光锤度
样液浓度(由校正到20℃的锤度乘上系数0.9854后查表4求得),g/mL。C
4.6.4.3允许误差
两次测定值之差不得超过4IU。
4.7混浊度的测定
4.7.1方法提要
当单色光透过含有悬浮粒子(混浊)的溶液时,由于悬浮粒子引起光的散射,单色光强度产生衰减,以光的衰减程度减去颜色的影响表示溶液的混浊度。4.7.2仪器、设备
同4.6.2条。
4.7.3步骤
4.7.3.1测定
取待测色值的未过滤糖液,在与测定色值相同的条件下,测其吸光度,并按式(8)计算其衰减指数。A420
衰减指数=
式中:A420…一在420nm波长下测得的未过滤样液的吸光度;b-—比色血厚度,cm;
一样液浓度(由校正到20℃的锤度乘上系数0.9854后查表4求得),g/mL。4.7.3.2计算及结果表示
混浊度用式(9)计算,单位为度,计算结果取整数。混浊度2
式中:\
过滤前糖液衰减指数,IU;
·(9)
过滤后溶糖色值指数,IU。
4.7.3.3允许误差
两次测定值之差不得超过1度。
4.8不溶于水杂质的测定
4.8.1方法提要
GB 1445-2000
用G3埚漏斗将糖液真空抽滤,再以较大量的蒸馏水洗涤滤渣,然后将滤渣干燥至恒重,计算出其在样品中的含量。
4.8.2仪器、设备
4.8.2.1G3漏斗:直径32mm。
4.8.2.2干燥箱。
4.8.2.3天平:感量0.0001g。
4.8.3试剂免费标准bzxz.net
4.8.3.11%α-萘酚乙醇溶液:称取α-萘酚1g,用95%乙醇溶解至100mL。4.8.3.2浓硫酸:含硫酸95%~98%。4.8.4步骤
4.8.4.1测定
称取绵白糖样品500.0g置于1000mL烧杯中,加约50℃蒸馏水700mL,搅拌至糖全部溶解,倾人经恒重的G3漏斗中进行真空抽滤。以蒸馏水充分洗涤滤渣,用α-酚乙醇溶液检查,至洗涤液不含糖分为止。将G3埚漏斗置于干燥箱内,在125~130℃下烘干1.0h,取出置于干燥器中冷却至室温后称量。然后再继续烘干0.5h,冷却后称量,重复操作,直至相继两次质量相差不超过0.001g为止,此时可认为达到恒重,记录其质量。微糖检验方法:取2mL洗涤液于试管中,加入数滴1%α-萘酚乙醇溶液,再沿管壁缓缓加人2mL浓硫酸。在水与酸的界面出现紫色环,说明有糖存在;若为黄绿色环,则说明无糖存在。4.8.4.2计算及结果表示
每千克绵白糖样品所含不溶于水杂质毫克数用式(10)计算,计算结果取整数。不溶于水杂质=㎡2二㎡× 106
-G3埚漏斗的质量,g;;
式中:m,-
-G3埚漏斗和不溶于水杂质的总质量,,m。--称取绵白糖样品的质量,g。4.8.4.3允许误差
两次测定值之差不得超过其平均值的15%。4.9黑点的测定
4.9.1方法提要
在瓷盘中盛满样品压平,检查表面黑点的个数后计算出单位面积内黑点的个数。4.9.2仪器、设备
4.9.2.1白瓷盘:表面积约0.25m2。4.9.2.2玻璃板。
4.9.3步骤
4. 9.3.1测定
在瓷盘中盛满样品,用玻璃板压平,然后在强光下检查长度大于0.2mm黑点的个数。4.9.3.2计算及结果表示
绵白糖样品黑点个数(个/m2)用式(11)计算。128
( 10)
GB 1445—2000
黑点个数 =× 4
式中:α——
查得瓷盘内样品中黑点个数,个。4.10螨的测定
4.10.1方法提要
取定量糖样用水溶于锥形瓶中,镜检糖液表面的漂浮物,以确定是否有螨及螨的数目。4.10.2仪器、设备
4.10.2.1显微镜。
4.10.2.2放大镜。
4.10.2.3锥形瓶:500mL。
4.10.3步骤
4.10.3.1测定
(11)
称取250g绵白糖样品置于500mL锥形瓶中,加人不高于25℃的蒸馏水并不断搅拌,使其完全溶解。再渐渐补充蒸馏水至瓶口处,以不使水溢出为止。然后用洁净的盖玻片置于瓶口处,使之与液面接触,静置15min,取下镜检。这一操作重复若干次,镜检所有的漂浮物。4.10.3.2计算及结果表示
镜检出的螨的数目即为250g绵白糖样品中的总螨数,以个为单位。5检验规则
5.1型式检验
5.1.1取样方法
每分离一罐糖膏为一个编号,在称量包装时,连续采取样品约5kg,放在带盖的容器中,混勾后为编号样品。该样品除供编号分析之用外,另取0.5kg放在带盖的容器中,积累24h后为日集合样品。取1.5kg日集合样品,用双层食品级塑料袋密封包装,或用磨砂口玻璃瓶盛装,标明产品编号、级别、生产日期、全批包数、检验结果及检验员,在相对湿度50%~70%、温度不超过30℃的环境中存留,供生产和质量管理查验之用。经供收双方认可,也可作为仲裁检验留样。5.1.2生产厂在保证质量的前提下,每编号样品和每日集合样品可按生产的实际情况进行指标的抽检。检验结果如有一项或多项不符合该级别的技术要求的,则按实达级别处理。达不到一级的按不合格处理。
5.1.3有下列情况之-时,应进行本标准的技术要求中的全部指标的检验。a)生产期开始时,洗罐后恢复生产时,因故障停机后重新开机时;b)生产所用原料变化时;
c)交收检验出现不合格批时;
d)质量监督部门提出要求时。
5.2交收检验
5.2.1每一次交货的绵白糖为一个交收批,每批绵白糖必须附有生产厂的产品合格证,收货方凭合格证收货,交收双方均有权提出在现场抽检或抽样封存。日后如有质量争议,符合贮存保管条件的样品作为仲裁检验样品,由质量仲裁机构出具的检验结果为该批绵白糖的仲裁检验结果。5.2.2绵白糖每个交收批为一个检验批。5.2.3抽样规则
5.2.3.1绵白糖抽样以堆为单位,从糖堆的四个侧面及上面共五个面抽样。上面抽中心一个点。每个侧面在其中一条对角线上按如下规定抽取若干点:300t以下(含300t)为三个点;300t以上每增加100t增加一个点,也即300t以下(含300t)的糖堆每堆抽取13个点,300t以上的堆抽取的点数按式(12)计算。
式中:m——样品质量,t,m/100取整数;n—抽样的点数,取整数。
GB 1445—2000
n = 4(m/100) + 1
(12)
5.2.3.2每点抽取绵白糖样品150g,每堆各点抽样混匀后作为该堆样品。如果每批有多个糖堆,则各糖堆的抽样混勾后作为该批样品。5.2.3.3抽样器、盛装样品容器应干净、无菌。5.2.4交收检验项目为理化要求的全部项目,需增加项目时,在供、收双方的书面合同中明确,并应注明国家认可的质量检测机构为仲裁检验机构。5.2.5抽检或仲裁检验结果,如有不合格指标应重新抽取样品对不合格指标进行复检,复检结果即作为该批的最终结果。
6标签、包装、运输、贮存
6.1绵白糖标签应符合GB7718的规定。6.1.1绵白糖标签须有下列内容:a)产品名称;
b)级别;
c)净含量(千克或克);
d)制造者的名称和地址,
e)产品标准号;
f)生产日期(可只标注年、月)。6.1.2绵白糖保存期不小于18个月。6.2包装
6.2.150kg包装
用内附一层聚乙烯薄膜的聚丙烯编织袋或其他符合食品包装要求的包装袋包装产品。包装袋必须干净、不破漏。每袋净含量偏差不得超过士0.1kg,批量产品平均偏差应大于或等于零。6.2.2小袋包装
用符合食品包装要求的包装袋包装产品,装箱后捆好。每袋净含量偏差不得超过其净含量的土2%,每箱产品净含量平均偏差应大于或等于零。6.3每批糖出厂时,由生产厂附产品合格证、运输与保管条件说明书各一份。6.4严禁与有害、有毒、有异味和其他易污染物品混贮、混运。6.5车辆运输时用苦布盖严;船舶运输和仓贮时糖堆下面应有垫层,严防受潮。6.6运输、仓贮时相对湿度应保持在50%~~70%之间,温度不应超过30℃,严防干燥。130
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
本标准3.3条为强制性的,其余为推荐性的。本标准是根据GB1445.1—1991《绵白糖》、GB/T1445.2-1991《绵白糖试验方法》及QB1681—1993《精制绵白糖》进行修订的,在技术要求上非等效采用CODEXSTAN6—1981《白糖》和《国际糖品统一分析方法》,其他条款是严格按照我国有关标准和法规的要求编写的。在技术要求中,将QB/T16811993《精制绵白糖》并人《绵白糖》国家标准,即在绵白糖的等级中增加了“精制”级别,同时取消了“二级”品等级标谁。理化要求中的“水不溶杂质”及卫生要求中的“二氧化硫”指标有所提高。
在试验方法中,“色值的测定”以缓冲溶液法代替了以往的调pH法,同时还增加了“螨的检验”。在“检验规则”中,规定了新的抽样方法。对“标签、包装、运输、贮存”一章,也根据有关最新标准和法规进行了修订。
本标准自实施之日起,同时代替GB1445.1—1991、GB/T1445.2—1991和QB/T1681-1993。本标准由国家轻工业局提出。
本标准由全国甜菜糖业标准化中心归口。本标准起草单位:国家轻工业局甜菜糖业研究所。本标推主要起草人:张继峰、王茹菊、陈枫柏。120
1范围
中华人民共和国国家标准
绵白糖
White soft sugar
GB1445--2000
代替GB1445.1-1991
GB/T1445.2--.1991
本标准规定了绵白糖的技术要求、试验方法、检验规则及标签、包装、运输、贮存的要求。本标准适用于制糖工业中利用甜菜、粗糖为原料生产的绵白糖。2引用标准
下列标准所包含的条文,通过在本标准中引用而构成为本标准的条文。本标准出版时,所示版本均为有效。所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。微生物学部分
GB4789.1~4789.31—1994食品卫生检验方法GB/T5009.55-1996食糖卫生标准的分析方法GB7718-1994食品标签通用标准
白糖卫生标准
GB 13104—1991
3技术要求
绵白糖按技术要求的规定分为精制、优级、一一级。3.1感官要求
3.1.1晶粒细小、均勾,颜色洁白,质地绵软。3.1.2晶体或其水溶液味甜、无异味。3.1.3产品的水溶液清澈、透明。3.1.4精制级别每平方米表面积内长度大于0.2mm的黑点数量不多于12个,其他级别不多于16个。
3.2理化要求
绵白糖的各项理化指标见表1。
总糖分,%
还原糖分,%
干燥失重,%
电导灰分,%
色值,IU
粒度,mm
混浊度.度
不溶于水杂质,mg/kg
国家质量技术监督局2000-11-21批准精制
0.80~1.60
0.80~2.00
1.5~2.5
0.80~2.00
2001-10-01实施
3.3卫生要求
绵白糖的各项卫生指标见表2。
砷(以As 计),mg/kg
铅(以 Pb计),mg/kg
铜(以Cu计),mg/kg
二氧化硫(以 S0),计),mg/kg
菌落总数,个/g
大肠菌群,个/100g
致病菌(系指肠道致病菌及致病球菌)螨(在250g糖中)
4试验方法
GB 1445--2000
不得检出
不得检出
不得检出
不得检出
不得检出
不得检出
卫生要求中的铅、砷、铜、二氧化硫按GB/T5009.55规定的方法进行测定,菌落总数、大肠菌群、致病菌按GB4789.1~4789.31规定的方法进行测定,其余各项均按本章相应方法进行测定。4.1粒度的测定
4.1.1方法提要
在显微镜下用测微尺测量出绵白糖晶粒长轴的平均长度。4.1.2仪器、设备
4.1.2.1显微镜。
4.1.3试剂
4.1.3.1无水乙醇。
4.1.3.2纯蔗糖。
4.1.3.3无水乙醇的饱和蔗糖溶液取足量纯蔗糖放入无水乙醇中,用玻璃棒充分搅拌,静止1h,将未溶解的燕糖过滤除去,即是无水乙醇的饱和蔗糖溶液。
4.1.4步骤
4.1.4.1测定
取少量样品放于50ml烧杯中,加入少量无水乙醇的饱和蔗糖溶液,用玻璃棒搅拌使粘在一起的晶粒分开,然后均勾铺于载玻片上,用80倍显微镜观察。选晶形整齐、大小居中的颗粒10个,用测微尺测量其长轴尺寸并记录。
4.1.4.2计算及结果表示
样品的颗粒度用式(1)计算,计算结果取到两位小数。颗粒度 一
式中:A-
-10个晶粒长轴尺寸总和。
4.2总糖分的测定
4.2.1方法提要
样品组分中去除·干燥失重和电导灰分含量后即为总糖分。4.2.2计算及结果表示
样品的总糖分用式(2)计算,计算结果取到两位小数总糖分100(X,+X)
(1)
GB 1445---2000
式中:X,—干燥失重以质量百分数表示);X2——电导灰分(以质量百分数表示)。4.3还原糖分的测定
4.3.1方法提要
在加热条件下,以四甲基蓝作指示剂,用配制好的糖溶液滴定标定过的费林氏液,根据消耗糖溶液的量,计算样品中还原糖的含量。4.3.2仪器、设备
4.3.2.1容量瓶:200ml.250mL,1000mL。4.3.2.2滴定管:50mL,刻度为0.1mL4.3.2.3吸液管:5mL。
4.3.2.4锥型管:250ml.。
4.3.2.5布氏斗及吸滤瓶。
4.3.3试剂
4.3.3.1费林氏甲液:取化学纯硫酸铜(CuSO.·5HzO)69.28g效人1000mL烧杯中,加蒸罐水约500mL后置于沸腾水浴中加热使其溶解,冷却后定容至1000mL。4.3.3.2费林氏乙液:取化学纯酒石酸钾钠(KNaC,H.O·4H,0)346g放入烧杯中,加人蒸馏水约500mL后加热使其溶解;用另一烧杯称取氢氧化钠100g,加人约500mL蒸馏水溶解;将两液混勾,冷却后定容至1000ml。
4.3.3.3纯蔗糖:取质量较好的白砂糖溶解于水中,在水浴上加热至70~80℃,继续加入白砂糖以玻璃棒搅拌,至不能溶解时为止。用少量脱脂梯作过滤介质,在保温漏斗中过滤。漏斗下放一杯无水乙醇,当热糖液滴下时不断搅拌,使自砂糖溶液在乙醇中生戒极细晶体。当杯中蔗糖晶体达到所需数量时,将部分结成小块的晶粒取出,用乳体研碎,然后一并在布氏漏斗中用真空吸滤法吸干。再将晶体溶解于70C~80℃水中至不能溶解为止。重复上述操作方法,将已经吸滤的蔗糖在乳钵中研碎,在50℃和一0.053MPa真空下于燥至恒重。4.3.3.4标准转化糖溶液(1转化糖/100mL):取9.500g纯蔗糖溶解于100mL蒸馏水中,缓慢加人分析纯浓盐酸(比重1.19)5ml,在20℃-~25C放置3天后于容量瓶中稀释至1000ml,倒人带有磨口的瓶中备用。此溶液是种稳定的储备液(可存放3~4个月),使用前随时稀释。4.3.3.5转化糖溶液(0.2g转化糖/100ml):吸取标准转化糖溶液50mL于250ml.容量瓶中,加入0.1mol氢氧化钠溶液中和后(氢氧化钠用量是以酚献为指示剂预先滴定计算雨得),加蒸罐水至标线。4.3.3.6四甲基蓝溶液(1g/100mL):称取分析纯四甲基蓝5g溶于蒸馏水中并稀释至500mL。4.3.4费林氏液的标定
吸取费林氏甲、乙液各5ml.于250mL锥形瓶中,用标准的滴定方法(见4.3.5.3)应耗用转化糖溶液(0.2g转化糖/100ml.)25.64mL。在需要进行少量调整时,可加人算好的硫铜量或水量后,随即充分摇勾。凡经调整后的溶液都应进行重新标定,直至恰好为25.64mL为止。4.3.5步骤
4.3.5.1样液的制备
称联20.00绵白糖样品,用蒸罐水溶解并定容至200ml.后装人50ml滴定管中备用。4.3.5.2预检
吸取费林氏甲、乙液各5mL手250mL维形瓶中,混匀。于滴定管中预加被检糖液15ml,在石棉网上用电炉加热至沸腾。溶液经煮沸10s~15后,如它的颜色显示费林氏液还没有还原完全,可再加糖液(一次10mL或5mL),每次沸腾后都要煮沸几秒钟直至铜离子变成橙色为止。记下滴定用去的被检糖液的总体积。
4.3.5.3标准的滴定方法
GB 1445—2000
吸取费林氏甲、乙液各5mL于250mL锥形瓶中,一次加入比预检糖液总量少0.5mL~~1.0mL的被检糖液,在石棉网上用电炉加热至沸腾,并缓和地煮沸2min(以瓶颈口不断地冒出蒸汽使费林氏液不被空气氧化为限),同时加几粒玻璃珠以防暴沸。然后加入四甲基蓝溶液2~3滴,维持沸腾并继续滴加被检糖液,滴加速度为每10s2~~~3滴,即正好在1min内完成,使整个煮沸时间为3min。记下滴定用去的被检糖液的总体积。
4.3.6计算及结果表示
还原糖含量用式(3)计算,以百分数表示,计算结果取到两位小数。还原糖(%)=
100mL被检糖液中所含还原糖的量,mg(从表3中查出);式中:1
s.--100mL被检糖液中样品量,g。4.3.7允许误差
两次测定值之差不得超过其平均值的15%。表3还原糖当量表
复检时滴定用去被
检糖液总体积,mL
100mL被检糖液含5g蔗糖时100mL被检糖液含10g蔗糖时100ml被检糖液含25g蔗糖时还原糖
100mL被检糖液
含还原糖量,mg
还原糖
100 mL被检糖液
含还原糖量,mg
还原糖
100mL被检糖液
含还原糖量,mg
复检时滴定用去被
检糖液总体积,mL
GB 1445-2000
表3(完)
100mL被检糖液含5g蔗糖时100mL被检糖液含10g蔗糖时|100mL被检糖液含25g蔗糖时还原糖
4.4电导灰分的测定
4.4.1方法提要
100mL被检糖液
含还原糖量,mg
还原糖
100mL被检糖液
含还原糖量,mg
还原糖
100mL被检糖液
含还原糖量,mg
糖品中的灰分是由无机盐类和有机盐类组成,它们在水中大部分解离成带电荷的离子。电导率表示离子化水溶性盐类的浓度。测定糖液的电导率,然后应用转换系数即可算出电导灰分。4.4.2仪器、设备
电导率仪:DDS-11A型或DDS-11型。4.4.3试剂
4.4.3.1蒸馏水或去离子水:精制绵白糖、优级白砂糖必须用电导率低于2uS/cm的蒸馏水或去离子水。一级绵白糖充允许用电导率低于15 μuS/cm的蒸馏水。4.4.3.20.01mol/L氯化钾溶液:取分析纯氯化钾,加热至500℃(呈暗红炽热)脱水30min后,称取0.7455g,溶解于1000mL容量瓶中,并加水至标线。此溶液在20℃时电导率为1278μS/cm。4.4.3.30.0025mol/L氯化钾溶液:吸取0.01mol/L氯化钾溶液250mL移人1000mL容量瓶内,加水稀释至标线。此溶液在20℃时电导率为328μS/cm。4.4.4步骤
4.4.4.1测定
称取(31.7士0.1)g绵白糖样品于干洁烧杯中,加蒸馏水溶解并移人100mL容量瓶中,用蒸馏水多次冲洗烧杯及玻璃棒,洗水一并移人容量瓶中,加水至标线,摇匀。先用样液冲洗电导电极2~3次,然后将样液倒人小烧杯中,用电导率仪测定样液的电导率,记录读数及当时样液的温度。电导池常数应用0.0025mol/L氯化钾溶液校核计量。4.4.4.2计算及结果表示
电导灰分用式(4)计算,以百分数表示,计算结果取到两位小数。电导灰分(%)=6×10-4(C—0.35C2)式中:C,---
被测糖液在(20士0.2)℃时的电导率,μS/cm;-溶糖所用蒸馏水在(20士0.2)℃时的电导率,μS/cm。4.4.4.3温度校正
(4)
测定电导率的标准温度为(20士0.2)℃,如测定电导率时温度不在(20士0.2)℃时,则按式(5)校正,但测量温度范围一般不应超过(20士5)℃。溶糖用蒸馏水的电导率,因温度对其影响甚微,故可忽略不计,不需校正。
C = Ct[1 + 0. 026(20 — t)J
式中:Ci
被测糖液在t℃时的电导率,uS/cm;-测定糖液电导率时糖液的温度;℃。t
·(5)
4.4.4.4允许误差
GB 1445—2000
两次测定值之差不得超过其平均值的10%。4.5干燥失重的测定
4.5.1方法提要
将样品在一定温度及真空度的条件下进行干燥后称量,根据干燥前后样品失去的质量计算出样品的干燥失重。
4.5.2仪器、设备
4.5.2.1真空干燥箱:0~0.1MPa,温度范围0~100℃。4.5.2.2称量皿:直径50mm,单层盖。4.5.2.3天平:感量0.0001g。
4.5.3步骤
4.5.3.1测定
用恒重过的称量皿称取绵白糖样品约10.000g,开盖置于真空干燥箱内干燥60min(温度70℃~75C,真空度0.067MPa)。盖盖后将称量血取出置于干燥器内冷却至室温后称量。4.5.3.2计算及结果表示
干燥失重用式(6)计算,以百分数表示,计算结果取到两位小数。W-w×100
干燥失重(%)=
式中:W.——称量皿的质量,g;W2——称量血和干燥前样品的总质量,g;W3一—称量血和干燥后样品的总质量,g。4.5.3.3允许误差
两次测定值之差不得超过0.05%。4.6色值的测定
4.6.1方法提要
绵白糖样品用pH7.0士0.1缓冲溶液溶解后,经滤膜过滤,然后在420nm波长条件下以蒸馏水做参比溶液,测量溶液的吸光系数,将吸光系数的数值乘以1000,即为ICUMSA色值,单位(IU)。4.6.2仪器、设备
4.6.2.1分光光度计:测试范围0~2A,精度0.01A,波长精度(4201)nm;4.6.2.2比色血:1~5cm;用于测定与作参比的两只比色血,透光度不应超过0.2%(用蒸馏水检查)。4.6.2.3滤膜过滤器:带有孔径为0.45um滤膜和吸滤瓶。4.6.2.4阿贝折射仪:糖用。
4.6.2.5pH(酸度)计:分度值或最小显示值0.02pH。4.6.3试剂
4.6.3.10.1mol/l.盐酸溶液。
4.6.3.2三乙醇胺-盐酸缓冲溶液:称取三乙醇胺[(HOCH,CH,)NJ14.920g,用蒸馏水溶解并定容至1000mL,然后移人2000mL烧杯内,加人0.1mol/盐酸溶液约800mL,搅拌均匀并继续用0.1mol/L盐酸调到pH7.0(用酸度计的电极浸于此溶液中测量pH值),于棕色玻璃瓶中。4.6.4步骤
4.6.4.1测定
称取绵白糖样品100.0g,置于200ml烧杯中,加人三乙醇胺-盐酸缓冲溶液135ml,搅拌至完全溶解。倒人已预先铺好孔径为0.45μm滤膜的过滤器中在真空下抽滤,弃去最初50mL滤液,收集不少于50mI.的滤液后测其锤度,然后用比色皿装盛糖液,以三乙醇胺-盐酸缓冲溶液作参比,在分光光度126
计上于420nm波长下测其吸光度。GB1445—2000
蔗糖溶液折光锤度与每毫升含蔗糖克数(在空气中)对照表表4方
折光锤度
4.6.4.2计算及结果表示
折光锤度
色值用式(7)计算,以IU表示,计算结果取整数。国际糖色值:
式中:A420
折光锤度
在420nm波长下测得样液的吸光度;比色皿厚度,cm;
× 1 000
折光锤度
样液浓度(由校正到20℃的锤度乘上系数0.9854后查表4求得),g/mL。C
4.6.4.3允许误差
两次测定值之差不得超过4IU。
4.7混浊度的测定
4.7.1方法提要
当单色光透过含有悬浮粒子(混浊)的溶液时,由于悬浮粒子引起光的散射,单色光强度产生衰减,以光的衰减程度减去颜色的影响表示溶液的混浊度。4.7.2仪器、设备
同4.6.2条。
4.7.3步骤
4.7.3.1测定
取待测色值的未过滤糖液,在与测定色值相同的条件下,测其吸光度,并按式(8)计算其衰减指数。A420
衰减指数=
式中:A420…一在420nm波长下测得的未过滤样液的吸光度;b-—比色血厚度,cm;
一样液浓度(由校正到20℃的锤度乘上系数0.9854后查表4求得),g/mL。4.7.3.2计算及结果表示
混浊度用式(9)计算,单位为度,计算结果取整数。混浊度2
式中:\
过滤前糖液衰减指数,IU;
·(9)
过滤后溶糖色值指数,IU。
4.7.3.3允许误差
两次测定值之差不得超过1度。
4.8不溶于水杂质的测定
4.8.1方法提要
GB 1445-2000
用G3埚漏斗将糖液真空抽滤,再以较大量的蒸馏水洗涤滤渣,然后将滤渣干燥至恒重,计算出其在样品中的含量。
4.8.2仪器、设备
4.8.2.1G3漏斗:直径32mm。
4.8.2.2干燥箱。
4.8.2.3天平:感量0.0001g。
4.8.3试剂免费标准bzxz.net
4.8.3.11%α-萘酚乙醇溶液:称取α-萘酚1g,用95%乙醇溶解至100mL。4.8.3.2浓硫酸:含硫酸95%~98%。4.8.4步骤
4.8.4.1测定
称取绵白糖样品500.0g置于1000mL烧杯中,加约50℃蒸馏水700mL,搅拌至糖全部溶解,倾人经恒重的G3漏斗中进行真空抽滤。以蒸馏水充分洗涤滤渣,用α-酚乙醇溶液检查,至洗涤液不含糖分为止。将G3埚漏斗置于干燥箱内,在125~130℃下烘干1.0h,取出置于干燥器中冷却至室温后称量。然后再继续烘干0.5h,冷却后称量,重复操作,直至相继两次质量相差不超过0.001g为止,此时可认为达到恒重,记录其质量。微糖检验方法:取2mL洗涤液于试管中,加入数滴1%α-萘酚乙醇溶液,再沿管壁缓缓加人2mL浓硫酸。在水与酸的界面出现紫色环,说明有糖存在;若为黄绿色环,则说明无糖存在。4.8.4.2计算及结果表示
每千克绵白糖样品所含不溶于水杂质毫克数用式(10)计算,计算结果取整数。不溶于水杂质=㎡2二㎡× 106
-G3埚漏斗的质量,g;;
式中:m,-
-G3埚漏斗和不溶于水杂质的总质量,,m。--称取绵白糖样品的质量,g。4.8.4.3允许误差
两次测定值之差不得超过其平均值的15%。4.9黑点的测定
4.9.1方法提要
在瓷盘中盛满样品压平,检查表面黑点的个数后计算出单位面积内黑点的个数。4.9.2仪器、设备
4.9.2.1白瓷盘:表面积约0.25m2。4.9.2.2玻璃板。
4.9.3步骤
4. 9.3.1测定
在瓷盘中盛满样品,用玻璃板压平,然后在强光下检查长度大于0.2mm黑点的个数。4.9.3.2计算及结果表示
绵白糖样品黑点个数(个/m2)用式(11)计算。128
( 10)
GB 1445—2000
黑点个数 =× 4
式中:α——
查得瓷盘内样品中黑点个数,个。4.10螨的测定
4.10.1方法提要
取定量糖样用水溶于锥形瓶中,镜检糖液表面的漂浮物,以确定是否有螨及螨的数目。4.10.2仪器、设备
4.10.2.1显微镜。
4.10.2.2放大镜。
4.10.2.3锥形瓶:500mL。
4.10.3步骤
4.10.3.1测定
(11)
称取250g绵白糖样品置于500mL锥形瓶中,加人不高于25℃的蒸馏水并不断搅拌,使其完全溶解。再渐渐补充蒸馏水至瓶口处,以不使水溢出为止。然后用洁净的盖玻片置于瓶口处,使之与液面接触,静置15min,取下镜检。这一操作重复若干次,镜检所有的漂浮物。4.10.3.2计算及结果表示
镜检出的螨的数目即为250g绵白糖样品中的总螨数,以个为单位。5检验规则
5.1型式检验
5.1.1取样方法
每分离一罐糖膏为一个编号,在称量包装时,连续采取样品约5kg,放在带盖的容器中,混勾后为编号样品。该样品除供编号分析之用外,另取0.5kg放在带盖的容器中,积累24h后为日集合样品。取1.5kg日集合样品,用双层食品级塑料袋密封包装,或用磨砂口玻璃瓶盛装,标明产品编号、级别、生产日期、全批包数、检验结果及检验员,在相对湿度50%~70%、温度不超过30℃的环境中存留,供生产和质量管理查验之用。经供收双方认可,也可作为仲裁检验留样。5.1.2生产厂在保证质量的前提下,每编号样品和每日集合样品可按生产的实际情况进行指标的抽检。检验结果如有一项或多项不符合该级别的技术要求的,则按实达级别处理。达不到一级的按不合格处理。
5.1.3有下列情况之-时,应进行本标准的技术要求中的全部指标的检验。a)生产期开始时,洗罐后恢复生产时,因故障停机后重新开机时;b)生产所用原料变化时;
c)交收检验出现不合格批时;
d)质量监督部门提出要求时。
5.2交收检验
5.2.1每一次交货的绵白糖为一个交收批,每批绵白糖必须附有生产厂的产品合格证,收货方凭合格证收货,交收双方均有权提出在现场抽检或抽样封存。日后如有质量争议,符合贮存保管条件的样品作为仲裁检验样品,由质量仲裁机构出具的检验结果为该批绵白糖的仲裁检验结果。5.2.2绵白糖每个交收批为一个检验批。5.2.3抽样规则
5.2.3.1绵白糖抽样以堆为单位,从糖堆的四个侧面及上面共五个面抽样。上面抽中心一个点。每个侧面在其中一条对角线上按如下规定抽取若干点:300t以下(含300t)为三个点;300t以上每增加100t增加一个点,也即300t以下(含300t)的糖堆每堆抽取13个点,300t以上的堆抽取的点数按式(12)计算。
式中:m——样品质量,t,m/100取整数;n—抽样的点数,取整数。
GB 1445—2000
n = 4(m/100) + 1
(12)
5.2.3.2每点抽取绵白糖样品150g,每堆各点抽样混匀后作为该堆样品。如果每批有多个糖堆,则各糖堆的抽样混勾后作为该批样品。5.2.3.3抽样器、盛装样品容器应干净、无菌。5.2.4交收检验项目为理化要求的全部项目,需增加项目时,在供、收双方的书面合同中明确,并应注明国家认可的质量检测机构为仲裁检验机构。5.2.5抽检或仲裁检验结果,如有不合格指标应重新抽取样品对不合格指标进行复检,复检结果即作为该批的最终结果。
6标签、包装、运输、贮存
6.1绵白糖标签应符合GB7718的规定。6.1.1绵白糖标签须有下列内容:a)产品名称;
b)级别;
c)净含量(千克或克);
d)制造者的名称和地址,
e)产品标准号;
f)生产日期(可只标注年、月)。6.1.2绵白糖保存期不小于18个月。6.2包装
6.2.150kg包装
用内附一层聚乙烯薄膜的聚丙烯编织袋或其他符合食品包装要求的包装袋包装产品。包装袋必须干净、不破漏。每袋净含量偏差不得超过士0.1kg,批量产品平均偏差应大于或等于零。6.2.2小袋包装
用符合食品包装要求的包装袋包装产品,装箱后捆好。每袋净含量偏差不得超过其净含量的土2%,每箱产品净含量平均偏差应大于或等于零。6.3每批糖出厂时,由生产厂附产品合格证、运输与保管条件说明书各一份。6.4严禁与有害、有毒、有异味和其他易污染物品混贮、混运。6.5车辆运输时用苦布盖严;船舶运输和仓贮时糖堆下面应有垫层,严防受潮。6.6运输、仓贮时相对湿度应保持在50%~~70%之间,温度不应超过30℃,严防干燥。130
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。