GB/T 22946-2008
基本信息
标准号: GB/T 22946-2008
中文名称:蜂王浆和蜂王浆冻干粉中林可霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、克林霉素、吉他霉素、交沙霉素残留量的测定 液相色谱-串联质谱法
标准类别:国家标准(GB)
标准状态:现行
发布日期:2008-12-31
实施日期:2009-05-01
出版语种:简体中文
下载格式:.rar.pdf
下载大小:632775
相关标签: 蜂王浆 林可霉素 红霉素 菌素 螺旋霉素 霉素 残留量 测定 色谱 串联 质谱法

标准分类号
标准ICS号:食品技术>>67.050食品试验和分析的一般方法
中标分类号:食品>>食品综合>>X04基础标准与通用方法
关联标准
出版信息
出版社:中国标准出版社
页数:16页
标准价格:16.0 元
计划单号:20079482-T-469
出版日期:2009-05-01
相关单位信息
首发日期:2008-12-31
起草人:王飞、王海洋、曹彦忠、贾光群、张进杰、石玉秋、庞国芳
起草单位:中华人民共和国秦皇岛出入境检验检疫局
归口单位:国家质量监督检验检疫总局
提出单位:国家质量监督检验检疫总局
发布部门:中华人民共和国国家质量监督检验检疫总局 中国国家标准化管理委员会
主管部门:国家标准化管理委员会
标准简介
本标准规定了蜂王浆和蜂王浆冻干粉中林可霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、克林霉素、吉他霉素和交沙霉素残留量的液相色谱?串联质谱测定方法。本标准适用于蜂王浆和蜂王浆冻干粉中林可霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、克林霉素、吉他霉素和交沙霉素残留量的测定。 GB/T 22946-2008 蜂王浆和蜂王浆冻干粉中林可霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、克林霉素、吉他霉素、交沙霉素残留量的测定 液相色谱-串联质谱法 GB/T22946-2008 标准下载解压密码:www.bzxz.net
标准图片预览




标准内容
ICS67.050
中华人民共和国国家标准
GB/T22946-2008
蜂王浆和蜂王浆冻干粉中林可霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、克林霉素、吉他霉素、交沙霉素残留量的测定液相色谱-串联质谱法Determination of lincomycin,erythromycin,tilmicosin,tylosin,spiramycinclindamycin,kitasamycin and josamycin residues in royal jelly andlyophilizedroyaljellypowderLC-MS-MSmethod2008-12-31发布
中华人民共和国国家质量监督检验检疫总局中国国家标准化管理委员会
2009-05-01实施
本标准的附录A、附录B为资料性附录。本标准由国家质量监督检验检疫总局提出并归口。本标准起草单位:中华人民共和国秦皇岛出入境检验检疫局。本标准主要起草人:王飞、王海洋、曹彦忠、贾光群、张进杰、石玉秋、庞国芳。GB/T22946—2008
1范围
蜂王浆和蜂王浆冻干粉中林可霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、克林霉素、吉他霉素、交沙霉素残留量的测定液相色谱-串联质谱法GB/T22946—2008
本标准规定了蜂王浆和蜂王浆冻干粉中林可霍素、红霍素、替米考星、泰乐菌素、螺旋霉素、克林霜素、吉他霉素和交沙霉素残留量的液相色谱-串联质谱测定方法。本标准适用于蜂王浆和蜂王浆冻干粉中林可霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、克林霉素、吉他霉素和交沙霉素残留量的测定。本标准的方法检出限:蜂王浆中的林可霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、克林霉素、吉他霉素、交沙霉素均为2.0μg/kg;蜂王浆冻干粉中的林可霉素、红霉素、泰乐菌素、克林霉素、交沙霉素均为2.0μg/kg,替米考星、螺旋霉素、吉他霉素均为5.0μg/kg。2规范性引用文件
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用手本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。GB/T6379.1测量方法与结果的准确度(正确度与精密度)第1部分:总则与定义(GB/T6379.1-2004,ISO5725-1:1994,IDT)GB/T6379.2测量方法与结果的准确度(正确度与精密度)第2部分:确定标准测量方法重复性与再现性的基本方法(GB/T6379.2—2004,ISO5725-2:1994,IDT)GB/T6682分析实验室用水规格和试验方法(GB/T6682—2008,ISO3696:1987,MOD)3原理
蜂王浆和蜂王浆冻干粉中林可霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、克林霉素、吉他霉素和交沙霉素的残留用Tris提取液提取,提取液经OasisHLB固相萃取柱\净化,甲醇洗脱,洗脱液浓缩定容后,供液相色谱串联质谱法测定。外标法定量。4试剂和材料
除另有说明外,所用试剂均为分析纯。4.1水:GB/T6682,一级。
4.2甲醇:色谱纯。
4.3乙酸铵。
4.4乙腈:色谱纯。
4.5盐酸。
OasisHLB固相萃取柱是Waters公司产品的商品名称,给出这一信息是为了方便本标准的使用者,并不是表1
示对该产品的认可。如果其他等效产品具有相同的效果,则可使用这些等效产品。GB/T22946—2008
4.6三羟甲基氨基甲烷(Tris):C,HiNOs。4.7氯化钙(CaClz·2H,O)。
4.8甲醇溶液(2+3):量取400mL甲醇(4.2)与600mL水混合。4.90.01mol/L乙酸铵溶液:0.77g乙酸铵(4.3)溶解于水中,定容于1000mL容量瓶中。4.10定容液:0.01mol/L乙酸铵溶液(4.9)十乙腈(4.4)(17+3)。4.11Tris提取液:称取12.0g三羟甲基氨基甲烷(4.6)和7.35g氯化钙(4.7)溶解于水中,用盐酸(4.5)调节pH值为9,定容至1000mL。4.12标准物质:林可霉素(CAS:7179-49-9)、红霉素(CAS:59319-72-1)、替米考星(CAS:108050-54-0)、泰乐菌素(CAS:74610-55-2)、螺旋霉素(CAS:8025-81-8)、克林霉素(CAS:21462-39-5)、吉他霉素(CAS:1392-21-8)和交沙霉素(CAS:16846-24-5)纯度≥95%。4.13标准储备溶液I:1.0mg/mL。分别准确称取每种标准物质(4.12)适量,分别放入相对应的10mL容量瓶中,用甲醇溶解并定容至刻度,混匀。4℃保存。4.14标准储备溶液Ⅱ:10.0μg/mL。分别吸取0.1mL各标准储备溶液(4.13),分别放人相对应的10mL容量瓶中,用甲醇定容至刻度。4℃保存。4.15标准工作溶液:2.0μg/mL。分别吸取2.0mL标准储备溶液(4.14),分别放入相对应的10mL容量瓶中,用甲醇定容至刻度
4.16OasisHLB固相萃取柱或相当者:500mg,6mL。使用前,依次用10mL甲醇和10mL水活化在抽真空前的各步骤中,都保持柱体湿润。4.17滤膜:0.2μm。
5仪器
5.1液相色谱-串联质谱仪:配有电喷雾离子源。5.2天平:感量0.01g,0.0001g。5.3固相萃取装置。
5.4氮气浓缩仪。
5.5具塞聚丙烯离心管:50mL。
5.6离心机。
5.7超声波清洗仪。
5.8pH计。
5.9振荡器。
6试样制备与保存
6.1试样的制备
从全部样品中取出有代表性样品约200g,充分混匀,均分成两份,分别装人洁净容器内。密封后作为试样,标明标记。在抽样和制样的操作过程中,应防止样品受到污染或发生残留物含量的变化6.2试样的保存
将蜂王浆试样于一18℃保存。蜂王浆冻干粉试样密封保存,防止吸潮。7测定步骤
7.1提取
称取2g蜂王浆试样(蜂王浆冻干粉取1g),精确至0.01g,置于50mL离心管(5.5)中,加人10.0mLTris提取液(4.11),于振荡器上剧烈振荡10min。以18000g离心力离心10min,取上清液以小于1.0mL/min的流速通过OasisHLB固相萃取柱(4.16)。再加人10.0mLTris提取液(4.11),2
GB/T22946—2008
于振荡器上剧烈振荡10min。以18000g离心力离心10min,取上清液以小于1.0mL/min的流速通过OasisHLB固相萃取柱。
7.2净化
待样液全部流出后,依次用10mL水和10mL甲醇溶液(4.8)洗柱,弃去全部流出液,将固相萃取柱用真空泵减压抽干1h。再用10mL甲醇(4.2)洗脱于15mL氮吹管中,用氮气浓缩仪于50℃水浴中吹至近于,准确加人1.0mL定容液(4.10)后,于超声波清洗仪中溶解残渣。过0.2μm滤膜(4.17后,供液相色谱-串联质谱仪测定。7.3基质标准混合工作溶液的制备7.3.1蜂王浆用基质标准混合工作溶液的制备:分别吸取1.0μL、2.0μL、5.0μL、25μL的林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素标准工作溶液(4.15),依次加入相对应的阴性样品中,按7.1、7.2步骤制备林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素分别为2.0ng/mL、5.0ng/mL,10.0ng/mL50.0ng/mL四个浓度水平的系列基质标准混合工作溶液。
7.3.2蜂王浆冻干粉用基质标准混合工作溶液的制备:分别吸取1.0μL、2.0μL、5.0μL、25μL林可霉素、红霉素、克林霉素、泰乐菌素、交沙霉素标准工作溶液(4.15)和2.5μL、5.0μL、10.0μL、25μL的替米考星、螺旋霉素、吉他霉素标准工作溶液(4.15),依次加人相对应的阴性样品中,按7.1、7.2步骤制备林可霉素、红霉素、克林霉素、泰乐菌素、交沙霉素分别为2.0ng/mL、4.0ng/mL、10.0ng/mL、50.0ng/mL和替米考星、螺旋霉素、吉他霉素分别为5.0ng/mL、10.0ng/mL、20.0ng/mL50.0ng/mL四个浓度水平的系列基质标准混合工作溶液。7.4测定条件
7.4.1液相色谱参考条件
a)色谱柱:AtlantisC8,3μm,150mmX2.1mm(内径)或相当者;b)
流动相:A:乙腈,B:0.1%甲酸水溶液,C:甲醇。梯度洗脱条件见表1;流速:0.2mL/min;
柱温:30℃;
进样量:20μL。
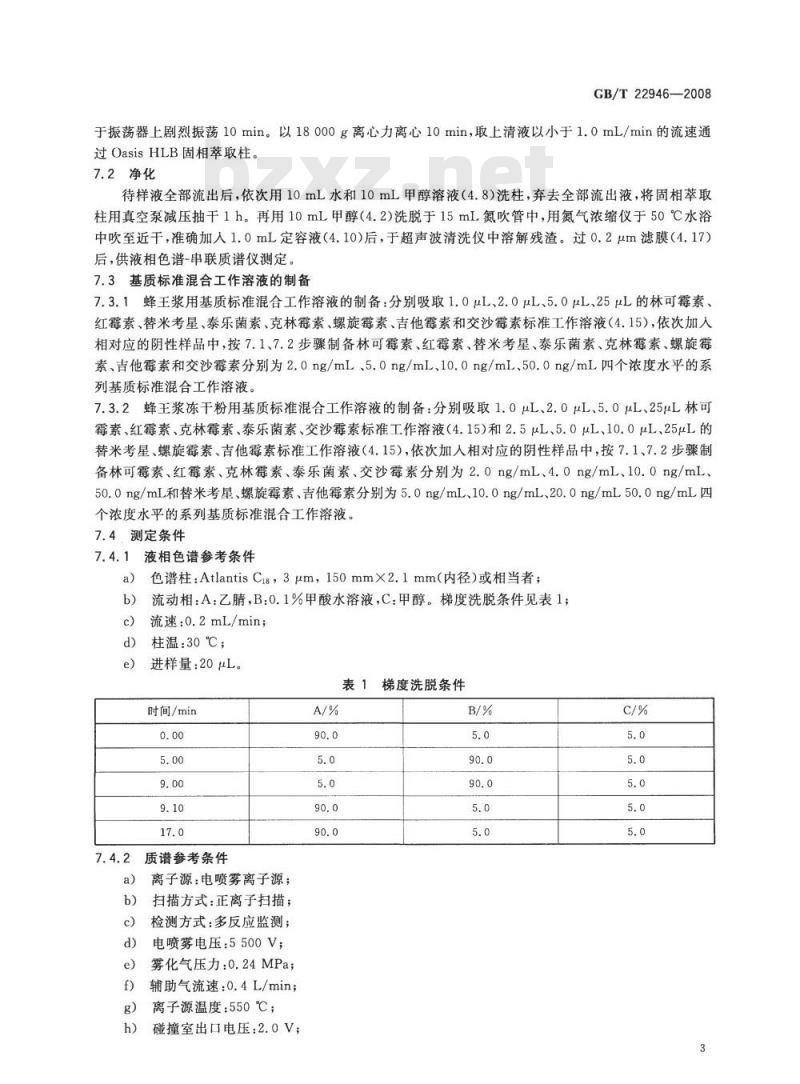
表1梯度洗脱条件
时间/min
质谱参考条件
离子源:电喷雾离子源;
扫描方式:正离子扫描;
检测方式:多反应监测;
电喷雾电压:5500V;
雾化气压力:0.24MPa;
辅助气流速:0.4L/min;
离子源温度:550℃;
碰撞室出口电压:2.0V;
GB/T22946—2008
定性离子对、定量离子对、碰撞气能量和去簇电压:见表2,表2林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素定性离子对、定量离子对、碰撞气能量和去簇电压化合物中文名称
林可霉素
红霉素
替米考星
泰乐菌素
克林霖素
螺旋霉素
吉他霉素
交沙霉素
化合物英文名称
lincomycin
erythromycin
tilmicosin
tylosin
clindamycin
spiramycin
kitasamycin
josamycin
7.5液相色谱-串联质谱测定
7.5.1定性测定
定性离子对(m/2)
407/126
407/359
734/158
734/576
869/174
869/132
916/174
916/145
425/126
425/377
843/142
843/174
772/215bzxZ.net
772/109
828/174
828/109
定量离子对(m/2)
407/126
734/158
869/174
916/174
425/126
843/142
772/215
828/174
碰撞气能量/V
去簇电压/V
被测组分选择1个母离子,2个以上子离子,在相同的试验条件下,样品中待测物质的保留时间与标准溶液中对应的保留时间偏差在士2.5%之内;且样品中各定性离子相对丰度与浓度接近的基质标准工作溶液中被测物的各定性离子相对丰度进行比较,若偏差不超过表3规定的范围,则可判定为样品中存在对应的待测物。
表3定性确证时相对离子丰度的最大允许偏差相对离子丰度K
允许最大偏差
7.5.2定量测定
2010以%表示
K≤10
在仪器最佳工作条件下,以基质标准工作溶液浓度为横坐标,以峰面积为纵坐标,绘制标准工作曲线。用基质标准工作溶液的工作曲线对样品进行定量,应使样品溶液中林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素的响应值在仪器测定的线性范围内。在上述色谱条件和质谱条件下,林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他素和交沙霉素的参考保留时间见表4。4
GB/T22946--2008
表4林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素参考保留时间
化合物名称
林可霉素
红霉素
替米考星
泰乐菌素
克林霉素
螺旋霉素
吉他莓素
交沙莓素
保留时间/min
林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素的标准物质多反应监测(MRM)色谱图参见附录A中的图A.1、图A.2、图A.3、图A.4、图A.5、图A.6、图A.7、图A.8。
林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素添加浓度及其平均回收率的试验数据参见附录B中的表B.1。7.6平行试验
按上述步骤,对同一试样进行平行试验测定。7.7空白试验
不称取样品,其余均按步骤7.1和7.2进行。8结果计算
林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素的残留量按式(1)计算:
式中:
-试样中被测组分残留量,单位为毫克每千克(mg/kg);从标准工作曲线得到的被测组分溶液浓度,单位为微克每毫升(ug/mL);试样溶液定容体积,单位为毫升(mL);V
试样溶液所代表试样的质量,单位为克(g)。计算结果应扣除空白值。
9精密度
9.1一般规定
本标准的精密度数据是按照GB/T6379.1和GB/T6379.2的规定确定的,其重复性和再现性的值是以95%的可信度来计算。
9.2重复性
在重复性试验条件下,获得的两次独立测试结果的绝对差值不超过重复性限r,林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素添加浓度范围及重复性方程见表5。5
GB/T22946—2008
5林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素表5
添加浓度范围及重复性和再现性方程化合物名称
林可霉素
红霉素
替米考星
泰乐菌素
克林霉素
螺旋霉素
吉他霉素
交沙霉素
添加浓度范围
注:m为两次测定值的算术平均值。重复性限,
lgr=0.9392lgm-1.0304
Ig r=0.7974lgm-0.981 1
lgr=1.0318lgm-0.9859
lgr=1.0569lgm0.9993
Igr=1. 0798lgm-1.1495
lgr=0.9125lgm-0.9751
Ig r=1.100 1 lgm-1. 0250
lgr=1.4389lgm-1.4185
单位为微克每千克
再现性R
lgR=0.8741lgm-0.5182
lgR=1.0506lgm-0.5775
lgR=0.9853lgm-0.5561
lgR=0.8513lgm-0.5616
lg R=0. 885 4 lg m-0. 414 6
lgR=1.0432lgm-0.5917
lgR=1.1453lgm-0.7665
lg R=1.1227lgm-0,6965
如果差值超过重复性限r,应舍弃试验结果并重新完成两次单个试验的测定。再现性
在再现性试验条件下,获得的两次独立测试结果的绝对差值不超过再现性限R,林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素的添加浓度范围及再现性方程见表5。附录A
(资料性附录)
标准物质多反应监测(MRM)色谱图GB/T22946—2008
林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素的标准物质多反应监测(MRM)色谱图分别见图A.1、图A.2、图A.3、图A.4、图A.5、图A.6、图A.7、图A.8。响应值
响应值
响应值
响应值
101112
林可霉素标准物质多反应监测(MRM)色谱图图A.1
89101112131415/min
红霉素标准物质多反应监测(MRM)色谱图8.36
替米考星标准物质多反应监测(MRM)色谱图图A3
15t/min
泰乐菌素标准物质多反应监测(MRM)色谱图7
GB/T22946-—2008
响应值
响应值
响应值
响应值
克林霉素标准物质多反应监测(MRM)色谱图8.67
螺旋霉素标准物质多反应监测(MRM)色谱图8.83
101112131415
吉他霉素标准物质多反应监测(MRM)色谱图9.14
交沙霉素标准物质多反应监测(MRM)色谱图t/min
15t/min
附录B
(资料性附录)
回收率
GB/T22946—2008
本方法中,林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素添加浓度及其平均回收率的试验数据见表B.1。表B.1林可霉素、红霉素、替米考星、泰乐茵素、克林霉素、螺旋霉素、吉他霉素和交沙霉素添加浓度及其平均回收率的试验数据化合物名称
林可霉素
红霉素
替米考星
泰乐菌素
克林霉素
螺旋霉素
吉他霉素
交沙霉素
添加浓度/(pg/kg)
平均回收率/%
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
中华人民共和国国家标准
GB/T22946-2008
蜂王浆和蜂王浆冻干粉中林可霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、克林霉素、吉他霉素、交沙霉素残留量的测定液相色谱-串联质谱法Determination of lincomycin,erythromycin,tilmicosin,tylosin,spiramycinclindamycin,kitasamycin and josamycin residues in royal jelly andlyophilizedroyaljellypowderLC-MS-MSmethod2008-12-31发布
中华人民共和国国家质量监督检验检疫总局中国国家标准化管理委员会
2009-05-01实施
本标准的附录A、附录B为资料性附录。本标准由国家质量监督检验检疫总局提出并归口。本标准起草单位:中华人民共和国秦皇岛出入境检验检疫局。本标准主要起草人:王飞、王海洋、曹彦忠、贾光群、张进杰、石玉秋、庞国芳。GB/T22946—2008
1范围
蜂王浆和蜂王浆冻干粉中林可霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、克林霉素、吉他霉素、交沙霉素残留量的测定液相色谱-串联质谱法GB/T22946—2008
本标准规定了蜂王浆和蜂王浆冻干粉中林可霍素、红霍素、替米考星、泰乐菌素、螺旋霉素、克林霜素、吉他霉素和交沙霉素残留量的液相色谱-串联质谱测定方法。本标准适用于蜂王浆和蜂王浆冻干粉中林可霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、克林霉素、吉他霉素和交沙霉素残留量的测定。本标准的方法检出限:蜂王浆中的林可霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、克林霉素、吉他霉素、交沙霉素均为2.0μg/kg;蜂王浆冻干粉中的林可霉素、红霉素、泰乐菌素、克林霉素、交沙霉素均为2.0μg/kg,替米考星、螺旋霉素、吉他霉素均为5.0μg/kg。2规范性引用文件
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用手本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。GB/T6379.1测量方法与结果的准确度(正确度与精密度)第1部分:总则与定义(GB/T6379.1-2004,ISO5725-1:1994,IDT)GB/T6379.2测量方法与结果的准确度(正确度与精密度)第2部分:确定标准测量方法重复性与再现性的基本方法(GB/T6379.2—2004,ISO5725-2:1994,IDT)GB/T6682分析实验室用水规格和试验方法(GB/T6682—2008,ISO3696:1987,MOD)3原理
蜂王浆和蜂王浆冻干粉中林可霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、克林霉素、吉他霉素和交沙霉素的残留用Tris提取液提取,提取液经OasisHLB固相萃取柱\净化,甲醇洗脱,洗脱液浓缩定容后,供液相色谱串联质谱法测定。外标法定量。4试剂和材料
除另有说明外,所用试剂均为分析纯。4.1水:GB/T6682,一级。
4.2甲醇:色谱纯。
4.3乙酸铵。
4.4乙腈:色谱纯。
4.5盐酸。
OasisHLB固相萃取柱是Waters公司产品的商品名称,给出这一信息是为了方便本标准的使用者,并不是表1
示对该产品的认可。如果其他等效产品具有相同的效果,则可使用这些等效产品。GB/T22946—2008
4.6三羟甲基氨基甲烷(Tris):C,HiNOs。4.7氯化钙(CaClz·2H,O)。
4.8甲醇溶液(2+3):量取400mL甲醇(4.2)与600mL水混合。4.90.01mol/L乙酸铵溶液:0.77g乙酸铵(4.3)溶解于水中,定容于1000mL容量瓶中。4.10定容液:0.01mol/L乙酸铵溶液(4.9)十乙腈(4.4)(17+3)。4.11Tris提取液:称取12.0g三羟甲基氨基甲烷(4.6)和7.35g氯化钙(4.7)溶解于水中,用盐酸(4.5)调节pH值为9,定容至1000mL。4.12标准物质:林可霉素(CAS:7179-49-9)、红霉素(CAS:59319-72-1)、替米考星(CAS:108050-54-0)、泰乐菌素(CAS:74610-55-2)、螺旋霉素(CAS:8025-81-8)、克林霉素(CAS:21462-39-5)、吉他霉素(CAS:1392-21-8)和交沙霉素(CAS:16846-24-5)纯度≥95%。4.13标准储备溶液I:1.0mg/mL。分别准确称取每种标准物质(4.12)适量,分别放入相对应的10mL容量瓶中,用甲醇溶解并定容至刻度,混匀。4℃保存。4.14标准储备溶液Ⅱ:10.0μg/mL。分别吸取0.1mL各标准储备溶液(4.13),分别放人相对应的10mL容量瓶中,用甲醇定容至刻度。4℃保存。4.15标准工作溶液:2.0μg/mL。分别吸取2.0mL标准储备溶液(4.14),分别放入相对应的10mL容量瓶中,用甲醇定容至刻度
4.16OasisHLB固相萃取柱或相当者:500mg,6mL。使用前,依次用10mL甲醇和10mL水活化在抽真空前的各步骤中,都保持柱体湿润。4.17滤膜:0.2μm。
5仪器
5.1液相色谱-串联质谱仪:配有电喷雾离子源。5.2天平:感量0.01g,0.0001g。5.3固相萃取装置。
5.4氮气浓缩仪。
5.5具塞聚丙烯离心管:50mL。
5.6离心机。
5.7超声波清洗仪。
5.8pH计。
5.9振荡器。
6试样制备与保存
6.1试样的制备
从全部样品中取出有代表性样品约200g,充分混匀,均分成两份,分别装人洁净容器内。密封后作为试样,标明标记。在抽样和制样的操作过程中,应防止样品受到污染或发生残留物含量的变化6.2试样的保存
将蜂王浆试样于一18℃保存。蜂王浆冻干粉试样密封保存,防止吸潮。7测定步骤
7.1提取
称取2g蜂王浆试样(蜂王浆冻干粉取1g),精确至0.01g,置于50mL离心管(5.5)中,加人10.0mLTris提取液(4.11),于振荡器上剧烈振荡10min。以18000g离心力离心10min,取上清液以小于1.0mL/min的流速通过OasisHLB固相萃取柱(4.16)。再加人10.0mLTris提取液(4.11),2
GB/T22946—2008
于振荡器上剧烈振荡10min。以18000g离心力离心10min,取上清液以小于1.0mL/min的流速通过OasisHLB固相萃取柱。
7.2净化
待样液全部流出后,依次用10mL水和10mL甲醇溶液(4.8)洗柱,弃去全部流出液,将固相萃取柱用真空泵减压抽干1h。再用10mL甲醇(4.2)洗脱于15mL氮吹管中,用氮气浓缩仪于50℃水浴中吹至近于,准确加人1.0mL定容液(4.10)后,于超声波清洗仪中溶解残渣。过0.2μm滤膜(4.17后,供液相色谱-串联质谱仪测定。7.3基质标准混合工作溶液的制备7.3.1蜂王浆用基质标准混合工作溶液的制备:分别吸取1.0μL、2.0μL、5.0μL、25μL的林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素标准工作溶液(4.15),依次加入相对应的阴性样品中,按7.1、7.2步骤制备林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素分别为2.0ng/mL、5.0ng/mL,10.0ng/mL50.0ng/mL四个浓度水平的系列基质标准混合工作溶液。
7.3.2蜂王浆冻干粉用基质标准混合工作溶液的制备:分别吸取1.0μL、2.0μL、5.0μL、25μL林可霉素、红霉素、克林霉素、泰乐菌素、交沙霉素标准工作溶液(4.15)和2.5μL、5.0μL、10.0μL、25μL的替米考星、螺旋霉素、吉他霉素标准工作溶液(4.15),依次加人相对应的阴性样品中,按7.1、7.2步骤制备林可霉素、红霉素、克林霉素、泰乐菌素、交沙霉素分别为2.0ng/mL、4.0ng/mL、10.0ng/mL、50.0ng/mL和替米考星、螺旋霉素、吉他霉素分别为5.0ng/mL、10.0ng/mL、20.0ng/mL50.0ng/mL四个浓度水平的系列基质标准混合工作溶液。7.4测定条件
7.4.1液相色谱参考条件
a)色谱柱:AtlantisC8,3μm,150mmX2.1mm(内径)或相当者;b)
流动相:A:乙腈,B:0.1%甲酸水溶液,C:甲醇。梯度洗脱条件见表1;流速:0.2mL/min;
柱温:30℃;
进样量:20μL。
表1梯度洗脱条件
时间/min
质谱参考条件
离子源:电喷雾离子源;
扫描方式:正离子扫描;
检测方式:多反应监测;
电喷雾电压:5500V;
雾化气压力:0.24MPa;
辅助气流速:0.4L/min;
离子源温度:550℃;
碰撞室出口电压:2.0V;
GB/T22946—2008
定性离子对、定量离子对、碰撞气能量和去簇电压:见表2,表2林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素定性离子对、定量离子对、碰撞气能量和去簇电压化合物中文名称
林可霉素
红霉素
替米考星
泰乐菌素
克林霖素
螺旋霉素
吉他霉素
交沙霉素
化合物英文名称
lincomycin
erythromycin
tilmicosin
tylosin
clindamycin
spiramycin
kitasamycin
josamycin
7.5液相色谱-串联质谱测定
7.5.1定性测定
定性离子对(m/2)
407/126
407/359
734/158
734/576
869/174
869/132
916/174
916/145
425/126
425/377
843/142
843/174
772/215bzxZ.net
772/109
828/174
828/109
定量离子对(m/2)
407/126
734/158
869/174
916/174
425/126
843/142
772/215
828/174
碰撞气能量/V
去簇电压/V
被测组分选择1个母离子,2个以上子离子,在相同的试验条件下,样品中待测物质的保留时间与标准溶液中对应的保留时间偏差在士2.5%之内;且样品中各定性离子相对丰度与浓度接近的基质标准工作溶液中被测物的各定性离子相对丰度进行比较,若偏差不超过表3规定的范围,则可判定为样品中存在对应的待测物。
表3定性确证时相对离子丰度的最大允许偏差相对离子丰度K
允许最大偏差
7.5.2定量测定
20
K≤10
在仪器最佳工作条件下,以基质标准工作溶液浓度为横坐标,以峰面积为纵坐标,绘制标准工作曲线。用基质标准工作溶液的工作曲线对样品进行定量,应使样品溶液中林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素的响应值在仪器测定的线性范围内。在上述色谱条件和质谱条件下,林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他素和交沙霉素的参考保留时间见表4。4
GB/T22946--2008
表4林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素参考保留时间
化合物名称
林可霉素
红霉素
替米考星
泰乐菌素
克林霉素
螺旋霉素
吉他莓素
交沙莓素
保留时间/min
林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素的标准物质多反应监测(MRM)色谱图参见附录A中的图A.1、图A.2、图A.3、图A.4、图A.5、图A.6、图A.7、图A.8。
林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素添加浓度及其平均回收率的试验数据参见附录B中的表B.1。7.6平行试验
按上述步骤,对同一试样进行平行试验测定。7.7空白试验
不称取样品,其余均按步骤7.1和7.2进行。8结果计算
林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素的残留量按式(1)计算:
式中:
-试样中被测组分残留量,单位为毫克每千克(mg/kg);从标准工作曲线得到的被测组分溶液浓度,单位为微克每毫升(ug/mL);试样溶液定容体积,单位为毫升(mL);V
试样溶液所代表试样的质量,单位为克(g)。计算结果应扣除空白值。
9精密度
9.1一般规定
本标准的精密度数据是按照GB/T6379.1和GB/T6379.2的规定确定的,其重复性和再现性的值是以95%的可信度来计算。
9.2重复性
在重复性试验条件下,获得的两次独立测试结果的绝对差值不超过重复性限r,林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素添加浓度范围及重复性方程见表5。5
GB/T22946—2008
5林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素表5
添加浓度范围及重复性和再现性方程化合物名称
林可霉素
红霉素
替米考星
泰乐菌素
克林霉素
螺旋霉素
吉他霉素
交沙霉素
添加浓度范围
注:m为两次测定值的算术平均值。重复性限,
lgr=0.9392lgm-1.0304
Ig r=0.7974lgm-0.981 1
lgr=1.0318lgm-0.9859
lgr=1.0569lgm0.9993
Igr=1. 0798lgm-1.1495
lgr=0.9125lgm-0.9751
Ig r=1.100 1 lgm-1. 0250
lgr=1.4389lgm-1.4185
单位为微克每千克
再现性R
lgR=0.8741lgm-0.5182
lgR=1.0506lgm-0.5775
lgR=0.9853lgm-0.5561
lgR=0.8513lgm-0.5616
lg R=0. 885 4 lg m-0. 414 6
lgR=1.0432lgm-0.5917
lgR=1.1453lgm-0.7665
lg R=1.1227lgm-0,6965
如果差值超过重复性限r,应舍弃试验结果并重新完成两次单个试验的测定。再现性
在再现性试验条件下,获得的两次独立测试结果的绝对差值不超过再现性限R,林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素的添加浓度范围及再现性方程见表5。附录A
(资料性附录)
标准物质多反应监测(MRM)色谱图GB/T22946—2008
林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素的标准物质多反应监测(MRM)色谱图分别见图A.1、图A.2、图A.3、图A.4、图A.5、图A.6、图A.7、图A.8。响应值
响应值
响应值
响应值
101112
林可霉素标准物质多反应监测(MRM)色谱图图A.1
89101112131415/min
红霉素标准物质多反应监测(MRM)色谱图8.36
替米考星标准物质多反应监测(MRM)色谱图图A3
15t/min
泰乐菌素标准物质多反应监测(MRM)色谱图7
GB/T22946-—2008
响应值
响应值
响应值
响应值
克林霉素标准物质多反应监测(MRM)色谱图8.67
螺旋霉素标准物质多反应监测(MRM)色谱图8.83
101112131415
吉他霉素标准物质多反应监测(MRM)色谱图9.14
交沙霉素标准物质多反应监测(MRM)色谱图t/min
15t/min
附录B
(资料性附录)
回收率
GB/T22946—2008
本方法中,林可霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉他霉素和交沙霉素添加浓度及其平均回收率的试验数据见表B.1。表B.1林可霉素、红霉素、替米考星、泰乐茵素、克林霉素、螺旋霉素、吉他霉素和交沙霉素添加浓度及其平均回收率的试验数据化合物名称
林可霉素
红霉素
替米考星
泰乐菌素
克林霉素
螺旋霉素
吉他霉素
交沙霉素
添加浓度/(pg/kg)
平均回收率/%
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。