GB/T 24401-2009
基本信息
标准号: GB/T 24401-2009
中文名称:α-淀粉酶制剂
标准类别:国家标准(GB)
标准状态:现行
发布日期:2009-09-30
出版语种:简体中文
下载格式:.rar .pdf
下载大小:6237770

标准分类号
关联标准
出版信息
出版社:中国标准出版社
标准价格:0.0 元
出版日期:2010-03-01
相关单位信息
发布部门:中华人民共和国国家质量监督检验检疫总局 中国国家标准化管理委员会
标准简介
GB/T 24401-2009 α-淀粉酶制剂 GB/T24401-2009 标准下载解压密码:www.bzxz.net
标准图片预览




标准内容
ICS07.100.30
中华人民共和国国家标准
GB/T24401—2009
α-淀粉酶制剂
Alpha-amylasepreparation
2009-09-30发布
中华人民共和国国家质量监督检验检疫总局中国国家标准化管理委员会
2010-03-01实施
GB/T24401—2009
本标准以QB/T1805.1—1993《工业用α-淀粉酶制剂》和QB/T2306—1997《耐高温α-淀粉酶制剂》为基础,首次制定。
本标准的附录A为规范性附录,附录B、附录C为资料性附录。本标准由全国食品工业标准化技术委员会提出。本标准由全国食品工业标准化技术委员会工业发酵分技术委员会归口。本标准起草单位:中国食品发酵工业研究院、无锡赛德生物工程有限公司、山东隆大生物工程有限公司、诺维信(中国)生物技术有限公司、江阴市百圣龙生物工程有限公司、邢台新欣翔宇生物工程有限责任公司。
本标准主要起草人:张蔚、吴炳炎、郭庆文、张晶雪、顾建龙、余波、郭新光、胡洪清、杨西江、曹振宇、陆志冲、魏坤。
1范围
α-淀粉酶制剂
GB/T244012009
本标准规定了α-淀粉酶制剂的术语和定义、产品分类、要求、试验方法、检验规则和标志、包装、运输、贮存要求。
本标准适用于以淀粉质(或糖质)为原料,经发酵、提纯制得的α-淀粉酶制剂产品的生产、检验和销售。主要用于食品工业、纺织工业等。其他来源的α-淀粉酶制剂可参照相关类别使用,用作饲料添加剂的α-淀粉酶制剂可参照A类产品执行。2规范性引用文件
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。GB/T191包装储运图示标志
GB/T601
化学试剂标准滴定溶液的制备
GB/T6682分析实验室用水规格和试验方法GB8275食品添加剂α-淀粉酶制剂QB/T1803—1993工业酶制剂通用试验方法3术语和定义
下列术语和定义适用于本标准。3.1
a-淀粉酶alpha-amylase
能水解淀粉分子链中的α-1,4-葡萄糖苷键,将淀粉链切断成为短链糊精和少量麦芽糖和葡萄糖,使淀粉粘度迅速下降的酶。
中温a-淀粉酶活力activityofmediumtemperaturealpha-amylase1g固体酶粉(或1mL液体酶),于60℃、pH值6.0条件下,1h液化1g可溶性淀粉,即为1个酶活力单位,以“u/g(u/mL)”表示。3.3
耐高温α-淀粉酶活力activityofheat-tolerantalpha-amylase1g固体酶粉(或1mL液体酶),于70℃、pH值6.0条件下,1min液化1mg可溶性淀粉,即为1个酶活力单位,以u/g(u/mL)”表示。4产品分类
4.1按产品的应用领域
A类:食品/饲料工业用酶。
B类:其他工业用酶。
4.2按产品的适用温度
中温α-淀粉酶制剂和耐高温α-淀粉酶制剂。1
GB/T24401—2009
4.3按产品形态
液体剂型酶制剂和固体剂型酶制剂。5要求
5.1外观
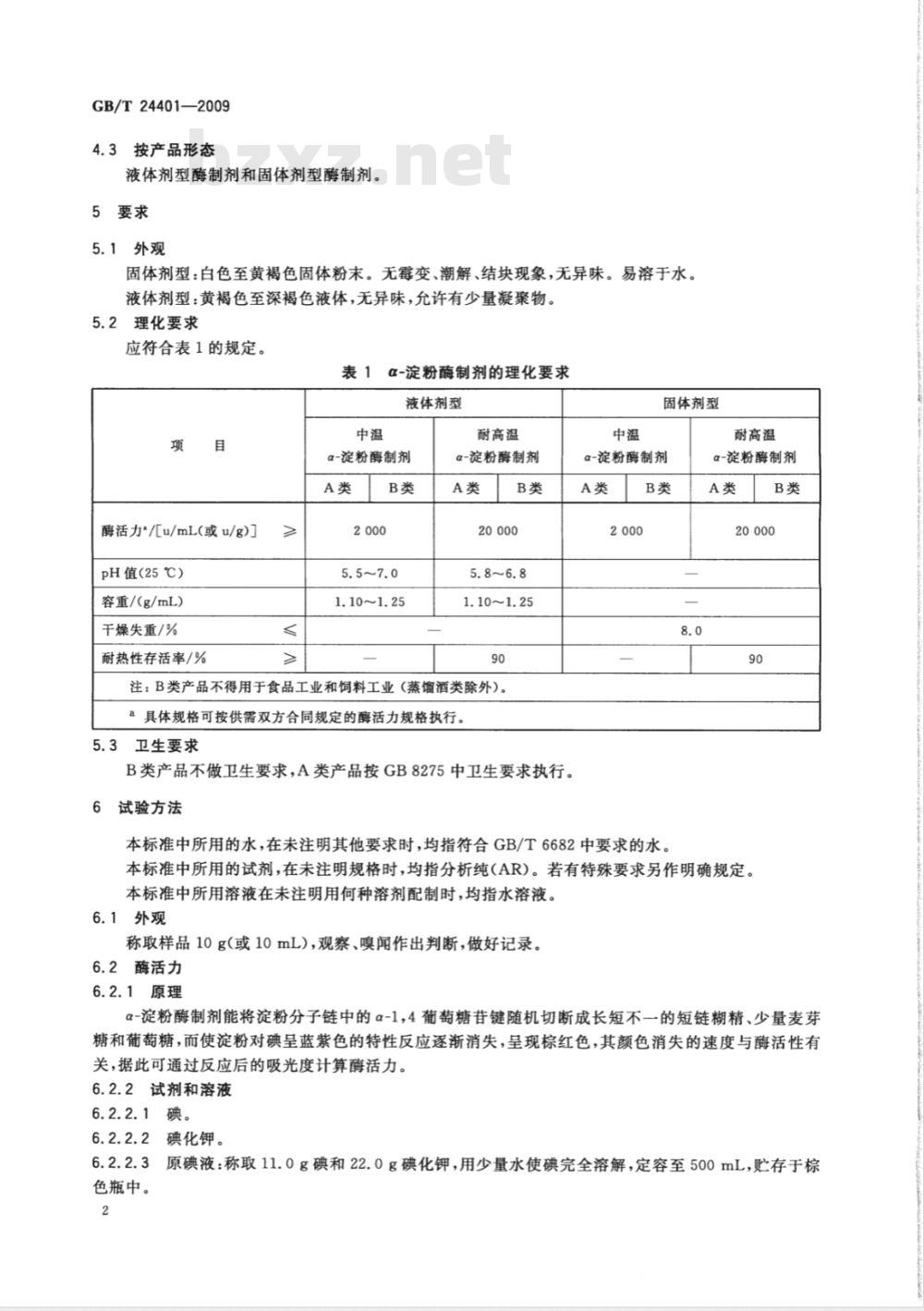
固体剂型:白色至黄褐色固体粉末。无霉变、潮解、结块现象,无异味。易溶于水。液体剂型:黄褐色至深褐色液体,无异味,允许有少量凝聚物。5.2理化要求
应符合表1的规定。
表1α-淀粉酶制剂的理化要求
液体剂型
酶活力*/[u/mL(或u/g)]
pH值(25℃)
容重/(g/mL)
干燥失重/%
耐热性存活率/%
α-淀粉酶制剂
1.10~1.25
耐高温
α-淀粉酶制剂
1.10~1.25
注:B类产品不得用于食品工业和饲料工业(蒸馏酒类除外)a具体规格可按供需双方合同规定的酶活力规格执行。5.3卫生要求
B类产品不做卫生要求,A类产品按GB8275中卫生要求执行。6试验方法
固体剂型
α-淀粉酶制剂
本标准中所用的水,在未注明其他要求时,均指符合GB/T6682中要求的水。8.0
耐高温
α-淀粉酶制剂Www.bzxZ.net
本标准中所用的试剂,在未注明规格时,均指分析纯(AR)。若有特殊要求另作明确规定。本标准中所用溶液在未注明用何种溶剂配制时,均指水溶液。6.1外观
称取样品10g(或10mL),观察、嗅闻作出判断,做好记录。6.2酶活力
6.2.1原理
α-淀粉酶制剂能将淀粉分子链中的α-1,4葡萄糖苷键随机切断成长短不一的短链糊精、少量麦芽糖和葡萄糖,而使淀粉对碘呈蓝紫色的特性反应逐渐消失,呈现棕红色,其颜色消失的速度与酶活性有关,据此可通过反应后的吸光度计算酶活力。6.2.2试剂和溶液
6.2.2.1碘。
6.2.2.2碘化钾。
6.2.2.3原碘液:称取11.0g碘和22.0g碘化钾,用少量水使碘完全溶解,定容至500mL,贮存于棕色瓶中。
GB/T24401—2009
6.2.2.4稀碘液:吸取原碘液2.00mL,加20.0g碘化钾用水溶解并定容至500mL,贮存于棕色瓶中。
6.2.2.5可溶性淀粉溶液(20g/L):称取2.000g(精确至0.001g)可溶性淀粉(以绝干计)于烧杯中,用少量水调成浆状物,边搅拌边缓缓加入70mL沸水中,然后用水分次冲洗装淀粉的烧杯,洗液倒入其中,搅拌加热至完全透明,冷却定容至100mL。溶液现配现用。注:可溶性淀粉采用酶制剂专用可溶性淀粉。6.2.2.6磷酸缓冲液(pH=6.0):称取45.23g磷酸氢二钠(Na2HPO4·12HzO)和8.07g柠檬酸(CHgO,·HzO),用水溶解并定容至1000mL。用pH计校正后使用。6.2.2.7盐酸溶液[c(HCI)=0.1mol/L]:按GB/T601配制。6.2.3仪器和设备
除实验室常规仪器外还有以下仪器和设备。6.2.3.1分光光度计。
6.2.3.2恒温水浴:精度士0.1℃。6.2.3.3自动移液器。
6.2.3.4试管:25mmX200mm。
6.2.3.5秒表。
6.2.4分析步骤
6.2.4.1待测酶液的制备
称取1g~2g酶粉(精确至0.0001g)或准确吸取酶液1.00mL,用少量磷酸缓冲液(6.2.2.6)充分溶解,将上清液小心倾入容量瓶中,若有剩余残渣,再加少量磷酸缓冲液(6.2.2.6)充分研磨,最终样品全部移入容量瓶中,用磷酸缓冲液(6.2.2.6)定容至刻度,摇匀。用四层纱布过滤,滤液待用。注:待测中温α-淀粉酶酶液酶活力浓度控制在3.4u/mL~4.5u/mL范围内,待测耐高温α-淀粉酶活力浓度控制在60u/mL~65u/mL范围内。
6.2.4.2测定
吸取20.0mL可溶性淀粉溶液(6.2.2.5)于试管(6.2.3.4)中,加人磷酸缓冲液(6.2.2.6)5.00mL,摇匀后,置于60℃士0.2℃(耐高温α-淀粉酶制剂置于70℃士0.2℃)恒温水浴中预热8min。
加人1.00mL稀释好的待测酶液(6.2.4.1),立即计时,摇匀,准确反应5min。立即用自动移液器吸取1.00mL反应液,加到预先盛有0.5mL盐酸溶液(6.2.2.7)和5.00mL稀碘液(6.2.2.4)的试管中,摇匀,并以0.5mL盐酸溶液和5.00mL稀碘液为空白,于660nm波长下,用10mm比色血迅速测定其吸光度(A)。根据吸光度查附录A,求得测试酶液的浓度。6.2.4.3计算
中温α-淀粉酶制剂的酶活力按式(1)计算:X,=c×n
式中:
X,——样品的酶活力,u/mL(或u/g);-测试酶样的浓度,u/mL(或u/g);n
样品的稀释倍数。
所得结果表示至整数,
耐高温α-淀粉酶制剂的酶活力按式(2)计算:X2=c×n×16.67
式中:
X2——样品的酶活力,u/mL(或u/g);(1)
·(2)
GB/T24401—2009
c——测试酶样的浓度,u/mL(或u/g);n——样品的稀释倍数;
16.67根据酶活力定义计算的换算系数。所得结果表示至整数。
6.2.5允许差
平行试验相对误差不得超过5%。6.3pH值
按QB/T1803—1993中第9章执行。6.4耐高温α-淀粉酶制剂耐热性存活率6.4.1试剂和溶液
6.4.1.1氢氧化钠溶液[c(NaOH)=0.1mol/L]:按GB/T601配制。6.4.1.2糊精溶液:称取糊精100.0g于烧杯中,加水300mL,搅匀,加人耐高温α-淀粉酶制剂(按每克糊精13u酶活力加人),置于电炉上加热至沸腾,冷却,用氢氧化钠溶液(6.4.1.1)调pH值至6.0~7.0,移入500mL容量瓶,稀释,定容,摇匀备用。6.4.2仪器和设备
恒温水浴:精度土0.1℃。
6.4.3分析步骤
6.4.3.1待测酶液的制备
除用糊精溶液(6.4.1.2)代替磷酸缓冲溶液(6.2.2.6)外,其余同6.2.4.1。6.4.3.2热处理
吸取25mL待测酶液于50mL比色管中,置于95℃恒温水浴中热处理60min,冷却,补水至原酶液体积,摇匀,备用。
6.4.3.3酶活力测定
按6.2.4.2测定制备6.4.3.1时所用酶制剂的酶活力;按6.2.4.2测定热处理后的待测酶液(6.4.3.2)的酶活力。
6.4.4计算
耐热性存活率按式(3)计算:
X=E/E×100
式中:
X.—-样品酶耐热性存活率,%;
E,———样品热处理后实测的酶活力,u/mL(或u/g);E—样品热处理前实测的酶活力,u/mL(或u/g)。所得结果表示至整数。
6.5容重
按QB/T1803—1993执行。
6.6干燥失重
按QB/T1803—1993执行。
7检验规则
7.1批次的确定
由生产单位按照其相应的规则负责确定产品的批号,批内产品的品质应均一。7.2取样规则和样本量
取样应均匀分布在整个灌装过程中,或均匀分布于灌装后的成品中。(3)
取样时应采用适宜的方法保证取样具有代表性,保证取样部位和取样瓶的清洁。对用于微生物检4
验的取样,应使用无菌操作。
GB/T24401-2009
成品抽样的样本量见表2。取样的样本量可按照估计的批量参照表2执行,或由生产企业和(或)相关方确定。
成品抽样的样本量
批量/桶(或箱)
51~500
注1:批取样量不得少于300mL(或300g),不足者应按比例适当加取。样本量/瓶(或袋)
注2:批量是指批中所包含的单位商品数,单位为桶(或箱)。样本量是指样本中所包含的单位样本数,单位为瓶(或袋)。
7.3出厂检验
每批产品出厂时,应对外观、酶活力、pH值、容重、干燥失重(固体),A类产品的菌落总数等逐项进行检验。
7.4型式检验
产品在正常生产情况下,每年至少进行一次型式检验,遇有下列情况之一时按本标准全部要求进行检验:
-正常生产时,至少每年对产品检验一次;正常生产时,如原料、配方或工艺有较大改变,可能影响产品质量时;更换设备,或产品长期停产又恢复生产时;出厂检验结果与平常记录有较大差别时;国家质量监督部门提出要求时。7.5判定规则
出厂检验和(或)型式检验合格时,由质量检验部门出具产品合格证。出厂检验和(或)型式检验不合格时,在原批次基础上加倍取样分析。如仍不合格,判定该产品为不合格品,不得出厂。
8标志、包装、运输及贮存
8.1标志
产品的外包装宜使用符合GB/T191要求的标志。产品的包装上应贴有牢固的标签。标识内容应包括品名、产地、厂名、卫生许可证号、规格、生产日期、批号或代号、保质期等。A类产品的标签的内容应符合相关规定。8.2包装
产品的内包装和(或)包装容器的内涂料应采用国家批准的材料,A类产品应符合相应的食品包装用或食品容器卫生标准的材料。8.3运输
产品在运输过程中应轻拿轻放,严防雨淋和曝晒。运输工具应清洁、无毒、无污染。严禁与有毒、有害、有腐蚀性的物质混装混运。8.4贮存
产品应贮存在阴凉干燥的环境下。严禁与有毒、有害、有腐蚀性的物质同存。8.5保质期
8.5.1在25℃以下,液体酶制剂保质期不少于90d;固体酶制剂保质期不少于180d,企业应按上述要求具体标示。
8.5.2在保质期内,实测酶活力不应低于标示酶活力。5
GB/T24401—2009
吸光度(A)
附录A
(规范性附录)
吸光度与测试α-淀粉酶酶浓度对照表表A.1
酶浓度(c)/(u/mL)
吸光度与测试α-淀粉酶酶浓度对照表吸光度(A)
酶浓度(c)/(u/mL)
吸光度(A)
酶浓度(c)/(u/mL)
吸光度(A)
酶浓度(c)/(u/mL)
表A.1(续)
吸光度(A)
酶浓度(c)/(u/mL)
吸光度(A)
GB/T24401—2009
酶浓度(c)/(u/mL)
GB/T24401—2009
吸光度(A)
酶浓度(c)/(u/mL)
表A.1(续)
吸光度(A)
酶浓度(c)/(u/mL)
吸光度(A)
酶浓度(c)/(u/mL)
吸光度(A)
酶浓度(c)/(u/mL)
表A.1(续)
吸光度(A)
酶浓度(c)/(u/mL)
吸光度(A)
GB/T24401—2009
酶浓度(c)/(u/mL)
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
中华人民共和国国家标准
GB/T24401—2009
α-淀粉酶制剂
Alpha-amylasepreparation
2009-09-30发布
中华人民共和国国家质量监督检验检疫总局中国国家标准化管理委员会
2010-03-01实施
GB/T24401—2009
本标准以QB/T1805.1—1993《工业用α-淀粉酶制剂》和QB/T2306—1997《耐高温α-淀粉酶制剂》为基础,首次制定。
本标准的附录A为规范性附录,附录B、附录C为资料性附录。本标准由全国食品工业标准化技术委员会提出。本标准由全国食品工业标准化技术委员会工业发酵分技术委员会归口。本标准起草单位:中国食品发酵工业研究院、无锡赛德生物工程有限公司、山东隆大生物工程有限公司、诺维信(中国)生物技术有限公司、江阴市百圣龙生物工程有限公司、邢台新欣翔宇生物工程有限责任公司。
本标准主要起草人:张蔚、吴炳炎、郭庆文、张晶雪、顾建龙、余波、郭新光、胡洪清、杨西江、曹振宇、陆志冲、魏坤。
1范围
α-淀粉酶制剂
GB/T244012009
本标准规定了α-淀粉酶制剂的术语和定义、产品分类、要求、试验方法、检验规则和标志、包装、运输、贮存要求。
本标准适用于以淀粉质(或糖质)为原料,经发酵、提纯制得的α-淀粉酶制剂产品的生产、检验和销售。主要用于食品工业、纺织工业等。其他来源的α-淀粉酶制剂可参照相关类别使用,用作饲料添加剂的α-淀粉酶制剂可参照A类产品执行。2规范性引用文件
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。GB/T191包装储运图示标志
GB/T601
化学试剂标准滴定溶液的制备
GB/T6682分析实验室用水规格和试验方法GB8275食品添加剂α-淀粉酶制剂QB/T1803—1993工业酶制剂通用试验方法3术语和定义
下列术语和定义适用于本标准。3.1
a-淀粉酶alpha-amylase
能水解淀粉分子链中的α-1,4-葡萄糖苷键,将淀粉链切断成为短链糊精和少量麦芽糖和葡萄糖,使淀粉粘度迅速下降的酶。
中温a-淀粉酶活力activityofmediumtemperaturealpha-amylase1g固体酶粉(或1mL液体酶),于60℃、pH值6.0条件下,1h液化1g可溶性淀粉,即为1个酶活力单位,以“u/g(u/mL)”表示。3.3
耐高温α-淀粉酶活力activityofheat-tolerantalpha-amylase1g固体酶粉(或1mL液体酶),于70℃、pH值6.0条件下,1min液化1mg可溶性淀粉,即为1个酶活力单位,以u/g(u/mL)”表示。4产品分类
4.1按产品的应用领域
A类:食品/饲料工业用酶。
B类:其他工业用酶。
4.2按产品的适用温度
中温α-淀粉酶制剂和耐高温α-淀粉酶制剂。1
GB/T24401—2009
4.3按产品形态
液体剂型酶制剂和固体剂型酶制剂。5要求
5.1外观
固体剂型:白色至黄褐色固体粉末。无霉变、潮解、结块现象,无异味。易溶于水。液体剂型:黄褐色至深褐色液体,无异味,允许有少量凝聚物。5.2理化要求
应符合表1的规定。
表1α-淀粉酶制剂的理化要求
液体剂型
酶活力*/[u/mL(或u/g)]
pH值(25℃)
容重/(g/mL)
干燥失重/%
耐热性存活率/%
α-淀粉酶制剂
1.10~1.25
耐高温
α-淀粉酶制剂
1.10~1.25
注:B类产品不得用于食品工业和饲料工业(蒸馏酒类除外)a具体规格可按供需双方合同规定的酶活力规格执行。5.3卫生要求
B类产品不做卫生要求,A类产品按GB8275中卫生要求执行。6试验方法
固体剂型
α-淀粉酶制剂
本标准中所用的水,在未注明其他要求时,均指符合GB/T6682中要求的水。8.0
耐高温
α-淀粉酶制剂Www.bzxZ.net
本标准中所用的试剂,在未注明规格时,均指分析纯(AR)。若有特殊要求另作明确规定。本标准中所用溶液在未注明用何种溶剂配制时,均指水溶液。6.1外观
称取样品10g(或10mL),观察、嗅闻作出判断,做好记录。6.2酶活力
6.2.1原理
α-淀粉酶制剂能将淀粉分子链中的α-1,4葡萄糖苷键随机切断成长短不一的短链糊精、少量麦芽糖和葡萄糖,而使淀粉对碘呈蓝紫色的特性反应逐渐消失,呈现棕红色,其颜色消失的速度与酶活性有关,据此可通过反应后的吸光度计算酶活力。6.2.2试剂和溶液
6.2.2.1碘。
6.2.2.2碘化钾。
6.2.2.3原碘液:称取11.0g碘和22.0g碘化钾,用少量水使碘完全溶解,定容至500mL,贮存于棕色瓶中。
GB/T24401—2009
6.2.2.4稀碘液:吸取原碘液2.00mL,加20.0g碘化钾用水溶解并定容至500mL,贮存于棕色瓶中。
6.2.2.5可溶性淀粉溶液(20g/L):称取2.000g(精确至0.001g)可溶性淀粉(以绝干计)于烧杯中,用少量水调成浆状物,边搅拌边缓缓加入70mL沸水中,然后用水分次冲洗装淀粉的烧杯,洗液倒入其中,搅拌加热至完全透明,冷却定容至100mL。溶液现配现用。注:可溶性淀粉采用酶制剂专用可溶性淀粉。6.2.2.6磷酸缓冲液(pH=6.0):称取45.23g磷酸氢二钠(Na2HPO4·12HzO)和8.07g柠檬酸(CHgO,·HzO),用水溶解并定容至1000mL。用pH计校正后使用。6.2.2.7盐酸溶液[c(HCI)=0.1mol/L]:按GB/T601配制。6.2.3仪器和设备
除实验室常规仪器外还有以下仪器和设备。6.2.3.1分光光度计。
6.2.3.2恒温水浴:精度士0.1℃。6.2.3.3自动移液器。
6.2.3.4试管:25mmX200mm。
6.2.3.5秒表。
6.2.4分析步骤
6.2.4.1待测酶液的制备
称取1g~2g酶粉(精确至0.0001g)或准确吸取酶液1.00mL,用少量磷酸缓冲液(6.2.2.6)充分溶解,将上清液小心倾入容量瓶中,若有剩余残渣,再加少量磷酸缓冲液(6.2.2.6)充分研磨,最终样品全部移入容量瓶中,用磷酸缓冲液(6.2.2.6)定容至刻度,摇匀。用四层纱布过滤,滤液待用。注:待测中温α-淀粉酶酶液酶活力浓度控制在3.4u/mL~4.5u/mL范围内,待测耐高温α-淀粉酶活力浓度控制在60u/mL~65u/mL范围内。
6.2.4.2测定
吸取20.0mL可溶性淀粉溶液(6.2.2.5)于试管(6.2.3.4)中,加人磷酸缓冲液(6.2.2.6)5.00mL,摇匀后,置于60℃士0.2℃(耐高温α-淀粉酶制剂置于70℃士0.2℃)恒温水浴中预热8min。
加人1.00mL稀释好的待测酶液(6.2.4.1),立即计时,摇匀,准确反应5min。立即用自动移液器吸取1.00mL反应液,加到预先盛有0.5mL盐酸溶液(6.2.2.7)和5.00mL稀碘液(6.2.2.4)的试管中,摇匀,并以0.5mL盐酸溶液和5.00mL稀碘液为空白,于660nm波长下,用10mm比色血迅速测定其吸光度(A)。根据吸光度查附录A,求得测试酶液的浓度。6.2.4.3计算
中温α-淀粉酶制剂的酶活力按式(1)计算:X,=c×n
式中:
X,——样品的酶活力,u/mL(或u/g);-测试酶样的浓度,u/mL(或u/g);n
样品的稀释倍数。
所得结果表示至整数,
耐高温α-淀粉酶制剂的酶活力按式(2)计算:X2=c×n×16.67
式中:
X2——样品的酶活力,u/mL(或u/g);(1)
·(2)
GB/T24401—2009
c——测试酶样的浓度,u/mL(或u/g);n——样品的稀释倍数;
16.67根据酶活力定义计算的换算系数。所得结果表示至整数。
6.2.5允许差
平行试验相对误差不得超过5%。6.3pH值
按QB/T1803—1993中第9章执行。6.4耐高温α-淀粉酶制剂耐热性存活率6.4.1试剂和溶液
6.4.1.1氢氧化钠溶液[c(NaOH)=0.1mol/L]:按GB/T601配制。6.4.1.2糊精溶液:称取糊精100.0g于烧杯中,加水300mL,搅匀,加人耐高温α-淀粉酶制剂(按每克糊精13u酶活力加人),置于电炉上加热至沸腾,冷却,用氢氧化钠溶液(6.4.1.1)调pH值至6.0~7.0,移入500mL容量瓶,稀释,定容,摇匀备用。6.4.2仪器和设备
恒温水浴:精度土0.1℃。
6.4.3分析步骤
6.4.3.1待测酶液的制备
除用糊精溶液(6.4.1.2)代替磷酸缓冲溶液(6.2.2.6)外,其余同6.2.4.1。6.4.3.2热处理
吸取25mL待测酶液于50mL比色管中,置于95℃恒温水浴中热处理60min,冷却,补水至原酶液体积,摇匀,备用。
6.4.3.3酶活力测定
按6.2.4.2测定制备6.4.3.1时所用酶制剂的酶活力;按6.2.4.2测定热处理后的待测酶液(6.4.3.2)的酶活力。
6.4.4计算
耐热性存活率按式(3)计算:
X=E/E×100
式中:
X.—-样品酶耐热性存活率,%;
E,———样品热处理后实测的酶活力,u/mL(或u/g);E—样品热处理前实测的酶活力,u/mL(或u/g)。所得结果表示至整数。
6.5容重
按QB/T1803—1993执行。
6.6干燥失重
按QB/T1803—1993执行。
7检验规则
7.1批次的确定
由生产单位按照其相应的规则负责确定产品的批号,批内产品的品质应均一。7.2取样规则和样本量
取样应均匀分布在整个灌装过程中,或均匀分布于灌装后的成品中。(3)
取样时应采用适宜的方法保证取样具有代表性,保证取样部位和取样瓶的清洁。对用于微生物检4
验的取样,应使用无菌操作。
GB/T24401-2009
成品抽样的样本量见表2。取样的样本量可按照估计的批量参照表2执行,或由生产企业和(或)相关方确定。
成品抽样的样本量
批量/桶(或箱)
51~500
注1:批取样量不得少于300mL(或300g),不足者应按比例适当加取。样本量/瓶(或袋)
注2:批量是指批中所包含的单位商品数,单位为桶(或箱)。样本量是指样本中所包含的单位样本数,单位为瓶(或袋)。
7.3出厂检验
每批产品出厂时,应对外观、酶活力、pH值、容重、干燥失重(固体),A类产品的菌落总数等逐项进行检验。
7.4型式检验
产品在正常生产情况下,每年至少进行一次型式检验,遇有下列情况之一时按本标准全部要求进行检验:
-正常生产时,至少每年对产品检验一次;正常生产时,如原料、配方或工艺有较大改变,可能影响产品质量时;更换设备,或产品长期停产又恢复生产时;出厂检验结果与平常记录有较大差别时;国家质量监督部门提出要求时。7.5判定规则
出厂检验和(或)型式检验合格时,由质量检验部门出具产品合格证。出厂检验和(或)型式检验不合格时,在原批次基础上加倍取样分析。如仍不合格,判定该产品为不合格品,不得出厂。
8标志、包装、运输及贮存
8.1标志
产品的外包装宜使用符合GB/T191要求的标志。产品的包装上应贴有牢固的标签。标识内容应包括品名、产地、厂名、卫生许可证号、规格、生产日期、批号或代号、保质期等。A类产品的标签的内容应符合相关规定。8.2包装
产品的内包装和(或)包装容器的内涂料应采用国家批准的材料,A类产品应符合相应的食品包装用或食品容器卫生标准的材料。8.3运输
产品在运输过程中应轻拿轻放,严防雨淋和曝晒。运输工具应清洁、无毒、无污染。严禁与有毒、有害、有腐蚀性的物质混装混运。8.4贮存
产品应贮存在阴凉干燥的环境下。严禁与有毒、有害、有腐蚀性的物质同存。8.5保质期
8.5.1在25℃以下,液体酶制剂保质期不少于90d;固体酶制剂保质期不少于180d,企业应按上述要求具体标示。
8.5.2在保质期内,实测酶活力不应低于标示酶活力。5
GB/T24401—2009
吸光度(A)
附录A
(规范性附录)
吸光度与测试α-淀粉酶酶浓度对照表表A.1
酶浓度(c)/(u/mL)
吸光度与测试α-淀粉酶酶浓度对照表吸光度(A)
酶浓度(c)/(u/mL)
吸光度(A)
酶浓度(c)/(u/mL)
吸光度(A)
酶浓度(c)/(u/mL)
表A.1(续)
吸光度(A)
酶浓度(c)/(u/mL)
吸光度(A)
GB/T24401—2009
酶浓度(c)/(u/mL)
GB/T24401—2009
吸光度(A)
酶浓度(c)/(u/mL)
表A.1(续)
吸光度(A)
酶浓度(c)/(u/mL)
吸光度(A)
酶浓度(c)/(u/mL)
吸光度(A)
酶浓度(c)/(u/mL)
表A.1(续)
吸光度(A)
酶浓度(c)/(u/mL)
吸光度(A)
GB/T24401—2009
酶浓度(c)/(u/mL)
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。