GB 1886.257-2016
基本信息
标准号: GB 1886.257-2016
中文名称:食品安全国家标准 食品添加剂 溶菌酶
标准类别:国家标准(GB)
标准状态:现行
出版语种:简体中文
下载格式:.rar .pdf
下载大小:214KB

标准分类号
关联标准
出版信息
相关单位信息
标准简介
GB 1886.257-2016 食品安全国家标准 食品添加剂 溶菌酶
GB1886.257-2016
标准压缩包解压密码:www.bzxz.net
标准图片预览




标准内容
中华人民共和国国家标准
GB1886.257—2016
食品安全国家标准
食品添加剂
2016-08-31发布
溶菌酶
2017-01-01实施
人民共和国
国家卫生和计划生育委员会
1范围
食品安全国家标准
食品添加剂
溶菌酶
本标准适用于以鸡蛋清为原料,经提取、精制等工艺制得的食品添加剂溶菌酶。2
技术要求
感官要求
感官要求应符合表1的规定。
理化指标
白色至淡黄色
理化指标应符合表2的规定。
酶活力/[U/mg(mL)
水分,/%
灰分,w/%
铅(Pb)/(mg/kg)
总碑(以As计)/(mg/kg)
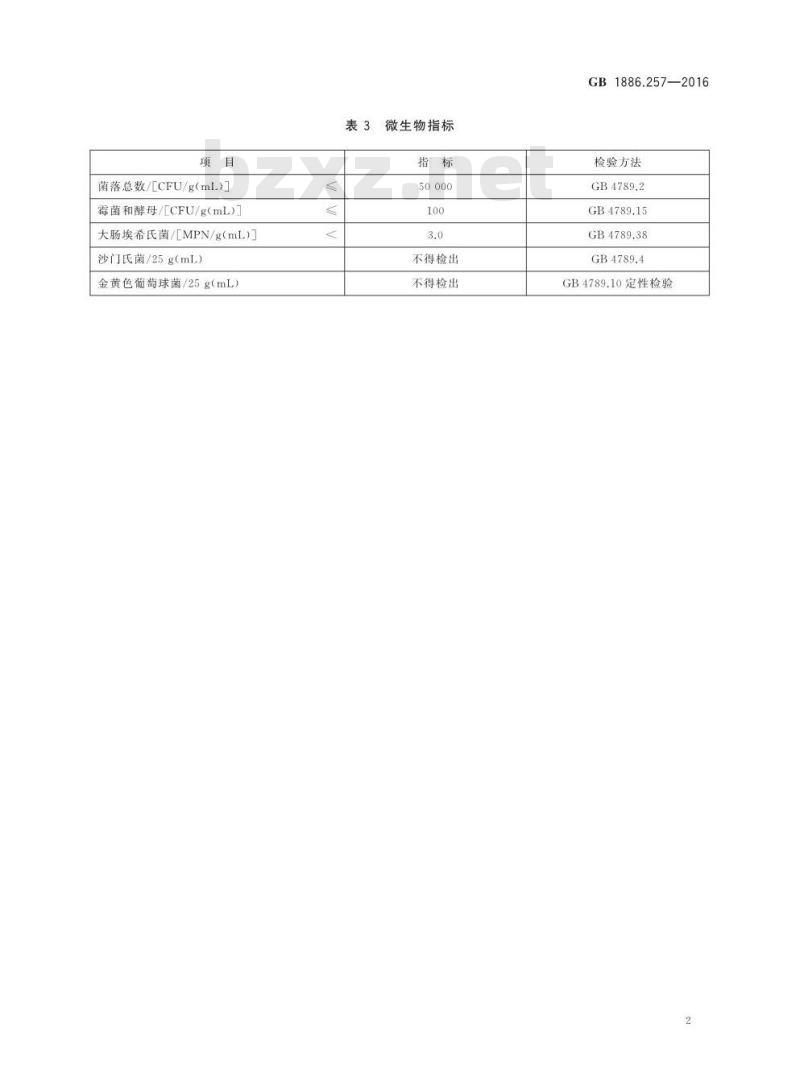
微生物指标
微生物指标应符合表3的规定。
感官要求
GB1886.257—2016
检验方法
浅黄色至深褐色
表2理化指标
将适量试样均匀置于烧杯或白瓷盘内,于自然光线下观察其色泽和状态
符合标示值
检验方法
附录A中A.2
附录A中A.3
GB5009.12
GB5009.11
菌落总数/[CFU/g(mL)]
霉菌和酵母/[CFU/g(mL)]
大肠埃希氏菌/[MPN/g(mL)
沙门氏菌/25g(mL)
金黄色葡萄球菌/25g(mL)
微生物指标
不得检出
不得检出
GB1886.257—2016
检验方法
GB4789.15
GB4789.38
GB4789.10定性检验
A.1一般规定
附录A
检验方法
GB1886.257—2016
本标准除另有规定外,所用试剂的纯度应在分析纯以上,所用标准滴定溶液、杂质测定用标准溶液制剂及制品,应按GB/T601.GB/T602、GB/T603的规定制备,实验用水应符合GB/T6682中三级水的规定。试验中所用溶液在未注明用何种溶剂配制时,均指水溶液A.2酶活力的测定
方法原理
溶菌酶可水解细菌的细胞壁,造成藤黄微球菌的溶解而引起溶液吸光度值的降低。二个溶菌酶活力单位定义为25℃,pH6.2条件下,使用藤黄微球菌悬浊液在450nm处每分钟引起吸光度变化为0.001所需溶菌酶的量。A.2.2
试剂和材料
A.2.2.1藤黄微球菌:ATCC4698或CICC10680。A.2.2.20.1mol/L磷酸盐缓冲液:pH6.2。称取11.70g磷酸二氢钠(NaH,PO,·2H,O)、7.86g磷酸氢二钠(NazHPO412H2O)及0.372g乙二胺四乙酸二钠(EDTA-2Na)于无菌水中并稀释定容至1000mL。调整缓冲溶液pH至6.2±0.1。
注:用小份缓冲溶液检查pH,以避免缓冲溶液被污染。如果需要,通过加人更多的磷酸二氢钠溶液或磷酸氢二钠溶液调整pH。
A.2.2.3溶菌酶标准品:蛋清溶菌酶A.2.2.4底物溶液:用磷酸盐缓冲液制备50mL藤黄微球菌悬浊液。使用前,底物于37℃培养30min。该底物溶液室温下可稳定2h。以磷酸盐缓冲液调分光光度计零点,然后测定底物溶液的吸光度,450nm下读数应为0.70±0.1。
仪器和设备
分光光度计:精度土0.001。
A.2.3.2pH计。
注:所用的器血应保持无菌,保证工作环境的清洁。A.2.4
分析步骤
试样溶液的制备
准确称取100mg土0.1mg试样,置于50mL容量瓶中用约25mL磷酸盐缓冲液搅拌溶解并稀释定容,充分混匀。再转移3mL上述试样制备溶液至100mL容量瓶中,用磷酸盐缓冲液搅拌溶解并稀释定容。
A.2.4.2标准溶液的制备
GB1886.257—2016
精确称取50mg蛋清溶菌酶标准品于50mL容量瓶中,用约25mL磷酸盐缓冲液搅拌溶解并稀释定容,充分混勾(如果需要,冷冻该溶液以备后续测定)。转移3mL上述标准制备溶液至100mL容量瓶中,用磷酸盐缓冲液搅拌溶解并稀释定容。A.2.4.3测定
取3份标准溶液和3份试样溶液进行测定25℃室温下,将1cm比色皿放入分光光度计,用磷酸盐缓冲液调整吸光度零点。吸2.9mL底物溶液于比色,最初450nm处吸光度应为0.70土0.10,3min之内初始吸光度值变化应小于或等于0.003时,方可开始测定。吸取0.1mL标准溶液加人底物溶液,充分混合。记录3min吸光度值的变化,每15s记录一次吸光度值。每分钟吸光度值变化应在0.03~0.08,若不在要求范围需调整试样溶液的浓度。重复操作测定试样溶液反应1min后稳定,计算时忽略最初1min的读数。A.2.4.4结果计算Www.bzxZ.net
酶活力X,按式(A.1)计算:
(A1—A2)
2×m×0.001
式中:
A——试样在450nm处反应1min时的吸光度;A2
试样在450nm处反应3min时的吸光度;用于分析的试样制备溶液中的溶菌酶质量,单位为毫克(mg);获得1min和3min吸光度读数所用的时间,单位为分钟(min);0.001一一由单位溶菌酶每分钟引起的吸光度降低的值。...(A.1)
试验结果以平行测定结果的算术平均值为准。在重复性条件下获得的两次独立测定结果的绝对差值不大于算术平均值的10%。
A.3pH的测定
A.3.1仪器
酸度计:精度0.01pH,备有玻璃电极和甘汞电极(或复合电极)。A.3.1.1
分析步骤
按仪器使用说明书调试和校正酸度计。用无菌水配制15g/L的溶菌酶待测液(液体产品直接测定)。用水冲洗电极探头,用滤纸轻轻吸于,将电极插人待测液中,调节温度调节器,使仪器指示温度与待测液温度相同,稳定后读数所得结果表示至一位小数。
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
GB1886.257—2016
食品安全国家标准
食品添加剂
2016-08-31发布
溶菌酶
2017-01-01实施
人民共和国
国家卫生和计划生育委员会
1范围
食品安全国家标准
食品添加剂
溶菌酶
本标准适用于以鸡蛋清为原料,经提取、精制等工艺制得的食品添加剂溶菌酶。2
技术要求
感官要求
感官要求应符合表1的规定。
理化指标
白色至淡黄色
理化指标应符合表2的规定。
酶活力/[U/mg(mL)
水分,/%
灰分,w/%
铅(Pb)/(mg/kg)
总碑(以As计)/(mg/kg)
微生物指标
微生物指标应符合表3的规定。
感官要求
GB1886.257—2016
检验方法
浅黄色至深褐色
表2理化指标
将适量试样均匀置于烧杯或白瓷盘内,于自然光线下观察其色泽和状态
符合标示值
检验方法
附录A中A.2
附录A中A.3
GB5009.12
GB5009.11
菌落总数/[CFU/g(mL)]
霉菌和酵母/[CFU/g(mL)]
大肠埃希氏菌/[MPN/g(mL)
沙门氏菌/25g(mL)
金黄色葡萄球菌/25g(mL)
微生物指标
不得检出
不得检出
GB1886.257—2016
检验方法
GB4789.15
GB4789.38
GB4789.10定性检验
A.1一般规定
附录A
检验方法
GB1886.257—2016
本标准除另有规定外,所用试剂的纯度应在分析纯以上,所用标准滴定溶液、杂质测定用标准溶液制剂及制品,应按GB/T601.GB/T602、GB/T603的规定制备,实验用水应符合GB/T6682中三级水的规定。试验中所用溶液在未注明用何种溶剂配制时,均指水溶液A.2酶活力的测定
方法原理
溶菌酶可水解细菌的细胞壁,造成藤黄微球菌的溶解而引起溶液吸光度值的降低。二个溶菌酶活力单位定义为25℃,pH6.2条件下,使用藤黄微球菌悬浊液在450nm处每分钟引起吸光度变化为0.001所需溶菌酶的量。A.2.2
试剂和材料
A.2.2.1藤黄微球菌:ATCC4698或CICC10680。A.2.2.20.1mol/L磷酸盐缓冲液:pH6.2。称取11.70g磷酸二氢钠(NaH,PO,·2H,O)、7.86g磷酸氢二钠(NazHPO412H2O)及0.372g乙二胺四乙酸二钠(EDTA-2Na)于无菌水中并稀释定容至1000mL。调整缓冲溶液pH至6.2±0.1。
注:用小份缓冲溶液检查pH,以避免缓冲溶液被污染。如果需要,通过加人更多的磷酸二氢钠溶液或磷酸氢二钠溶液调整pH。
A.2.2.3溶菌酶标准品:蛋清溶菌酶A.2.2.4底物溶液:用磷酸盐缓冲液制备50mL藤黄微球菌悬浊液。使用前,底物于37℃培养30min。该底物溶液室温下可稳定2h。以磷酸盐缓冲液调分光光度计零点,然后测定底物溶液的吸光度,450nm下读数应为0.70±0.1。
仪器和设备
分光光度计:精度土0.001。
A.2.3.2pH计。
注:所用的器血应保持无菌,保证工作环境的清洁。A.2.4
分析步骤
试样溶液的制备
准确称取100mg土0.1mg试样,置于50mL容量瓶中用约25mL磷酸盐缓冲液搅拌溶解并稀释定容,充分混匀。再转移3mL上述试样制备溶液至100mL容量瓶中,用磷酸盐缓冲液搅拌溶解并稀释定容。
A.2.4.2标准溶液的制备
GB1886.257—2016
精确称取50mg蛋清溶菌酶标准品于50mL容量瓶中,用约25mL磷酸盐缓冲液搅拌溶解并稀释定容,充分混勾(如果需要,冷冻该溶液以备后续测定)。转移3mL上述标准制备溶液至100mL容量瓶中,用磷酸盐缓冲液搅拌溶解并稀释定容。A.2.4.3测定
取3份标准溶液和3份试样溶液进行测定25℃室温下,将1cm比色皿放入分光光度计,用磷酸盐缓冲液调整吸光度零点。吸2.9mL底物溶液于比色,最初450nm处吸光度应为0.70土0.10,3min之内初始吸光度值变化应小于或等于0.003时,方可开始测定。吸取0.1mL标准溶液加人底物溶液,充分混合。记录3min吸光度值的变化,每15s记录一次吸光度值。每分钟吸光度值变化应在0.03~0.08,若不在要求范围需调整试样溶液的浓度。重复操作测定试样溶液反应1min后稳定,计算时忽略最初1min的读数。A.2.4.4结果计算Www.bzxZ.net
酶活力X,按式(A.1)计算:
(A1—A2)
2×m×0.001
式中:
A——试样在450nm处反应1min时的吸光度;A2
试样在450nm处反应3min时的吸光度;用于分析的试样制备溶液中的溶菌酶质量,单位为毫克(mg);获得1min和3min吸光度读数所用的时间,单位为分钟(min);0.001一一由单位溶菌酶每分钟引起的吸光度降低的值。...(A.1)
试验结果以平行测定结果的算术平均值为准。在重复性条件下获得的两次独立测定结果的绝对差值不大于算术平均值的10%。
A.3pH的测定
A.3.1仪器
酸度计:精度0.01pH,备有玻璃电极和甘汞电极(或复合电极)。A.3.1.1
分析步骤
按仪器使用说明书调试和校正酸度计。用无菌水配制15g/L的溶菌酶待测液(液体产品直接测定)。用水冲洗电极探头,用滤纸轻轻吸于,将电极插人待测液中,调节温度调节器,使仪器指示温度与待测液温度相同,稳定后读数所得结果表示至一位小数。
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。