GB 1886.361-2022
基本信息
标准号: GB 1886.361-2022
中文名称:食品安全国家标准 食品添加剂 叶绿素铜
标准类别:国家标准(GB)
标准状态:现行
发布日期:2022-06-30
实施日期:2022-12-30
出版语种:简体中文
下载格式:.pdf .zip
下载大小:1437769

标准分类号
中标分类号:食品>>食品综合>>X09卫生、安全、劳动保护
关联标准
出版信息
出版社:中国标准出版社
页数:12页
标准价格:29.0
相关单位信息
发布部门:国家卫生健康委员会 国家市场监督管理总局
标准简介
本标准适用于以蚕沙或草类(如高羊茅、紫花苜蓿.荨麻等)、螺旋藻等植物为原料提取叶绿素,或者直接以叶绿素为原料,再经铜代反应制得的食品添加剂叶绿素铜。使用溶剂为丙酮、二氯甲烷、甲醇、乙醇、异丙醇、正已烷和(或)石油醚(沸程为90 °C~120°C。
标准图片预览




标准内容
中华人民共和国国家标准
GB1886.361—2022
食品安全国家标准
食品添加剂
2022-06-30发布
叶绿素铜
2022-12-30实施
中华人民共和国国家卫生健康委员会国家市场监督管理总局
1范围
食品安全国家标准
食品添加剂
叶绿素铜
GB1886.361—2022
本标准适用于以蚕沙或草类(如高羊茅、紫花首猎、荨麻等)、螺旋藻等植物为原料提取叶绿素,或者直接以叶绿素为原料,再经铜代反应制得的食品添加剂叶绿素铜。使用溶剂为丙酮、二氯甲烷、甲醇、乙醇、异丙醇、正已烷和(或)石油醚(沸程为90℃~120℃)。2
分子式和相对分子质量
分子式
叶绿酸铜a(C55Hz2CuN4Os)
叶绿酸铜b(CssHzCuN4O)
2相对分子质量
叶绿酸铜a:932.75(按2018年国际相对原子质量)叶绿酸铜b:946.73(按2018年国际相对原子质量)3
技术要求
感官要求
感官要求应符合表1的规定
感官要求
理化指标
青绿色至深绿色
蜡状或胶状固体
理化指标应符合表2的规定
叶绿素含量,w/%
总铜(Cu),w/%
表2理化指标
检验方法
取适量试样置于清洁、干燥的白瓷盘中,在自然光线下观察其色泽和状态
检验方法
附录A中A.3
附录A中A.4
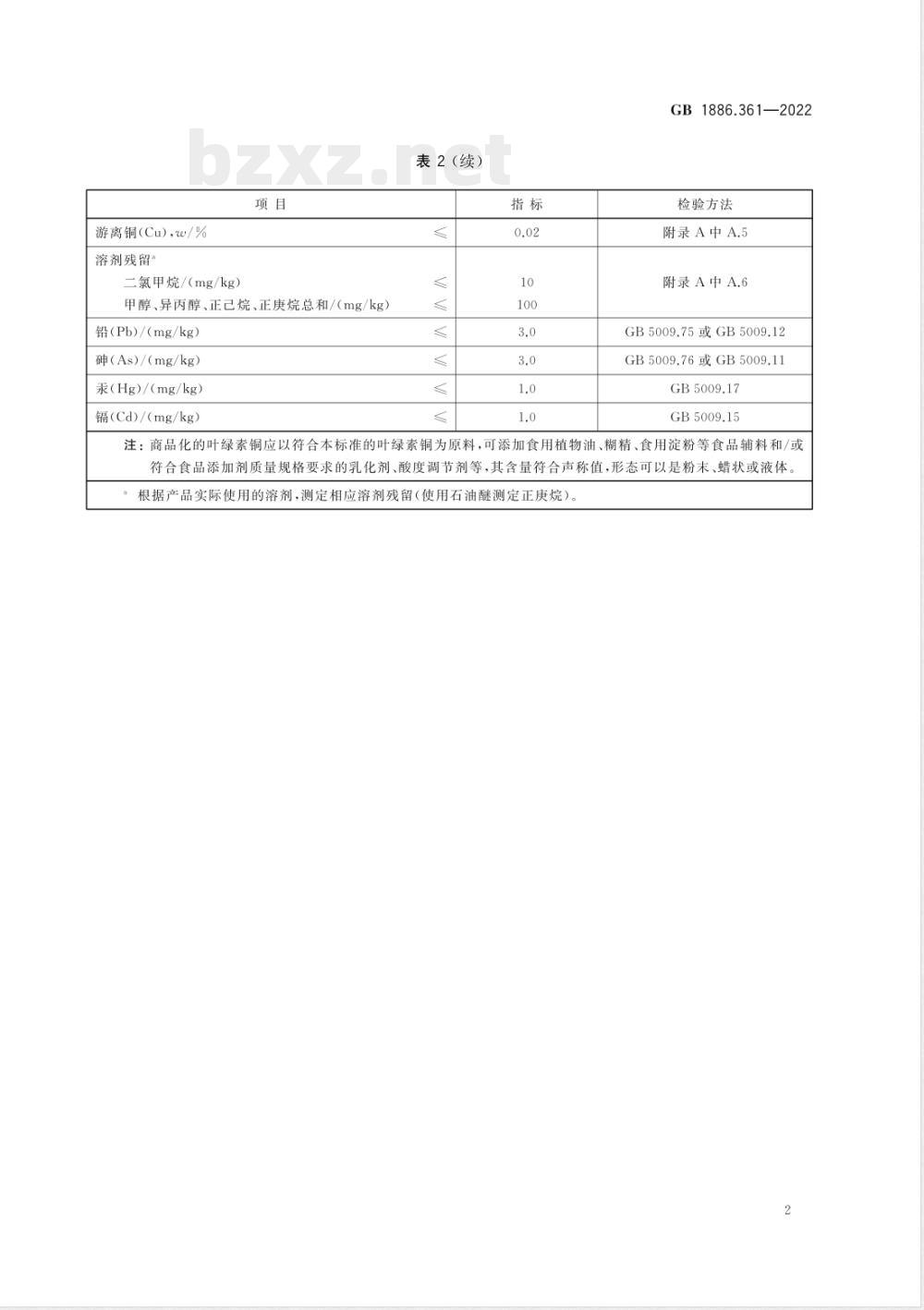
游离铜(Cu),w/%
溶剂残留”
二氯甲烷/(mg/kg)
甲醇、异丙醇、正己烷、正庚烷总和/(mg/kg)铅(Pb)/(mg/kg)
砷(As)/(mg/kg)
汞(Hg)/(mg/kg)
镉(Cd)/(mg/kg)
表2(续)
GB1886.361—2022
检验方法
附录A中A.5
附录A中A.6
GB5009.75或GB5009.12
GB5009.76或GB5009.11
GB5009.17
GB5009.15
注:商品化的叶绿素铜应以符合本标准的叶绿素铜为原料,可添加食用植物油、糊精、食用淀粉等食品辅料和/或符合食品添加剂质量规格要求的乳化剂、酸度调节剂等,其含量符合声称值,形态可以是粉末、蜡状或液体,根据产品实际使用的溶剂,测定相应溶剂残留(使用石油醚测定正庚烷)。2
A.1一般规定
附录A
检验方法
GB1886.361—2022
本标准所用试剂和水在未注明其他要求时,均指分析纯试剂和GB/T6682规定的三级水。试验中所用标准溶液、杂质测定用标准溶液、制剂和制品在未注明其他要求时,均按GB/T601、GB/T602、GB/T603的规定制备。试验中所用溶液在未注明用何种溶剂配制时,均指水溶液。A.2鉴别试验
最大吸收峰及吸光度比值范围
取A.3.3.1叶绿素含量测定中的试样溶液,在405nm士3nm和635nm士5nm的两个波长范围内均有最大吸收峰,且两处测得的吸光度比值在3.2~4.0之间。A.2.2
铜离子试验
试剂和材料
A.2.2.1.1硫酸。
A.2.2.1.2盐酸溶液:1+3。
二乙基二硫代氨基甲酸钠溶液:1g/L。A.2.2.1.3
A.2.2.2分析步骤
取1g试样,置于已在800℃土25℃下灼烧至恒重的埚中,缓缓加热直至试样完全炭化。将炭化的试样冷却,用0.5mL~1mL硫酸润湿残渣,继续加热至硫酸蒸汽逸尽,并在800℃土25℃的高温炉中灼烧残渣至恒重。在残渣中加入10mL盐酸溶液,在水浴上加热溶解,过滤后补充水至10mL。取5mL上述溶液,加人0.5mL二乙基二硫代氨基甲酸钠溶液,产生红褐色沉淀。A.3叶绿素含量的测定
A.3.1试剂和材料
A.3.1.1无水乙醚。
A.3.1.2磷酸氢二钠溶液(0.15mol/L):称取53.7g磷酸氢二钠(Na2HPO4·12H2O),加水溶解,稀释定容至1000mL。
A.3.1.3磷酸二氢钾溶液(0.15mol/L):称取20.4g磷酸二氢钾(KHzPO4),加水溶解,稀释定容至1000mL。
A.3.1.4磷酸盐缓冲液(pH7.5):分别量取磷酸氢二钠溶液(0.15mol/L)与磷酸二氢钾溶液(0.15mol/L)按体积比21:4混合。A.3.1.5A液:氯化铜-甲醇溶液(5%)。A.3.1.6B液:氢氧化钠-甲醇溶液(10%)。3
仪器和设备
分光光度计。
A.3.2.2恒温水浴。
A.3.2.3分液漏斗(250mL)。
分析步骤
试样溶液的制备
GB 1886.361—2022
称取1g试样,精确至0.0002g,置于锥形瓶中,加50mL~60mL无水乙醚溶解。加入A液1mL,在50℃士2℃恒温水浴中加热回流15min,取下再加人B液2mL,摇匀,继续在50℃士2℃恒温水浴中加热回流20min,整个过程间断振摇,保证反应完全。反应后取下锥形瓶后冷却,加入少量水,摇勾,移人分液漏斗中,再用适量水分次洗涤锥形瓶,洗液一并移入分液漏斗中,充分振摇后至少静置1h。
分液漏斗中的液体分层后,将下层液体过滤,注意界面层留在分液漏斗中,不要过滤下来,以免堵塞滤纸。过滤完毕,用水冲洗上层乙醚层和界面,直至洗出的水层无色,洗液并人下层滤液,弃掉上层乙醚层和界面。滤纸用水洗涤数次至近乎无色,洗液并人下层滤液。全部滤液保留。将滤液移入另一分液漏斗中,用40mL无水乙醚振摇洗涤后,静置15min,将下层液体移人250mL容量瓶中用水稀释定容,弃掉上层乙醚层。取1mL上述溶液,用磷酸盐缓冲液(pH7.5)稀释定容至50mL,摇匀。
A.3.3.2测定
取试样溶液置于1cm比色皿中,以磷酸盐缓冲液(pH7.5)做空白对照,用分光光度计在405nm土3nm波长范围内的最大吸收波长处测定吸光度。A.3.4结果计算
叶绿素含量的质量分数w1按式(A.1)计算。A×12500
Wi=565×100×m
式中:
试样溶液的吸光度值;
——试样的质量,单位为克(g);)—体积换算系数;
—一1cm比色皿中浓度为1%(100mL溶剂含1g叶绿素)的溶液消光值;浓度换算系数。
...(A.1)
试验结果以平行测定结果的算术平均值为准。在重复性条件下获得的两次独立测定结果的绝对差值不大于算术平均值的5.0%。
A.4总铜(Cu)的测定
A.4.1试剂和材料
同GB5009.13。
2仪器和设备
同GB5009.13。
3试样处理
微波消解
GB1886.361—2022
称取0.2g~0.5g,精确至0.0002g,置于微波消解罐中,加人5mL硝酸,按照微波消解的操作步骤消解试样,消解条件参考B.1。冷却后取出消解罐,于120℃~140℃赶酸至1mL左右。消解罐放冷后,将消化液转移至25mL容量瓶中,用少量二级水洗涤消解罐2次~3次,合并洗涤液于容量瓶中,用二级水定容至刻度,混匀备用。同时做试剂空白试验。A.4.3.2干法灰化
称取0.1g试样,精确至0.0002g,于埚中小火加热,炭化至无烟,转移至550℃马弗炉中,灰化3h~4h,冷却后取出。对于灰化不彻底的试样,加数滴硝酸,小火加热,小心蒸干,再转入550℃马弗炉中,继续灰化1h~2h,至试样呈白灰状,冷却后取出。用适量硝酸溶液(1十1)溶解并用水定容至10mL,混匀备用。同时做空白试验。A.4.4分析步骤
除试样处理外,其余步骤按GB5009.13规定的方法测定A.5游离铜(Cu)的测定
试剂和材料
同GB5009.13。
仪器和设备
同GB5009.13。
3试样处理
称取0.1g试样,精确至0.0002g,置于锥形瓶中,加20mL无水乙醚溶解,再加人100mL水,盖塞,振摇1min,移入125mL分液漏斗中,静置30min。将分液漏斗中的下层液体用双层滤纸过滤,如滤液有颜色,再次用双层滤纸过滤,直至滤液无色,滤液即为试样液。A.5.4分析步骤
除试样处理外,其余步骤按GB5009.13规定的方法测定A.6溶剂残留(二氯甲烷、甲醇、异丙醇、正已烷、正庚烷)的测定A.6.1试剂和材料
A.6.1.1水:GB/T6682规定的一级水。A.6.1.2待测组分标准品:二氯甲烷、甲醇、异丙醇、正已烷、正庚烷,色谱纯。A.6.1.3内标物:3-甲基-2-戊酮,色谱纯。5
A.6.1.4N-甲基吡咯烷酮。
A.6.2仪器和设备
气相色谱仪:配备氢火焰离子化检测器(FID)和顶空进样器。A.6.3参考色谱条件
GB1886.361—2022
色谱柱:石英毛细管柱(s0.53mm×30m),涂层为二甲基聚硅氧烷,厚度为5μm,或同等性A.6.3.1
能的色谱柱。
A.6.3.2载气:氮气。
A.6.3.3载气流速:5mL/min。
A.6.3.4柱温:35℃保持5min,以5℃/min升温至90℃,保持6min。A.6.3.5
进样口温度:140℃。
检测器温度:300℃。
进样量:1.0mL。
参考顶空进样条件
试样加热温度:60℃。
试样加热时间:10min。
注射器温度:90℃。
传质温度:100℃。
5分析步骤
A.6.5.1内标溶液的制备
移取50.0mL水至一个50mL进样瓶中,称重进样瓶,精确至0.0001g。移取15μL3-甲基-2-戊酮,将其注人进样瓶,混匀,再称重进样瓶,精确至0.01g。A.6.5.2空白溶液的制备
分别量取5.0mL水和1.0mL内标溶液,移人顶空瓶中,移取20μLN-甲基吡咯烷酮,将其注人顶空瓶,封盖,60℃加热10min并剧烈振摇,混匀。A.6.5.3标准溶液的制备
分别量取5.0mL水和1.0mL内标溶液,移入顶空瓶中,称取10mg待测组分标准品(对每个溶剂分别分析),用N-甲基吡咯烷酮溶解稀释定容至100mL,移取20μL注人顶空瓶,封盖,60℃加热10min并剧烈振摇,混匀。
A.6.5.4试样溶液的制备
称取0.2g试样,精确至0.0001g,置于顶空瓶中,加人5.0mL水和1.0mL内标溶液,移取20μLN-甲基吡咯烷酮,将其注入顶空瓶,封盖,60℃加热10min并剧烈振摇,混匀。A.6.5.5测定免费标准bzxz.net
在A.6.3和A.6.4参考操作条件下,分别对空白溶液、标准溶液和试样溶液顶空处理后进行色谱分析。试样溶液中溶剂残留的参考气相色谱图见图C.1。6
5结果计算
校准因子f:
校准因子f按式(A.2)计算。
式中:
mXAf-A)
标准溶液中待测组分的质量,单位为毫克(mg);质量换算系数;
标准溶液中内标物的质量,单位为毫克(mg);标准溶液色谱图中待测组分峰面积与内标物峰面积的比值;空白溶液色谱图中待测组分峰面积与内标物峰面积的比值。待测组分含量
GB1886.361—2022
试样中待测组分(二氯甲烷、甲醇、异丙醇、正已烷、正庚烷)的含量W;,单位为毫克每千克(mg/kg),按式(A.3)计算。A.Xm。×f:×1000
式中:
试样溶液色谱图中待测组分峰面积与内标物峰面积的比值;内标溶液中内标物的质量,单位为毫克(mg);校准因子;
质量换算系数;
试样的质量,单位为克(g);
体积换算系数。
*.(A.3)
由式(A.3)计算得到二氯甲烷的含量为W2,甲醇、异丙醇、正已烷、正庚烷的含量分别为wW3、W4、w5、W6,四者之和即为试样中甲醇、异丙醇、正已烷、正庚烷总和。试验结果以平行测定结果的算术平均值为准。在重复性条件下获得的两次独立测定结果的绝对差值不大于算术平均值的10.0%。
微波消解升温程序见表B.1。
设定温度/℃
微波消解升温程序
微波消解升温程序
升温时间/min
GB1886.361—2022
恒温时间/min
附录C
试样溶液中溶剂残留的参考气相色谱图试样溶液中溶剂残留的参考气相色谱图见图C.1。800
说明:
1—-甲醇;
异丙醇;
二氯甲烷;
4——正己烷;
正庚烷;
内标物(3-甲基-2-戊酮)。
试样溶液中溶剂残留的参考气相色谱图GB1886.361—2022
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
GB1886.361—2022
食品安全国家标准
食品添加剂
2022-06-30发布
叶绿素铜
2022-12-30实施
中华人民共和国国家卫生健康委员会国家市场监督管理总局
1范围
食品安全国家标准
食品添加剂
叶绿素铜
GB1886.361—2022
本标准适用于以蚕沙或草类(如高羊茅、紫花首猎、荨麻等)、螺旋藻等植物为原料提取叶绿素,或者直接以叶绿素为原料,再经铜代反应制得的食品添加剂叶绿素铜。使用溶剂为丙酮、二氯甲烷、甲醇、乙醇、异丙醇、正已烷和(或)石油醚(沸程为90℃~120℃)。2
分子式和相对分子质量
分子式
叶绿酸铜a(C55Hz2CuN4Os)
叶绿酸铜b(CssHzCuN4O)
2相对分子质量
叶绿酸铜a:932.75(按2018年国际相对原子质量)叶绿酸铜b:946.73(按2018年国际相对原子质量)3
技术要求
感官要求
感官要求应符合表1的规定
感官要求
理化指标
青绿色至深绿色
蜡状或胶状固体
理化指标应符合表2的规定
叶绿素含量,w/%
总铜(Cu),w/%
表2理化指标
检验方法
取适量试样置于清洁、干燥的白瓷盘中,在自然光线下观察其色泽和状态
检验方法
附录A中A.3
附录A中A.4
游离铜(Cu),w/%
溶剂残留”
二氯甲烷/(mg/kg)
甲醇、异丙醇、正己烷、正庚烷总和/(mg/kg)铅(Pb)/(mg/kg)
砷(As)/(mg/kg)
汞(Hg)/(mg/kg)
镉(Cd)/(mg/kg)
表2(续)
GB1886.361—2022
检验方法
附录A中A.5
附录A中A.6
GB5009.75或GB5009.12
GB5009.76或GB5009.11
GB5009.17
GB5009.15
注:商品化的叶绿素铜应以符合本标准的叶绿素铜为原料,可添加食用植物油、糊精、食用淀粉等食品辅料和/或符合食品添加剂质量规格要求的乳化剂、酸度调节剂等,其含量符合声称值,形态可以是粉末、蜡状或液体,根据产品实际使用的溶剂,测定相应溶剂残留(使用石油醚测定正庚烷)。2
A.1一般规定
附录A
检验方法
GB1886.361—2022
本标准所用试剂和水在未注明其他要求时,均指分析纯试剂和GB/T6682规定的三级水。试验中所用标准溶液、杂质测定用标准溶液、制剂和制品在未注明其他要求时,均按GB/T601、GB/T602、GB/T603的规定制备。试验中所用溶液在未注明用何种溶剂配制时,均指水溶液。A.2鉴别试验
最大吸收峰及吸光度比值范围
取A.3.3.1叶绿素含量测定中的试样溶液,在405nm士3nm和635nm士5nm的两个波长范围内均有最大吸收峰,且两处测得的吸光度比值在3.2~4.0之间。A.2.2
铜离子试验
试剂和材料
A.2.2.1.1硫酸。
A.2.2.1.2盐酸溶液:1+3。
二乙基二硫代氨基甲酸钠溶液:1g/L。A.2.2.1.3
A.2.2.2分析步骤
取1g试样,置于已在800℃土25℃下灼烧至恒重的埚中,缓缓加热直至试样完全炭化。将炭化的试样冷却,用0.5mL~1mL硫酸润湿残渣,继续加热至硫酸蒸汽逸尽,并在800℃土25℃的高温炉中灼烧残渣至恒重。在残渣中加入10mL盐酸溶液,在水浴上加热溶解,过滤后补充水至10mL。取5mL上述溶液,加人0.5mL二乙基二硫代氨基甲酸钠溶液,产生红褐色沉淀。A.3叶绿素含量的测定
A.3.1试剂和材料
A.3.1.1无水乙醚。
A.3.1.2磷酸氢二钠溶液(0.15mol/L):称取53.7g磷酸氢二钠(Na2HPO4·12H2O),加水溶解,稀释定容至1000mL。
A.3.1.3磷酸二氢钾溶液(0.15mol/L):称取20.4g磷酸二氢钾(KHzPO4),加水溶解,稀释定容至1000mL。
A.3.1.4磷酸盐缓冲液(pH7.5):分别量取磷酸氢二钠溶液(0.15mol/L)与磷酸二氢钾溶液(0.15mol/L)按体积比21:4混合。A.3.1.5A液:氯化铜-甲醇溶液(5%)。A.3.1.6B液:氢氧化钠-甲醇溶液(10%)。3
仪器和设备
分光光度计。
A.3.2.2恒温水浴。
A.3.2.3分液漏斗(250mL)。
分析步骤
试样溶液的制备
GB 1886.361—2022
称取1g试样,精确至0.0002g,置于锥形瓶中,加50mL~60mL无水乙醚溶解。加入A液1mL,在50℃士2℃恒温水浴中加热回流15min,取下再加人B液2mL,摇匀,继续在50℃士2℃恒温水浴中加热回流20min,整个过程间断振摇,保证反应完全。反应后取下锥形瓶后冷却,加入少量水,摇勾,移人分液漏斗中,再用适量水分次洗涤锥形瓶,洗液一并移入分液漏斗中,充分振摇后至少静置1h。
分液漏斗中的液体分层后,将下层液体过滤,注意界面层留在分液漏斗中,不要过滤下来,以免堵塞滤纸。过滤完毕,用水冲洗上层乙醚层和界面,直至洗出的水层无色,洗液并人下层滤液,弃掉上层乙醚层和界面。滤纸用水洗涤数次至近乎无色,洗液并人下层滤液。全部滤液保留。将滤液移入另一分液漏斗中,用40mL无水乙醚振摇洗涤后,静置15min,将下层液体移人250mL容量瓶中用水稀释定容,弃掉上层乙醚层。取1mL上述溶液,用磷酸盐缓冲液(pH7.5)稀释定容至50mL,摇匀。
A.3.3.2测定
取试样溶液置于1cm比色皿中,以磷酸盐缓冲液(pH7.5)做空白对照,用分光光度计在405nm土3nm波长范围内的最大吸收波长处测定吸光度。A.3.4结果计算
叶绿素含量的质量分数w1按式(A.1)计算。A×12500
Wi=565×100×m
式中:
试样溶液的吸光度值;
——试样的质量,单位为克(g);)—体积换算系数;
—一1cm比色皿中浓度为1%(100mL溶剂含1g叶绿素)的溶液消光值;浓度换算系数。
...(A.1)
试验结果以平行测定结果的算术平均值为准。在重复性条件下获得的两次独立测定结果的绝对差值不大于算术平均值的5.0%。
A.4总铜(Cu)的测定
A.4.1试剂和材料
同GB5009.13。
2仪器和设备
同GB5009.13。
3试样处理
微波消解
GB1886.361—2022
称取0.2g~0.5g,精确至0.0002g,置于微波消解罐中,加人5mL硝酸,按照微波消解的操作步骤消解试样,消解条件参考B.1。冷却后取出消解罐,于120℃~140℃赶酸至1mL左右。消解罐放冷后,将消化液转移至25mL容量瓶中,用少量二级水洗涤消解罐2次~3次,合并洗涤液于容量瓶中,用二级水定容至刻度,混匀备用。同时做试剂空白试验。A.4.3.2干法灰化
称取0.1g试样,精确至0.0002g,于埚中小火加热,炭化至无烟,转移至550℃马弗炉中,灰化3h~4h,冷却后取出。对于灰化不彻底的试样,加数滴硝酸,小火加热,小心蒸干,再转入550℃马弗炉中,继续灰化1h~2h,至试样呈白灰状,冷却后取出。用适量硝酸溶液(1十1)溶解并用水定容至10mL,混匀备用。同时做空白试验。A.4.4分析步骤
除试样处理外,其余步骤按GB5009.13规定的方法测定A.5游离铜(Cu)的测定
试剂和材料
同GB5009.13。
仪器和设备
同GB5009.13。
3试样处理
称取0.1g试样,精确至0.0002g,置于锥形瓶中,加20mL无水乙醚溶解,再加人100mL水,盖塞,振摇1min,移入125mL分液漏斗中,静置30min。将分液漏斗中的下层液体用双层滤纸过滤,如滤液有颜色,再次用双层滤纸过滤,直至滤液无色,滤液即为试样液。A.5.4分析步骤
除试样处理外,其余步骤按GB5009.13规定的方法测定A.6溶剂残留(二氯甲烷、甲醇、异丙醇、正已烷、正庚烷)的测定A.6.1试剂和材料
A.6.1.1水:GB/T6682规定的一级水。A.6.1.2待测组分标准品:二氯甲烷、甲醇、异丙醇、正已烷、正庚烷,色谱纯。A.6.1.3内标物:3-甲基-2-戊酮,色谱纯。5
A.6.1.4N-甲基吡咯烷酮。
A.6.2仪器和设备
气相色谱仪:配备氢火焰离子化检测器(FID)和顶空进样器。A.6.3参考色谱条件
GB1886.361—2022
色谱柱:石英毛细管柱(s0.53mm×30m),涂层为二甲基聚硅氧烷,厚度为5μm,或同等性A.6.3.1
能的色谱柱。
A.6.3.2载气:氮气。
A.6.3.3载气流速:5mL/min。
A.6.3.4柱温:35℃保持5min,以5℃/min升温至90℃,保持6min。A.6.3.5
进样口温度:140℃。
检测器温度:300℃。
进样量:1.0mL。
参考顶空进样条件
试样加热温度:60℃。
试样加热时间:10min。
注射器温度:90℃。
传质温度:100℃。
5分析步骤
A.6.5.1内标溶液的制备
移取50.0mL水至一个50mL进样瓶中,称重进样瓶,精确至0.0001g。移取15μL3-甲基-2-戊酮,将其注人进样瓶,混匀,再称重进样瓶,精确至0.01g。A.6.5.2空白溶液的制备
分别量取5.0mL水和1.0mL内标溶液,移人顶空瓶中,移取20μLN-甲基吡咯烷酮,将其注人顶空瓶,封盖,60℃加热10min并剧烈振摇,混匀。A.6.5.3标准溶液的制备
分别量取5.0mL水和1.0mL内标溶液,移入顶空瓶中,称取10mg待测组分标准品(对每个溶剂分别分析),用N-甲基吡咯烷酮溶解稀释定容至100mL,移取20μL注人顶空瓶,封盖,60℃加热10min并剧烈振摇,混匀。
A.6.5.4试样溶液的制备
称取0.2g试样,精确至0.0001g,置于顶空瓶中,加人5.0mL水和1.0mL内标溶液,移取20μLN-甲基吡咯烷酮,将其注入顶空瓶,封盖,60℃加热10min并剧烈振摇,混匀。A.6.5.5测定免费标准bzxz.net
在A.6.3和A.6.4参考操作条件下,分别对空白溶液、标准溶液和试样溶液顶空处理后进行色谱分析。试样溶液中溶剂残留的参考气相色谱图见图C.1。6
5结果计算
校准因子f:
校准因子f按式(A.2)计算。
式中:
mXAf-A)
标准溶液中待测组分的质量,单位为毫克(mg);质量换算系数;
标准溶液中内标物的质量,单位为毫克(mg);标准溶液色谱图中待测组分峰面积与内标物峰面积的比值;空白溶液色谱图中待测组分峰面积与内标物峰面积的比值。待测组分含量
GB1886.361—2022
试样中待测组分(二氯甲烷、甲醇、异丙醇、正已烷、正庚烷)的含量W;,单位为毫克每千克(mg/kg),按式(A.3)计算。A.Xm。×f:×1000
式中:
试样溶液色谱图中待测组分峰面积与内标物峰面积的比值;内标溶液中内标物的质量,单位为毫克(mg);校准因子;
质量换算系数;
试样的质量,单位为克(g);
体积换算系数。
*.(A.3)
由式(A.3)计算得到二氯甲烷的含量为W2,甲醇、异丙醇、正已烷、正庚烷的含量分别为wW3、W4、w5、W6,四者之和即为试样中甲醇、异丙醇、正已烷、正庚烷总和。试验结果以平行测定结果的算术平均值为准。在重复性条件下获得的两次独立测定结果的绝对差值不大于算术平均值的10.0%。
微波消解升温程序见表B.1。
设定温度/℃
微波消解升温程序
微波消解升温程序
升温时间/min
GB1886.361—2022
恒温时间/min
附录C
试样溶液中溶剂残留的参考气相色谱图试样溶液中溶剂残留的参考气相色谱图见图C.1。800
说明:
1—-甲醇;
异丙醇;
二氯甲烷;
4——正己烷;
正庚烷;
内标物(3-甲基-2-戊酮)。
试样溶液中溶剂残留的参考气相色谱图GB1886.361—2022
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。