GB 17378.6-1998
基本信息
标准号: GB 17378.6-1998
中文名称:海洋监测规范 第6部分:生物体分析
标准类别:国家标准(GB)
英文名称:The specification for marine monitoringPart 6:Organisim analysis
标准状态:已作废
发布日期:1998-06-22
实施日期:1999-01-01
作废日期:2008-05-01
出版语种:简体中文
下载格式:.rar.pdf
下载大小:4912739

标准分类号
标准ICS号:数学、自然科学>>07.060地质学、气象学、水文学
中标分类号:综合>>基础学科>>A45海洋学
关联标准
替代情况:被GB 17378.6-2007代替
出版信息
出版社:中国标准出版社
页数:平装16开, 页数:74, 字数:143千字
标准价格:35.0 元
相关单位信息
首发日期:1998-06-22
复审日期:2004-10-14
起草单位:国家海洋局第三海洋研究所
发布部门:国家质量技术监督局
主管部门:国家海洋局
标准简介
本标准规定了海洋生物(贻贝、虾及鱼)中13项有害物质含量的测定方法,并对样品采集、运输、贮存、预处理和测定结果的计算等提出技术要求。本标准适用于大洋,近海和沿海水域的海洋生物污染调查与监测。 GB 17378.6-1998 海洋监测规范 第6部分:生物体分析 GB17378.6-1998 标准下载解压密码:www.bzxz.net
本标准规定了海洋生物(贻贝、虾及鱼)中13项有害物质含量的测定方法,并对样品采集、运输、贮存、预处理和测定结果的计算等提出技术要求。本标准适用于大洋,近海和沿海水域的海洋生物污染调查与监测。
本标准规定了海洋生物(贻贝、虾及鱼)中13项有害物质含量的测定方法,并对样品采集、运输、贮存、预处理和测定结果的计算等提出技术要求。本标准适用于大洋,近海和沿海水域的海洋生物污染调查与监测。
标准图片预览




标准内容
G 17378. 6—1998
本标准是海洋监测规范》的第6部分,是在HY003.6一91行业标准的基础上修订而戒的。本标规定了生物体分析的要求和分析方法。海洋胜测规范\包括下列部分:GB 17378.1 1998
第1部分;总则
海洋监测规范
GB 17378. 2—1998
GB 17378- 3—1998
GB 17378. 4—1998
GB 17378. 5-1998
GH 17378.6—1998
CB 17378. 71998
海洋监测规范
海洋监测规范
海洋监测规范
海洋监测规范
海洋监测规范
海洋壁測规范
本标准的谢录A是标准的附录。
本标准由国家海洋局提出。
第2部分:数处理与分析质盘控制第 3 部分;样品果集,吡存与运输第1部分:海水分析
第5部分:沉积物分析
第6部分生物体分析
第7部分:近海污染生态调查和生物监测本标推由国家游洋标唯计壁中心归口,本标摊由国家海洋厨第三海洋研究所负责起草。本标推主要起草人,许昆灿、张卷明、陈维岳、洪君超、陈邦龙。614
1范围
中华人民共和国国家标准
海洋监测规范
第6部分:生物体分析
The specificution for marine monituringPart 6:Organisim analysis
CB 17378. 6 1998
本标准规定了海洋生物(贮贝,虾及鱼)中13项有害物质含量的测定方法,并对样品采集、运输、存、预处理和测定结果的计算等提出技术要求。本标准适用于大洋,近游和沿海水域的海洋生物污染调查与监测,2引用标准
下列标准所包含的条文,通过在本标准中引用而构成为本标准的条文。本标准出版时,所示版本均为有效。所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。GB17378.2—1998海洋监测规范第2部分:数据处理与分析质量控制CB17378、4-1998海洋临测规范第4部分:海水分析GB17378.5—1998海洋监测规范第5部分:沉积物分析3定义
本标准采用下列楚义。
3.1蒸至近干evaporation to dryness将溶剂蒸发至小体积(0.2 mL~心.3mL),若有残渣时,残湾应湿润状。4—般规定
4.1样品的采集与制备
4.1.1采样对象
贻所、虾和鱼类。
4. 1.2试剂
4.1.2.1去离子水或等效蒸馏水,其痕量金属含量应低于分析方法的检出限。或用米受沾污的表层海水。
4.1.2.2合成洗漆剂。
4.1.3仪器和设备
塑料冷冻箱,配有。用于贻贝贮存和运输时,底部必须具有板,以免样品浸入求中;一冰箱
低温冰箱:
乙烯袋:
国家质量技术监督鼠1998-06-22批准1999-01 -01 实施
--塑料板和尺子;用下长度测量;塑料刀
GB 17378.61998
玻璃或陶瓷碟(供制备样品用);锻子:塑料制品或其他合适材料的制品1高密度聚乙烯袋和塑料容器:供速冻保存样品用,装样前,须用合成洗涤剂清洗,并用蒸馅水洗净:
高密度聚乙烯膜:供罩工作台用;小张案乙烯膜:供称重用,
.分析天平感量0.1mg;
塑料洗瓶;
刮刀:供来集贻贝用:
塑料桶:20~-50L;
大号金属力,无锈斑,供切取鱼组织用;勾浆器:不锈钢或其他适宜材料的制品;塑料刷:毛刷紧硬,用以去除贻贝外壳的附着物;称量瓶:50mL,
电热烘箱:
干燥箱:
一冷冻干燥设备。
4.1.4采样与运输
4. 1.4. 1 准备 1.作
用合成洗涤剂(4.1.2.2)清洗冷冻箱、高密度聚乙烯袋、塑料板及尺、大号金属刀、刮刀.再用溜水或表层海水(4.1.2.1)漂洗干净。4.1.4.2贴贝采集
用清洁刮刀从其附着物上采集始贝样。选取足够数量的完好贻贝存十冷冻箱中。若需长途运输(炎热天超过2h),应把贻贝伴品盛于塑料桶中,将现场采集的清洁海水淋酒在贻贝.E,样品保持润湿状但不能没人水中。若样品处理须在采样24h后进行,可将贻具样存于高密度塑料袋中,历出袋内空气,将袋口打结或热封,将此和样品标签··起放入聚乙烯袋中并封口,存于低温冰箱中。4.1.4.3虾与中小型鱼样采集
按一定要求选取足够数微的完好的生物样,放入干净的聚乙烯袋中,要防止刺破袋子。挤山袋内空气,将袋!打纬或热封,将此和样品标签一起故人另一聚乙烯發中,并封口,低温冷藏。只有在贮存期不太长时(热天不超过48h),方可便用冰箱或冷冻箱存放样品。4.1.4.4大型鱼样采集
测量并记下鱼样的叉长,体再和性别。用清道的金展刀切下至少1006肌肉组续厚度至少5cm,以便在样品处理(4.1.5.5>时.切除沾污或内脏部分,存\清洁的聚乙烯袋中,挤出空气并封口,将此袋与样品标签一起放入另一案乙烯袋中,封口,于低温冰箱中贮存。若保存时间不太长(热天不超过48h),可用冰箱冷冻籍贮效样品。4.1.5样品预处理
4. 1. 5. 1准备工作
若必要时将冷冻样在冰箱(—2~4C)中放置过夜.使部分解冻以便切片。用台成洗涤剂(4.1.2.2)清洗塑料刀、碟、子、塑料板及尺和称重塑料膜,用蒸馏水或清洁海水(4.1.2.1)漂洗干净。工作台用洗净的塑料膜罩上。用合成洗涤剂4.1.2.2)仔细地洗手,后用蒸馏水或h.6
清洁的海水(4.1.2.1)漂洗干净。4.1.5.2赔贝样的制备
GB 17378. 6—1998
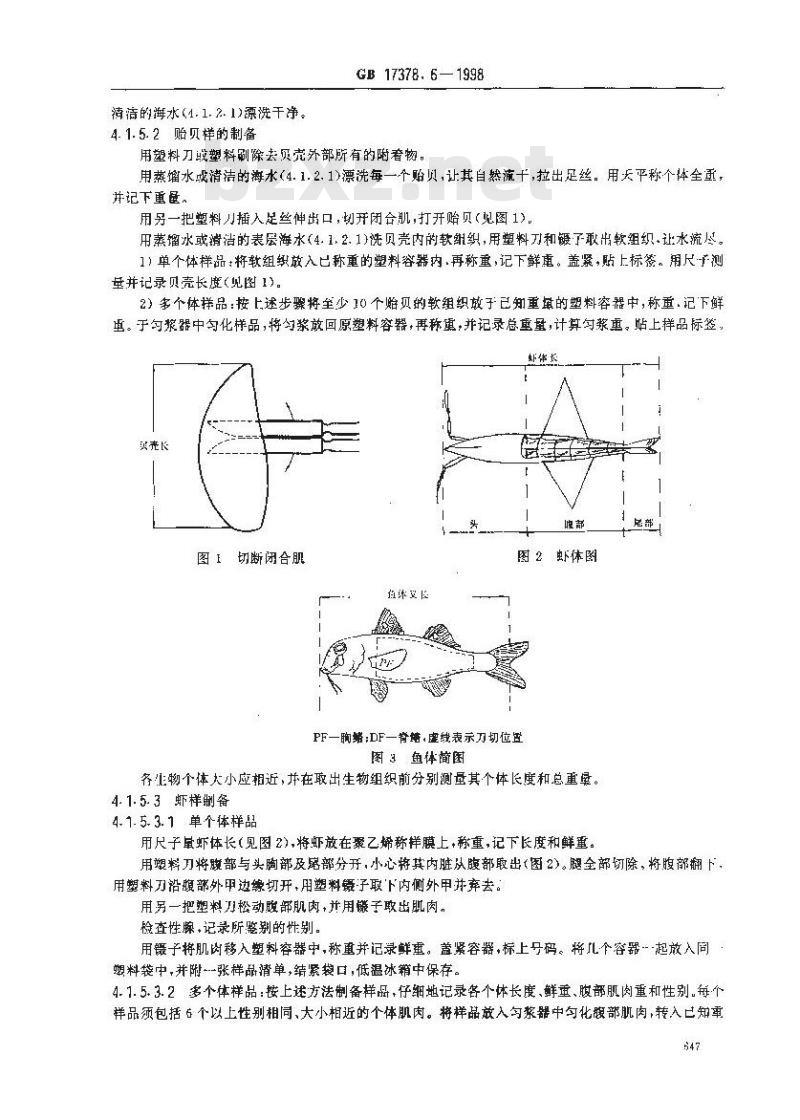
用塑料刀战塑料刷除去贝壳外部所有的附者物。用蒸馏水或清洁的海水(4.1.2.1)漂洗每一个贻贝,让其自然流十,拉出足丝。用天平称个体全重,并记下重晟。
用另一把塑料刀插入足丝伸出口,切开闭合肌,打开贻贝(见图1),用蒸馏水或消洁的表层海水(4.1.2.1)洗贝壳内的软组织,用塑料刀和镀了取出软组织·让水流尽。1)单个体样品:将软组织放入已称重的塑料容器内,再称重,记下鲜重。盖紧,贴上标签。用尺-F测并记录贝壳长度(见图1)。
2)多个体样品:接上述步骤将至少10个始贝的软组织效子已知重的塑料容器中,称重.记下鲜重。于勾浆器中匀化样品,将勾浆放回原塑料容器,再称重,并记录总重量,计算匀浆惠。站上样品标签,虾体长
灭充长
切断闭合肌
迫许文区
图2虾体图
PF一胸蜡;DF一脊墙,虚线表示刀切位宣图3鱼体简围
各1物个体大小应担近,并在取出生物组织前分别测量其个体长度和总重。4.1.5.3虾样制备
4.1. 5. 3. 1单个体样品
用尺子鼠虾体长(见图2),将虾放在聚乙烯称样膜上+称重,记下长度和鲜重。尼部
用塑料刀将耽部与头胸部及露部分开,小心将其内脏从腹部取出(图2)。腿全部切除,将腹部翻下用塑料刀沿腹部外甲边缘切开,用塑料摄子取下内侧外甲并弃去。用另一把塑料刀松动腹部肌肉,并用镰子取出肌肉,检查性腺,记录所整剃的性别。用氰子将肌肉移入塑料容器中,称重并记录鲜重。盖紧容器,标上号码。将儿个容器一起放入同塑料袋中,并附-张样晶精单,结紧袋口,低温冰箱中保存。4. 1. 5. 3.2多个体样品:按上述方法制备样品,仔细地记录各个体长度、鲜重、腹部肌肉重和性别.每·个样品须包括6个以上性别相同、大小相近的个体肌肉。将样品放入勾浆器中句化腰部肌肉,转入已知率647
GB 17378. 6—1998
盐的塑料容器中盖紧,标上号码,称重,记下鲜重和其他数据。游几个塑料器放作同-塑料袋甲+并附上样品清革,结紧袋口在低冰箱中保存4.1.5.4中小型鱼样制备
4. 1. 5. 4. 1单个体样品:测量鱼的艾长,并于聚乙烯称样膜于称重。记下文长和体重。用蒸馏水或清洁表层海水(4.1.2.1)洗涤鱼样,将它放在工作台上,用蝴料刀切乐胸鳞并切开背鳝近自头至尾部的色皮(图3)。
在鳃附近尾祁,横过鱼体各切一刀;在腹部,鳃和尾部两侧各切一刀。四刀只切在角体一侧,且不得切太深,以免切开内脏,沾污肉片。最好在切片时,由另人帮助按住鱼的头尾。用羧子将鱼皮与肉片分离,谨贴外表皮沾污肉片。用另一把塑料力将航肉与餐椎离,并用摄子取下肌肉。将组织燃手塑料容器,称重并记录车量,若则的肌肉不能满足分析用量,取另一侧肌肉补充。盖紧容器,贴上标签或记号,记录各所有数据,于低温冰箱中保存。鉴定性腺性别。
4.1.5.4.2多个休试伴:制备方法如下。仔细记下各个体体长,鲜重,肌肉重。鉴定性别。个休数不应少于6个+耳性别应相同,人小相近。用勾浆器勾化色组织,将匀浆转人已知重量的塑料容器中,盖紧,贴上标签井称重记下对浆重和!他数据。暨于低温冰稍中存放。4.1.5.5人塑鱼样制备
若必要,将现场采巢的样品(4.1.4.4)放在一2~4冰箱中过夜,使部分解冻以便」切片。用蒸馏水或清洁海水(4.1.2.1)洗涤鱼样,置于清洁的工作台上。剔除残存的皮和骨,用塑料月切去丧层,再用另-把塑料刀重复操作一次.留下不受污柴的均匀的肌肉组织。将班肉组织放人魏料容器巾盖紧,贴上标签,称重,将全部数据记入记录表,样品存于低温冰箱中。4.1.5.6千样涮备
将部分新鲜试样按4.1.6-1或4.1.6.2步骤烘十,计算1/湿比,以校正水分含量,十燥后的样品用码脑研钵磨碎,全部筛过80~100目(尼龙筛),供痕元素分析用。4. 1. 6千重测定
4. 1. 6. 1烘 1-
半开称整瓶的磨口盖,放入105℃烘箱巾。2h后,取出称量瓶,置于干媒器中冷却30min。盖好瓶盖,分析犬平称重,记下重量。取5~10多生物制备样(1.1.5)于称量瓶中,盖好瓶益所称重(+0. 5 mx>并记下重率。
将盛样品的称量瓶半开盖放入105C:烘箱中。24h后取出,置于干燥器中冷却30min,盖好瓶盖后称重并记录所称重最。
重复烘干操作,至前后两次烘干后的重量差小于总重量的0.5%。计算干重和干/湿比。4.1-6.2冷添下燥
对类脂物含量高的生物样品,不能烘于至恒重,则须用冷冻干燥。准确称取 1~2 g生物制备样(1. 1. 5)于干净的冷冻干烘的样品容器中,冷冻干 24 h,再称重次。冉饮冷冻十燥24h,再称重。两饮称重的重量差应小于总重量的0.5%。否则,成继续十燥至符含要求
让算重和/湿比(F)。
4.1.7注意事项
4.1,1非实验室附近来集始贝,不存在特殊的运输和戴同题。运往实验室时,仗须使赔成样通风用海水保持润湿。采自潮间带的贻贝,在空气中可生存24h。浸在海水中的始贝,会吸水并排泄废物.始贝在牢气中,贝壳闭合,代谢速度大大降低,故运输时,不应将始类放在水中。RA
GB 17378.6—1998
4.1.7.2于洗净之后,不应接触解剖组织,最好带上于套:若条件许可,准备工作和样品制备均应在洁净条件下进行。
4.1.7.3制备多个体样品时,应取性别相同、个休大小和近的生物。取出软组织之前,应分别测量各个体体长和重量。
4.1.7.4样品消化前,将盛有样品的容得总重量与必存时之重量进行比较,可发现贮存期间详品是否失重。
4.1.7.5不同部位肌肉的痕盘金属个量可能存在差别故实际样品的有关资料应尽可能记录详细。4.1.7.6用有机氛农药和石油烃测定的生物样品,样品采集和预处理的设备和试剂作适当的应改变,应避免采用塑料器血和含有卤代烃或有油烃的试剂。4.1.7.7牛物体中总求及有害有机物的测定,不官用干燥后的样品。该时,用湿样测,结果仍以干样中被测物的个量来表示。
4.2要求
4.2-1分析样品的烘十:未注明干嫩温度及时间时,均指105℃士1℃,干燥2h,4.2.2标准溶液配制中,所有的移液管均应事先进行容量校正。量瓶均用一级品。4.2.3所有容器的净化除另有注明外,均先用(1十3)硝酸浸泡2~3d后,冉用去离子水存细淋洗1净,惊丁后备用。
4.2.4数据处理按GB17378.2--1998要求执行。4.2.5文内pH值除注明测量方法外,均可用精密或广泛pH试纸测量,表1从分析样中抽取检查样的比例分析样个数
检查样抽取百分数
10-~30
4.2.6为检奔分析结果的质量,由业务主管部门从一批分析样中按表1任意轴取检查样,分别装装另编样号.将基本样与检查样交有关人员进行测定。4.2.6.1查样的测项与基本样相同。4.2.6.2当分析样数量较多时,基本样与检查样可不必安排在同批内进行测试,4.2.6.3测试所得的结果由业务卡管部门汇.总,按表2所列双样相对偏差值控制分析质量。当某测项双样检查结果超差率大于30%时,此批基本样中该测项要全部重新称样进行测定。若仍山现上述超差情况,主管部门应与分析人员认真检查分析原因(如标准落液的配制,环境质量,所有仪器设备石尤不正常情况等)后,再进行这批分析样(基本样与检查样)的测定。当某测项双样检查结果超差率小于:3(%时,超差的样品需重新称样进行测定,直至新测定结果合格为止。按平行双样的均值报山结果。衣2平行双样相对偏差表
分积结果所在数虽级
相对偏差筹许限(%)
Blxia%
计笋:
每批分析的样品(20个左右)由业务主管部门插人2~3个标催生物样品(另行编号),以检验有尺系统误差。
4.3.1各种酸碱的密度(0)足指20C时的g/ml。4.3.2下燥剂在不指明具体名称时,均指变色硅胶,4.3.3所配制的元素的标准溶液的浓度均指该元案的浓度。4.3.4没有指明溶剂的溶液都是水溶液。S19
5测定项目.方法及捡出限
测定项目方法及出限见表3。
分析方法
冷原子吸收光度法
双疏腺分光光度法
无火焰原子吸收分光光度法
阳极落山伏安法
火焰原子吸收分光光度法
二乙基硫代肢基甲酸偿
分光光度法
无火焰原半吸收分光光度法
阳极溶出伏安法
火焰原了吸收分光光度法
「双蔬踪分光光法
丁火筛原子吸妆分光光度法
阳极潜出伏安法
欢疏临分光光度法
石浊烃
6总汞
荧光分光光法
气相色潜法
6.1冷原子吸收光度法
6-1、1适用范固和应用领域
GB17378.6—1998
丧3测凝项月方法检消限
1均出限W(10\)
1(湿量)
a-6663pg
Y6667pg
β-6668pg免费标准下载网bzxz
g-666 9pg
p'- 8
-DT 40Pg
分析方法
年碳数二饼分光光度送
无火焰源子吸收分光光度法
砷铅酸-绢晶紫分光光度达
愉出限W0)
急化物原子吸收分光光度法!
催化极谐法
无火原子吸收价光光漫法
极落出伏安法
火焰源子吸收分光光度法
双硫腺分光光度达
荧光分光光迎临
二氨基联茉胺四盐酸益分
光光度法
催化谱法
多氧联装气相色谐法
秋氏剂
气相色谱法
本方法适用于海洋生物体中总汞的测定,对含碘量高的生物样品:应添加适量硝酸银消除碘对测定的于扰。
检出下限(W):0.01X10-6
6. 1.2 方法原理
以五氧化二钒作催化剂,用硝酸-硫酸消化生物样品,将有机汞全部转化为无机汞,再用氯化亚铸将汞离子还原成金属汞,用气-液平衡开路吸气冷原子吸收测定系统于253.?nm波长测定总求个,6.1.3试剂及其配制
除非另作说明,所用试剂均为分析纯,水为去离子水或等效纯水。6.1.3.1五氧化二钒(V0.)
6.1.3.2无水氟化钙(CaCl,),用于装填于煤管。6.1.3.3硝酸(HNO,):0=1.42g/mL.6.1.3.4硫酸(H,SO,):0-1.84g/mL,工艺超纯。6. 1. 3. 5 硫酸溶液:0. 5 mol/LAS!
GB17378.61998
在不断揽拌下,将28mL硫酸(6.1.3.4)徐途加入972mL水中。6.1.3.6盐酸溶液:1+1
将盐酸HCE.p=1.19%/mL)与等体积水混合。6、1.3.7硝酸落液:1+19
用1份硝酸(6.1.3.3)与19份水混合。6.1.3.8氮化业锡溶液:100g/1,称取10g氛化亚于烧杯中+加入100ml.盐酸溶液(6.1.3.6),加热至溶解,冷却后装于棕色瓶内,使用时用等体积水稀释,若汞杂质含量高,可用鼓泡法去除,直至溶液中汞含量不能检出。6.1.3.9低汞海水;表层海水经滤纸过滤,向每升海水徐徐加入28mL硫酸(6.1.3.4)酸化,海水求含量应低于0.005g/L
6.1.3.10标准忙备液:1.00tmg/mL称取0.1354g氧化汞(HgCl)(预先在硫酸干燥器中干燥)于10mL烧杯中,用硝酸落液(6.1.3.7)溶解。全量转入100ml.量瓶中,用硝酸溶液(6.1.3.7)稀释至标线,混匀,保存期一年。6.1.3.11汞标准中间溶液:10.0g/ml量取1.00ml.录标贮备溶波(6.1.3.10)于100mL量瓶中,用硝酸溶液(6.1.3.7)稀释至标线,混句。保存期一星期。
6.1.3.12录标准使用溶液:0.100g/ml量取1.00mL求标准中间济液(6.1.3.11)于100m.量瓶中,用硫酸游液(6.1.3.5)稀释至标线,混勺当犬配制。
6.1.4仪器及设备
测汞装置(图4)4
1抽气泵;2空气流量调节阀;3-含求废气吸收器:4—测汞仪;5-光吸收池+6--干燥管;?—三通附,8汞蒸气发生瓶:9-空气净化装置+11一气体流盘计图4冷原子吸收测汞装置
汞燕气发生瓶:250ml.锥形洗瓶改制.将洗瓶通气管下端截断,使管端刚离开待测游液液面,一电热板:铺 上约 3 cm厚细砂;实验室常备仪器皮设备。
6. 1.5分析步骤
6.1.5.1绘制标准曲线
6.1.5.1.1取6个250mL求蒸气发生瓶,加100mL低汞海水(6.1.3.9),然后分别加人0,0.10.0.20.0.30,0.400.50mL汞标准使用溶液(6.1.3.12),混勺。6.1.5.1.2将测汞仪上的=通开关转至调零档,以1~1.51,/min流速的签气流通过光吸收池。6.1.5.1.3将求蒸气发生瓶依次连接于测汞仪.上.加入2mL氯化亚锅溶液(6.1.3.8),迅速案紧录蒸气发生瓶的塞了,振摇1min。
6.1.5.1.4调节测求仪零点,将三通开关转到测定档,测其吸光值A;及标准空白吸光值A。6.1.5.1.5将数据填入衣GB17378.4—1998附录表A5中。以吸光值A:一A。为纵坐标,相应的求含量(ug)为横坐标,绘制标准曲线。6.1.5.2样品消化
GB 17378.61998
准确称取2.5g(工0.0018)混样放人100tmL高型烧杯中,加入40mg在氧化二钒(6.1.3.1)8mi.硝酸(6.1.3.3),盖上表面血,置于140~160C电热板上加热10min。取下稍冷后加入15ml.硫酸(6.1.3.4),继续加热20min。取下,销冷后加10mL水,再加热30min,取下.冷却后全量转入100ml。录瓶中,加水稀至标线.混勾、得样品消化液。同时制备分析空口试液。6.1-5.3样品测定
鼠取适基样品制备液于乘蒸气发生瓶中,加水至100mL。其余按6.1.5.1.2~6.1.5.1.4步骤测定吸光值(A,)及分析空自吸光值(A)。以(A。一A)的值从标雅曲线上查出相应的汞的(μg)。6.1- 6 记录与计算
将样品测延数据填入A1中,按式(1)计算样品上样中汞的含量:说
Wa—V,MF
式中:W——生物下样中总汞的含世质最比.10‘;m-从标准曲线上查得的汞的量·rgV.\:样品消化液的体积,ml.;V2——谢定分样体积.tmI.;
M..样品的称取基..
F——样品的下/湿比。
6.1.7精密度和推确度
平行测定6个样品,其汞含量(质量比)为0.25×10-,相对标准偏差为1%+4个实验测定同一社抛丘校样,其结巢相对标准偏差为9.1%。6. 1. 8 注意事项
6.1.8.1幕血均用(1+3)硝酸溶液浸泡3d以上,洗净,并检查是否合格。6.1.8.2用过的乘蒸气发生瓶,须用酸性高锰酸钾溶液漂洗,用水洗净。6.1.8.3绘制汞标准曲线时,也可用氯化钠溶被代举低汞海水。6.2双硫踪分光光度法
6.2.1适用范围和应用领域
本法适用丁海洋生物体中总汞的测定。碘有下扰,故海中总求的测定不宜直接用此法。检出限:0. 01×10-,
6.2.2方法原埋
样品经硝酸-过氧化氢-高锰酸钾消化,用氯化亚锡将汞离子还原为金属末。用曦气法使汞蒸气吸收于高锰酸钾溶液中,浆离子与双硫踪反应后用叫氯化碳举取其生成的橙色整合物,于485nm波长处逊行分光光度测定:
6.2.3试剂及其配制
除非另作说明,所用试剂均为分析纯,水为无汞去离子水或等效纯水。6.2.3.1硝酸(H0),):0=1.42g/mL,优级纯。6.2.3.2过氧化氢(H))30%,优级纯。6.2.3.3硫酸溶液:1+1,1+40
在搅拌下,将1休积硫酸(H.S0,P=1.81g/mL,优级纯)徐徐加到1及40体积水中。6.2.3.4氧氨化铵溶液c(NH,OH)=1mol/L。6.2.3.5高锰酸钾溶液:50&/L。(盛十棕色试剂瓶中,暗处保存)。6.2.3.6氧化亚锡溶液:200名/L称取100g氮化亚锅(SnCl2H,0)于500ml.烧杯中.加入500mL(1十1)盐酸溶液,加热至氯化亚锡完全溶解,冷却店,盘于棕色试剂瓶中若求杂质含量商,可用鼓泡法去除之直至溶液中汞检不出。552
6.2.3.7高锰酸钾吸收液:5g/1.
GB 17378. 6— 1998
将101ml.(1+1)硫酸溶液(6.2.3.3)加到10ml.高锰酸钾溶滤(6.2.3.5)中,加水至100mL,混勺(盛于棕色试剂瓶中,暗处保存)。6.2.3.B盐酸羟胺溶液:1008/L
称取10g盐酸羟胺(NH,OH·HC)用水溶解,加水至100mL。用5mL双硫晾使用游液(6.2.3.12)提取数次,至有机相是绿色为止,弃太有机相,水相盛于试剂瓶中。6.2.3.9乙二胺四乙酸二溶液:50区/L称取5gEDTA(二钠),用水溶解,加水至100nl.。用5mL双硫腺使用溶液(6.2.3.12)提取数次。军有机相呈绿色为止,弃去有机相,水相盛“滴瓶中。6-2:3.10四氯化碳(CCL)
6.2.3.11双硫踪贮备溶液
称取100mg双硫腺(C,H,N:NCSNHNHC.H,)溶于100mL四氛化碳(6.2.3.10)中,盛于棕色试剂瓶中。置冰箱中保存。
6.2.3.12双硫腺使用溶液:透光率70%按下列方法确定双硫腺贮备溶液(6.2.3.11)的吸光值,取1.00mL双硫踪整备裕液(6.2.3.11)于10叫L量瓶中,加四氟化碳(6.2.3.10)率标线,混约。以四氯化碳(6-2.3.10)调零,于500nm处用1cm测定池测定其吸光值A1。根据稀释因于,得双硫踪贮备溶液(6.2.3.11)的吸光值为10A1。根据式(2)计算配制一定体积双硫踪使用溶液所需贮备溶液的体积:Vle
V,=-10A,
式中;V,一配制V,体积双硫踪使用溶液时,所需双硫踪贮备溶液的体积,mL:欲配制的双硫踪使用溶液的体积,mLI一双硫腺贮备游液稀释10倍后的吸光值,A
一欲配制效硫腺使用溶液的避光率,%。本法采用了0%透光率。(2)
量取V。体积双硫腺备溶液(6.2.3.11)、加四氯化碳(6.2.3.10)至V.体积,混句,得透光率为70%的双确踪使用溶液(使用时配制)。6.2.3.13求标准贮备溶液:100μg/mL称取0.1354g氯化汞(HgCl2.优级纯)于100mL烧杯,用5mL(1+1)硫酸游液(6.2.3.3)溶解后.全转入1000mL量瓶中,加水至标线,混勾。6.2.3.14汞标准使用溶液:1.00临/mL最取1.00mL汞标准贮备溶液(6.2.3.13)于100ml.量瓶中,用(1+40)硫酸济液(6.2.3.3)稀释至标线,混匀,使用时配制。
6.2.4仪器及设备
分光光度计;
永蒸气发生瓶:见6.1.42,
吸收管;10mL,
抽气泵;
·气体流量计:
一电热恒温水浴锅:
实验室常备仪幕及设备,
6.2.5分析步骤
6.2.5.1样品浒化
CB17378.6:1998
准确称取10 g(±0.01g)生物湿样于 150 mL锥形瓶T,加入 20 mL硝酸(6.2. 3. 1),于室温下消化过夜.补加5TmL硝酸(6.2.3.1),于90C水浴中消化1.5h,每20min播动-次。滴加2mL过减化领(6-2.3.2),继续消化半小时,取出稍冷后,加人高锰酸钾溶液(6.2.3.5)至有大量褐色沉淀产生:且半小时内不消失,否则冉外加高锰酸钾游液(6.2.3.5)。制得拌品消化液.同时制备分析空自试液,6.2.5.2绘制标准曲线
6.2. 5.2.1取心支2 mL 具塞比色管,加入.10 ml. 高锰酸钾吸收液(6.2.3.7),分别移人 0,1. 00,2.00,3.00,4.00,5.00 mL的录标准使用溶液(6.2.3.14),加水全20 mL,滴加盐酸羟胺弊液(6.2.3.8)至红色消失:再多那2滴。
6.2.5. 2.2 加入 5. 00 ml,双硫使用液(6.2. 3. 12),剧烈振满 2 min(注意放气),静置分层。吸去上层水相。再用水洗涤有机相2~3次(每次用水20 mL),吸去水相。6-2.5.2.3加入2滴EDTA(二钠)溶液(6.2.3.9),用氢氧化铵(6.2.3. 4)溶液洗漆 2次,每饮 10 mL,有机相移人60mI.锥形分液瀚斗(管颈塞有脱脂棉)中。6.2.5.2.4将有机相滤人1cm测楚池中,以四氯化碳(6.2.3.10)调零,于波长485nm处测定吸光值A.及标准空白吸光值A:。
6.2.5.2.5将测定数值记入GB17378.4—1998附录表A4中,以吸光值(A.—A,)为纵坐标,和应的汞的量()为横坐标,绘制标准曲线。6.2.5.3样品测定
6.2.5.3.1滴加盐酸羟胺溶液(6.2.3.8)于样品制备液中,至红色完全消失,全量转入250ml.乘蒸气发生瓶中,用100IiL水分三次洗涤锥形瓶,洗涤波合并于求蒸气发生瓶中,6.2.5.3.2取两支10mL吸收管,各加入10mL吸收液(6.2.3.7),一支作空气净化管,一支作样品求蒸气吸收管。按曝气-吸收装置示意图将气路系统接好,空气净化吸收管不必每饮更换,提抽气系
1-…-气体流量计,2一括芯气体采样管,3一求蒸气发生瓶图5曦气-吸收装置图
6.2.5.3.3加2mI.氮化亚锡溶液(6.2.3.6)于汞蒸气发生瓶中,立即塞紧瓶塞。接通气泵,以1500mL/min空气漩速暖气15min。6.2.5.3.4取下聚蒸气吸收管,将吸收液移人25mL具塞比色管中,用10ml.水分三次洗涤吸收管,洗涤被准入比色管中。滴加盐殿羟胺溶液(6.2.3.8)至红色褪尽,冉多加2滴,充分振满,开益放置30 min.
6.2.5.3.5以下接6.2.5.2. 2~6.2.5.2.4步骤测定样品制备液的吸形值(A,2同时,按.上述步骤测定分折空自的吸光值A。6. 2.6记录与计算
称测得数据记人表A1中,按式(3)计算生物干样中总汞的含量:Wue=FM
式中:W一一生物下样中总汞的含量质量比,10-;654
GB17378.6-1998
m—从标准曲线上查得的乘的量,;F…一样品的下湿比;
M——样品称取基,g。
6-2.7精密度和准确度
五个实验室测定含乘的质量比为0.29×10-6的样品,重复性相对标准偏慈为0.95%。在0.5g猪肝成分分析标准物质(GBW08551)中加人2汞,平均回收率为95.9%。6.2.8注意事项
6.2.8.1样品消化时,过氧化氢需逐滴加入,以防过氧化愈剧烈分解,消化液溅溢,造成求损失。6.2.8.2样品测定步6.2.5.3.4中,开盖放置30min,是为消除反应产生的氟气及氮氧化物的影啊。
6.2.8.3样品测定步骤6.2.5.2.2中,水洗存机相是为了消除价锰的于扰。6.2.8.4玻器血均需用(1+3)硝酸溶液浸泡1天后洗净使用。7铜
7.1无火焰源子吸收分光光度法
7.1.1适用范围和应用领域
本法适用于海洋生物中的测定。检山限(W):0.4X10*。
7.1.2方法原理
生物样品经硝酸-过氧化氢消化,于波长324,7nm处直接进行石殿炉原子吸收分光光度测定。7.1.3试剂及其配制
除非另作说明、所用试剂均为分析纯,水为二次去离子水或等效纯水。7.1.3.1硝酸(HNO.>:P1.42&/ml优级纯,经石英亚沸蒸馏器蒸馏7.1.3.2过氟化氢(H0,)130%,7.1.3.3铜标准览备溶液:1.000mg/ml称取0.2000g金属铜粉(纯度99.99%)于50mL.烧杯中,加人5mL(1+2)硝酸溶液,加热溶解冷却后,全量转入200mL量瓶中,加水至标线,混匀。7.1.3.4标准中溶液:100/ml.
量取10.0ml.铜标准贮备溶液(7.1.3.3)于100mL基瓶中,加(1+99)硝酸溶液至标线,混勾。使用时配制。
7.1.3.5铜标准使用溶液:2.000μg/mL量取2.00mL铜标准中间溶液(7.1.3.4)于100ml量瓶中,加1十99)硝酸溶液至标线,混勺。使用时配制。
7.1.4、仪器及设备
石墨炉原子吸收分光光度计:配有自动进样装置-铜空心阴极灯+
氩气钢瓶:纯度99.99%:
一洁净工作台(洁净100级);
电热板。
7.1.5分析步骤
7.1.5.1样品消化
7.1.5.1.1准确称取0.1g(±0.001g)于样于50mL烧杯中,用几滴水湿润样品,加入2ml.硝酸(7.1.3.1),盖上表面血,于电热板上,低温加热至泡沫基本消尖。655
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
本标准是海洋监测规范》的第6部分,是在HY003.6一91行业标准的基础上修订而戒的。本标规定了生物体分析的要求和分析方法。海洋胜测规范\包括下列部分:GB 17378.1 1998
第1部分;总则
海洋监测规范
GB 17378. 2—1998
GB 17378- 3—1998
GB 17378. 4—1998
GB 17378. 5-1998
GH 17378.6—1998
CB 17378. 71998
海洋监测规范
海洋监测规范
海洋监测规范
海洋监测规范
海洋监测规范
海洋壁測规范
本标准的谢录A是标准的附录。
本标准由国家海洋局提出。
第2部分:数处理与分析质盘控制第 3 部分;样品果集,吡存与运输第1部分:海水分析
第5部分:沉积物分析
第6部分生物体分析
第7部分:近海污染生态调查和生物监测本标推由国家游洋标唯计壁中心归口,本标摊由国家海洋厨第三海洋研究所负责起草。本标推主要起草人,许昆灿、张卷明、陈维岳、洪君超、陈邦龙。614
1范围
中华人民共和国国家标准
海洋监测规范
第6部分:生物体分析
The specificution for marine monituringPart 6:Organisim analysis
CB 17378. 6 1998
本标准规定了海洋生物(贮贝,虾及鱼)中13项有害物质含量的测定方法,并对样品采集、运输、存、预处理和测定结果的计算等提出技术要求。本标准适用于大洋,近游和沿海水域的海洋生物污染调查与监测,2引用标准
下列标准所包含的条文,通过在本标准中引用而构成为本标准的条文。本标准出版时,所示版本均为有效。所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。GB17378.2—1998海洋监测规范第2部分:数据处理与分析质量控制CB17378、4-1998海洋临测规范第4部分:海水分析GB17378.5—1998海洋监测规范第5部分:沉积物分析3定义
本标准采用下列楚义。
3.1蒸至近干evaporation to dryness将溶剂蒸发至小体积(0.2 mL~心.3mL),若有残渣时,残湾应湿润状。4—般规定
4.1样品的采集与制备
4.1.1采样对象
贻所、虾和鱼类。
4. 1.2试剂
4.1.2.1去离子水或等效蒸馏水,其痕量金属含量应低于分析方法的检出限。或用米受沾污的表层海水。
4.1.2.2合成洗漆剂。
4.1.3仪器和设备
塑料冷冻箱,配有。用于贻贝贮存和运输时,底部必须具有板,以免样品浸入求中;一冰箱
低温冰箱:
乙烯袋:
国家质量技术监督鼠1998-06-22批准1999-01 -01 实施
--塑料板和尺子;用下长度测量;塑料刀
GB 17378.61998
玻璃或陶瓷碟(供制备样品用);锻子:塑料制品或其他合适材料的制品1高密度聚乙烯袋和塑料容器:供速冻保存样品用,装样前,须用合成洗涤剂清洗,并用蒸馅水洗净:
高密度聚乙烯膜:供罩工作台用;小张案乙烯膜:供称重用,
.分析天平感量0.1mg;
塑料洗瓶;
刮刀:供来集贻贝用:
塑料桶:20~-50L;
大号金属力,无锈斑,供切取鱼组织用;勾浆器:不锈钢或其他适宜材料的制品;塑料刷:毛刷紧硬,用以去除贻贝外壳的附着物;称量瓶:50mL,
电热烘箱:
干燥箱:
一冷冻干燥设备。
4.1.4采样与运输
4. 1.4. 1 准备 1.作
用合成洗涤剂(4.1.2.2)清洗冷冻箱、高密度聚乙烯袋、塑料板及尺、大号金属刀、刮刀.再用溜水或表层海水(4.1.2.1)漂洗干净。4.1.4.2贴贝采集
用清洁刮刀从其附着物上采集始贝样。选取足够数量的完好贻贝存十冷冻箱中。若需长途运输(炎热天超过2h),应把贻贝伴品盛于塑料桶中,将现场采集的清洁海水淋酒在贻贝.E,样品保持润湿状但不能没人水中。若样品处理须在采样24h后进行,可将贻具样存于高密度塑料袋中,历出袋内空气,将袋口打结或热封,将此和样品标签··起放入聚乙烯袋中并封口,存于低温冰箱中。4.1.4.3虾与中小型鱼样采集
按一定要求选取足够数微的完好的生物样,放入干净的聚乙烯袋中,要防止刺破袋子。挤山袋内空气,将袋!打纬或热封,将此和样品标签一起故人另一聚乙烯發中,并封口,低温冷藏。只有在贮存期不太长时(热天不超过48h),方可便用冰箱或冷冻箱存放样品。4.1.4.4大型鱼样采集
测量并记下鱼样的叉长,体再和性别。用清道的金展刀切下至少1006肌肉组续厚度至少5cm,以便在样品处理(4.1.5.5>时.切除沾污或内脏部分,存\清洁的聚乙烯袋中,挤出空气并封口,将此袋与样品标签一起放入另一案乙烯袋中,封口,于低温冰箱中贮存。若保存时间不太长(热天不超过48h),可用冰箱冷冻籍贮效样品。4.1.5样品预处理
4. 1. 5. 1准备工作
若必要时将冷冻样在冰箱(—2~4C)中放置过夜.使部分解冻以便切片。用台成洗涤剂(4.1.2.2)清洗塑料刀、碟、子、塑料板及尺和称重塑料膜,用蒸馏水或清洁海水(4.1.2.1)漂洗干净。工作台用洗净的塑料膜罩上。用合成洗涤剂4.1.2.2)仔细地洗手,后用蒸馏水或h.6
清洁的海水(4.1.2.1)漂洗干净。4.1.5.2赔贝样的制备
GB 17378. 6—1998
用塑料刀战塑料刷除去贝壳外部所有的附者物。用蒸馏水或清洁的海水(4.1.2.1)漂洗每一个贻贝,让其自然流十,拉出足丝。用天平称个体全重,并记下重晟。
用另一把塑料刀插入足丝伸出口,切开闭合肌,打开贻贝(见图1),用蒸馏水或消洁的表层海水(4.1.2.1)洗贝壳内的软组织,用塑料刀和镀了取出软组织·让水流尽。1)单个体样品:将软组织放入已称重的塑料容器内,再称重,记下鲜重。盖紧,贴上标签。用尺-F测并记录贝壳长度(见图1)。
2)多个体样品:接上述步骤将至少10个始贝的软组织效子已知重的塑料容器中,称重.记下鲜重。于勾浆器中匀化样品,将勾浆放回原塑料容器,再称重,并记录总重量,计算匀浆惠。站上样品标签,虾体长
灭充长
切断闭合肌
迫许文区
图2虾体图
PF一胸蜡;DF一脊墙,虚线表示刀切位宣图3鱼体简围
各1物个体大小应担近,并在取出生物组织前分别测量其个体长度和总重。4.1.5.3虾样制备
4.1. 5. 3. 1单个体样品
用尺子鼠虾体长(见图2),将虾放在聚乙烯称样膜上+称重,记下长度和鲜重。尼部
用塑料刀将耽部与头胸部及露部分开,小心将其内脏从腹部取出(图2)。腿全部切除,将腹部翻下用塑料刀沿腹部外甲边缘切开,用塑料摄子取下内侧外甲并弃去。用另一把塑料刀松动腹部肌肉,并用镰子取出肌肉,检查性腺,记录所整剃的性别。用氰子将肌肉移入塑料容器中,称重并记录鲜重。盖紧容器,标上号码。将儿个容器一起放入同塑料袋中,并附-张样晶精单,结紧袋口,低温冰箱中保存。4. 1. 5. 3.2多个体样品:按上述方法制备样品,仔细地记录各个体长度、鲜重、腹部肌肉重和性别.每·个样品须包括6个以上性别相同、大小相近的个体肌肉。将样品放入勾浆器中句化腰部肌肉,转入已知率647
GB 17378. 6—1998
盐的塑料容器中盖紧,标上号码,称重,记下鲜重和其他数据。游几个塑料器放作同-塑料袋甲+并附上样品清革,结紧袋口在低冰箱中保存4.1.5.4中小型鱼样制备
4. 1. 5. 4. 1单个体样品:测量鱼的艾长,并于聚乙烯称样膜于称重。记下文长和体重。用蒸馏水或清洁表层海水(4.1.2.1)洗涤鱼样,将它放在工作台上,用蝴料刀切乐胸鳞并切开背鳝近自头至尾部的色皮(图3)。
在鳃附近尾祁,横过鱼体各切一刀;在腹部,鳃和尾部两侧各切一刀。四刀只切在角体一侧,且不得切太深,以免切开内脏,沾污肉片。最好在切片时,由另人帮助按住鱼的头尾。用羧子将鱼皮与肉片分离,谨贴外表皮沾污肉片。用另一把塑料力将航肉与餐椎离,并用摄子取下肌肉。将组织燃手塑料容器,称重并记录车量,若则的肌肉不能满足分析用量,取另一侧肌肉补充。盖紧容器,贴上标签或记号,记录各所有数据,于低温冰箱中保存。鉴定性腺性别。
4.1.5.4.2多个休试伴:制备方法如下。仔细记下各个体体长,鲜重,肌肉重。鉴定性别。个休数不应少于6个+耳性别应相同,人小相近。用勾浆器勾化色组织,将匀浆转人已知重量的塑料容器中,盖紧,贴上标签井称重记下对浆重和!他数据。暨于低温冰稍中存放。4.1.5.5人塑鱼样制备
若必要,将现场采巢的样品(4.1.4.4)放在一2~4冰箱中过夜,使部分解冻以便」切片。用蒸馏水或清洁海水(4.1.2.1)洗涤鱼样,置于清洁的工作台上。剔除残存的皮和骨,用塑料月切去丧层,再用另-把塑料刀重复操作一次.留下不受污柴的均匀的肌肉组织。将班肉组织放人魏料容器巾盖紧,贴上标签,称重,将全部数据记入记录表,样品存于低温冰箱中。4.1.5.6千样涮备
将部分新鲜试样按4.1.6-1或4.1.6.2步骤烘十,计算1/湿比,以校正水分含量,十燥后的样品用码脑研钵磨碎,全部筛过80~100目(尼龙筛),供痕元素分析用。4. 1. 6千重测定
4. 1. 6. 1烘 1-
半开称整瓶的磨口盖,放入105℃烘箱巾。2h后,取出称量瓶,置于干媒器中冷却30min。盖好瓶盖,分析犬平称重,记下重量。取5~10多生物制备样(1.1.5)于称量瓶中,盖好瓶益所称重(+0. 5 mx>并记下重率。
将盛样品的称量瓶半开盖放入105C:烘箱中。24h后取出,置于干燥器中冷却30min,盖好瓶盖后称重并记录所称重最。
重复烘干操作,至前后两次烘干后的重量差小于总重量的0.5%。计算干重和干/湿比。4.1-6.2冷添下燥
对类脂物含量高的生物样品,不能烘于至恒重,则须用冷冻干燥。准确称取 1~2 g生物制备样(1. 1. 5)于干净的冷冻干烘的样品容器中,冷冻干 24 h,再称重次。冉饮冷冻十燥24h,再称重。两饮称重的重量差应小于总重量的0.5%。否则,成继续十燥至符含要求
让算重和/湿比(F)。
4.1.7注意事项
4.1,1非实验室附近来集始贝,不存在特殊的运输和戴同题。运往实验室时,仗须使赔成样通风用海水保持润湿。采自潮间带的贻贝,在空气中可生存24h。浸在海水中的始贝,会吸水并排泄废物.始贝在牢气中,贝壳闭合,代谢速度大大降低,故运输时,不应将始类放在水中。RA
GB 17378.6—1998
4.1.7.2于洗净之后,不应接触解剖组织,最好带上于套:若条件许可,准备工作和样品制备均应在洁净条件下进行。
4.1.7.3制备多个体样品时,应取性别相同、个休大小和近的生物。取出软组织之前,应分别测量各个体体长和重量。
4.1.7.4样品消化前,将盛有样品的容得总重量与必存时之重量进行比较,可发现贮存期间详品是否失重。
4.1.7.5不同部位肌肉的痕盘金属个量可能存在差别故实际样品的有关资料应尽可能记录详细。4.1.7.6用有机氛农药和石油烃测定的生物样品,样品采集和预处理的设备和试剂作适当的应改变,应避免采用塑料器血和含有卤代烃或有油烃的试剂。4.1.7.7牛物体中总求及有害有机物的测定,不官用干燥后的样品。该时,用湿样测,结果仍以干样中被测物的个量来表示。
4.2要求
4.2-1分析样品的烘十:未注明干嫩温度及时间时,均指105℃士1℃,干燥2h,4.2.2标准溶液配制中,所有的移液管均应事先进行容量校正。量瓶均用一级品。4.2.3所有容器的净化除另有注明外,均先用(1十3)硝酸浸泡2~3d后,冉用去离子水存细淋洗1净,惊丁后备用。
4.2.4数据处理按GB17378.2--1998要求执行。4.2.5文内pH值除注明测量方法外,均可用精密或广泛pH试纸测量,表1从分析样中抽取检查样的比例分析样个数
检查样抽取百分数
10-~30
4.2.6为检奔分析结果的质量,由业务主管部门从一批分析样中按表1任意轴取检查样,分别装装另编样号.将基本样与检查样交有关人员进行测定。4.2.6.1查样的测项与基本样相同。4.2.6.2当分析样数量较多时,基本样与检查样可不必安排在同批内进行测试,4.2.6.3测试所得的结果由业务卡管部门汇.总,按表2所列双样相对偏差值控制分析质量。当某测项双样检查结果超差率大于30%时,此批基本样中该测项要全部重新称样进行测定。若仍山现上述超差情况,主管部门应与分析人员认真检查分析原因(如标准落液的配制,环境质量,所有仪器设备石尤不正常情况等)后,再进行这批分析样(基本样与检查样)的测定。当某测项双样检查结果超差率小于:3(%时,超差的样品需重新称样进行测定,直至新测定结果合格为止。按平行双样的均值报山结果。衣2平行双样相对偏差表
分积结果所在数虽级
相对偏差筹许限(%)
Blxia%
计笋:
每批分析的样品(20个左右)由业务主管部门插人2~3个标催生物样品(另行编号),以检验有尺系统误差。
4.3.1各种酸碱的密度(0)足指20C时的g/ml。4.3.2下燥剂在不指明具体名称时,均指变色硅胶,4.3.3所配制的元素的标准溶液的浓度均指该元案的浓度。4.3.4没有指明溶剂的溶液都是水溶液。S19
5测定项目.方法及捡出限
测定项目方法及出限见表3。
分析方法
冷原子吸收光度法
双疏腺分光光度法
无火焰原子吸收分光光度法
阳极落山伏安法
火焰原子吸收分光光度法
二乙基硫代肢基甲酸偿
分光光度法
无火焰原半吸收分光光度法
阳极溶出伏安法
火焰原了吸收分光光度法
「双蔬踪分光光法
丁火筛原子吸妆分光光度法
阳极潜出伏安法
欢疏临分光光度法
石浊烃
6总汞
荧光分光光法
气相色潜法
6.1冷原子吸收光度法
6-1、1适用范固和应用领域
GB17378.6—1998
丧3测凝项月方法检消限
1均出限W(10\)
1(湿量)
a-6663pg
Y6667pg
β-6668pg免费标准下载网bzxz
g-666 9pg
p'- 8
-DT 40Pg
分析方法
年碳数二饼分光光度送
无火焰源子吸收分光光度法
砷铅酸-绢晶紫分光光度达
愉出限W0)
急化物原子吸收分光光度法!
催化极谐法
无火原子吸收价光光漫法
极落出伏安法
火焰源子吸收分光光度法
双硫腺分光光度达
荧光分光光迎临
二氨基联茉胺四盐酸益分
光光度法
催化谱法
多氧联装气相色谐法
秋氏剂
气相色谱法
本方法适用于海洋生物体中总汞的测定,对含碘量高的生物样品:应添加适量硝酸银消除碘对测定的于扰。
检出下限(W):0.01X10-6
6. 1.2 方法原理
以五氧化二钒作催化剂,用硝酸-硫酸消化生物样品,将有机汞全部转化为无机汞,再用氯化亚铸将汞离子还原成金属汞,用气-液平衡开路吸气冷原子吸收测定系统于253.?nm波长测定总求个,6.1.3试剂及其配制
除非另作说明,所用试剂均为分析纯,水为去离子水或等效纯水。6.1.3.1五氧化二钒(V0.)
6.1.3.2无水氟化钙(CaCl,),用于装填于煤管。6.1.3.3硝酸(HNO,):0=1.42g/mL.6.1.3.4硫酸(H,SO,):0-1.84g/mL,工艺超纯。6. 1. 3. 5 硫酸溶液:0. 5 mol/LAS!
GB17378.61998
在不断揽拌下,将28mL硫酸(6.1.3.4)徐途加入972mL水中。6.1.3.6盐酸溶液:1+1
将盐酸HCE.p=1.19%/mL)与等体积水混合。6、1.3.7硝酸落液:1+19
用1份硝酸(6.1.3.3)与19份水混合。6.1.3.8氮化业锡溶液:100g/1,称取10g氛化亚于烧杯中+加入100ml.盐酸溶液(6.1.3.6),加热至溶解,冷却后装于棕色瓶内,使用时用等体积水稀释,若汞杂质含量高,可用鼓泡法去除,直至溶液中汞含量不能检出。6.1.3.9低汞海水;表层海水经滤纸过滤,向每升海水徐徐加入28mL硫酸(6.1.3.4)酸化,海水求含量应低于0.005g/L
6.1.3.10标准忙备液:1.00tmg/mL称取0.1354g氧化汞(HgCl)(预先在硫酸干燥器中干燥)于10mL烧杯中,用硝酸落液(6.1.3.7)溶解。全量转入100ml.量瓶中,用硝酸溶液(6.1.3.7)稀释至标线,混匀,保存期一年。6.1.3.11汞标准中间溶液:10.0g/ml量取1.00ml.录标贮备溶波(6.1.3.10)于100mL量瓶中,用硝酸溶液(6.1.3.7)稀释至标线,混句。保存期一星期。
6.1.3.12录标准使用溶液:0.100g/ml量取1.00mL求标准中间济液(6.1.3.11)于100m.量瓶中,用硫酸游液(6.1.3.5)稀释至标线,混勺当犬配制。
6.1.4仪器及设备
测汞装置(图4)4
1抽气泵;2空气流量调节阀;3-含求废气吸收器:4—测汞仪;5-光吸收池+6--干燥管;?—三通附,8汞蒸气发生瓶:9-空气净化装置+11一气体流盘计图4冷原子吸收测汞装置
汞燕气发生瓶:250ml.锥形洗瓶改制.将洗瓶通气管下端截断,使管端刚离开待测游液液面,一电热板:铺 上约 3 cm厚细砂;实验室常备仪器皮设备。
6. 1.5分析步骤
6.1.5.1绘制标准曲线
6.1.5.1.1取6个250mL求蒸气发生瓶,加100mL低汞海水(6.1.3.9),然后分别加人0,0.10.0.20.0.30,0.400.50mL汞标准使用溶液(6.1.3.12),混勺。6.1.5.1.2将测汞仪上的=通开关转至调零档,以1~1.51,/min流速的签气流通过光吸收池。6.1.5.1.3将求蒸气发生瓶依次连接于测汞仪.上.加入2mL氯化亚锅溶液(6.1.3.8),迅速案紧录蒸气发生瓶的塞了,振摇1min。
6.1.5.1.4调节测求仪零点,将三通开关转到测定档,测其吸光值A;及标准空白吸光值A。6.1.5.1.5将数据填入衣GB17378.4—1998附录表A5中。以吸光值A:一A。为纵坐标,相应的求含量(ug)为横坐标,绘制标准曲线。6.1.5.2样品消化
GB 17378.61998
准确称取2.5g(工0.0018)混样放人100tmL高型烧杯中,加入40mg在氧化二钒(6.1.3.1)8mi.硝酸(6.1.3.3),盖上表面血,置于140~160C电热板上加热10min。取下稍冷后加入15ml.硫酸(6.1.3.4),继续加热20min。取下,销冷后加10mL水,再加热30min,取下.冷却后全量转入100ml。录瓶中,加水稀至标线.混勾、得样品消化液。同时制备分析空口试液。6.1-5.3样品测定
鼠取适基样品制备液于乘蒸气发生瓶中,加水至100mL。其余按6.1.5.1.2~6.1.5.1.4步骤测定吸光值(A,)及分析空自吸光值(A)。以(A。一A)的值从标雅曲线上查出相应的汞的(μg)。6.1- 6 记录与计算
将样品测延数据填入A1中,按式(1)计算样品上样中汞的含量:说
Wa—V,MF
式中:W——生物下样中总汞的含世质最比.10‘;m-从标准曲线上查得的汞的量·rgV.\:样品消化液的体积,ml.;V2——谢定分样体积.tmI.;
M..样品的称取基..
F——样品的下/湿比。
6.1.7精密度和推确度
平行测定6个样品,其汞含量(质量比)为0.25×10-,相对标准偏差为1%+4个实验测定同一社抛丘校样,其结巢相对标准偏差为9.1%。6. 1. 8 注意事项
6.1.8.1幕血均用(1+3)硝酸溶液浸泡3d以上,洗净,并检查是否合格。6.1.8.2用过的乘蒸气发生瓶,须用酸性高锰酸钾溶液漂洗,用水洗净。6.1.8.3绘制汞标准曲线时,也可用氯化钠溶被代举低汞海水。6.2双硫踪分光光度法
6.2.1适用范围和应用领域
本法适用丁海洋生物体中总汞的测定。碘有下扰,故海中总求的测定不宜直接用此法。检出限:0. 01×10-,
6.2.2方法原埋
样品经硝酸-过氧化氢-高锰酸钾消化,用氯化亚锡将汞离子还原为金属末。用曦气法使汞蒸气吸收于高锰酸钾溶液中,浆离子与双硫踪反应后用叫氯化碳举取其生成的橙色整合物,于485nm波长处逊行分光光度测定:
6.2.3试剂及其配制
除非另作说明,所用试剂均为分析纯,水为无汞去离子水或等效纯水。6.2.3.1硝酸(H0),):0=1.42g/mL,优级纯。6.2.3.2过氧化氢(H))30%,优级纯。6.2.3.3硫酸溶液:1+1,1+40
在搅拌下,将1休积硫酸(H.S0,P=1.81g/mL,优级纯)徐徐加到1及40体积水中。6.2.3.4氧氨化铵溶液c(NH,OH)=1mol/L。6.2.3.5高锰酸钾溶液:50&/L。(盛十棕色试剂瓶中,暗处保存)。6.2.3.6氧化亚锡溶液:200名/L称取100g氮化亚锅(SnCl2H,0)于500ml.烧杯中.加入500mL(1十1)盐酸溶液,加热至氯化亚锡完全溶解,冷却店,盘于棕色试剂瓶中若求杂质含量商,可用鼓泡法去除之直至溶液中汞检不出。552
6.2.3.7高锰酸钾吸收液:5g/1.
GB 17378. 6— 1998
将101ml.(1+1)硫酸溶液(6.2.3.3)加到10ml.高锰酸钾溶滤(6.2.3.5)中,加水至100mL,混勺(盛于棕色试剂瓶中,暗处保存)。6.2.3.B盐酸羟胺溶液:1008/L
称取10g盐酸羟胺(NH,OH·HC)用水溶解,加水至100mL。用5mL双硫晾使用游液(6.2.3.12)提取数次,至有机相是绿色为止,弃太有机相,水相盛于试剂瓶中。6.2.3.9乙二胺四乙酸二溶液:50区/L称取5gEDTA(二钠),用水溶解,加水至100nl.。用5mL双硫腺使用溶液(6.2.3.12)提取数次。军有机相呈绿色为止,弃去有机相,水相盛“滴瓶中。6-2:3.10四氯化碳(CCL)
6.2.3.11双硫踪贮备溶液
称取100mg双硫腺(C,H,N:NCSNHNHC.H,)溶于100mL四氛化碳(6.2.3.10)中,盛于棕色试剂瓶中。置冰箱中保存。
6.2.3.12双硫腺使用溶液:透光率70%按下列方法确定双硫腺贮备溶液(6.2.3.11)的吸光值,取1.00mL双硫踪整备裕液(6.2.3.11)于10叫L量瓶中,加四氟化碳(6.2.3.10)率标线,混约。以四氯化碳(6-2.3.10)调零,于500nm处用1cm测定池测定其吸光值A1。根据稀释因于,得双硫踪贮备溶液(6.2.3.11)的吸光值为10A1。根据式(2)计算配制一定体积双硫踪使用溶液所需贮备溶液的体积:Vle
V,=-10A,
式中;V,一配制V,体积双硫踪使用溶液时,所需双硫踪贮备溶液的体积,mL:欲配制的双硫踪使用溶液的体积,mLI一双硫腺贮备游液稀释10倍后的吸光值,A
一欲配制效硫腺使用溶液的避光率,%。本法采用了0%透光率。(2)
量取V。体积双硫腺备溶液(6.2.3.11)、加四氯化碳(6.2.3.10)至V.体积,混句,得透光率为70%的双确踪使用溶液(使用时配制)。6.2.3.13求标准贮备溶液:100μg/mL称取0.1354g氯化汞(HgCl2.优级纯)于100mL烧杯,用5mL(1+1)硫酸游液(6.2.3.3)溶解后.全转入1000mL量瓶中,加水至标线,混勾。6.2.3.14汞标准使用溶液:1.00临/mL最取1.00mL汞标准贮备溶液(6.2.3.13)于100ml.量瓶中,用(1+40)硫酸济液(6.2.3.3)稀释至标线,混匀,使用时配制。
6.2.4仪器及设备
分光光度计;
永蒸气发生瓶:见6.1.42,
吸收管;10mL,
抽气泵;
·气体流量计:
一电热恒温水浴锅:
实验室常备仪幕及设备,
6.2.5分析步骤
6.2.5.1样品浒化
CB17378.6:1998
准确称取10 g(±0.01g)生物湿样于 150 mL锥形瓶T,加入 20 mL硝酸(6.2. 3. 1),于室温下消化过夜.补加5TmL硝酸(6.2.3.1),于90C水浴中消化1.5h,每20min播动-次。滴加2mL过减化领(6-2.3.2),继续消化半小时,取出稍冷后,加人高锰酸钾溶液(6.2.3.5)至有大量褐色沉淀产生:且半小时内不消失,否则冉外加高锰酸钾游液(6.2.3.5)。制得拌品消化液.同时制备分析空自试液,6.2.5.2绘制标准曲线
6.2. 5.2.1取心支2 mL 具塞比色管,加入.10 ml. 高锰酸钾吸收液(6.2.3.7),分别移人 0,1. 00,2.00,3.00,4.00,5.00 mL的录标准使用溶液(6.2.3.14),加水全20 mL,滴加盐酸羟胺弊液(6.2.3.8)至红色消失:再多那2滴。
6.2.5. 2.2 加入 5. 00 ml,双硫使用液(6.2. 3. 12),剧烈振满 2 min(注意放气),静置分层。吸去上层水相。再用水洗涤有机相2~3次(每次用水20 mL),吸去水相。6-2.5.2.3加入2滴EDTA(二钠)溶液(6.2.3.9),用氢氧化铵(6.2.3. 4)溶液洗漆 2次,每饮 10 mL,有机相移人60mI.锥形分液瀚斗(管颈塞有脱脂棉)中。6.2.5.2.4将有机相滤人1cm测楚池中,以四氯化碳(6.2.3.10)调零,于波长485nm处测定吸光值A.及标准空白吸光值A:。
6.2.5.2.5将测定数值记入GB17378.4—1998附录表A4中,以吸光值(A.—A,)为纵坐标,和应的汞的量()为横坐标,绘制标准曲线。6.2.5.3样品测定
6.2.5.3.1滴加盐酸羟胺溶液(6.2.3.8)于样品制备液中,至红色完全消失,全量转入250ml.乘蒸气发生瓶中,用100IiL水分三次洗涤锥形瓶,洗涤波合并于求蒸气发生瓶中,6.2.5.3.2取两支10mL吸收管,各加入10mL吸收液(6.2.3.7),一支作空气净化管,一支作样品求蒸气吸收管。按曝气-吸收装置示意图将气路系统接好,空气净化吸收管不必每饮更换,提抽气系
1-…-气体流量计,2一括芯气体采样管,3一求蒸气发生瓶图5曦气-吸收装置图
6.2.5.3.3加2mI.氮化亚锡溶液(6.2.3.6)于汞蒸气发生瓶中,立即塞紧瓶塞。接通气泵,以1500mL/min空气漩速暖气15min。6.2.5.3.4取下聚蒸气吸收管,将吸收液移人25mL具塞比色管中,用10ml.水分三次洗涤吸收管,洗涤被准入比色管中。滴加盐殿羟胺溶液(6.2.3.8)至红色褪尽,冉多加2滴,充分振满,开益放置30 min.
6.2.5.3.5以下接6.2.5.2. 2~6.2.5.2.4步骤测定样品制备液的吸形值(A,2同时,按.上述步骤测定分折空自的吸光值A。6. 2.6记录与计算
称测得数据记人表A1中,按式(3)计算生物干样中总汞的含量:Wue=FM
式中:W一一生物下样中总汞的含量质量比,10-;654
GB17378.6-1998
m—从标准曲线上查得的乘的量,;F…一样品的下湿比;
M——样品称取基,g。
6-2.7精密度和准确度
五个实验室测定含乘的质量比为0.29×10-6的样品,重复性相对标准偏慈为0.95%。在0.5g猪肝成分分析标准物质(GBW08551)中加人2汞,平均回收率为95.9%。6.2.8注意事项
6.2.8.1样品消化时,过氧化氢需逐滴加入,以防过氧化愈剧烈分解,消化液溅溢,造成求损失。6.2.8.2样品测定步6.2.5.3.4中,开盖放置30min,是为消除反应产生的氟气及氮氧化物的影啊。
6.2.8.3样品测定步骤6.2.5.2.2中,水洗存机相是为了消除价锰的于扰。6.2.8.4玻器血均需用(1+3)硝酸溶液浸泡1天后洗净使用。7铜
7.1无火焰源子吸收分光光度法
7.1.1适用范围和应用领域
本法适用于海洋生物中的测定。检山限(W):0.4X10*。
7.1.2方法原理
生物样品经硝酸-过氧化氢消化,于波长324,7nm处直接进行石殿炉原子吸收分光光度测定。7.1.3试剂及其配制
除非另作说明、所用试剂均为分析纯,水为二次去离子水或等效纯水。7.1.3.1硝酸(HNO.>:P1.42&/ml优级纯,经石英亚沸蒸馏器蒸馏7.1.3.2过氟化氢(H0,)130%,7.1.3.3铜标准览备溶液:1.000mg/ml称取0.2000g金属铜粉(纯度99.99%)于50mL.烧杯中,加人5mL(1+2)硝酸溶液,加热溶解冷却后,全量转入200mL量瓶中,加水至标线,混匀。7.1.3.4标准中溶液:100/ml.
量取10.0ml.铜标准贮备溶液(7.1.3.3)于100mL基瓶中,加(1+99)硝酸溶液至标线,混勾。使用时配制。
7.1.3.5铜标准使用溶液:2.000μg/mL量取2.00mL铜标准中间溶液(7.1.3.4)于100ml量瓶中,加1十99)硝酸溶液至标线,混勺。使用时配制。
7.1.4、仪器及设备
石墨炉原子吸收分光光度计:配有自动进样装置-铜空心阴极灯+
氩气钢瓶:纯度99.99%:
一洁净工作台(洁净100级);
电热板。
7.1.5分析步骤
7.1.5.1样品消化
7.1.5.1.1准确称取0.1g(±0.001g)于样于50mL烧杯中,用几滴水湿润样品,加入2ml.硝酸(7.1.3.1),盖上表面血,于电热板上,低温加热至泡沫基本消尖。655
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。