GB/T 4789.12-2003
基本信息
标准号: GB/T 4789.12-2003
中文名称:食品卫生微生物学检验 肉毒梭菌及肉毒毒素检验
标准类别:国家标准(GB)
标准状态:现行
发布日期:2003-08-11
实施日期:2003-08-01
出版语种:简体中文
下载格式:.rar.pdf
下载大小:143953

标准分类号
标准ICS号:数学、自然科学>>微生物学>>07.100.30
中标分类号:医药、卫生、劳动保护>>卫生>>C53食品卫生
关联标准
替代情况:GB/T 4789.12-1994
出版信息
出版社:中国标准出版社
页数:6页
标准价格:8.0 元
出版日期:2003-08-01
相关单位信息
首发日期:1984-12-25
复审日期:2004-10-14
起草人:王成怀、冉陆、付萍、姚景会
起草单位:兰州生物制品所
提出单位:中华人民共和国卫生部
发布部门:中华人民共和国卫生部 中国国家标准化管理委员会
主管部门:卫生部
标准简介
本标准规定了肉毒梭菌及肉毒毒素的检验方法。本标准适用于各类食品和食物中毒样品中肉毒梭菌及肉毒毒素的检验。 GB/T 4789.12-2003 食品卫生微生物学检验 肉毒梭菌及肉毒毒素检验 GB/T4789.12-2003 标准下载解压密码:www.bzxz.net
标准图片预览




标准内容
ICS07.100.30
中华人民共和国国家标准
GB/T4789.12—2003
代替GB/T4789.12—1994
食品卫生微生物学检验
肉毒梭菌及肉毒毒素检验
Microbiological examination of foodhygiene-Examination of Clostridium botulinum and botulinus toxin2003-08-11发布
中华人民共和国卫生部
中宝国家标准化管理委员会
2004-01-01实施
GB/T4789.12—2003
本标准对GB/T4789.12—1994《食品卫生微生物学检验肉毒梭菌及肉毒毒素检验》进行修订。本标准与GB/T4789.12—1994相比主要修改如下:按照GB/T1.1一2000对标准文本格式和文字进行修改。一一修改并规范原标准中的“设备和材料”本标准自实施之日起,GB/T4789.12-1994同时废止。本标准由中华人民共和国卫生部提出并归口。本标准起草单位:卫生部兰州生物制品研究所、中国疾病预防控制中心营养与食品安全所。本标准主要起草人王成怀、冉陆、付萍、姚景会。本标准于1984年首次发布,1994年第一次修订,本次为第二次修订。84
1范围
食品卫生微生物学检验
肉毒梭菌及肉毒毒素检验
本标准规定了肉毒梭菌及肉毒毒素的检验方法。本标准适用于各类食品和食物中毒样品中肉毒梭菌及肉毒毒素的检验。2规范性引用文件
GB/T 4789.12-2003
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。GB/T4789.28—2003食品卫生微生物学检验染色法、培养基和试剂3设备和材料
3.1冰箱:0℃~4℃。
3.2恒温培养箱:30℃士1℃,35℃士1℃36℃±1℃。3.3离心机:3000r/min。
3.4显微镜:10×~100×。
3.5相差显微镜。
3.6均质器或灭菌乳钵。
3.7架盘药物天平:0g~500g,精确至0.5g。3.8厌氧培养装置:常温催化除氧式或碱性焦性没石子酸除氧式。3.9灭菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)。3.10灭菌平皿:直径90mm。
灭菌锥形瓶:500mL。
灭菌注射器:1mL。
3.13小白鼠:12g~15g。
4.培养基和试剂
4.1肉培养基:GB/T4789.28—2003中4.67。4.2卵黄琼脂培养基:GB/T4789.28—2003中4.68。4.3明胶磷酸盐缓冲液:GB/T4789.28—2003中3.23。4.4肉毒分型抗毒诊断血清。
4.5胰酶:活力1:250。
4.6革兰氏染色液:GB/T4789.28—2003中2.25检验程序
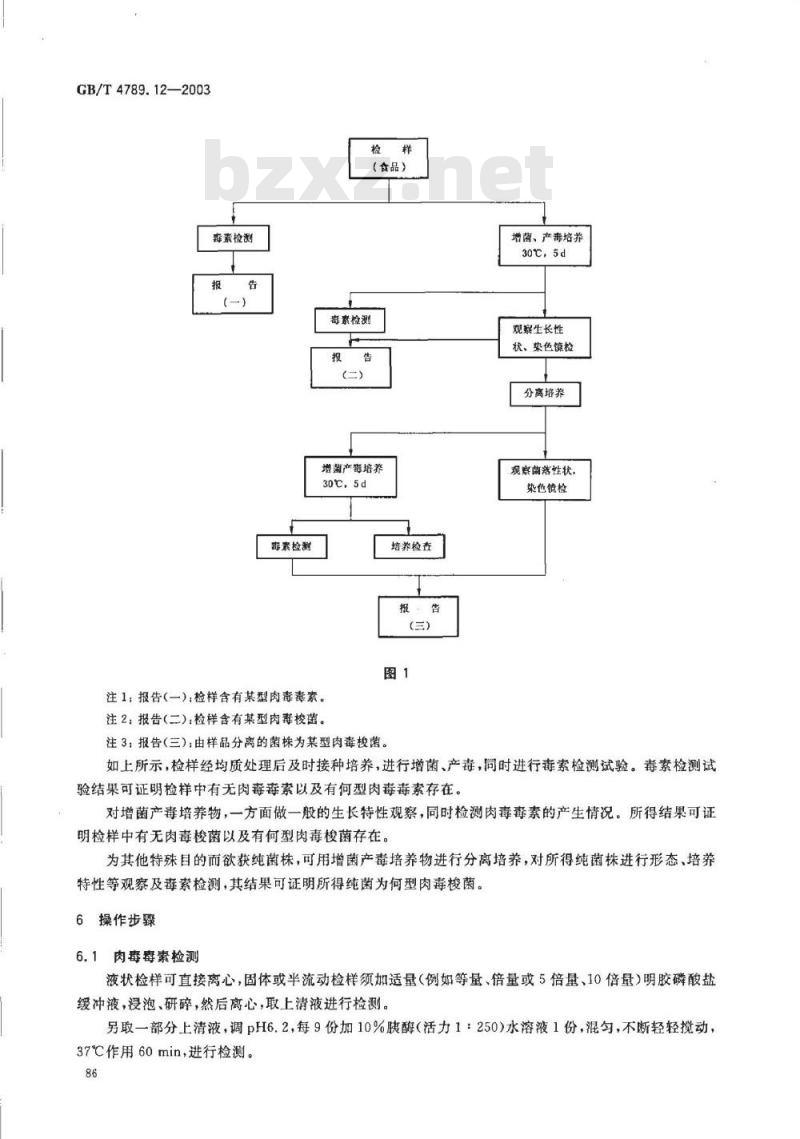
肉毒梭菌及肉毒毒素检验程序见图1。85
GB/T4789.12—2003
毒素检测
毒囊检测
(食品)
毒素检测
增菌产毒培养
30℃,5d
培养检查
注1:报告(一),检样含有某型肉毒毒素。注2:报告(二):检样含有某型肉毒梭菌。注3:报告(三):由样品分离的菌株为某型肉毒梭菌。增菌、产毒培养
30℃,5dbzxZ.net
观察生长性
状、染色镜检
分离培养
观察菌落性状,
染色镜检
如上所示,检样经均质处理后及时接种培养,进行增菌、产毒,同时进行毒素检测试验。毒素检测试验结果可证明检样中有无肉毒毒索以及有何型肉毒毒素存在。对增菌产毒培养物,一方面做一般的生长特性观察,同时检测肉毒毒素的产生情况。所得结果可证明检样中有无肉毒梭菌以及有何型肉毒梭菌存在。为其他特殊目的而欲获纯菌株,可用增菌产毒培养物进行分离培养,对所得纯菌株进行形态、培养特性等观察及毒素检测,其结果可证明所得纯菌为何型肉毒梭菌。操作步骤
6.1肉毒毒索检测
液状检样可直接离心,固体或半流动检样须加适量(例如等量、倍量或5倍量,10倍量)明胶磷酸盐缓冲液,浸泡、研碎,然后离心,取上清液进行检测。另取一部分上清液,调pH6.2,每9份加10%胰酶(活力1:250)水溶液1份,混匀,不断轻轻搅动,37℃作用60min,进行检测。
肉毒毒素检测以小白鼠腹腔注射法为标准方法,GB/T4789.12—2003
6.1.1检出试验:取上述离心上清液及其胰酶激活处理液分别注射小白鼠三只,每只0.5mL,观察4d。注射液中若有肉毒毒素存在,小白鼠一般多在注射后24h内发病、死亡。主要症状为竖毛、四肢瘫软,呼吸困难,呼吸皇风箱式,腰部凹陷,宛若蜂腰,最终死于呼吸麻痹。如遇小鼠猝死以至症状不明显时,则可将注射液做适当稀释,重做试验。6.1.2确证试验:不论上清液或其胰酶激活处理液,凡能致小鼠发病、死亡者,取样分成三份进行试验,一份加等量多型混合肉毒抗毒诊断血清,混匀,37℃作用30min,一份加等量明胶磷酸盐缓冲液,混匀,煮沸10min;一份加等量明胶磷酸盐缓冲液,混匀即可,不做其他处理。三份混合液分别注射小白鼠各两只,每只0.5mL,观察4d,若注射加诊断血清与煮沸加热的两份混合液的小白鼠均获保护存活,而唯有注射未经其他处理的混合液的小白鼠以特有的症状死亡,则可判定检样中的肉毒毒素存在,必要时要进行毒力测定及定型试验。
6.1.3毒力测定,取已判定含有肉毒毒素的检样离心上清液,用明胶磷酸盐缓冲液做成50倍、500倍及5000倍的稀释液,分别注射小白鼠各两只,每只0.5mL,观察4d。根据动物死亡情况,计算检样所含肉毒毒素的大体毒力(MLD/mL或MLD/g)。例如:5倍、50倍及500倍稀释致动物全部死亡,而注射5000倍稀释液的动物全部存活,则可大体判定检样上清液所含毒素的毒力为1000MLD/mL~10000MLD/mL
6.1.4定型试验:按毒力测定结果,用明胶磷酸盐缓冲液将检样上清液稀释至所含毒素的毒力大体在10MLD/mL~1000MLD/mL的范围,分别与各单型肉毒抗诊断血清等量混匀,37℃作用30min,各注射小鼠两只,每只0.5mL,观察4d。同时以明胶磷酸盐缓冲液代替诊断血清,与稀释毒素液等量混合作为对照。能保护动物免于发病、死亡的诊断血清型即为检样所含肉毒毒素的型别。注1:未经胰酶激活处理的检样的毒素检出试验或确证试验若为阳性结果,则践酶激活处理液可省略毒力测定及定型试验。
注2:为争取时间尽快得出结果,毒素检测的客项试验也可同时进行。注3:根据具体条件和可能性,定型试验可酌情先省略C、D、F及G型。注4:进行确证及定型等中和试验时,检样的稀释应参照所用肉毒诊断血清的效价,注5:试验动物的观察可按阳性结果的出现随时结束,以缩短观察时间;唯有出现阴性结果时,应保留充分的观察时间
6.2肉毒梭菌检出(增菌产毒培养试验)取肉培养基三支,煮沸10min~15min,做如下处理:a)第一支:急速冷却,接种检样均质液1mL~2mL;b)第二支:冷却至60℃,接种检样,继续于60℃保温10min,急速冷却;c)第三支:接种检样,继续煮沸加热10min,急速冷却。以上接种物于30℃培养5d,若无生长,可再培养10d。培养到期,若有生长,取培养液离心,以其上清液进行毒索检测试验,方法同6.1,阳性结果证明检样中有肉毒梭菌存在。6.3分离培养
选取经毒素检测试验证实含有肉毒梭菌的前述增菌产毒培养物(必要时可重复一次适宜的加热处理)接种卵黄琼脂平板,35℃厌氧培养48h。肉毒梭菌在卵黄琼脂平板上生长时,菌落及周围培养基表面覆盖着特有的虹彩样(或珍珠层样)薄层,但G型菌无此现象。根据菌落形态及菌体形态挑取可疑菌落,接种疱肉培养基,于30℃培养5d,进行毒素检测及培养特性检查确证试验。
6.3.1毒素检测:试验方法同6.1。87
GB/T4789.12—2003
6.3.2培养特性检查:接种卵黄琼脂平板,分成两份,分别在35℃的需氧和厌氧条件下培养48h,观察生长情况及菌落形态。肉毒梭菌只有在厌氧条件下才能在卵黄琼脂平板上生长并形成具有上述特征的菌落,而在需氧条件下则不生长。注:为检出蜂蜜中存在的肉毒梭菌,蜂蜜检样需预温37℃(流质蜂蜜),或52℃~53℃(晶质蜂蜜),充分搅拌后立即称取20g,溶于100mL灭菌蒸馏水(37℃或52℃~53℃),搅拌稀释,以8000r/min~10000r/min,离心30min(20℃),沉淀,加灭菌蒸馏水1mL,充分摇匀,等分各半,接种府肉培养基(8mL~10mL)各一支,分别在30℃及37℃下厌氧培养7d,按6.2进行肉毒毒索检测。88
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
中华人民共和国国家标准
GB/T4789.12—2003
代替GB/T4789.12—1994
食品卫生微生物学检验
肉毒梭菌及肉毒毒素检验
Microbiological examination of foodhygiene-Examination of Clostridium botulinum and botulinus toxin2003-08-11发布
中华人民共和国卫生部
中宝国家标准化管理委员会
2004-01-01实施
GB/T4789.12—2003
本标准对GB/T4789.12—1994《食品卫生微生物学检验肉毒梭菌及肉毒毒素检验》进行修订。本标准与GB/T4789.12—1994相比主要修改如下:按照GB/T1.1一2000对标准文本格式和文字进行修改。一一修改并规范原标准中的“设备和材料”本标准自实施之日起,GB/T4789.12-1994同时废止。本标准由中华人民共和国卫生部提出并归口。本标准起草单位:卫生部兰州生物制品研究所、中国疾病预防控制中心营养与食品安全所。本标准主要起草人王成怀、冉陆、付萍、姚景会。本标准于1984年首次发布,1994年第一次修订,本次为第二次修订。84
1范围
食品卫生微生物学检验
肉毒梭菌及肉毒毒素检验
本标准规定了肉毒梭菌及肉毒毒素的检验方法。本标准适用于各类食品和食物中毒样品中肉毒梭菌及肉毒毒素的检验。2规范性引用文件
GB/T 4789.12-2003
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。GB/T4789.28—2003食品卫生微生物学检验染色法、培养基和试剂3设备和材料
3.1冰箱:0℃~4℃。
3.2恒温培养箱:30℃士1℃,35℃士1℃36℃±1℃。3.3离心机:3000r/min。
3.4显微镜:10×~100×。
3.5相差显微镜。
3.6均质器或灭菌乳钵。
3.7架盘药物天平:0g~500g,精确至0.5g。3.8厌氧培养装置:常温催化除氧式或碱性焦性没石子酸除氧式。3.9灭菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)。3.10灭菌平皿:直径90mm。
灭菌锥形瓶:500mL。
灭菌注射器:1mL。
3.13小白鼠:12g~15g。
4.培养基和试剂
4.1肉培养基:GB/T4789.28—2003中4.67。4.2卵黄琼脂培养基:GB/T4789.28—2003中4.68。4.3明胶磷酸盐缓冲液:GB/T4789.28—2003中3.23。4.4肉毒分型抗毒诊断血清。
4.5胰酶:活力1:250。
4.6革兰氏染色液:GB/T4789.28—2003中2.25检验程序
肉毒梭菌及肉毒毒素检验程序见图1。85
GB/T4789.12—2003
毒素检测
毒囊检测
(食品)
毒素检测
增菌产毒培养
30℃,5d
培养检查
注1:报告(一),检样含有某型肉毒毒素。注2:报告(二):检样含有某型肉毒梭菌。注3:报告(三):由样品分离的菌株为某型肉毒梭菌。增菌、产毒培养
30℃,5dbzxZ.net
观察生长性
状、染色镜检
分离培养
观察菌落性状,
染色镜检
如上所示,检样经均质处理后及时接种培养,进行增菌、产毒,同时进行毒素检测试验。毒素检测试验结果可证明检样中有无肉毒毒索以及有何型肉毒毒素存在。对增菌产毒培养物,一方面做一般的生长特性观察,同时检测肉毒毒素的产生情况。所得结果可证明检样中有无肉毒梭菌以及有何型肉毒梭菌存在。为其他特殊目的而欲获纯菌株,可用增菌产毒培养物进行分离培养,对所得纯菌株进行形态、培养特性等观察及毒素检测,其结果可证明所得纯菌为何型肉毒梭菌。操作步骤
6.1肉毒毒索检测
液状检样可直接离心,固体或半流动检样须加适量(例如等量、倍量或5倍量,10倍量)明胶磷酸盐缓冲液,浸泡、研碎,然后离心,取上清液进行检测。另取一部分上清液,调pH6.2,每9份加10%胰酶(活力1:250)水溶液1份,混匀,不断轻轻搅动,37℃作用60min,进行检测。
肉毒毒素检测以小白鼠腹腔注射法为标准方法,GB/T4789.12—2003
6.1.1检出试验:取上述离心上清液及其胰酶激活处理液分别注射小白鼠三只,每只0.5mL,观察4d。注射液中若有肉毒毒素存在,小白鼠一般多在注射后24h内发病、死亡。主要症状为竖毛、四肢瘫软,呼吸困难,呼吸皇风箱式,腰部凹陷,宛若蜂腰,最终死于呼吸麻痹。如遇小鼠猝死以至症状不明显时,则可将注射液做适当稀释,重做试验。6.1.2确证试验:不论上清液或其胰酶激活处理液,凡能致小鼠发病、死亡者,取样分成三份进行试验,一份加等量多型混合肉毒抗毒诊断血清,混匀,37℃作用30min,一份加等量明胶磷酸盐缓冲液,混匀,煮沸10min;一份加等量明胶磷酸盐缓冲液,混匀即可,不做其他处理。三份混合液分别注射小白鼠各两只,每只0.5mL,观察4d,若注射加诊断血清与煮沸加热的两份混合液的小白鼠均获保护存活,而唯有注射未经其他处理的混合液的小白鼠以特有的症状死亡,则可判定检样中的肉毒毒素存在,必要时要进行毒力测定及定型试验。
6.1.3毒力测定,取已判定含有肉毒毒素的检样离心上清液,用明胶磷酸盐缓冲液做成50倍、500倍及5000倍的稀释液,分别注射小白鼠各两只,每只0.5mL,观察4d。根据动物死亡情况,计算检样所含肉毒毒素的大体毒力(MLD/mL或MLD/g)。例如:5倍、50倍及500倍稀释致动物全部死亡,而注射5000倍稀释液的动物全部存活,则可大体判定检样上清液所含毒素的毒力为1000MLD/mL~10000MLD/mL
6.1.4定型试验:按毒力测定结果,用明胶磷酸盐缓冲液将检样上清液稀释至所含毒素的毒力大体在10MLD/mL~1000MLD/mL的范围,分别与各单型肉毒抗诊断血清等量混匀,37℃作用30min,各注射小鼠两只,每只0.5mL,观察4d。同时以明胶磷酸盐缓冲液代替诊断血清,与稀释毒素液等量混合作为对照。能保护动物免于发病、死亡的诊断血清型即为检样所含肉毒毒素的型别。注1:未经胰酶激活处理的检样的毒素检出试验或确证试验若为阳性结果,则践酶激活处理液可省略毒力测定及定型试验。
注2:为争取时间尽快得出结果,毒素检测的客项试验也可同时进行。注3:根据具体条件和可能性,定型试验可酌情先省略C、D、F及G型。注4:进行确证及定型等中和试验时,检样的稀释应参照所用肉毒诊断血清的效价,注5:试验动物的观察可按阳性结果的出现随时结束,以缩短观察时间;唯有出现阴性结果时,应保留充分的观察时间
6.2肉毒梭菌检出(增菌产毒培养试验)取肉培养基三支,煮沸10min~15min,做如下处理:a)第一支:急速冷却,接种检样均质液1mL~2mL;b)第二支:冷却至60℃,接种检样,继续于60℃保温10min,急速冷却;c)第三支:接种检样,继续煮沸加热10min,急速冷却。以上接种物于30℃培养5d,若无生长,可再培养10d。培养到期,若有生长,取培养液离心,以其上清液进行毒索检测试验,方法同6.1,阳性结果证明检样中有肉毒梭菌存在。6.3分离培养
选取经毒素检测试验证实含有肉毒梭菌的前述增菌产毒培养物(必要时可重复一次适宜的加热处理)接种卵黄琼脂平板,35℃厌氧培养48h。肉毒梭菌在卵黄琼脂平板上生长时,菌落及周围培养基表面覆盖着特有的虹彩样(或珍珠层样)薄层,但G型菌无此现象。根据菌落形态及菌体形态挑取可疑菌落,接种疱肉培养基,于30℃培养5d,进行毒素检测及培养特性检查确证试验。
6.3.1毒素检测:试验方法同6.1。87
GB/T4789.12—2003
6.3.2培养特性检查:接种卵黄琼脂平板,分成两份,分别在35℃的需氧和厌氧条件下培养48h,观察生长情况及菌落形态。肉毒梭菌只有在厌氧条件下才能在卵黄琼脂平板上生长并形成具有上述特征的菌落,而在需氧条件下则不生长。注:为检出蜂蜜中存在的肉毒梭菌,蜂蜜检样需预温37℃(流质蜂蜜),或52℃~53℃(晶质蜂蜜),充分搅拌后立即称取20g,溶于100mL灭菌蒸馏水(37℃或52℃~53℃),搅拌稀释,以8000r/min~10000r/min,离心30min(20℃),沉淀,加灭菌蒸馏水1mL,充分摇匀,等分各半,接种府肉培养基(8mL~10mL)各一支,分别在30℃及37℃下厌氧培养7d,按6.2进行肉毒毒索检测。88
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。