GB/T 5413.16-1997
基本信息
标准号: GB/T 5413.16-1997
中文名称:婴幼儿配方食品和乳粉 叶酸(叶酸盐活性)的测定
标准类别:国家标准(GB)
英文名称: Determination of folic acid (folate activity) in infant formula and milk powder
标准状态:现行
发布日期:1997-05-28
实施日期:1998-09-01
出版语种:简体中文
下载格式:.rar.pdf
下载大小:163314

标准分类号
标准ICS号:食品技术>>奶和奶制品>>67.100.10奶及加工奶产品
中标分类号:食品>>特种食品>>X82儿童食品
出版信息
出版社:中国标准出版社
页数:5页
标准价格:8.0 元
相关单位信息
首发日期:1985-09-28
复审日期:2004-10-14
起草单位:国家乳制品质量监督检验中心
发布部门:国家技术监督局
主管部门:国家标准化管理委员会
标准简介
本标准规定了用微生物法测定叶酸(叶酸盐活性)的方法。本标准适用于婴幼儿配方食品和乳粉中叶酸(叶酸盐活性)的测定。 GB/T 5413.16-1997 婴幼儿配方食品和乳粉 叶酸(叶酸盐活性)的测定 GB/T5413.16-1997 标准下载解压密码:www.bzxz.net
标准图片预览




标准内容
GB/T5413.16-1997
本标准等效采用美国公职分析化学师协会(AOAC)方法。本系列标推从实施之日起,代替GB5413—85。本标准由中国轻工总会提出。
本标准由全国乳品标推化中心归口。本标准负责起草单位:国家乳制品质量监督检验中心。本标准参加起草单位:卫生部食品卫生监督检验所、浙江省轻工业研究所、哈尔滨森永乳品有限公司、雀巢(中国)投资服务有限公司。本标准主要起草人:殷晓红、王芸、杨金宝、张玉杰。287
中华人民共和国国家标准
婴幼儿配方食品和乳粉
叶酸(叶酸盐活性)的测定
Milk powder and formula foods for infant and young children--Determinatfon of folic acid (folate activity)1范围
本标准规定了用微生物法测定叶酸(叶酸盐活性)的方法。本标准适用于婴幼儿配方食品和乳粉中叶酸(叶酸盐活性)的测定。2方法原理
叶酸盐的活性通过干酪乳杆菌(Lactobacillus casei)的生长情况来评价。3试剂、菌种和培养基
GB/T 5413.16—1997
代替GB5413—85
所有试剂,如未注明规格,均指分析纯;所有实验用水,如未注明其他要求,均指三级水。3.1鸡胰腺:称取100mg干燥的鸡胰腺,20mL.蒸馏水,搅拌15min,离心10min(3000r/min),取上清液用。现用现配。
3.2生理盐水:称0.9g氟化钠(分析纯)于100mL容量瓶中,稀释至刻度,振荡溶解。分装10mL到每个培养管中,盖上盖,121℃灭菌20min,每周准备一次。3.3磷酸缓冲液:c(H,PO,)为0.05mol/L,含有抗坏血酸。溶解50mg抗坏血酸于100mL0.05mol/L磷酸缓冲液中,现用现配。
3.4叶酸,标准品。
3.5浓氨水。
3.6甲苯。
3.7菌种:干酪乳杆菌(Lactobacillus casei)。3.8培养基。
3.8.1乳酸杆菌琼脂培养基:陈化乳15g,酵母漫裔5g,葡萄糖10g,番茄汁100mL,磷酸二氢钾2g,聚山梨糖单油酸酯1g,琼脂10g,加蒸馏水至1000mL,pH6.8士0.2(25℃)。3.8.2乳酸杆菌肉汤培养基:陈化乳15g,酵母浸膏5g,葡萄糖10g,番茄汁100mL,磷酸二氢钾2g,聚山梨糖单油酸酯1g,加蒸馏水至100mL,pH6.8土0.2(25℃)。3. 8. 3 叶酸测定用培养基:酪蛋白陈 10g,葡萄糖 40g,乙酸钠 40g,磷酸氢二钾 1g,磷酸二氢钾 1g,DL色氨酸0.2g,L-天门冬氨酸0.6g,L-半胱氨酸盐酸盐0.5g,硫酸腺嘌呤10mg,盐酸鸟嘌呤10mg,尿嘧啶10mg,黄嘌呤20mg,聚山梨糖0.1g,谷光甘肽5mg,硫酸镁0.4g,氟化钠20mg,硫酸亚铁20mg,硫酸锰 15mg,核黄素 1mg,p-氨基苯甲酸 2mg,维生素 B.4mg,盐酸硫胺素 400μg,泛酸钙 800μg,烟酸800μg,生物素20μg,加蒸馏水至1000mL,pH6.7士0.1(25℃)。3.9氢氧化钠溶液:c(NaOH)为0.1mol/L。国家技术监督局1997-05-28批准288
1998-09-01实施
4仪器
常用实验室仪器及:
4.1培养箱。
4.2灭菌釜。
4.3培养管和帽。
4.4试管振荡架。
4.5接种针和接种环。
4.6 pH计。
4.7离心机。
5制备
5.1菌种的制备
GB/T 5413.16—1997
5.1. 1将纯菌种植物乳杆菌(Lactobacillus casei)从菌种培养基上接种到三个转接培养基试管中,37℃培养24h,每月接种一次,标好,贮于冰箱中。再以每月接种的培养管(4.3)的一支中再接种1支转接培养基,37℃培养24h,每周做一次这样的转接,每周从接种管中接种4~5支转接培养基接种管,37℃培养24h,标好,作为每日测定用。每月月初从月接种管中重新接种3个转接管保存新菌种。5.1.2从日接种管中接种一管于菌种培养基中,37℃培养24h。在无菌条件下离心该培养液10min(2000r/min),倾去上清液,再用10mL生理盐水(3.2)将细菌细胞清洗,再离心10min(2000r/min),倾去上清液,再用另外的10mL生理盐水(3.2)清洗。如前面一样离心,弃去上清液,再加10mL生理盐水(3.2)。吸1mL该菌悬液于10mL生理盐水(3.2)中,混合均匀。5.2标准溶液的制备
5.2.1标准贮备液,叶酸的浓度500μg/mL。精确称取55~~56mg叶酸标准品(3.4),用50mL蒸馏水定量地转入100mL容量瓶中,加2mL氨水(3.5)。溶液制备后,计算溶液的体积,要求贮备液中叶酸盐的浓度为500μg/mL:贮备液体积(mL)=㎡×,1000×c
100×500
或简化为:
贮备液体积(mL)
式中:m标样的质量,mg;
c——标样的纯度,这/100g。
用蒸馏水稀释溶液至刻度,用吸管加蒸馏水到所要求的计算得到的体积,充分混合,放入红色或棕色瓶子中,于冰箱。保存期为4个月。5.2.2标准中间液,叶酸的浓度50μg/mL。精确吸取10mL标准贮备液(5.2.1)液于100mL棕色或红色容量瓶中,用蒸馏水稀至刻度,充分混合,贮于冰箱中,保存期1个月。5.2.3标准工作液,叶酸的浓度0.1ng/mL。吸取1mL标准中间液(5.2.2)于100mL棕色容量瓶中,用蒸馏水定容至刻度,混合。再吸该液1mL于100mL棕色容量瓶中,定容,混合。再从上液中吸5mL于250mL棕色容量瓶中,用0.05mol/L磷酸缓冲液定容到刻度,混合,即为标289
精确称取定量的样品(样品中约含有5μg叶酸)于100mL烧杯中,用25~30mL水复原样品,定吸1mL稀释样品和1mL鸡胰腺(3.1)于一个18mm×150mm的带螺旋盖的培养试管中,充分混合。加18mL0.05mol/L含抗坏血酸的磷酸缓冲液(3.3),再加1mL甲苯(3.5)。作一个空白对照管,吸于37℃C培辨样品管和空白管16h,再于121℃灭菌10min,之后离心,用0.05mol/L磷酸缓冲液稀1mL蒸馏水和1mL鸡胰腺于空白管中,也加0.05mol/L缓冲液(3.3)18mL及1mL甲苯(3.5)。10
吸取定量的样品,大约含5μg的叶酸于100mL容量瓶中,用水定容至刻度,接6.1.3。5
直接灭菌所有的试管,制冷到培养温度或迅速放入循环水浴内,以使颜色形成最浅。保证加热和制1www.bzxz.net
无菌的接种每个管,均加入一滴适当的接种物。除标准管No.7以外。盖上盖,充分振荡混合所有4
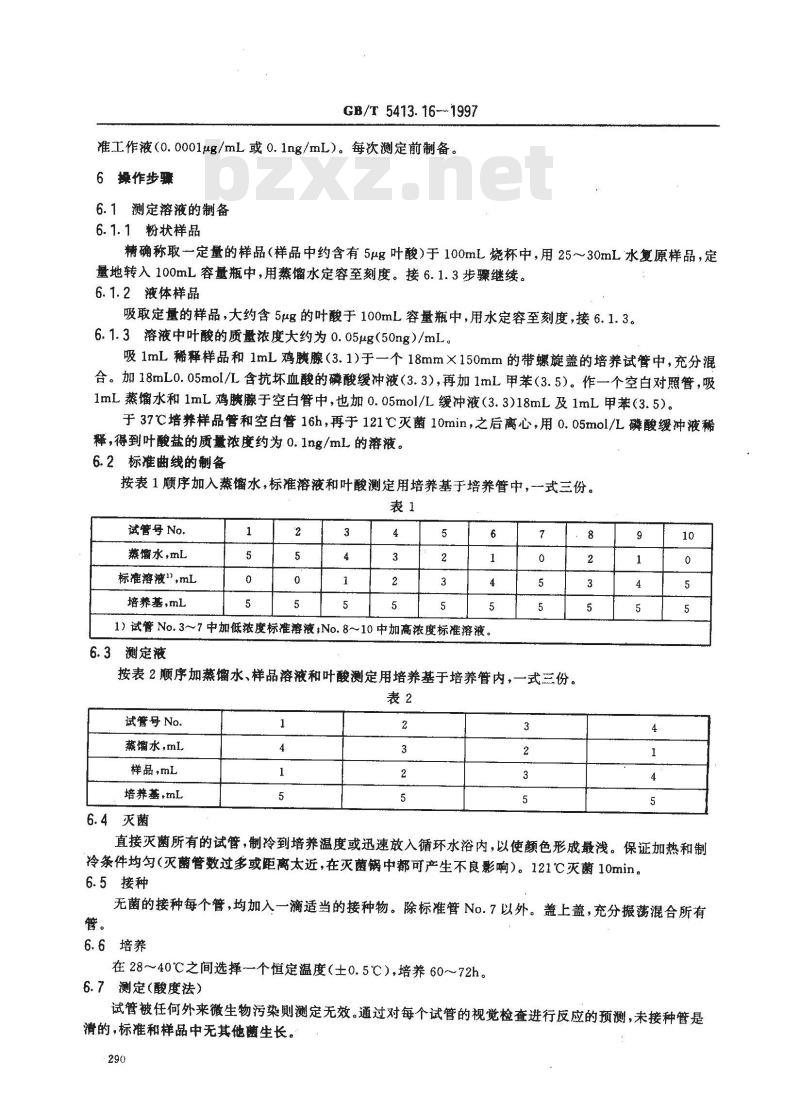
按表1顺序加入蒸馏水,标溶液和叶酸测定用培养基于培养管中,一式三份。5
试管被任何外来微生物污染则测定无效。通过对每个试管的视觉检查进行反应的预测,未接种管是2
量地转入100mL容量瓶中,用蒸馏水定容至刻度。接6.1.3步骤继续。5
GB/T 5413. 16-1997
冷条件均匀(灭菌管数过多或距离太近,在灭菌锅中都可产生不良影响)。121℃灭菌10min。7
按表2顺序加蒸馏水、样品溶液和叶酸测定用培养基于培养管内,一式三份。准工作液(0.0001ug/mL或0.1ng/mL)。每次测定前制备。0
6.1.3溶液中叶酸的质量浓度大约为0.05μg(50ng)/mL。3
1)试管 No.3~7中加低浓度标准溶液;No. 8~10中加高浓度标准溶液5
释,得到叶酸盐的质量浓度约为.0.1ng/mL的溶液。4
在28~~40℃之间选择一个恒定温度(±0.5℃),培养60~72h。5
6.1测定溶液的制备
6.1.1粉状样品
6.1.2液体样品
6操作步骤
6.2标准曲线的制备
标准溶液\,mL
试管号 No.
清的,标准和样品中无其他生长。蒸馏水,mL
培养基,mL
6.3测定液
试管号No.
蒸馏水,mL
样品,mL
培养基,mL
6.4灭菌
6.5接种
6.6培养
6.7测定(酸度法)
6.7.1滴定
GB/T5413.16—1997
用溴麝香草酚蓝作指示剂,用0.1mol/L氢氧化钠(3.9)滴定每个管中溶液,或以pH6.8作为电位滴定终点。如果接种空白滴定反应等于或高于未接种空白水平的1.5mL,则测定结果应忽略不计。通常标准溶液在5.0mL的反应等于0.1mol/L氢氧化钠8~12mL的滴定度。6.7.2测pH值
在培养之后读出管内容物的pH值,近似至0.01pH值单位。6.8计算
对于每个标准溶液作出一个浓度反应曲线(酸度,pH值,透射率或吸收值),每个管中分别含有相对应的参考标准含量。
对每个水平的检验溶液进行维生素的定量测定,废弃任何低于0.5mL标准溶液的吸收值或高于4.5mL标准溶液的吸收值。
对每个水平的检验溶液,计算其每毫升中的维生素含量。计算所得值的平均数,每个管的测得值不得超过该平均值的士15%。如果所得到的管数少于所测定的四种水乎的稀释液的管数的2/3,用于计算样品浓度的数据就是不充分的。如果剩余管数是原来管数的2/3或更多,则可根据平均值计算其样品中的含量。
7分析结果的表述
样品中叶酸含量(mg/100g或100mL)=[(X× D)EB}×式中:X—不同水平检验溶液其每毫升中的叶酸含量值,ng;D—1mL样品在经过酶处理后的稀释度;EB—酶处理液空白管中叶酸含量值,ng/mL;m
8允许差
最初称(吸)取样品的质量,g(或mL)。同一样品的两次测定值之差不得超过两次测定平均值的10%。100
(2)
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
本标准等效采用美国公职分析化学师协会(AOAC)方法。本系列标推从实施之日起,代替GB5413—85。本标准由中国轻工总会提出。
本标准由全国乳品标推化中心归口。本标准负责起草单位:国家乳制品质量监督检验中心。本标准参加起草单位:卫生部食品卫生监督检验所、浙江省轻工业研究所、哈尔滨森永乳品有限公司、雀巢(中国)投资服务有限公司。本标准主要起草人:殷晓红、王芸、杨金宝、张玉杰。287
中华人民共和国国家标准
婴幼儿配方食品和乳粉
叶酸(叶酸盐活性)的测定
Milk powder and formula foods for infant and young children--Determinatfon of folic acid (folate activity)1范围
本标准规定了用微生物法测定叶酸(叶酸盐活性)的方法。本标准适用于婴幼儿配方食品和乳粉中叶酸(叶酸盐活性)的测定。2方法原理
叶酸盐的活性通过干酪乳杆菌(Lactobacillus casei)的生长情况来评价。3试剂、菌种和培养基
GB/T 5413.16—1997
代替GB5413—85
所有试剂,如未注明规格,均指分析纯;所有实验用水,如未注明其他要求,均指三级水。3.1鸡胰腺:称取100mg干燥的鸡胰腺,20mL.蒸馏水,搅拌15min,离心10min(3000r/min),取上清液用。现用现配。
3.2生理盐水:称0.9g氟化钠(分析纯)于100mL容量瓶中,稀释至刻度,振荡溶解。分装10mL到每个培养管中,盖上盖,121℃灭菌20min,每周准备一次。3.3磷酸缓冲液:c(H,PO,)为0.05mol/L,含有抗坏血酸。溶解50mg抗坏血酸于100mL0.05mol/L磷酸缓冲液中,现用现配。
3.4叶酸,标准品。
3.5浓氨水。
3.6甲苯。
3.7菌种:干酪乳杆菌(Lactobacillus casei)。3.8培养基。
3.8.1乳酸杆菌琼脂培养基:陈化乳15g,酵母漫裔5g,葡萄糖10g,番茄汁100mL,磷酸二氢钾2g,聚山梨糖单油酸酯1g,琼脂10g,加蒸馏水至1000mL,pH6.8士0.2(25℃)。3.8.2乳酸杆菌肉汤培养基:陈化乳15g,酵母浸膏5g,葡萄糖10g,番茄汁100mL,磷酸二氢钾2g,聚山梨糖单油酸酯1g,加蒸馏水至100mL,pH6.8土0.2(25℃)。3. 8. 3 叶酸测定用培养基:酪蛋白陈 10g,葡萄糖 40g,乙酸钠 40g,磷酸氢二钾 1g,磷酸二氢钾 1g,DL色氨酸0.2g,L-天门冬氨酸0.6g,L-半胱氨酸盐酸盐0.5g,硫酸腺嘌呤10mg,盐酸鸟嘌呤10mg,尿嘧啶10mg,黄嘌呤20mg,聚山梨糖0.1g,谷光甘肽5mg,硫酸镁0.4g,氟化钠20mg,硫酸亚铁20mg,硫酸锰 15mg,核黄素 1mg,p-氨基苯甲酸 2mg,维生素 B.4mg,盐酸硫胺素 400μg,泛酸钙 800μg,烟酸800μg,生物素20μg,加蒸馏水至1000mL,pH6.7士0.1(25℃)。3.9氢氧化钠溶液:c(NaOH)为0.1mol/L。国家技术监督局1997-05-28批准288
1998-09-01实施
4仪器
常用实验室仪器及:
4.1培养箱。
4.2灭菌釜。
4.3培养管和帽。
4.4试管振荡架。
4.5接种针和接种环。
4.6 pH计。
4.7离心机。
5制备
5.1菌种的制备
GB/T 5413.16—1997
5.1. 1将纯菌种植物乳杆菌(Lactobacillus casei)从菌种培养基上接种到三个转接培养基试管中,37℃培养24h,每月接种一次,标好,贮于冰箱中。再以每月接种的培养管(4.3)的一支中再接种1支转接培养基,37℃培养24h,每周做一次这样的转接,每周从接种管中接种4~5支转接培养基接种管,37℃培养24h,标好,作为每日测定用。每月月初从月接种管中重新接种3个转接管保存新菌种。5.1.2从日接种管中接种一管于菌种培养基中,37℃培养24h。在无菌条件下离心该培养液10min(2000r/min),倾去上清液,再用10mL生理盐水(3.2)将细菌细胞清洗,再离心10min(2000r/min),倾去上清液,再用另外的10mL生理盐水(3.2)清洗。如前面一样离心,弃去上清液,再加10mL生理盐水(3.2)。吸1mL该菌悬液于10mL生理盐水(3.2)中,混合均匀。5.2标准溶液的制备
5.2.1标准贮备液,叶酸的浓度500μg/mL。精确称取55~~56mg叶酸标准品(3.4),用50mL蒸馏水定量地转入100mL容量瓶中,加2mL氨水(3.5)。溶液制备后,计算溶液的体积,要求贮备液中叶酸盐的浓度为500μg/mL:贮备液体积(mL)=㎡×,1000×c
100×500
或简化为:
贮备液体积(mL)
式中:m标样的质量,mg;
c——标样的纯度,这/100g。
用蒸馏水稀释溶液至刻度,用吸管加蒸馏水到所要求的计算得到的体积,充分混合,放入红色或棕色瓶子中,于冰箱。保存期为4个月。5.2.2标准中间液,叶酸的浓度50μg/mL。精确吸取10mL标准贮备液(5.2.1)液于100mL棕色或红色容量瓶中,用蒸馏水稀至刻度,充分混合,贮于冰箱中,保存期1个月。5.2.3标准工作液,叶酸的浓度0.1ng/mL。吸取1mL标准中间液(5.2.2)于100mL棕色容量瓶中,用蒸馏水定容至刻度,混合。再吸该液1mL于100mL棕色容量瓶中,定容,混合。再从上液中吸5mL于250mL棕色容量瓶中,用0.05mol/L磷酸缓冲液定容到刻度,混合,即为标289
精确称取定量的样品(样品中约含有5μg叶酸)于100mL烧杯中,用25~30mL水复原样品,定吸1mL稀释样品和1mL鸡胰腺(3.1)于一个18mm×150mm的带螺旋盖的培养试管中,充分混合。加18mL0.05mol/L含抗坏血酸的磷酸缓冲液(3.3),再加1mL甲苯(3.5)。作一个空白对照管,吸于37℃C培辨样品管和空白管16h,再于121℃灭菌10min,之后离心,用0.05mol/L磷酸缓冲液稀1mL蒸馏水和1mL鸡胰腺于空白管中,也加0.05mol/L缓冲液(3.3)18mL及1mL甲苯(3.5)。10
吸取定量的样品,大约含5μg的叶酸于100mL容量瓶中,用水定容至刻度,接6.1.3。5
直接灭菌所有的试管,制冷到培养温度或迅速放入循环水浴内,以使颜色形成最浅。保证加热和制1www.bzxz.net
无菌的接种每个管,均加入一滴适当的接种物。除标准管No.7以外。盖上盖,充分振荡混合所有4
按表1顺序加入蒸馏水,标溶液和叶酸测定用培养基于培养管中,一式三份。5
试管被任何外来微生物污染则测定无效。通过对每个试管的视觉检查进行反应的预测,未接种管是2
量地转入100mL容量瓶中,用蒸馏水定容至刻度。接6.1.3步骤继续。5
GB/T 5413. 16-1997
冷条件均匀(灭菌管数过多或距离太近,在灭菌锅中都可产生不良影响)。121℃灭菌10min。7
按表2顺序加蒸馏水、样品溶液和叶酸测定用培养基于培养管内,一式三份。准工作液(0.0001ug/mL或0.1ng/mL)。每次测定前制备。0
6.1.3溶液中叶酸的质量浓度大约为0.05μg(50ng)/mL。3
1)试管 No.3~7中加低浓度标准溶液;No. 8~10中加高浓度标准溶液5
释,得到叶酸盐的质量浓度约为.0.1ng/mL的溶液。4
在28~~40℃之间选择一个恒定温度(±0.5℃),培养60~72h。5
6.1测定溶液的制备
6.1.1粉状样品
6.1.2液体样品
6操作步骤
6.2标准曲线的制备
标准溶液\,mL
试管号 No.
清的,标准和样品中无其他生长。蒸馏水,mL
培养基,mL
6.3测定液
试管号No.
蒸馏水,mL
样品,mL
培养基,mL
6.4灭菌
6.5接种
6.6培养
6.7测定(酸度法)
6.7.1滴定
GB/T5413.16—1997
用溴麝香草酚蓝作指示剂,用0.1mol/L氢氧化钠(3.9)滴定每个管中溶液,或以pH6.8作为电位滴定终点。如果接种空白滴定反应等于或高于未接种空白水平的1.5mL,则测定结果应忽略不计。通常标准溶液在5.0mL的反应等于0.1mol/L氢氧化钠8~12mL的滴定度。6.7.2测pH值
在培养之后读出管内容物的pH值,近似至0.01pH值单位。6.8计算
对于每个标准溶液作出一个浓度反应曲线(酸度,pH值,透射率或吸收值),每个管中分别含有相对应的参考标准含量。
对每个水平的检验溶液进行维生素的定量测定,废弃任何低于0.5mL标准溶液的吸收值或高于4.5mL标准溶液的吸收值。
对每个水平的检验溶液,计算其每毫升中的维生素含量。计算所得值的平均数,每个管的测得值不得超过该平均值的士15%。如果所得到的管数少于所测定的四种水乎的稀释液的管数的2/3,用于计算样品浓度的数据就是不充分的。如果剩余管数是原来管数的2/3或更多,则可根据平均值计算其样品中的含量。
7分析结果的表述
样品中叶酸含量(mg/100g或100mL)=[(X× D)EB}×式中:X—不同水平检验溶液其每毫升中的叶酸含量值,ng;D—1mL样品在经过酶处理后的稀释度;EB—酶处理液空白管中叶酸含量值,ng/mL;m
8允许差
最初称(吸)取样品的质量,g(或mL)。同一样品的两次测定值之差不得超过两次测定平均值的10%。100
(2)
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。