GB/T 17999.2-1999
基本信息
标准号: GB/T 17999.2-1999
中文名称:SPF 鸡 血清中和试验
标准类别:国家标准(GB)
标准状态:已作废
发布日期:1999-11-10
实施日期:2000-04-01
作废日期:2009-05-01
出版语种:简体中文
下载格式:.rar.pdf
下载大小:115432

标准分类号
标准ICS号:农业>>农业和林业>>65.020.30动物饲养和繁殖
中标分类号:农业、林业>>畜牧>>B41动物检疫、兽医与疫病防治
关联标准
替代情况:被GB/T 17999.3-2008代替
出版信息
出版社:中国标准出版社
页数:平装16开, 页数:4, 字数:8千字
标准价格:8.0 元
出版日期:2000-04-01
相关单位信息
首发日期:1999-11-10
复审日期:2004-10-14
起草人:赵立红、陈德威、张秀美、秦卓明
起草单位:农业部实验动物研究中心、山东省农科院家禽研究所
归口单位:农业部畜牧兽医司
提出单位:中华人民共和国农业部、国家科学技术部
发布部门:国家质量技术监督局
主管部门:农业部
标准简介
本标准规定了血清中和试验所用试剂、材料,操作程序及结果判定等。本标准适用于SPF鸡感染以下病毒后的中和抗体的监测:禽脑脊髓炎病毒(Avian Encephalomyelitis Virus)、传染传支气管炎病毒(Infectious Bronchitis Virus)、传染性喉气管炎病毒(Infectious Laryngotracheitis Virus)、传染性法氏囊病病毒(Infectious Bursal Disease Virus)。 GB/T 17999.2-1999 SPF 鸡 血清中和试验 GB/T17999.2-1999 标准下载解压密码:www.bzxz.net
标准图片预览


标准内容
GB/T 17999.2.-. 1999
本标准参照美国SPAFAS公司的血清中和试验(SN)操作规程编制而成。SPF鸡微生物学质量控制国家系列标准,包括SPF鸡微生物学监测总则和9种SPF鸡微生物学检测方法。本标准为《SPF鸡血清中和试验》。SPF鸡微生物学检测方法还包括以下部分:GB/T17999.1-1999SPF鸡
红细胞凝集抑制试验;
GB/T17999.3 1999SPF鸡
GB/T 17999. 4 --1999
GB/T 17999.5- 1999
GB/T 17999. 6-1999
SPF鸡
血清平板凝集试验;
琼脂扩散试验;
SPF鸡
酶联免疫吸附试验;
SPF鸡
胚敏感试验;
GB/T 17999.7--1999$
SPF鸡鸡白痫沙门氏菌检验;
GB/T 17999.8..- 1999
试管凝集试验;
SPF鸡
GB/T 17999.9 1999
SPF鸡间接免疫荧光试验。
本标准出中华人民共和国农业部、国家科学技术部提出。本标准出农业部畜牧兽医司归口。本标准起草单位:农业部实验动物研究中心、山东省农科院家禽研究所。本标准主要起草人:赵立红、陈德威、张秀美、秦卓明。70
1范围
中华人民共和国国家标准
SPF鸡血清中和试验
SPF chicken -S
Serum neutralization test
本标准规定了血清中和试验所用试剂、材料,操作程序及结果判定等。GB/T 17999.2-:1999
本标准适用于SPF鸡感染以下病毒后的中和抗体的监测:禽脑脊髓炎病毒(AvianEncephalomyelitisVirus)、传染性支气管炎病毒(Infectious BronchitisVirus)、传染性喉气管炎病毒(In-fectious Laryngotracheitis Virus)、传染性法氏囊病病毒(Infectious Bursal Disease Virus)。2原理
中和试验系指有生物活性的病毒与相应的抗体结合后,可失去原有的生物活性的中和反应。中和反应不仅有高度特异性,且具有严格的量的关系。因此可用中和试验鉴定病毒,也可用于相应抗体的定量检测。
3试剂和器材
3.1试剂
3.1.1蛋白脉磷酸肉汤。
3.1.2背霉素/链霉素(双抗)液。3.1.33%碘溶液。
3.1.4 SPF 蛋。
3.2器材
3.2.1蛋钻(打孔器)。
3.2.26\针头。
3.2.37针头。
3.2.4混合器。
3.2.5照蛋器。
3.2.6常规实验设备。
4操作程序
4.1试验准备
4.1.1血清样品处理
被检血清和阳性对照血清经56℃30min~45min灭活,保存于-20C条件下备用。4.1.2SPF蛋准备
4.1.2.1共需12枚蛋。
4.1.2.2照蛋检查胚体活力,试验只用健康胚。4.1.2.3根据病毒种类选择接种方法(见表1)。用3%碘溶液消毒胚蛋接种部位。国家质量技术监督局1999-11-10批准2000-04-01实施
禽脑脊髓炎病毒
传染性支气管炎病毒
传染性法氏囊病病毒
传染性喉气管炎病毒
注YS卵黄囊CAS.
4.1.3稀释病毒www.bzxz.net
GB/T 17999.2—1999
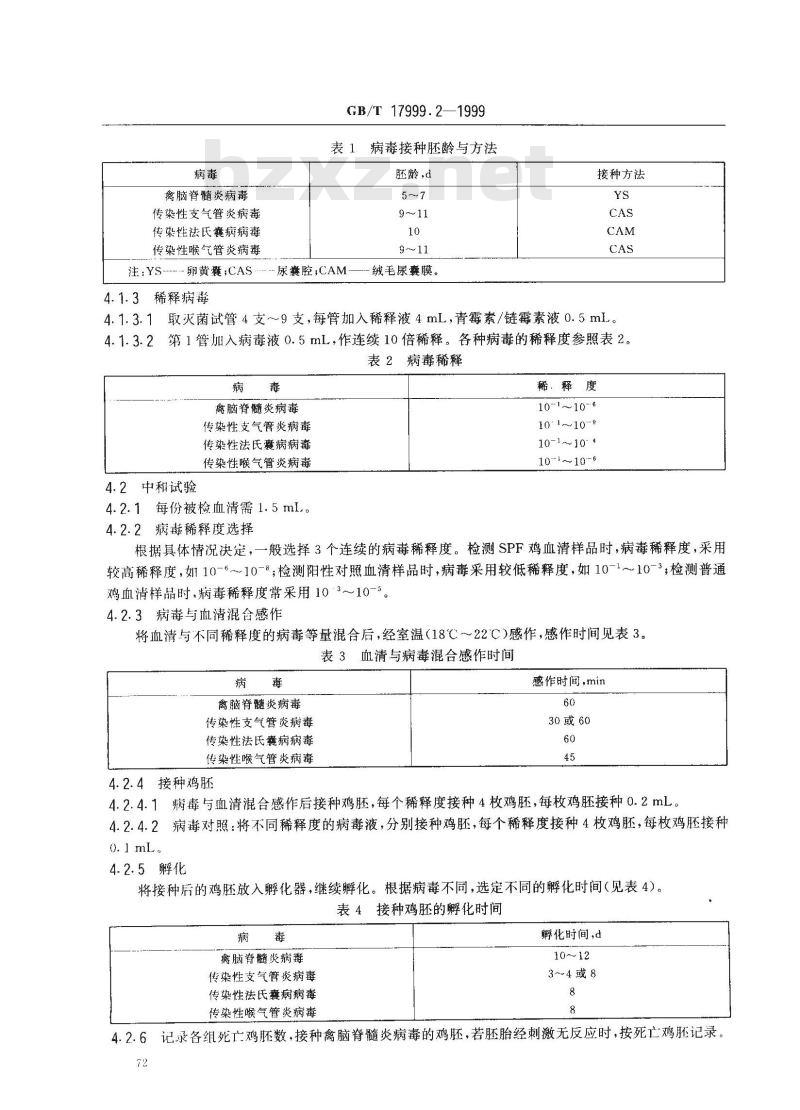
病毒接种胚龄与方法
胚龄,d
尿囊腔;CAM
绒毛尿囊膜。
接种方法
4.1.3.1取灭菌试管4支~~9支,每管加入稀释液4mL,青霉素/链霉素液0.5mL。4.1.3.2第1管加入病毒液0.5mL,作连续10倍稀释。各种病毒的稀释度参照表2。表 2病毒稀释
禽脑脊髓炎病毒
传染性支气管炎病毒
传染性法氏囊病病毒
传染性喉气管炎病毒
4.2中和试验
4.2.1每份被检血清需1.5ml.。
4.2.2病毒稀释度选择
稀、释度
10-1~10-6
10 1~10-9
10-1~10-4
10-1~10-6
根据具体情况决定,一般选择3个连续的病毒稀释度。检测SPF鸡血清样品时,病毒稀释度,采用较高稀释度,如10-6~~10-8;检测阳性对照血清样品时,病毒采用较低稀释度,如10-1~10-3;检测普通鸡血清样品时,病毒稀释度常采用103~10-54.2.3病毒与血清混含感作
将血清与不同稀释度的病毒等量混合后,经室温(18℃~22℃)感作,感作时间见表3。表3血清与病毒混合感作时间
禽脑脊髓炎病毒
传染性支气管炎病毒
传染性法氏囊病病毒
传染性喉气管炎病毒
4.2.4接种鸡胚
感作时间,min
30或60
4.2.4.1病毒与血清混合感作后接种鸡胚,每个稀释度接种4枚鸡胚,每枚鸡胚接种0.2mL,4.2.4.2病毒对照:将不同稀释度的病毒液,分别接种鸡胚,每个稀释度接种4枚鸡胚,每枚鸡胚接种0. 1 mLe
4.2.5孵化
将接种后的鸡胚放入孵化器,继续孵化。根据病毒不同,选定不同的孵化时间(见表4)。表 4接种鸡胚的孵化时间
禽脑脊髓炎病毒
传染性支气管炎病毒
传染性法氏囊病病毒
传染性喉气管炎病毒
孵化时间,d
3~~4或8
4.2.6记录各组死亡鸡胚数,接种禽脑脊髓炎病毒的鸡胚,若胚胎经刺激无反应时,按死亡鸡肝记录。72
4.2.7计算中和指数
GB/T 17999.2---1999
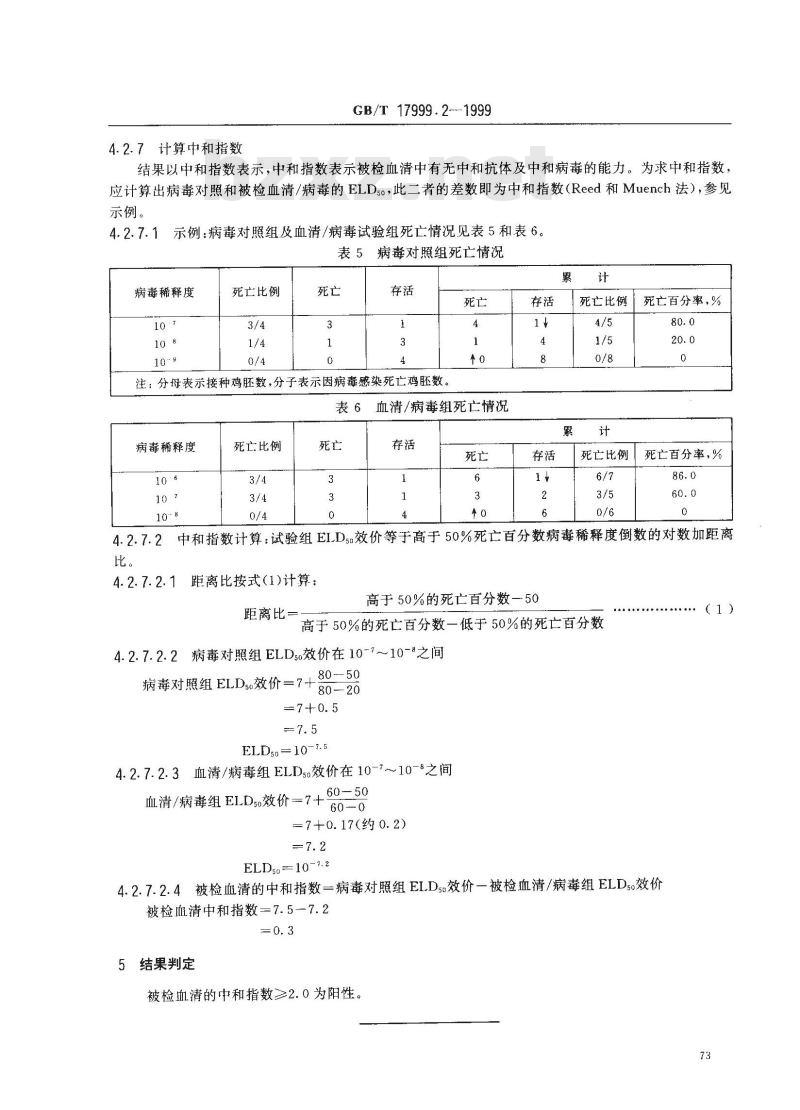
结果以中和指数表示,中和指数表示被检血清中有无中和抗体及中和病毒的能力。为求中和指数,应计算出病毒对照和被检血清/病毒的ELD5o,此二者的差数即为中和指数(Reed和Muench法),参见示例。
4.2.7.1示例:病毒对照组及血清/病毒试验组死亡情况见表5和表6。表 5病毒对照组死亡情况
病毒稀释度
死亡比例
注:分母表示接种鸡胚数,分子表示因病毒感染死亡鸡胚数。表6
病毒稀释度
死亡比例
血清/病毒组死亡情况
死亡比例
死亡比例
死亡百分率,%
死亡百分率,%
4.2.7.2中和指数计算:试验组EIL.D5.效价等于高于50%死亡百分数病毒稀释度倒数的对数加距离比。
距离比按式(1)计算:
4. 2. 7. 2. 1
距离比一
高于50%的死亡百分数一50
高于50%的死亡百分数一低于50%的死亡百分数4.2.7.2.2病毒对照组ELD5o效价在10-7~10-8之间80—50
病毒对照组 ELDs.效价=7+
80--20
= 7+ 0. 5
ELD5o =10-7. 5
4.2.7.2.3血清/病毒组ELD5效价在10-7~10-8之间血清/病毒组 ELD:o效价=7+60=5060-0
=7+0. 17(约 0. 2)
ELD5o10-7.2
4.2.7.2.4被检血清的中和指数一病毒对照组ELDs效价一被检血清/病毒组ELDs.效价被检血清中和指数=7.5--7.2
5结果判定
被检血清的中和指数≥2.0为阳性。(1)
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
本标准参照美国SPAFAS公司的血清中和试验(SN)操作规程编制而成。SPF鸡微生物学质量控制国家系列标准,包括SPF鸡微生物学监测总则和9种SPF鸡微生物学检测方法。本标准为《SPF鸡血清中和试验》。SPF鸡微生物学检测方法还包括以下部分:GB/T17999.1-1999SPF鸡
红细胞凝集抑制试验;
GB/T17999.3 1999SPF鸡
GB/T 17999. 4 --1999
GB/T 17999.5- 1999
GB/T 17999. 6-1999
SPF鸡
血清平板凝集试验;
琼脂扩散试验;
SPF鸡
酶联免疫吸附试验;
SPF鸡
胚敏感试验;
GB/T 17999.7--1999$
SPF鸡鸡白痫沙门氏菌检验;
GB/T 17999.8..- 1999
试管凝集试验;
SPF鸡
GB/T 17999.9 1999
SPF鸡间接免疫荧光试验。
本标准出中华人民共和国农业部、国家科学技术部提出。本标准出农业部畜牧兽医司归口。本标准起草单位:农业部实验动物研究中心、山东省农科院家禽研究所。本标准主要起草人:赵立红、陈德威、张秀美、秦卓明。70
1范围
中华人民共和国国家标准
SPF鸡血清中和试验
SPF chicken -S
Serum neutralization test
本标准规定了血清中和试验所用试剂、材料,操作程序及结果判定等。GB/T 17999.2-:1999
本标准适用于SPF鸡感染以下病毒后的中和抗体的监测:禽脑脊髓炎病毒(AvianEncephalomyelitisVirus)、传染性支气管炎病毒(Infectious BronchitisVirus)、传染性喉气管炎病毒(In-fectious Laryngotracheitis Virus)、传染性法氏囊病病毒(Infectious Bursal Disease Virus)。2原理
中和试验系指有生物活性的病毒与相应的抗体结合后,可失去原有的生物活性的中和反应。中和反应不仅有高度特异性,且具有严格的量的关系。因此可用中和试验鉴定病毒,也可用于相应抗体的定量检测。
3试剂和器材
3.1试剂
3.1.1蛋白脉磷酸肉汤。
3.1.2背霉素/链霉素(双抗)液。3.1.33%碘溶液。
3.1.4 SPF 蛋。
3.2器材
3.2.1蛋钻(打孔器)。
3.2.26\针头。
3.2.37针头。
3.2.4混合器。
3.2.5照蛋器。
3.2.6常规实验设备。
4操作程序
4.1试验准备
4.1.1血清样品处理
被检血清和阳性对照血清经56℃30min~45min灭活,保存于-20C条件下备用。4.1.2SPF蛋准备
4.1.2.1共需12枚蛋。
4.1.2.2照蛋检查胚体活力,试验只用健康胚。4.1.2.3根据病毒种类选择接种方法(见表1)。用3%碘溶液消毒胚蛋接种部位。国家质量技术监督局1999-11-10批准2000-04-01实施
禽脑脊髓炎病毒
传染性支气管炎病毒
传染性法氏囊病病毒
传染性喉气管炎病毒
注YS卵黄囊CAS.
4.1.3稀释病毒www.bzxz.net
GB/T 17999.2—1999
病毒接种胚龄与方法
胚龄,d
尿囊腔;CAM
绒毛尿囊膜。
接种方法
4.1.3.1取灭菌试管4支~~9支,每管加入稀释液4mL,青霉素/链霉素液0.5mL。4.1.3.2第1管加入病毒液0.5mL,作连续10倍稀释。各种病毒的稀释度参照表2。表 2病毒稀释
禽脑脊髓炎病毒
传染性支气管炎病毒
传染性法氏囊病病毒
传染性喉气管炎病毒
4.2中和试验
4.2.1每份被检血清需1.5ml.。
4.2.2病毒稀释度选择
稀、释度
10-1~10-6
10 1~10-9
10-1~10-4
10-1~10-6
根据具体情况决定,一般选择3个连续的病毒稀释度。检测SPF鸡血清样品时,病毒稀释度,采用较高稀释度,如10-6~~10-8;检测阳性对照血清样品时,病毒采用较低稀释度,如10-1~10-3;检测普通鸡血清样品时,病毒稀释度常采用103~10-54.2.3病毒与血清混含感作
将血清与不同稀释度的病毒等量混合后,经室温(18℃~22℃)感作,感作时间见表3。表3血清与病毒混合感作时间
禽脑脊髓炎病毒
传染性支气管炎病毒
传染性法氏囊病病毒
传染性喉气管炎病毒
4.2.4接种鸡胚
感作时间,min
30或60
4.2.4.1病毒与血清混合感作后接种鸡胚,每个稀释度接种4枚鸡胚,每枚鸡胚接种0.2mL,4.2.4.2病毒对照:将不同稀释度的病毒液,分别接种鸡胚,每个稀释度接种4枚鸡胚,每枚鸡胚接种0. 1 mLe
4.2.5孵化
将接种后的鸡胚放入孵化器,继续孵化。根据病毒不同,选定不同的孵化时间(见表4)。表 4接种鸡胚的孵化时间
禽脑脊髓炎病毒
传染性支气管炎病毒
传染性法氏囊病病毒
传染性喉气管炎病毒
孵化时间,d
3~~4或8
4.2.6记录各组死亡鸡胚数,接种禽脑脊髓炎病毒的鸡胚,若胚胎经刺激无反应时,按死亡鸡肝记录。72
4.2.7计算中和指数
GB/T 17999.2---1999
结果以中和指数表示,中和指数表示被检血清中有无中和抗体及中和病毒的能力。为求中和指数,应计算出病毒对照和被检血清/病毒的ELD5o,此二者的差数即为中和指数(Reed和Muench法),参见示例。
4.2.7.1示例:病毒对照组及血清/病毒试验组死亡情况见表5和表6。表 5病毒对照组死亡情况
病毒稀释度
死亡比例
注:分母表示接种鸡胚数,分子表示因病毒感染死亡鸡胚数。表6
病毒稀释度
死亡比例
血清/病毒组死亡情况
死亡比例
死亡比例
死亡百分率,%
死亡百分率,%
4.2.7.2中和指数计算:试验组EIL.D5.效价等于高于50%死亡百分数病毒稀释度倒数的对数加距离比。
距离比按式(1)计算:
4. 2. 7. 2. 1
距离比一
高于50%的死亡百分数一50
高于50%的死亡百分数一低于50%的死亡百分数4.2.7.2.2病毒对照组ELD5o效价在10-7~10-8之间80—50
病毒对照组 ELDs.效价=7+
80--20
= 7+ 0. 5
ELD5o =10-7. 5
4.2.7.2.3血清/病毒组ELD5效价在10-7~10-8之间血清/病毒组 ELD:o效价=7+60=5060-0
=7+0. 17(约 0. 2)
ELD5o10-7.2
4.2.7.2.4被检血清的中和指数一病毒对照组ELDs效价一被检血清/病毒组ELDs.效价被检血清中和指数=7.5--7.2
5结果判定
被检血清的中和指数≥2.0为阳性。(1)
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。