GB/T 14550-1993
基本信息
标准号: GB/T 14550-1993
中文名称:土壤质量 六六六和滴滴涕的测定 气相色谱法
标准类别:国家标准(GB)
标准状态:已作废
发布日期:1993-08-06
实施日期:1994-01-15
作废日期:2004-04-01
出版语种:简体中文
下载格式:.rar.pdf
下载大小:325993

标准分类号
标准ICS号:环保、保健与安全>>13.080土质、土壤学
中标分类号:环境保护>>环境保护采样、分析测试方法>>Z18土壤环境质量分析方法
关联标准
替代情况:被GB/T 14550-2003代替
出版信息
页数:10页
标准价格:15.0 元
相关单位信息
标准简介
GB/T 14550-1993 土壤质量 六六六和滴滴涕的测定 气相色谱法 GB/T14550-1993 标准下载解压密码:www.bzxz.net
标准图片预览




标准内容
1适用范
中华人民共和国国家标准
土壤质量
六六六和滴滴涕的测定
气相色谱法Www.bzxZ.net
Soil quality-Determination of BHC andDDT- Gas chromatography
1.1本标准适用于土壤巾六六六、滴滴沸的分析。GB/T14550-93
1.2本法采州丙酮石油醚提取,以浓硫酸净化,川带电子捕获检测器的气相色谱仪测定。1. 3本方法的最低检测浓度0. 000 05~~0. 00487mg/kg。2试剂和材料
2.1载气
气,纯度99.99%,经去氧管过滤,氧的含量小于5ppm,氯的含量小于1.0Ppm。2.2配制标准样品和试样预处理时使用的试剂和材料使用的试剂系分析纯,有机溶剂经重蒸,浓缩20借用气谱测定无干扰峰。2.2.1色谱标样品:a-六六六、β六六六、Y-六六六、&六六六、P,P'-DDE.0p-DDT、PP-DI)D、P,p-DDT,含量98%~99%,色谱纯。2.2.2石油醛,沸程60~90℃。
2.2.3丙解(CH,COCH,)。
2.2.4异辛烷(C,H)。
2.2.5苯(C,H):优级纯。
2.2.6浓硫酸(H,S),):密度为1.84g/mL,2.2.7无水硫酸钠(Na,S0),)在300℃烘箱中烘烤4h,备用。2.2.8硫酸钠溶液:20g/1.。
2.2.9硅藻土:试剂级。
三氯甲烷(CHCI,)。
2.2.11液
脱脂梯(或玻璃棉):用丙酮回流16h,取出晾干后备用。2.3制备色谱柱时使用的试剂材料2.3.1色谱柱和填充物(3.6.5),2.3.2涂溃固定液所用溶剂三氮甲烷(2.2.10)。3仅器
3.1士要仪器:带电了捕获检测器的气相色谱仪。3.2控制载气的压力表及流计。
3.3进样器:全璃系统进样器。
国家环境保护局1993-07-19批准1994-01-15实施
3.4记录仪:与仪器相匹配的记录仪。3.5检测器:
3.5.1类型:电了捕张检测器。
GB/T 14550.-93
3.5.2游件的特征.可采用Ni放射源或高\H效射源。3.5.3检测器极化电压:可采用直流电源或脉冲电源。3.6色谱柱:
3. 6. 1 色谱柱数量;2~ 3 支。3.6.2色谱栏特征:
3.6.2.1材料:硬质玻璃。
3.6.2.2尺寸:长1.8~2.0m,内径2~3mm。3.6.3色谱柱类型;螺锭状填充柱。3.6.4色谱柱颜处理经水冲洗后,在玻璃注管内注满热洗液(60~70℃)。浸泡4h,然后用水冲洗至中性,再用蒸馏水冲洗,烘·F后进行硅烷化处理,将6%10%的二二甲基硅烷甲醇溶液注满玻璃柱,浸泡2h,然后用甲醇清洗至中性,烘干备用。3.6.5填充物:
3.6.5.1载体:chromosorb WAw-DMcS或者chromasorbW AW-DMCs-HP,80~100目。3.6.5.2固定液:0V-17(甲基硅酮),最高使用温度350CQF-1或OV-210(三氯丙基甲基硅酮),最高使用温度250℃或275。
3.6.5.2.1液相载荷,(V-17为1.5%;OV-210或QF-1为1.95%。3.6.5.2.2涂溃固定液的方法:根据担体的重量称取一定量的固定液,游在三氛甲烷中,待完全溶解后,倒入盛有担体的烧怀中,再向其中加入三氮甲烷(2.2.10)至液面高出1~2cm,摇匀后浸2h。然后在红外灯下将溶剂摔发十或在旋转蒸发器上慢速蒸于,再置于120℃烘箱中,放置4h后备用。3.6.5.3色谱注的填充方法:将色谱杆的-端(接检测器)用硅烷化玻璃棉塞住,接真空泵,另一端接漏斗,开动真空泵后将固定相徐徐倾入色谐柱内,并轻轻拍打色谱柱,使固定相在色谱柱内填充紧密,至固定相不再栅入柱内为止,装填完毕后,用硅烷化玻璃棉寒住色谱柱另一。3.6.5.4色谱柱的老化:将填充好的色谱柱进口按正常接在汽化室上,出口空着不接检测器,先用较低教气流速,在略高于实际使用温度而不超过固定液的使用温度下处理4~6h。然后逐渐提高温度,载气流速老化24~48h。再降低至使用温度,接上检测器后,如基线稳定即可使用。3.6.6柱效能:
在给定条件1,色谱柱总分离效能即分离度要求不小于90%。3.7试样预处理时使用的仅器:
3.7.1样品瓶:适宜的玻璃磨口瓶。3.7.2蒸发浓缩器。
3. 7. 3脂肪提取器。
3.7.4 水浴锅。
3.7.5振药器。
3.7.6玻璃器血;300mL分液漏斗,300mlL其塞锥形瓶,100mL量筒,250ml平底烧瓶,25、50100 ml.容盘瓶。
3.7.7微基注射器,5μ110μL。3.7.8离心机.
4样品
4.1样品性质
4.1.1样品名称:士壤样品。
4.1.2样品状态质体
CH/T 14550 93
4.1.3样品的定似::十样品六六六,滴滴滞化学性质稳定,A.2样品内采美及行方法
4.2.1样品的米架
4.2.1.11壤,在出间根不同的分析目的多点采集,风下去杂物,研碎过60日筛,充分混勾,取500g装人群品瓶备明。
4.2.2样品的保存
1堰样品采集后应尽快分析,如暂不分析成保存在…18心冷冻箱中4.3试样的纳处理
4.3.1提取
准确称取20g七城(4.2.1.1)置」小烧杯中,加蒸留水2m1..硅巢士4g(2.2.9),充分勺.无摄地移入滤纸简内,上部盖-片滤纸,将滤纸简装入索提取器中,加100mL行油醚-丙谢(1:1),用30ml.漫泡样12情在75--95℃恒温水浴上加热提取4h,待冷却后.将提取液移入300mL的分液漏斗中,10m.石油醚分三次冲洗提取器及烧瓶+将洗液并入分液漏斗中,加入100mL硫酸钠溶液(2.2.8).振据1min,静止分层后·弃去下层丙翻水溶液,留下石油醚提取液待净化。4.3.2净化
4.3.2.1浓硫酸净化法:适用于.十堰、生物样品。在分液爆斗中加入石油醚提取液体积的十分之-的浓巯酸,摄摇1min,静做分层后,齐去疏酸层(注总:用酸净化过程中,要防止发热燥炸,加碗酸后,开始要慢慢振摇,不断放气,然后再剧烈振播),按上述步骤重复数次,直至加人的石油提取二相界面清晰与星无色透明时止。然后向弃去硫酸层的右油醚提取液中加人其体积盘一半左右的(2.2.8)硫酸钠浴波。报操1余次。待其静置分层后弃去水层。如此重复至提取波呈中性时止(一般2~4次),石油醛揭取液再经装有少量无水硫酸钠的筒型斗脱水,滤入适当规格的容量瓶中,定容,供气相色谱测定。5色谱测定操作步骤
5.1仪器的调整
5.1.1汽化室溢度,220℃
5.1.2柱温度:195C。
5.1.3检测器温度245Y。
5.1.4较代流速:40~~70ml/min根据器的情况选用。5.1.5记录仪纸速:5mm/min
5.1.6塞减:根据样品中被测组分含基适当调节记录器衰减。5.2校雅
5.2.1定量方法
外标法。
5.2.2标雅样品
5.2.2.1使用次数:使用标准样品周期性的重复校准,视仪器的稳定性决定周期长短,若仪器稳定,司测案4-~5个试校推一次。
5.2.2.2标准样品的制备:准确称取一定量的色谱纯标准样品每种(2.2.1)100mg溶于异辛烷(2.2.1)(六六八先用少插苯溶解).在容量瓶中定容100mL,在4℃下照存。5.2.2.3中间济液:川移液管量取八种储备液,移至100ml.容量瓶中.用异辛烷稀释至刻度。八种储备液取的体积lt为V:Vx::V+Vo:Vpre:Vepy!Vr-n:Vopr-1:1:3. 6 : 1: 3. 5: 5: 3 : 8.
GB/T 14550—93
5.2.2.4标准1.作液的配制:根据检测器的灵敏度及线性要求,用石油醛(2.2.2)稀释中问溶液,配制成儿种浓度的标准工作液,在4℃下贮存。5.2.2.5气相色谱4使用标准溶液的条件:5.2.2.5.1标渊样品的进样体积与试样进样体积相同.标准样品的响应值接近试样的响应值。5.2.2.5.2调节仪器重复性条件:个样品连续注射进样两次,其峰高相对偏养不大于7%,即认为仪器处理工稳定状态。
5.2.2.5.3标摊样品与试样尽可能同时进样分析。5.2.3校准数据的表示
试样中组分按式(1)校准:
式:X,——试样中组分i的含或,mg/kg;E,—标推溶液中组分 t 的含基,mg /kg :A.—试样中组分:的峰高,cm(或峰面积cm\)Ar一-标推溶液中组分的峰高,cm(或蜂面积cm))5.3进样试验
5.3.1进样
5.3.1.1进样方式注射进样。
5. 3. 1.2进样量—饮进样量 3--6 μL。++-++(1)
5.3.1.3操作:用清洁注射器(3.7、7)在待测样品中抽吸几次,播除所有气泡后,抽取所带进样体积,迅速注射人色谱仪中,并立即拔出注射器。5.4色谱图的号察
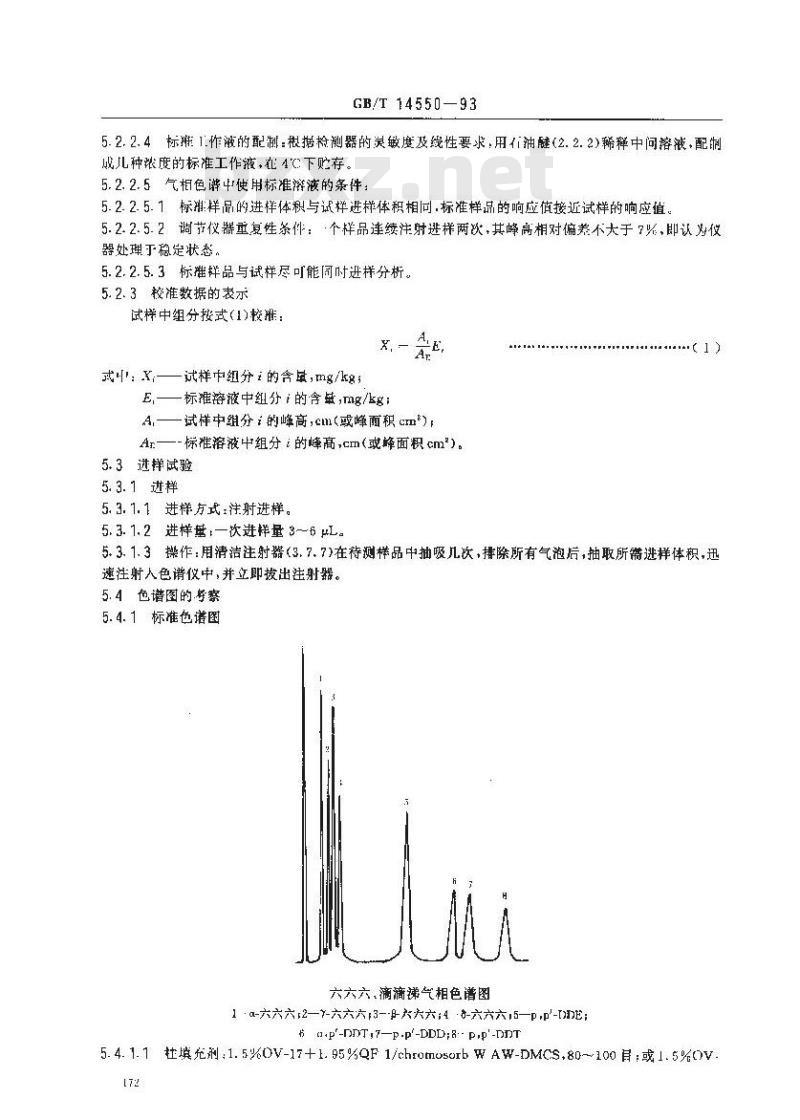
5.4. 1标准色谱图
六六六,滴滴涕气相色谱图
1:a-六六六:2—-六六六—-六;4·-六六六15—-6α-p-DDT,7—P-'-DDD;8--P-P'-DDT5.4.1.1杜填充剂.1.5%0V-17+1.95%QF1/chromo5orbWAW-DMCs,80~100月:或1.5%V172
GB/T14550—93
17+1.95%OV-210/chromosorhWAW.DMCS-HP.80~100d。5.4.1.2载气:氢气,40~70mL/min。柱温185195C。5. 4. 2定性分析
5.4.2.1组分的出峰次序,α-六六六、Y-八六六,β六六六,六六入P,P*-DDE,o,p-DDT,PP'-DDD,P.p'-DDT.
5.4.2.2检验可能存在的干扰,采用双柱定性。用另一根色谱柱(1.5%()V-17+1.95%QF-1/chromasnrhWAW-DMCS,80~100目)进行准确检验色谱分析,可确定各组分及有无干扰。5.4.3定量分析
5.4.3.1色谱峰的测量
以睡的起点和终点的联线作为峰底,以峰高极大值对时间轴作垂线,对应的时间即为保留时间,此线从峰顶至峰底间的线段即为峰高。5. 4. 3.2计算
式中:R,
样品中i组分农药的含量,mg/kgl样品中i组分农药的蜂高,cm(或峰面积cm),标样中1组分农药的绝对鹭,ng1-G(g)样品定容体积,mL
h—标样中组分农药的峰高,cm(或峰面积cm):一样品的进样盖,,
C—样品的重量8。
6结果的衰示
6.1定性结果
根据标准色谱图各组分的保留时间来确定被测试样中出现的组分数目和组分名称。6.2定量结果
6.2.1含量的表示方法根据5.4.3.2计算出的各组分的含量,以mg/kg表示。6.2.2精密度见表1。
6.2.3准确度见表2。
6.2.4检测限:当气相色谱仅仪器的灵敏度最大时,以噪音的2.0倍作为仪器的检测限,本方法要求仪器的最小检测量低于10-1g(见.表3)。173
重垂复性
墨复性
再现性
再现性
再现性
协作实验室数量
注H-商裱度;M
中浓度-
六六六
L - 0. 004
低浓度,
表1、精密度(重复性和再现性)民六六六
6.4×10°
了-六六六
H—0.200
E.= 0. 004
1.2×10-3
6. 9×10r2
1.9×10m*
2. 00×10-*
合六六
P·DDE
TI=0. 500
1. --0. 010
5. 0 × 10-
M -D, 200
6. 0×10+
8.1×10-2
(士壤样)
p-p'-non
4.0×10-1
tng/kg
4. 0×10*
8.6人101
14550—93
加人量
回收率,%
回收率
回收率,
协作实验室数量
α-六六
表2准确度(土壤样加标同收率,%)六六六
2-六六六
I. = D. D64
存六六六
1. =[0. 010
H= 0. 50)
L-[,010
L - 0. 020
pp'-DD
L = 0. 020
14550--
附加说明:
农药种类
0六六六
丫六六六
P-p'-DDE
OP'-TDT
GB/T14550—93
表3检测限
本标准由国家环境保护同科技标准司和农业部环能司提出。本标准出农业部环境保护科研监测所负责起草。品小检测母,
3. 577× 10~ :
2.523×1c22
1.190×10--2
9.770×10-a
1.756×102
6.96010*2
5.572×10-12
1.460×10-1s
本标准主要起草人黄上忠、陈国光,王继军、李治祥,张俊享、万兆良、袁秀文、玛秀琼。176
上壤和污泥中苯并(a)花的测定白然界:1壤中含有一系列多环芳香烃化合物,其中苯并(a)花已被公认为强烈的效痛物质,但它的人然本底很低,实际上作用并不明显。当土壤受到污染后,苯并(a)花含量发生变化,引起一系列较为复杂的致癌作用问题。因此.掌握不同条件下土壤中苯并(a)花量的变化规律性,对进一步评价与防治环境污染具有重要意义。
1原理
土壤中含有一系列多环劳香径化合物(PAH),成分复杂,含最很低。采用二步柱展析力法,其分离效果主要取决于吸附剂对PAH各组成的“吸附力”,以及“展开剂\对各组成分的“洗脱力”这两种相互矛盾和对立力量的相互作用。实践证明:采用吸附力较弱的吸附剂(>0.1mm中性层析氧化铝),结合洗脱力较弱的溶剂(环已烷)作为一级分离,再以较强吸附力的吸附剂(<0.1mm中性层析氧化铝),结合洗脱力较强的溶剂(12-二氯乙烷)作二级分离,可使PAH各组分达到较好分离,分离所得苯并(a)芪试样用紫外分光光度计进行定性和定量鉴定2仪器和试剂
2.1恒温水浴。
2.2国产中性层析氧化铝。
2. 3 孔径 0. 1 mm 筛网。
2.4内径1.0cm和0.5cm啵璃层析节,高度分为30cm和50cm。2.5氯仿(二氯用烷)A、R。
2.6坏烷(重蒸馅)。
2.」,2·二氯乙烷(重热馏)。2.83600%紫外灯。
2.9紫外分光光度计。
3土填中PAH的握取
为考虑有机落剂的安全与效果、通过对比试验,决定放弃举而采用氣作为土填凝提剂。取通过\.25tt1筛孔的七填试样20g,(两份,作平行测定),置于125mL三第瓶中,加氯仿50mL,加盖,用手轻轻振荡5min,静置过夜。第二天,将三角瓶置于50℃水浴继续提取1h,过滤。再加上50mL氯仿,照前振荡5min,骨于50C水裕继续提取1h,过滤,然后分别用25mL氯仿继续洗涤三角瓶中试样握合物二遍。滤液在同一个100mL的小玻璃撬杯或浓缩器中前后分三次用水浴进行蒸发,最后一次蒸发到杯底快处干时取下,马上用环已烷进行溶解,备分离纯化。4分离纯化
如果上壤中毕并(a)花含量>5g/kg+可采用两次氧化铝柱层与紫外分光法,如含鼠5/k,则采氧化铝柱层,纸层荧光分光法。4.1紫外分光法
4.1.1PAH的初级分离
取国产中性层析氧化,通过0.1mm筛孔滤去细颗粒(留作二级分离用),将筛网上的氧化铝,在F燥器挡板上铺-薄层,千燥器内用35%硫酸配制成70%左右的相对湿度:在此条件下平衡两叠夜以177
I.,便氧化铝含水率达了7.5左右,分离前将其装填于内径1rm层析管巾。图「为分离纯化示意图。
三氯甲烷浓缩强滴
敏化铝柱
黄外分光法鉴室
化组柱
最层析
荧光分光法定
图1分离纯化示意图
于内径1cm层析管中,要求氧化铝在层析管中装填时做到致密义均勺高度为20cm,然后加2ml环已烷于提取PAH的小烧杯中将残清溶解,并用滴管将此溶液滴入层析柱上端便其吸附,为避免损耗,再分别用0.5mL环已烷洗涤小烧杯两次,并将洗涨液一并滴人层析柱土端吸附。以同样操作做3的举并芪标准柱待吸附完毕后,再其上加人环已烷展开剂,在暗室中展开1h以L,并在3600%紫外光照射下观赛层析柱的分层情况,至明显分层止。注意发紫蓝色荧光的色层即为含行举并()范的色层,一般分层达再层以上(见图2)。.糖色
3.淡面啡色
3.蓝绿免蚁光
d.蓝紫色荧光
5.整绿色樊光
6.黄色荧光
图2一级分离系统程上荧光光谱示意图4.1.2PAH的-级分离
取内径0.5cm层析玻璃管.置于烘箱中,在100下烘干,将.上.述通过0.1mm筛孔的细氧化铝在使用前置于磁蒸发血内.在煤气灯上高温灼烧半小时以上,使其完全脱去水分,在未完全冷却时郎装人层析挂中,高度25cm左右,要求密实均勾。层析柱填装完毕后,将初级分离层析中发紫蓝色炭光的次,小心用锉刀锉断取出,并直接装人本层析柱的上谢,然后在层析普上端加人5mL1,2-二氯乙烷,在暗处展开半小时,于3600%紫外光下观察,至层析柱上各荧光色层充分分开为止(见图3)。1. 淡紫
血,淡螺
6. 亮紫荧冶
6. 亦素蓝
一搬分高翘望化铝
图3二级分离系统样上炎光光谱示意图与标准杜比较,挂出样品中发亮紫的色层即含苯并(a)花的(其中提取液在3600紫外线照射下发蓝紫荧光)荧光段。
将亮紫荧光层用锉刀小心取出,避免和上下连结的层次干扰,取出氧化铝,装人填有脱脂棉的玻璃178
漏斗中.以10mI.1,2-二氯乙烷分数次加增洗提,将提取于水浴上蒸于。最后准确助加5ml.坏己烷游解残清,文即在紫外分光光度计上测定350~410nm波段的吸收光谱曲线。苯并(a)诺在365m385日m,403几nI处有-三个待征波峰,可作为定性的参考依据。4. 1. 3标准苯并(a)芪溶液的标定感望0.1mg天平(用标推磁码进行校准)称取本并()范501g,落解:f:100L经过重蒸懈的坏己烷中+配成浓度为50μg/mL的母液.然后用微量吸管吸母液分别配制成浓度为2.4,8.10,20g/5Tml.的:·红标准溶液,在紫外分光光度计上分别测定350,365,375,385.403m处的光谢度值,以375+385395nm处的光密度值按基线法计算出385nm处的实际光密度俏,按式(1)计算:1 Is
aln)
式中:1、:385I处的实际光辫度值.a:--385nm处的光密度观察值:Im—375处的光密度观察值
us——3951m处的光密度观察值
........+..++++...I)
上式得出不同浓度标准来并(a)范在385.nm处的实际光密度值,以浓度为横坐标,光帮度为纵整标制备工作曲线。
为检查以上结果的准确性,重新配制一组浓度为5,10,20μg/5mL的苯并(a)标推穿液,测定它们在紫外光375~395nml被段的光密度值,用同样底线法求出实际光密度值。在浓度为0~20μg/5mL的范围内标准苯并(a)花浓度与波峰高度的光密度值为线性关系,4.1.4土壤中萃并(a)花的定型
土填中PAH的成分复杂,经过一步柱层分离所得萃并(a)花试样只能保持相对的纯度,而不能完全排除其他杂质干扰,故在紫外分光光度计上描记所得的吸收光谱曲线,常出现365nm波峰高于385nnl波峰的现象(因PAH中很多其他成分的吸收偏向紫外短波方面,致使365nm波峰增高)。因此,在实际小应以385nm的实际光密度值作为定量依据。并且要严格遵守下列规则:即为了排除杂质的十扰,位按照配制标准曲线时相同的\底线法”加以校正。将分离样品按“底线法\测得的实际光密度值,板据标准曲线求出土壤苯并(a)茂的相应含量。4.1.5结果计算
士澳莱并(a)按式(2)计算:
土境苯并(a)花含量(μR/kg)-号X1000
式中,Q—从标谁曲线聋得苯并(a)范的含量,W.-样品重屋,。
4.2荧光分光法
4.2.1氧化锯柱层分离
游中性70~2(00目的氧化铝于140~-160℃活化4~6h,装人内径1cm的玻璃中,要求致密均勾,商度5~cm。然后将土壤氯伤提取液的浓缩残渣用25ml.环己烷分次溶解,滴人氧化铝柱中,加压过滤,待过滤完毕,弃去下部环已烷接收液,再手住上加50mL重热苯,接收苯的洗脱获,瘀蟾后进行纸层分。
4.2.2纸层分离取乙酰化滤纸条.将以上苯的浓缩液定容取一定盘进行带状点样,点样究毕于乙醇-氮甲烷(2十1)展开液中密封、避光展开2-~3h,于3600紫外光下规察,与苯并(a)标准荧光斑点比较,划出样品巾苯井(a)花的荧光带.用剪刀剪下,置于5mL磨口指形管中,加2mL手醇加盖,于蜡处过夜·欲于50-~60水浴加热15~-20min冷却后备荧光测定。4.2.3光测定
在激发光波长386nm光带宽10nm,发射光带1.5tm的条件下测定395~440nt处的荧光光E79
谱,取406刀m处的荧光比谱峰作为计算峰,按“基线法”与标准获比较,计算出样品中举并a)比含量。同时应做空白试验,以同样条件做不同浓度0.02.0.04,0.06,0.08u/ml在400,406410nm处的荧4.2.4结果计算
土壤中苯并()花含量按式(3)计算:土壤中苯并(a)芪含量(/kg)w
式中—标谁曲线苯并(a)薛的含,g/mL:W.----样品质画·&;
备点样液总体积,mL,
实际点样液体积,ml-;
5说明
样品纸层甲醇用盘,ml。
X 2 × 1 000
5.1PAH的各组分离效果,与氧化铝吸附剂的含水率即活性等级密切相关,一级分离用粗氧化销的在70%相对湿度下平衡时间保持两昼夜以上为宜,二级分离用细氧化铝必须在煤气灯上高溢烘烤卡小时以上.,以保证有足够的活性
5.2本方法中最难掌握的地方是在3600\紫外光下区分含苯并(a)花的炎光色层,有时容易滤滑,需要有一定的实毁经验才能准确尤误地得到所需要的分析结果。5.3苯并(a)花对光化学反应较强烈,样品的摄取、浓缩和分高操作需要在暗室中进行。180
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
中华人民共和国国家标准
土壤质量
六六六和滴滴涕的测定
气相色谱法Www.bzxZ.net
Soil quality-Determination of BHC andDDT- Gas chromatography
1.1本标准适用于土壤巾六六六、滴滴沸的分析。GB/T14550-93
1.2本法采州丙酮石油醚提取,以浓硫酸净化,川带电子捕获检测器的气相色谱仪测定。1. 3本方法的最低检测浓度0. 000 05~~0. 00487mg/kg。2试剂和材料
2.1载气
气,纯度99.99%,经去氧管过滤,氧的含量小于5ppm,氯的含量小于1.0Ppm。2.2配制标准样品和试样预处理时使用的试剂和材料使用的试剂系分析纯,有机溶剂经重蒸,浓缩20借用气谱测定无干扰峰。2.2.1色谱标样品:a-六六六、β六六六、Y-六六六、&六六六、P,P'-DDE.0p-DDT、PP-DI)D、P,p-DDT,含量98%~99%,色谱纯。2.2.2石油醛,沸程60~90℃。
2.2.3丙解(CH,COCH,)。
2.2.4异辛烷(C,H)。
2.2.5苯(C,H):优级纯。
2.2.6浓硫酸(H,S),):密度为1.84g/mL,2.2.7无水硫酸钠(Na,S0),)在300℃烘箱中烘烤4h,备用。2.2.8硫酸钠溶液:20g/1.。
2.2.9硅藻土:试剂级。
三氯甲烷(CHCI,)。
2.2.11液
脱脂梯(或玻璃棉):用丙酮回流16h,取出晾干后备用。2.3制备色谱柱时使用的试剂材料2.3.1色谱柱和填充物(3.6.5),2.3.2涂溃固定液所用溶剂三氮甲烷(2.2.10)。3仅器
3.1士要仪器:带电了捕获检测器的气相色谱仪。3.2控制载气的压力表及流计。
3.3进样器:全璃系统进样器。
国家环境保护局1993-07-19批准1994-01-15实施
3.4记录仪:与仪器相匹配的记录仪。3.5检测器:
3.5.1类型:电了捕张检测器。
GB/T 14550.-93
3.5.2游件的特征.可采用Ni放射源或高\H效射源。3.5.3检测器极化电压:可采用直流电源或脉冲电源。3.6色谱柱:
3. 6. 1 色谱柱数量;2~ 3 支。3.6.2色谱栏特征:
3.6.2.1材料:硬质玻璃。
3.6.2.2尺寸:长1.8~2.0m,内径2~3mm。3.6.3色谱柱类型;螺锭状填充柱。3.6.4色谱柱颜处理经水冲洗后,在玻璃注管内注满热洗液(60~70℃)。浸泡4h,然后用水冲洗至中性,再用蒸馏水冲洗,烘·F后进行硅烷化处理,将6%10%的二二甲基硅烷甲醇溶液注满玻璃柱,浸泡2h,然后用甲醇清洗至中性,烘干备用。3.6.5填充物:
3.6.5.1载体:chromosorb WAw-DMcS或者chromasorbW AW-DMCs-HP,80~100目。3.6.5.2固定液:0V-17(甲基硅酮),最高使用温度350CQF-1或OV-210(三氯丙基甲基硅酮),最高使用温度250℃或275。
3.6.5.2.1液相载荷,(V-17为1.5%;OV-210或QF-1为1.95%。3.6.5.2.2涂溃固定液的方法:根据担体的重量称取一定量的固定液,游在三氛甲烷中,待完全溶解后,倒入盛有担体的烧怀中,再向其中加入三氮甲烷(2.2.10)至液面高出1~2cm,摇匀后浸2h。然后在红外灯下将溶剂摔发十或在旋转蒸发器上慢速蒸于,再置于120℃烘箱中,放置4h后备用。3.6.5.3色谱注的填充方法:将色谱杆的-端(接检测器)用硅烷化玻璃棉塞住,接真空泵,另一端接漏斗,开动真空泵后将固定相徐徐倾入色谐柱内,并轻轻拍打色谱柱,使固定相在色谱柱内填充紧密,至固定相不再栅入柱内为止,装填完毕后,用硅烷化玻璃棉寒住色谱柱另一。3.6.5.4色谱柱的老化:将填充好的色谱柱进口按正常接在汽化室上,出口空着不接检测器,先用较低教气流速,在略高于实际使用温度而不超过固定液的使用温度下处理4~6h。然后逐渐提高温度,载气流速老化24~48h。再降低至使用温度,接上检测器后,如基线稳定即可使用。3.6.6柱效能:
在给定条件1,色谱柱总分离效能即分离度要求不小于90%。3.7试样预处理时使用的仅器:
3.7.1样品瓶:适宜的玻璃磨口瓶。3.7.2蒸发浓缩器。
3. 7. 3脂肪提取器。
3.7.4 水浴锅。
3.7.5振药器。
3.7.6玻璃器血;300mL分液漏斗,300mlL其塞锥形瓶,100mL量筒,250ml平底烧瓶,25、50100 ml.容盘瓶。
3.7.7微基注射器,5μ110μL。3.7.8离心机.
4样品
4.1样品性质
4.1.1样品名称:士壤样品。
4.1.2样品状态质体
CH/T 14550 93
4.1.3样品的定似::十样品六六六,滴滴滞化学性质稳定,A.2样品内采美及行方法
4.2.1样品的米架
4.2.1.11壤,在出间根不同的分析目的多点采集,风下去杂物,研碎过60日筛,充分混勾,取500g装人群品瓶备明。
4.2.2样品的保存
1堰样品采集后应尽快分析,如暂不分析成保存在…18心冷冻箱中4.3试样的纳处理
4.3.1提取
准确称取20g七城(4.2.1.1)置」小烧杯中,加蒸留水2m1..硅巢士4g(2.2.9),充分勺.无摄地移入滤纸简内,上部盖-片滤纸,将滤纸简装入索提取器中,加100mL行油醚-丙谢(1:1),用30ml.漫泡样12情在75--95℃恒温水浴上加热提取4h,待冷却后.将提取液移入300mL的分液漏斗中,10m.石油醚分三次冲洗提取器及烧瓶+将洗液并入分液漏斗中,加入100mL硫酸钠溶液(2.2.8).振据1min,静止分层后·弃去下层丙翻水溶液,留下石油醚提取液待净化。4.3.2净化
4.3.2.1浓硫酸净化法:适用于.十堰、生物样品。在分液爆斗中加入石油醚提取液体积的十分之-的浓巯酸,摄摇1min,静做分层后,齐去疏酸层(注总:用酸净化过程中,要防止发热燥炸,加碗酸后,开始要慢慢振摇,不断放气,然后再剧烈振播),按上述步骤重复数次,直至加人的石油提取二相界面清晰与星无色透明时止。然后向弃去硫酸层的右油醚提取液中加人其体积盘一半左右的(2.2.8)硫酸钠浴波。报操1余次。待其静置分层后弃去水层。如此重复至提取波呈中性时止(一般2~4次),石油醛揭取液再经装有少量无水硫酸钠的筒型斗脱水,滤入适当规格的容量瓶中,定容,供气相色谱测定。5色谱测定操作步骤
5.1仪器的调整
5.1.1汽化室溢度,220℃
5.1.2柱温度:195C。
5.1.3检测器温度245Y。
5.1.4较代流速:40~~70ml/min根据器的情况选用。5.1.5记录仪纸速:5mm/min
5.1.6塞减:根据样品中被测组分含基适当调节记录器衰减。5.2校雅
5.2.1定量方法
外标法。
5.2.2标雅样品
5.2.2.1使用次数:使用标准样品周期性的重复校准,视仪器的稳定性决定周期长短,若仪器稳定,司测案4-~5个试校推一次。
5.2.2.2标准样品的制备:准确称取一定量的色谱纯标准样品每种(2.2.1)100mg溶于异辛烷(2.2.1)(六六八先用少插苯溶解).在容量瓶中定容100mL,在4℃下照存。5.2.2.3中间济液:川移液管量取八种储备液,移至100ml.容量瓶中.用异辛烷稀释至刻度。八种储备液取的体积lt为V:Vx::V+Vo:Vpre:Vepy!Vr-n:Vopr-1:1:3. 6 : 1: 3. 5: 5: 3 : 8.
GB/T 14550—93
5.2.2.4标准1.作液的配制:根据检测器的灵敏度及线性要求,用石油醛(2.2.2)稀释中问溶液,配制成儿种浓度的标准工作液,在4℃下贮存。5.2.2.5气相色谱4使用标准溶液的条件:5.2.2.5.1标渊样品的进样体积与试样进样体积相同.标准样品的响应值接近试样的响应值。5.2.2.5.2调节仪器重复性条件:个样品连续注射进样两次,其峰高相对偏养不大于7%,即认为仪器处理工稳定状态。
5.2.2.5.3标摊样品与试样尽可能同时进样分析。5.2.3校准数据的表示
试样中组分按式(1)校准:
式:X,——试样中组分i的含或,mg/kg;E,—标推溶液中组分 t 的含基,mg /kg :A.—试样中组分:的峰高,cm(或峰面积cm\)Ar一-标推溶液中组分的峰高,cm(或蜂面积cm))5.3进样试验
5.3.1进样
5.3.1.1进样方式注射进样。
5. 3. 1.2进样量—饮进样量 3--6 μL。++-++(1)
5.3.1.3操作:用清洁注射器(3.7、7)在待测样品中抽吸几次,播除所有气泡后,抽取所带进样体积,迅速注射人色谱仪中,并立即拔出注射器。5.4色谱图的号察
5.4. 1标准色谱图
六六六,滴滴涕气相色谱图
1:a-六六六:2—-六六六—-六;4·-六六六15—-6α-p-DDT,7—P-'-DDD;8--P-P'-DDT5.4.1.1杜填充剂.1.5%0V-17+1.95%QF1/chromo5orbWAW-DMCs,80~100月:或1.5%V172
GB/T14550—93
17+1.95%OV-210/chromosorhWAW.DMCS-HP.80~100d。5.4.1.2载气:氢气,40~70mL/min。柱温185195C。5. 4. 2定性分析
5.4.2.1组分的出峰次序,α-六六六、Y-八六六,β六六六,六六入P,P*-DDE,o,p-DDT,PP'-DDD,P.p'-DDT.
5.4.2.2检验可能存在的干扰,采用双柱定性。用另一根色谱柱(1.5%()V-17+1.95%QF-1/chromasnrhWAW-DMCS,80~100目)进行准确检验色谱分析,可确定各组分及有无干扰。5.4.3定量分析
5.4.3.1色谱峰的测量
以睡的起点和终点的联线作为峰底,以峰高极大值对时间轴作垂线,对应的时间即为保留时间,此线从峰顶至峰底间的线段即为峰高。5. 4. 3.2计算
式中:R,
样品中i组分农药的含量,mg/kgl样品中i组分农药的蜂高,cm(或峰面积cm),标样中1组分农药的绝对鹭,ng1-G(g)样品定容体积,mL
h—标样中组分农药的峰高,cm(或峰面积cm):一样品的进样盖,,
C—样品的重量8。
6结果的衰示
6.1定性结果
根据标准色谱图各组分的保留时间来确定被测试样中出现的组分数目和组分名称。6.2定量结果
6.2.1含量的表示方法根据5.4.3.2计算出的各组分的含量,以mg/kg表示。6.2.2精密度见表1。
6.2.3准确度见表2。
6.2.4检测限:当气相色谱仅仪器的灵敏度最大时,以噪音的2.0倍作为仪器的检测限,本方法要求仪器的最小检测量低于10-1g(见.表3)。173
重垂复性
墨复性
再现性
再现性
再现性
协作实验室数量
注H-商裱度;M
中浓度-
六六六
L - 0. 004
低浓度,
表1、精密度(重复性和再现性)民六六六
6.4×10°
了-六六六
H—0.200
E.= 0. 004
1.2×10-3
6. 9×10r2
1.9×10m*
2. 00×10-*
合六六
P·DDE
TI=0. 500
1. --0. 010
5. 0 × 10-
M -D, 200
6. 0×10+
8.1×10-2
(士壤样)
p-p'-non
4.0×10-1
tng/kg
4. 0×10*
8.6人101
14550—93
加人量
回收率,%
回收率
回收率,
协作实验室数量
α-六六
表2准确度(土壤样加标同收率,%)六六六
2-六六六
I. = D. D64
存六六六
1. =[0. 010
H= 0. 50)
L-[,010
L - 0. 020
pp'-DD
L = 0. 020
14550--
附加说明:
农药种类
0六六六
丫六六六
P-p'-DDE
OP'-TDT
GB/T14550—93
表3检测限
本标准由国家环境保护同科技标准司和农业部环能司提出。本标准出农业部环境保护科研监测所负责起草。品小检测母,
3. 577× 10~ :
2.523×1c22
1.190×10--2
9.770×10-a
1.756×102
6.96010*2
5.572×10-12
1.460×10-1s
本标准主要起草人黄上忠、陈国光,王继军、李治祥,张俊享、万兆良、袁秀文、玛秀琼。176
上壤和污泥中苯并(a)花的测定白然界:1壤中含有一系列多环芳香烃化合物,其中苯并(a)花已被公认为强烈的效痛物质,但它的人然本底很低,实际上作用并不明显。当土壤受到污染后,苯并(a)花含量发生变化,引起一系列较为复杂的致癌作用问题。因此.掌握不同条件下土壤中苯并(a)花量的变化规律性,对进一步评价与防治环境污染具有重要意义。
1原理
土壤中含有一系列多环劳香径化合物(PAH),成分复杂,含最很低。采用二步柱展析力法,其分离效果主要取决于吸附剂对PAH各组成的“吸附力”,以及“展开剂\对各组成分的“洗脱力”这两种相互矛盾和对立力量的相互作用。实践证明:采用吸附力较弱的吸附剂(>0.1mm中性层析氧化铝),结合洗脱力较弱的溶剂(环已烷)作为一级分离,再以较强吸附力的吸附剂(<0.1mm中性层析氧化铝),结合洗脱力较强的溶剂(12-二氯乙烷)作二级分离,可使PAH各组分达到较好分离,分离所得苯并(a)芪试样用紫外分光光度计进行定性和定量鉴定2仪器和试剂
2.1恒温水浴。
2.2国产中性层析氧化铝。
2. 3 孔径 0. 1 mm 筛网。
2.4内径1.0cm和0.5cm啵璃层析节,高度分为30cm和50cm。2.5氯仿(二氯用烷)A、R。
2.6坏烷(重蒸馅)。
2.」,2·二氯乙烷(重热馏)。2.83600%紫外灯。
2.9紫外分光光度计。
3土填中PAH的握取
为考虑有机落剂的安全与效果、通过对比试验,决定放弃举而采用氣作为土填凝提剂。取通过\.25tt1筛孔的七填试样20g,(两份,作平行测定),置于125mL三第瓶中,加氯仿50mL,加盖,用手轻轻振荡5min,静置过夜。第二天,将三角瓶置于50℃水浴继续提取1h,过滤。再加上50mL氯仿,照前振荡5min,骨于50C水裕继续提取1h,过滤,然后分别用25mL氯仿继续洗涤三角瓶中试样握合物二遍。滤液在同一个100mL的小玻璃撬杯或浓缩器中前后分三次用水浴进行蒸发,最后一次蒸发到杯底快处干时取下,马上用环已烷进行溶解,备分离纯化。4分离纯化
如果上壤中毕并(a)花含量>5g/kg+可采用两次氧化铝柱层与紫外分光法,如含鼠5/k,则采氧化铝柱层,纸层荧光分光法。4.1紫外分光法
4.1.1PAH的初级分离
取国产中性层析氧化,通过0.1mm筛孔滤去细颗粒(留作二级分离用),将筛网上的氧化铝,在F燥器挡板上铺-薄层,千燥器内用35%硫酸配制成70%左右的相对湿度:在此条件下平衡两叠夜以177
I.,便氧化铝含水率达了7.5左右,分离前将其装填于内径1rm层析管巾。图「为分离纯化示意图。
三氯甲烷浓缩强滴
敏化铝柱
黄外分光法鉴室
化组柱
最层析
荧光分光法定
图1分离纯化示意图
于内径1cm层析管中,要求氧化铝在层析管中装填时做到致密义均勺高度为20cm,然后加2ml环已烷于提取PAH的小烧杯中将残清溶解,并用滴管将此溶液滴入层析柱上端便其吸附,为避免损耗,再分别用0.5mL环已烷洗涤小烧杯两次,并将洗涨液一并滴人层析柱土端吸附。以同样操作做3的举并芪标准柱待吸附完毕后,再其上加人环已烷展开剂,在暗室中展开1h以L,并在3600%紫外光照射下观赛层析柱的分层情况,至明显分层止。注意发紫蓝色荧光的色层即为含行举并()范的色层,一般分层达再层以上(见图2)。.糖色
3.淡面啡色
3.蓝绿免蚁光
d.蓝紫色荧光
5.整绿色樊光
6.黄色荧光
图2一级分离系统程上荧光光谱示意图4.1.2PAH的-级分离
取内径0.5cm层析玻璃管.置于烘箱中,在100下烘干,将.上.述通过0.1mm筛孔的细氧化铝在使用前置于磁蒸发血内.在煤气灯上高温灼烧半小时以上,使其完全脱去水分,在未完全冷却时郎装人层析挂中,高度25cm左右,要求密实均勾。层析柱填装完毕后,将初级分离层析中发紫蓝色炭光的次,小心用锉刀锉断取出,并直接装人本层析柱的上谢,然后在层析普上端加人5mL1,2-二氯乙烷,在暗处展开半小时,于3600%紫外光下观察,至层析柱上各荧光色层充分分开为止(见图3)。1. 淡紫
血,淡螺
6. 亮紫荧冶
6. 亦素蓝
一搬分高翘望化铝
图3二级分离系统样上炎光光谱示意图与标准杜比较,挂出样品中发亮紫的色层即含苯并(a)花的(其中提取液在3600紫外线照射下发蓝紫荧光)荧光段。
将亮紫荧光层用锉刀小心取出,避免和上下连结的层次干扰,取出氧化铝,装人填有脱脂棉的玻璃178
漏斗中.以10mI.1,2-二氯乙烷分数次加增洗提,将提取于水浴上蒸于。最后准确助加5ml.坏己烷游解残清,文即在紫外分光光度计上测定350~410nm波段的吸收光谱曲线。苯并(a)诺在365m385日m,403几nI处有-三个待征波峰,可作为定性的参考依据。4. 1. 3标准苯并(a)芪溶液的标定感望0.1mg天平(用标推磁码进行校准)称取本并()范501g,落解:f:100L经过重蒸懈的坏己烷中+配成浓度为50μg/mL的母液.然后用微量吸管吸母液分别配制成浓度为2.4,8.10,20g/5Tml.的:·红标准溶液,在紫外分光光度计上分别测定350,365,375,385.403m处的光谢度值,以375+385395nm处的光密度值按基线法计算出385nm处的实际光密度俏,按式(1)计算:1 Is
aln)
式中:1、:385I处的实际光辫度值.a:--385nm处的光密度观察值:Im—375处的光密度观察值
us——3951m处的光密度观察值
........+..++++...I)
上式得出不同浓度标准来并(a)范在385.nm处的实际光密度值,以浓度为横坐标,光帮度为纵整标制备工作曲线。
为检查以上结果的准确性,重新配制一组浓度为5,10,20μg/5mL的苯并(a)标推穿液,测定它们在紫外光375~395nml被段的光密度值,用同样底线法求出实际光密度值。在浓度为0~20μg/5mL的范围内标准苯并(a)花浓度与波峰高度的光密度值为线性关系,4.1.4土壤中萃并(a)花的定型
土填中PAH的成分复杂,经过一步柱层分离所得萃并(a)花试样只能保持相对的纯度,而不能完全排除其他杂质干扰,故在紫外分光光度计上描记所得的吸收光谱曲线,常出现365nm波峰高于385nnl波峰的现象(因PAH中很多其他成分的吸收偏向紫外短波方面,致使365nm波峰增高)。因此,在实际小应以385nm的实际光密度值作为定量依据。并且要严格遵守下列规则:即为了排除杂质的十扰,位按照配制标准曲线时相同的\底线法”加以校正。将分离样品按“底线法\测得的实际光密度值,板据标准曲线求出土壤苯并(a)茂的相应含量。4.1.5结果计算
士澳莱并(a)按式(2)计算:
土境苯并(a)花含量(μR/kg)-号X1000
式中,Q—从标谁曲线聋得苯并(a)范的含量,W.-样品重屋,。
4.2荧光分光法
4.2.1氧化锯柱层分离
游中性70~2(00目的氧化铝于140~-160℃活化4~6h,装人内径1cm的玻璃中,要求致密均勾,商度5~cm。然后将土壤氯伤提取液的浓缩残渣用25ml.环己烷分次溶解,滴人氧化铝柱中,加压过滤,待过滤完毕,弃去下部环已烷接收液,再手住上加50mL重热苯,接收苯的洗脱获,瘀蟾后进行纸层分。
4.2.2纸层分离取乙酰化滤纸条.将以上苯的浓缩液定容取一定盘进行带状点样,点样究毕于乙醇-氮甲烷(2十1)展开液中密封、避光展开2-~3h,于3600紫外光下规察,与苯并(a)标准荧光斑点比较,划出样品巾苯井(a)花的荧光带.用剪刀剪下,置于5mL磨口指形管中,加2mL手醇加盖,于蜡处过夜·欲于50-~60水浴加热15~-20min冷却后备荧光测定。4.2.3光测定
在激发光波长386nm光带宽10nm,发射光带1.5tm的条件下测定395~440nt处的荧光光E79
谱,取406刀m处的荧光比谱峰作为计算峰,按“基线法”与标准获比较,计算出样品中举并a)比含量。同时应做空白试验,以同样条件做不同浓度0.02.0.04,0.06,0.08u/ml在400,406410nm处的荧
土壤中苯并()花含量按式(3)计算:土壤中苯并(a)芪含量(/kg)w
式中—标谁曲线苯并(a)薛的含,g/mL:W.----样品质画·&;
备点样液总体积,mL,
实际点样液体积,ml-;
5说明
样品纸层甲醇用盘,ml。
X 2 × 1 000
5.1PAH的各组分离效果,与氧化铝吸附剂的含水率即活性等级密切相关,一级分离用粗氧化销的在70%相对湿度下平衡时间保持两昼夜以上为宜,二级分离用细氧化铝必须在煤气灯上高溢烘烤卡小时以上.,以保证有足够的活性
5.2本方法中最难掌握的地方是在3600\紫外光下区分含苯并(a)花的炎光色层,有时容易滤滑,需要有一定的实毁经验才能准确尤误地得到所需要的分析结果。5.3苯并(a)花对光化学反应较强烈,样品的摄取、浓缩和分高操作需要在暗室中进行。180
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。