ICS11.040.30
中华人民共和国医药行业标准
YY0053—2016
代替YY0053—2008
血液透析及相关治疗
血液透析器、
血液透析滤过器、血液滤过器和血液浓缩器
Hemodialysis and relevant therapies-Haemodialysers,haemodiafiltershaemofiltersandhaemoconcentrators(ISO8637:2010,MOD)
2016-03-23发布
国家食品药品监督管理总局
2018-01-01实施
YY0053—2016
规范性引用文件
试验方法
标志·
附录A(资料性附录)
本标准与ISO8637:2010的技术性差异及其原因参考文献
本标准按照GB/T1.1一2009给出的规则起草。YY0053—-2016
本标准代替YY0053一2008《心血管植入物和人工器官血液透析器、血液透析滤过器、血液滤过器和血液浓缩器》。本标准与YY0053一2008的主要技术差异如下:根据国际标准的内容,筛选系数增加了2-微球蛋白,删除了透析液室压力降的要求,删除了多次使用器件的要求;
一根据国际标准的相关内容,对清除率、筛选系数的试验方法进行补充;根据国家相关法规规定,增加了化学性能及β2-微球蛋白清除率的内容,按国内通行的方法与项目进行检验,适合我国国情
血液透析器、血液透析滤过器、本标准修改采用ISO8637:2010《心血普植人物和体外循环系统血液滤过器和血液浓缩器》本标准与ISO8637:2010相比,主要差异见表A.1。请注意本文件的某些内容可能涉及专利。本文件的发布机构不承担识别这些专利的责任。本标准由国家食品药品监督管理总局提出。本标准由全国医用体外循环设备标准化技术委员会(SAC/TC158)归口。本标准起草单位:威海威高血液净化制品有限公司、国家食品药品监督管理总局广州医疗器械质量监督检验中心。
本标准主要起草人:吴静标、傅音波、何晓帆,牟倡骏。本标准首次发布于1991年,2008年第1次修订。I
HiiKAoNiKAca
1范围
血液透析及相关治疗血液透析器、血液透析滤过器、血液滤过器和血液浓缩器
YY0053—2016
本标准规定了在人体上使用的血液透析器,血液透析滤过器,血液滤过器和血液浓缩器的技术要求,在本文中涉及的“器件”特指上述产品。本标准不适用于:
体外循环血液管路;
血浆分离器;
一血液灌注装置;
血管通路装置;
血泵:
体外循环血液管路的压力监测器:空气监测器;
制备、供给和监控透析液的系统;用于进行血液透析,血液滤过或血液透析滤过治疗的系统:再处理步骤和设备。
注:血液透析器、血液透析滤过器和血液滤过器的体外循环血液管路的要求按照YY0267—2016的规定。2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB/T1962.2注射器、注射针及其他医疗器械6%(鲁尔)圆锥接头第2部分:锁定接头(GB/T1962.2--2001:ISO594-2.1998IDT))GB/T14233.1一2008医用输液、输血、注射器具检验方法第1部分:化学分析方法GB/T16886.1医疗器械生物学评价第1部分:风险管理过程中的评价与试验(GB/T16886.1-2011;ISO10993-1:2009,IDT)
中华人民共和国药典2010年版
3要求
3.1生物学评价
对于产品中与血液直接或间接接触的部分应进行生物学危害的评价3.2无菌
产品应经过一确认过的灭菌过程使之无菌。1
TiiKAoNnKAca
YY0053—2016
无热原
产品应无热原。
3.4机械性能
3.4.1结构密合性
血液透析器、血液透析滤过器、血液滤过器和血液浓缩器应无渗漏。产品的密合性应按下列条件进行确认:
按规定的最大正压的1.5倍,和;a)
按生产企业规定的最大负压的1.5倍,如超过93.3kPa(700mmHg),则应施加93.3kPab)
(700mmHg);若在高海拔地区应按4.5.1测试其可获得的最大负压。注:本要求针对的是器件的外部完整性。3.4.2血室密合性
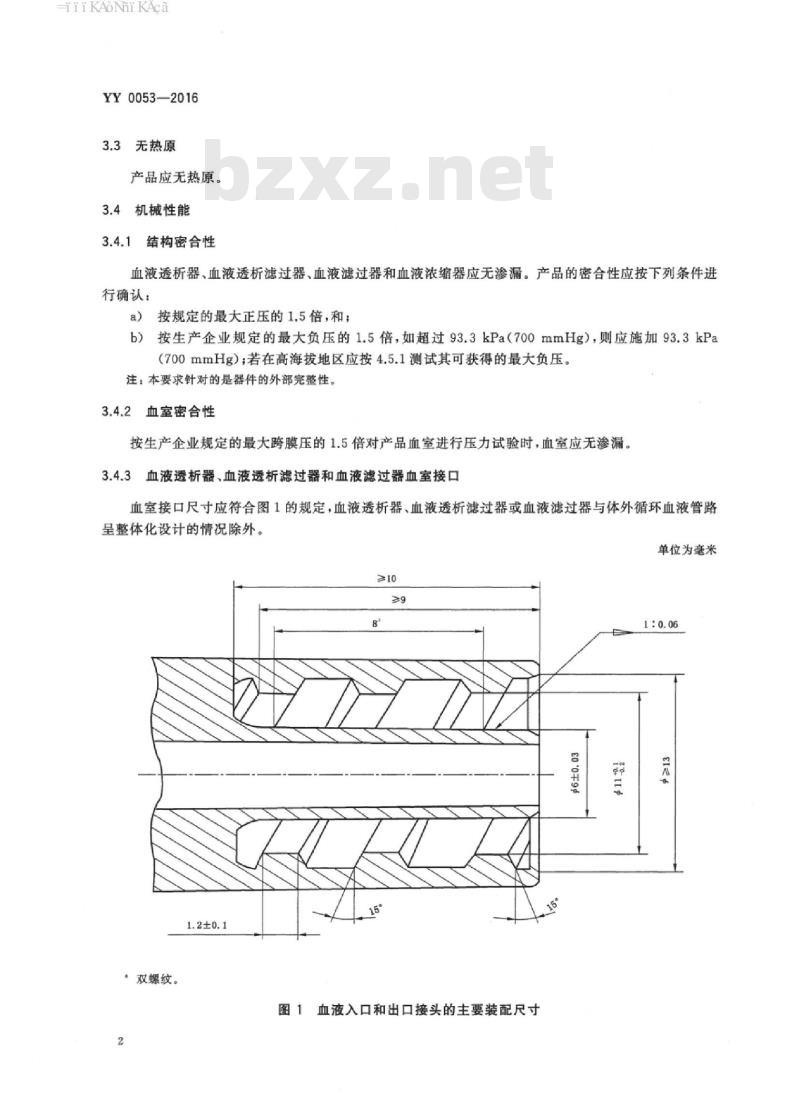
按生产企业规定的最大跨膜压的1.5倍对产品血室进行压力试验时,血室应无渗漏。3.4.3血液透析器、血液透析滤过器和血液滤过器血室接口血室接口尺寸应符合图1的规定,血液透析器、血液透析滤过器或血液滤过器与体外循环血液管路呈整体化设计的情况除外。
单位为毫米
00干99
双螺纹。
下载标准就来标准下载网图1血液入口和出口接头的主要装配尺寸A
HiiKAoNiAca
3.4.4血液透析器和血液透析滤过器透析液室接口YY0053-2016
透析液室接口尺寸应符合图2的规定,血液透析器,血液透析滤过器与透析液循环呈整体化设计的情况除外。
单位为毫米
1'0干#
10.2±0.1
13.1±0.1
图2透析液入口和出口的主要装配尺寸3.4.5血液滤过器滤过液接口
血液滤过器的滤过液接口应符合图2的规定或GB/T1962.2中鲁尔锥度锁定接头的要求。3.4.6血液浓缩器血液和滤过液接口血液浓缩器血液和滤过液的接口应能提供一个与配套使用产品可靠的连接。3.5使用性能
3.5.1血液透析器和血液透析滤过器的清除率3.5.1.1对尿素、肌酐、磷酸盐和维生素B12的清除率应符合生产企业的规定。血液及透析液的流速应覆盖生产企业规定的范围。
注:作为一个补充,可以包括K。A结果。3.5.1.2对于高通量透析器,应在临床常用血液流速(可以选择单一流量)下评价β2-微球蛋白的清除率,该试验不适用于出厂检验。3.5.2血液透析滤过器、血液滤过器和血液浓缩器的筛选系数白蛋白、菊粉和肌红蛋白或β2-微球蛋白的筛选系数应符合生产企业的规定。试验条件应按照生产企业给定的信息。
HiiKAoNiKAca
YY0053—2016
3.5.3超滤率
超滤率应符合生产厂的规定。试验应覆盖生产厂规定的跨膜压和血液流速的范围。3.5.4血室容量
血室容量应符合生产企业的规定,试验条件应覆盖生产企业规定的跨膜压范围。如果血室没有顺应性,确定在任一个特定的跨膜压下的容量都是可以接受的。3.5.5血室压力降
血室压力降应符合生产企业的规定。3.6化学性能
3.6.1还原物质(易氧化物)
20mL检验液和同批空白液消耗高锰酸钾溶液[c(KMnO.)=0.002mol/L]的体积之差应不超过2.0mL。
3.6.2金属离子
3.6.2.1原子吸收分光光度计
检验液与同批空白液pH之差应不超1.5。3.6.4蒸发残渣
50mL检验液蒸发残渣的总量应不超过2.0mg。3.6.5紫外吸光度
检验液的吸光度应不大于0.1。
3.6.6环氧乙烷残留量
产品用环氧乙烷气体灭菌时,其环氧乙烷残留量应不大于10mg/kg。3.7有效期
按照有效期的规定,产品的性能应在有效期内得到保证。4试验方法
4.1总则
在新产品投入市场之前和改型产品需要进行重新评价时,4.5中规定的使用性能的项目应预先确认。
试验所需的样品应在生产企业的合格品(经过所有的质量控制程序,并灭菌可使用的)中随机抽取。4
HiiKAoNiKAca
产品应按生产企业推荐的临床使用的要求准备好。YY0053-—2016
试验应在37℃士1℃的体外条件下进行。当各变量关系是非线性时,应进行充分测量以便在各数据间作插值法。本章给出的检测方法是仲裁试验方法。如可以证明其他的试验方法在精度和重现性方面具有可比性,则也可使用。
图示的各个测试装置并未标明所有切实可行的测试仪器的必要细节。实测装置的形式,结构以及安放情况也会带来许多引起检测误差的因素,包括(但不局限于)因静态压差效应和动态压力下降而引起的压力误差,参数稳定时间,在非恒定流率下的不可控制的温度变化,PH,热,光和时间引起的测试物质的降解,试验液的除气,收集的空气,以及因杂质、藻类和细菌引起对装置的污染等。4.2生物学评价
血液透析器,血液透析滤过器,血液滤过器和血液浓缩器直接或间接与病人的血液接触的部分应按GB/T16886.1的规定进行生物学评价。4.3无菌
4.3.1按中华人民共和国药典的规定进行,应符合3.2的规定。注:该方法不宜用于出厂检验。4.3.2适宜的灭菌方法参见相关标准。4.4无热原
应选择适当的试验方法来评价血液透析器,血液透析滤过器,血液滤过器和血液浓缩器的致热原性。按中华人民共和国药典的规定进行检验,应符合3.3的规定。4.5机械性能
4.5.1结构密合性
4.5.1.1总则
按4.5.1.2~4.5.1.3进行检测,应符合3.4.1的要求。4.5.1.2正压试验
将器件装满脱气蒸馅水,放置手37C土1C,除与压力测试装置连接的接口外,所有接口均应封闭。对产品施加一个生产企业规定压力1.5倍的正压,并封闭测试装置。10min后,记录压力值并目视检查产品是否有泄漏。
4.5.1.3负压试验
将器件装满脱气蒸馏水,放置于37℃士1℃,除与压力测试装置连接的接口外,所有接口均应封闭。对产品施加一个生产企业规定的压力1.5倍的负压;除非负压超过93.3kPa(700mmHg)或不作规定,此时应施加93.3kPa(700mmHg)负压并封闭测试装置。若在高海拔地区则施加可获得的最高负压值,10min后,记录压力值并目视检查产品是否有泄漏。4.5.2血室密合性
按生产企业规定的最大跨膜压的1.5倍对器件血室进行压力试验时,血室应无渗漏。4.5.3血液透析器,血液透析滤过器和血液滤过器血室接口用通用量具或专用量具进行检验,应符合3.4.3的要求。见图1和图3。5
iiiKAoNikAca
YY0053—2016
4.5.4血液透析器或血液透析滤过器透析液室接口目力检查,应符合3.4.4的要求。见图2。4.5.5血液滤过器滤过液接口
目力检查并按图2的要求或GB1962.2的要求,应符合3.4.5的要求。>9
说明:
外圆锥:
内圆锥。
820g-94
图3血液入口和出口接头内锥和外锥的啮合长度6血液浓缩器血液和滤过液接口
对器件施加15N静态轴向拉力,持续15s,不应发生分离,应符合3.4.6的要求。5使用性能
4.6.1清除率
4.6.1.1总则
按4.6.1.2~4.6.1.4进行检测,应符合3.5.1的要求。4.6.1.2试验液
单位为毫米
使用包含一种或几种试验物质(按表1中列出的物质)的模拟液(透析液、生理盐水、磷酸盐缓冲液或水)灌注血室。
使用透析液、生理盐水,磷酸盐缓冲液或水灌注血液透析器和血液透析滤过器透析液室。注1:灌注血室和透析液室的宜采用相近离子强度的溶液组分。注2:根据试验步骤的条件变化,按表1列出的溶液的摩尔浓度。列出的溶液只给出一个初始浓度。注3:3a-微球蛋白模拟液推荐采用抗凝牛血浆或者抗凝牛全血进行配制:β2-微球蛋白模拟液摩尔浓度由生产企业进行规定。
HiiKAoNiKAca
尿素/(mmol/L)
肌酐/(μmol/L)
磷酸盐/(mmol/L)
维生素Brz/(μmol/L)
4.6.1.3清除率试验步骤
表1试验液的标准浓度
500~1000
15,调节pH7.4士0.1
YY0053—2016
按图4装配试验回路。调节血液及透析液流率至稳定。确定温度、压力和超滤率平稳。在达到指定血液和透析液流率范围后,平稳运行一段时间后,收集样品。在每一个条件下均应进行超滤率的检测。进行样品分析,并按4.6.1.4中的式(1)进行清除率的计算。注1:虽然图4显示,液体是通过透析器或透析滤过器的底部进人血室,但本试验也可以设计为液体通过透析器或透析滤过器的顶部进人血室,只要通过血室和透析液室的液体是对流的,本实验也可设计为透析器或透析滤过器处于水平位置,只要证明这种布置能取得与透析器或透析滤过器处于垂直位置时同样的试验结果,注2:确定测试可靠性的可能方法是监测质量平衡误差。4.6.1.4清除率计算公式
对于血液透析和血液透析滤过,清除率K的计算应用式(1:K=
式中:
CBI-CBO
血液透析器或血液透析滤过器血液人口的溶液浓度;CBO——血液透析器或血液透析滤过器血液出口的溶液浓度;产品人口端的血液流率;
滤过液流率(超滤率)。
式(1)中,Cs和CBo采用的浓度单位相同。血液滤过器、血液透析滤过器和血液浓缩器的筛选系数4.6.2
4.6.2.1总则
按4.6.2.2~4.6.2.4进行检测,应符合3.5.2的要求。4.6.2.2试验液
首选的试验液为含蛋白浓度为60g/L士5g/L的抗凝牛血浆或者抗凝牛全血(血球压积为32%土3%和血浆蛋白浓度为60g/L士5g/L)使用3.5.2中列出的含一种或儿种溶质的试验液灌注血室。7
YY0053—2016
4.6.2.3试验步骤
按图5装配试验回路。调节血液及滤过液流率至稳定(包括温度、流率和压力)。调节超滤率的大小,以覆盖生产企业给定的范围,成对收集血液样品和滤过液样品,并按4.6.2.4中的式(2)进行筛选系数的计算。
注:虽然图4显示,液体是通过透析器或透析滤过器的底部进人血室,但本试验也可以设计为液体通过透析器或透析滤过器的顶部进入血室,本实验也可设计为透析器或透析滤过器处于水平位置,只要证明这种布置能取得与透析器或透析滤过器处于垂直位置时同样的试验结果。10
说明:
压力控制;
血液透析器;
带超滤控制的透析液供给装置:废液:
试验液;
血泵;
测量血液进口侧压力值P
测量血液出口侧压力值PBOi
测量透析液进口侧压力值力D:
测量透析液出口侧压力值PDO。
图4测定血液透析器或血液透析滤过器清除率的开环式装置示意图4.6.2.4筛选系数计算公式
CEr+CBO
##(2)
式中:
S—筛选系数;
血液透析滤过器、血液滤过器或血液浓缩器血液人口的溶液浓度CBO
血液透析滤过器、血液滤过器或血液浓缩器血液出口的溶液浓度;CF一血液透析滤过器、血液滤过器或血液浓缩器滤过液端的溶液浓度。式(2)中,CBrCBo和C采用的浓度单位相同。4.6.3超滤率
4.6.3.1试验液
YY0053—2016
透析器,透析滤过器,滤过器的试验液应为抗凝牛血或人血,蛋白浓度为60g/L土5g/L,血球压积为32%土3%。或蛋白浓度为60g/L土5g/L的新鲜抗凝牛血浆,血液浓缩器的试验液可以使用抗读牛血或人血,蛋白浓度为50g/L土5g/L,血球压积为25%士3%。不应用溶液灌注透析液室或滤过液室。4.6.3.2试验步骤
按图5装配试验回路。调节血液及滤过液流率至稳定(包括温度、流率和压力)。测量超滤率的大小,以覆盖生产厂给定的范围。按跨膜压从小到大的顺序测量超滤率的值。4.6.4血室容量
对于空心纤维透析器,腔室的容积按透析器尺寸和成束纤维的根数计算。如果已知膜的尺寸在接触过溶液之后发生显著变化,则应选择使用下列试验方法。作为另一种选择,用一种易于抽取但文不透过膜的溶液充满血室,测量充满血室的溶液的体积。按给定的跨膜压范围进行测量。如血室容量没有变化,则在单独一个压力下进行检测也是可以接受的4.6.5
血室压力降
4.6.5.1总则
按4.6.5.2~4.6.5.3试验方法进行检测,应符合3.5.5的要求4.6.5.2试验液
用蛋白浓度为60g/L士5g/L,血球压积为32%土3%。的抗凝牛血的试验液或相近黏度(如甘油水溶液或黄原胶/甘油溶液)的溶液充满血室。用一般透析液或生理盐水填充透析液室或滤过液室。4.6.5.3试验步骤
调整血液流率,读取血室出口压力值,计算压力降。按生产企业提供的血液流率范围重复上述检测。
对于平板型透析器,调整透析液流率,检测压力及血液流率也是必要的。9





 ✕
✕