YY/T 1443-2016
基本信息
标准号: YY/T 1443-2016
中文名称:甲型流感病毒抗原检测试剂盒(免疫层析法)
标准类别:医药行业标准(YY)
标准状态:现行
出版语种:简体中文
下载格式:.zip .pdf
下载大小:1707804

标准分类号
关联标准
出版信息
相关单位信息
标准简介
YY/T 1443-2016.Influenza A virus antigen detection kit( immunochromatographic assay).
YY/T 1443规定了甲型流感病毒抗原检测试剂盒(免疫层析法)的术语和定义,要求.实验方法.标识、标签、使用说明书.包装.运输和贮存。.
YY/T 1443适用于通过胶体金或乳胶颗粒等免疫层析法原理,定性检测呼吸道分泌物及其培养物中的甲型流感病毒,以快速检出甲型流感病毒抗原的诊断试剂盒。
YY/T 1443不适用于以酶相关的免疫层析法等为基本原理,用于甲型流感辅助诊断的试剂盒。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注8期的引用文件,其最新版本(包括所有的修改单)适用于本文件.
GB/T 191包装 储运图示标志
YY/T 0466.1医疗器械用于医疗 器械标签、标记和提供信息的符号第 1部分:通用要求
3术语和定义
以下术语和定义适用于本文件。
3.1
甲型流感病毒抗原检测试剂盒(免疫层析法) influenza A virus antigen detection kit ( immuno-chromatographic assay)应用免疫层析法的原理,检测人体呼吸道分泌物及其培养物中的甲型流感病毒抗原的试剂盒。
4要求
4.1物理性状
4.1.1外观
a)外包装应 整洁无污染。检测试剂应无破损、完整、无毛刺,材料附着牢固。
b)试剂盒组分应齐全,应包括前期处理流感病毒的液体组分及检测条(卡)等。
4.1.2膜条宽度
膜条宽度应不小于2.5 mm。
4.1.3液体移行速度
YY/T 1443规定了甲型流感病毒抗原检测试剂盒(免疫层析法)的术语和定义,要求.实验方法.标识、标签、使用说明书.包装.运输和贮存。.
YY/T 1443适用于通过胶体金或乳胶颗粒等免疫层析法原理,定性检测呼吸道分泌物及其培养物中的甲型流感病毒,以快速检出甲型流感病毒抗原的诊断试剂盒。
YY/T 1443不适用于以酶相关的免疫层析法等为基本原理,用于甲型流感辅助诊断的试剂盒。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注8期的引用文件,其最新版本(包括所有的修改单)适用于本文件.
GB/T 191包装 储运图示标志
YY/T 0466.1医疗器械用于医疗 器械标签、标记和提供信息的符号第 1部分:通用要求
3术语和定义
以下术语和定义适用于本文件。
3.1
甲型流感病毒抗原检测试剂盒(免疫层析法) influenza A virus antigen detection kit ( immuno-chromatographic assay)应用免疫层析法的原理,检测人体呼吸道分泌物及其培养物中的甲型流感病毒抗原的试剂盒。
4要求
4.1物理性状
4.1.1外观
a)外包装应 整洁无污染。检测试剂应无破损、完整、无毛刺,材料附着牢固。
b)试剂盒组分应齐全,应包括前期处理流感病毒的液体组分及检测条(卡)等。
4.1.2膜条宽度
膜条宽度应不小于2.5 mm。
4.1.3液体移行速度
标准图片预览




标准内容
ICS11.100
中华人民共和国医药行业标准
YY/T1443—2016
甲型流感病毒抗原检测试剂盒
(免疫层析法)
Influenza A virus antigen detection kit(immunochromatographic assay)2016-01-26发布
国家食品药品监督管理总局
2017-01-01实施
本标准按照GB/T1.1一2009给出的规则起草。YY/T1443—2016
请注意本文件的某些内容可能涉及专利。本文件的发布机构不承担识别这些专利的责任。本标准由国家食品药品监督管理总局提出,本标准由全国医用临床检验实验室和体外诊断系统标准化技术委员会(SAC/TC136)归口。本标准起草单位:中国食品药品检定研究院、广州万孚生物技术股份有限公司。本标准主要起草人:沈舒、石大伟、张春涛、黎梅兰。1范围
甲型流感病毒抗原检测试剂盒
(免疫层析法)
YY/T1443—2016
本标准规定了甲型流感病毒抗原检测试剂盒(免疫层析法)的术语和定义、要求、实验方法、标识、标签、使用说明书、包装、运输和贮存。本标准适用于通过胶体金或乳胶颗粒等免疫层析法原理,定性检测呼吸道分泌物及其培养物中的甲型流感病毒,以快速检出甲型流感病毒抗原的诊断试剂盒。本标准不适用于以酶相关的免疫层析法等为基本原理,用于甲型流感辅助诊断的试剂盒。2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB/T191包装储运图示标志
YY/T0466.1医疗器械用于医疗器械标签,标记和提供信息的符号第1部分:通用要求3术语和定义
以下术语和定义适用于本文件。3.1
甲型流感病毒抗原检测试剂盒(免疫层析法)influenza Avirusantigendetectionkit(immunochromatographic assay)
应用免疫层析法的原理,检测人体呼吸道分泌物及其培养物中的甲型流感病毒抗原的试剂盒。4要求
4.1物理性状
4.1.1外观
a)外包装应整洁无污染。检测试剂应无破损、完整、无毛刺,材料附着牢固。b)试剂盒组分应齐全,应包括前期处理流感病毒的液体组分及检测条(卡)等。4.1.2
2膜条宽度
膜条宽度应不小于2.5mm。
3液体移行速度
液体移行速度应不低于10mm/min。1
HiiKAoNiKAca
YY/T1443—2016
4.2阳性参考品符合率
用国家阳性参考品或经标化的阳性参考品进行检测,结果均应为甲型流感病毒抗原阳性。注:阳性参考品种类宜覆盖我国常见甲型流感病毒亚型包括季节性H1N1、H3N2、甲型H1N1等。3阴性参考品符合率
用国家阴性参考品或经标化的阴性参考品进行检测,结果均应为甲型流感病毒抗原阴性。注:阴性参考品种类宜覆盖乙型流感病毒及能引起相似呼吸道症状的其他病原体等。4.4最低检测限
用国家最低检测限参考品或经标化的最低检测限参考品进行检测,结果应符合最低检测限参考品相应要求。
4.5重复性
用国家重复性参考品或经标化的重复性参考品进行检测,结果应均为甲型流感病毒抗原阳性且显色度均一。
批间精密度
取3个批号试剂盒,对重复性进行检测,3个批号的试剂盒结果均应符合4.5的要求。4.7稳定性
可对效期稳定性和热稳定性进行验证。4.7.1效期稳定性
生产企业应规定产品的有效期。取到效期后一定时间内的产品,检验物理性状、阳性参考品符合率、阴性参考品符合率、最低检测限和重复性,结果应符合4.1、4.2、4.3、4.4、4.5的要求。4.7.2热稳定性试验
在规定条件下处理试剂盒,检验物理性状、阳性参考品符合率、阴性参考品符合率、最低检测限和重复性,结果应符合4.1、4.2、4.3、4.4、4.5的要求。注1:热稳定性试验不能用于推导产品有效期,除非是采用基于大量的稳定性研究数据建立的推导公式。注2:一般地,效期为1年时选择不超过1个月的产品,效期为半年时选择不超过半个月的产品,以此类推。但如超过规定时间,产品符合要求时也可以接受。注3:根据产品特性可选择4.7.1.4.7.2方法的任意组合,但所选用方法宜能验证产品的稳定性,以保证在效期内产品性能符合标准要求。
5试验方法
5.1物理性状
5.1.1外观
在自然光下以正常视力或矫正视力目视检查,应符合4.1.1要求。5.1.2膜条宽度
随机取试剂盒内1条膜条,使用游标卡尺测量其宽度,结果应符合4.1.2的要求。2
TiiKAoNiKAca
5.1.3液体移行速度
YY/T14432016
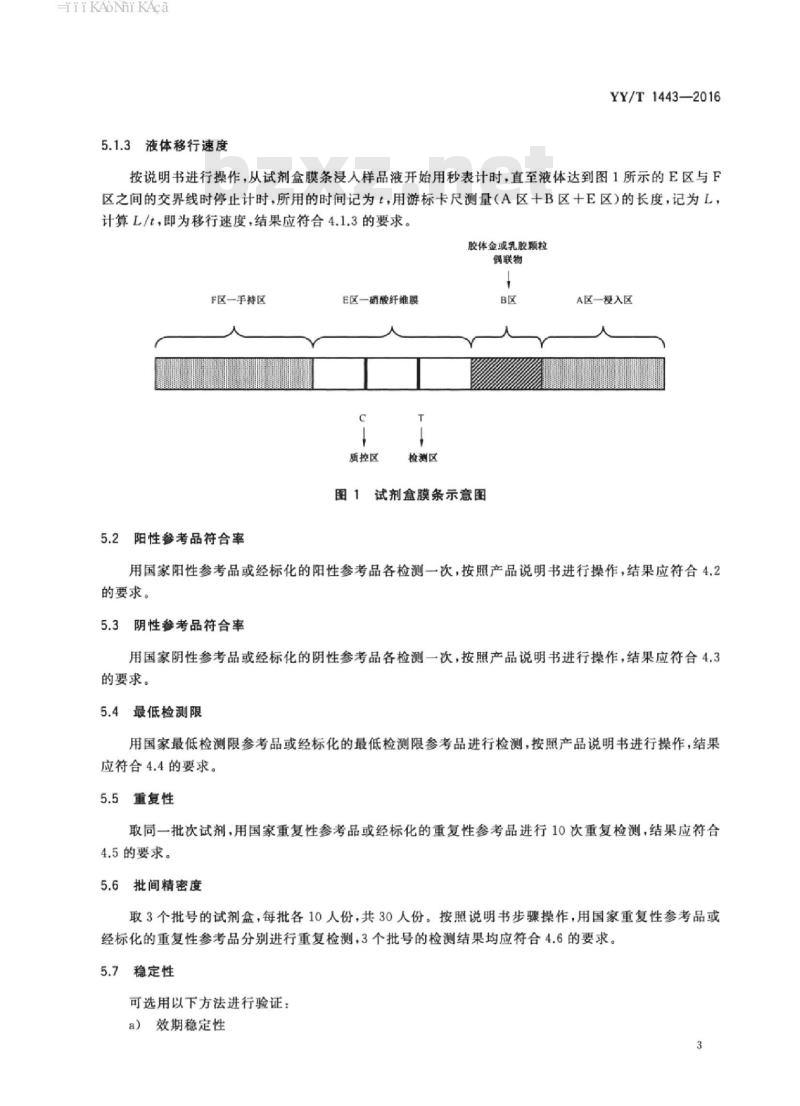
按说明书进行操作,从试剂盒膜条浸人样品液开始用秒表计时,直至液体达到图1所示的E区与F区之间的交界线时停止计时,所用的时间记为t,用游标卡尺测量(A区十B区十E区)的长度,记为L,计算L/t,即为移行速度,结果应符合4.1.3的要求。胶体金或乳胶颗粒
偶联物
F区一手持区
5.2阳性参考品符合率
E区一硝酸纤维膜
质控区
检测区
图1试剂盒膜条示意图
A区一浸入区
用国家阳性参考品或经标化的阳性参考品各检测一次,按照产品说明书进行操作,结果应符合4.2的要求。
5.3阴性参考品符合率
用国家阴性参考品或经标化的阴性参考品各检测一次,按照产品说明书进行操作,结果应符合4.3的要求。
5.4最低检测限
用国家最低检测限参考品或经标化的最低检测限参考品进行检测,按照产品说明书进行操作,结果应符合4.4的要求。
5.5重复性
取同一批次试剂,用国家重复性参考品或经标化的重复性参考品进行10次重复检测,结果应符合4.5的要求。
批间精密度
取3个批号的试剂盒,每批各10人份,共30人份。按照说明书步骤操作,用国家重复性参考品或经标化的重复性参考品分别进行重复检测,3个批号的检测结果均应符合4.6的要求。5.7稳定性
可选用以下方法进行验证:
a)效期稳定性
TiiKAoNiKAca
YY/T1443—2016
取到效期后一定时间内的产品,按产品说明书进行操作,结果应符合4.7.1的要求。b)
热稳定性试验
将试剂盒在一定温度条件下放置一定时间(通常为37C放置21d),按产品说明书进行操作,结果应符合4.7.2的规定。
6标识、标签和使用说明书
6.1试剂盒外包装标识标签
所使用的符号应满足YY/T0466.1的要求,至少应包含如下内容:a)产品名称及包装规格:Www.bzxZ.net
生产企业或售后服务单位的名称、地址、联系方式:b)
医疗器械注册证书编号:
产品标准编号;
e)产品批号:
失效期或有效期;
贮存条件。
试剂盒各组分包装标识,标签
所使用的符号应满足YY/T0466.1的要求,至少应包含如下内容:产品各组分名称和包装规格:
b)生产企业名称或标志:
c)产品批号:
失效期或有效期;
贮存条件。
6.3试剂盒使用说明书
所使用的符号应满足YY/T0466.1的要求,至少应包含如下内容:产品名称;
包装规格;
预期用途:
检验原理;
主要组成成分;
贮存条件及有效期;
适用仪器;
样本要求:
检验方法;
参考值(参考区间)):
检验结果的解释;
检验方法的局限性;
m)产品性能指标;
注意事项;
参考文献;
生产企业或售后服务单位的名称、地址、联系方式;HiiKAoNiKAca
医疗器械生产企业许可证编号(仅限于国有企业):医疗器械注册证书编号:
产品标准编号;
说明书批准及修改日期。
包装、运输、贮存
YY/T1443—2016
包装储运图示标志应符合GB/T191的规定。包装容器应保证密封性良好,完整,无泄漏,无破损。运输
试剂盒应按生产企业的要求运输。在运输过程中,应防潮,防止重物堆压,避免阳光直射和雨雪浸淋,防止与酸碱物质接触,防止内外包装破损。购存
试剂盒应在生产企业规定条件下保存。5
HiiKAoNiKAca
YY/T1443—2016
GB/T21415—2008
值的计量学溯源性
则,2011
GB/T9969.1—2008
GB/T18990—2008
参考文献
体外诊断医疗器械生物源性样品中量的测量校准品和控制物质赋工业产品使用说明书
促黄体生成素检测试纸(胶体金免疫层析法)中华人民共和国药典(2010年版三部)
YY/T1164—2009
人绒毛膜促性腺激素(HCG)检测试纸(胶体金免疫层析法)国家食品药品监督管理总局.流行性感冒病毒抗原检测试剂注册申报资料技术审评指导原
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
中华人民共和国医药行业标准
YY/T1443—2016
甲型流感病毒抗原检测试剂盒
(免疫层析法)
Influenza A virus antigen detection kit(immunochromatographic assay)2016-01-26发布
国家食品药品监督管理总局
2017-01-01实施
本标准按照GB/T1.1一2009给出的规则起草。YY/T1443—2016
请注意本文件的某些内容可能涉及专利。本文件的发布机构不承担识别这些专利的责任。本标准由国家食品药品监督管理总局提出,本标准由全国医用临床检验实验室和体外诊断系统标准化技术委员会(SAC/TC136)归口。本标准起草单位:中国食品药品检定研究院、广州万孚生物技术股份有限公司。本标准主要起草人:沈舒、石大伟、张春涛、黎梅兰。1范围
甲型流感病毒抗原检测试剂盒
(免疫层析法)
YY/T1443—2016
本标准规定了甲型流感病毒抗原检测试剂盒(免疫层析法)的术语和定义、要求、实验方法、标识、标签、使用说明书、包装、运输和贮存。本标准适用于通过胶体金或乳胶颗粒等免疫层析法原理,定性检测呼吸道分泌物及其培养物中的甲型流感病毒,以快速检出甲型流感病毒抗原的诊断试剂盒。本标准不适用于以酶相关的免疫层析法等为基本原理,用于甲型流感辅助诊断的试剂盒。2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB/T191包装储运图示标志
YY/T0466.1医疗器械用于医疗器械标签,标记和提供信息的符号第1部分:通用要求3术语和定义
以下术语和定义适用于本文件。3.1
甲型流感病毒抗原检测试剂盒(免疫层析法)influenza Avirusantigendetectionkit(immunochromatographic assay)
应用免疫层析法的原理,检测人体呼吸道分泌物及其培养物中的甲型流感病毒抗原的试剂盒。4要求
4.1物理性状
4.1.1外观
a)外包装应整洁无污染。检测试剂应无破损、完整、无毛刺,材料附着牢固。b)试剂盒组分应齐全,应包括前期处理流感病毒的液体组分及检测条(卡)等。4.1.2
2膜条宽度
膜条宽度应不小于2.5mm。
3液体移行速度
液体移行速度应不低于10mm/min。1
HiiKAoNiKAca
YY/T1443—2016
4.2阳性参考品符合率
用国家阳性参考品或经标化的阳性参考品进行检测,结果均应为甲型流感病毒抗原阳性。注:阳性参考品种类宜覆盖我国常见甲型流感病毒亚型包括季节性H1N1、H3N2、甲型H1N1等。3阴性参考品符合率
用国家阴性参考品或经标化的阴性参考品进行检测,结果均应为甲型流感病毒抗原阴性。注:阴性参考品种类宜覆盖乙型流感病毒及能引起相似呼吸道症状的其他病原体等。4.4最低检测限
用国家最低检测限参考品或经标化的最低检测限参考品进行检测,结果应符合最低检测限参考品相应要求。
4.5重复性
用国家重复性参考品或经标化的重复性参考品进行检测,结果应均为甲型流感病毒抗原阳性且显色度均一。
批间精密度
取3个批号试剂盒,对重复性进行检测,3个批号的试剂盒结果均应符合4.5的要求。4.7稳定性
可对效期稳定性和热稳定性进行验证。4.7.1效期稳定性
生产企业应规定产品的有效期。取到效期后一定时间内的产品,检验物理性状、阳性参考品符合率、阴性参考品符合率、最低检测限和重复性,结果应符合4.1、4.2、4.3、4.4、4.5的要求。4.7.2热稳定性试验
在规定条件下处理试剂盒,检验物理性状、阳性参考品符合率、阴性参考品符合率、最低检测限和重复性,结果应符合4.1、4.2、4.3、4.4、4.5的要求。注1:热稳定性试验不能用于推导产品有效期,除非是采用基于大量的稳定性研究数据建立的推导公式。注2:一般地,效期为1年时选择不超过1个月的产品,效期为半年时选择不超过半个月的产品,以此类推。但如超过规定时间,产品符合要求时也可以接受。注3:根据产品特性可选择4.7.1.4.7.2方法的任意组合,但所选用方法宜能验证产品的稳定性,以保证在效期内产品性能符合标准要求。
5试验方法
5.1物理性状
5.1.1外观
在自然光下以正常视力或矫正视力目视检查,应符合4.1.1要求。5.1.2膜条宽度
随机取试剂盒内1条膜条,使用游标卡尺测量其宽度,结果应符合4.1.2的要求。2
TiiKAoNiKAca
5.1.3液体移行速度
YY/T14432016
按说明书进行操作,从试剂盒膜条浸人样品液开始用秒表计时,直至液体达到图1所示的E区与F区之间的交界线时停止计时,所用的时间记为t,用游标卡尺测量(A区十B区十E区)的长度,记为L,计算L/t,即为移行速度,结果应符合4.1.3的要求。胶体金或乳胶颗粒
偶联物
F区一手持区
5.2阳性参考品符合率
E区一硝酸纤维膜
质控区
检测区
图1试剂盒膜条示意图
A区一浸入区
用国家阳性参考品或经标化的阳性参考品各检测一次,按照产品说明书进行操作,结果应符合4.2的要求。
5.3阴性参考品符合率
用国家阴性参考品或经标化的阴性参考品各检测一次,按照产品说明书进行操作,结果应符合4.3的要求。
5.4最低检测限
用国家最低检测限参考品或经标化的最低检测限参考品进行检测,按照产品说明书进行操作,结果应符合4.4的要求。
5.5重复性
取同一批次试剂,用国家重复性参考品或经标化的重复性参考品进行10次重复检测,结果应符合4.5的要求。
批间精密度
取3个批号的试剂盒,每批各10人份,共30人份。按照说明书步骤操作,用国家重复性参考品或经标化的重复性参考品分别进行重复检测,3个批号的检测结果均应符合4.6的要求。5.7稳定性
可选用以下方法进行验证:
a)效期稳定性
TiiKAoNiKAca
YY/T1443—2016
取到效期后一定时间内的产品,按产品说明书进行操作,结果应符合4.7.1的要求。b)
热稳定性试验
将试剂盒在一定温度条件下放置一定时间(通常为37C放置21d),按产品说明书进行操作,结果应符合4.7.2的规定。
6标识、标签和使用说明书
6.1试剂盒外包装标识标签
所使用的符号应满足YY/T0466.1的要求,至少应包含如下内容:a)产品名称及包装规格:Www.bzxZ.net
生产企业或售后服务单位的名称、地址、联系方式:b)
医疗器械注册证书编号:
产品标准编号;
e)产品批号:
失效期或有效期;
贮存条件。
试剂盒各组分包装标识,标签
所使用的符号应满足YY/T0466.1的要求,至少应包含如下内容:产品各组分名称和包装规格:
b)生产企业名称或标志:
c)产品批号:
失效期或有效期;
贮存条件。
6.3试剂盒使用说明书
所使用的符号应满足YY/T0466.1的要求,至少应包含如下内容:产品名称;
包装规格;
预期用途:
检验原理;
主要组成成分;
贮存条件及有效期;
适用仪器;
样本要求:
检验方法;
参考值(参考区间)):
检验结果的解释;
检验方法的局限性;
m)产品性能指标;
注意事项;
参考文献;
生产企业或售后服务单位的名称、地址、联系方式;HiiKAoNiKAca
医疗器械生产企业许可证编号(仅限于国有企业):医疗器械注册证书编号:
产品标准编号;
说明书批准及修改日期。
包装、运输、贮存
YY/T1443—2016
包装储运图示标志应符合GB/T191的规定。包装容器应保证密封性良好,完整,无泄漏,无破损。运输
试剂盒应按生产企业的要求运输。在运输过程中,应防潮,防止重物堆压,避免阳光直射和雨雪浸淋,防止与酸碱物质接触,防止内外包装破损。购存
试剂盒应在生产企业规定条件下保存。5
HiiKAoNiKAca
YY/T1443—2016
GB/T21415—2008
值的计量学溯源性
则,2011
GB/T9969.1—2008
GB/T18990—2008
参考文献
体外诊断医疗器械生物源性样品中量的测量校准品和控制物质赋工业产品使用说明书
促黄体生成素检测试纸(胶体金免疫层析法)中华人民共和国药典(2010年版三部)
YY/T1164—2009
人绒毛膜促性腺激素(HCG)检测试纸(胶体金免疫层析法)国家食品药品监督管理总局.流行性感冒病毒抗原检测试剂注册申报资料技术审评指导原
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。