YY 0115-1993
标准分类号
关联标准
出版信息
相关单位信息
标准简介
YY 0115-1993.
3.2产品 标记
符合本标准要求、出气器件与采血器分离的采血器产品标记为:
采血器TK-S YY 0115
符合本标准要求、出气器件与采血器为一体的采血器产品标记为:
采血器TK-C YY 0115
4技术要求
4.1使用性能 .
4.1.1尺寸
4.1.1.1采血 器瓶塞穿刺针针管长度应不小于35mm,外径应不小于2. 0mm,内径应不小于外径的70%。
4.1.1.2采血器的出气针针管长度应不大于25mm ,外径应不大于1. 6mm,内径应不小于0.9mm.
4.1.1.3采血器的采血针针管长度应不小于35mm,外径应不大于2.0mm,内径应不小于外径的70%。
4.1.1.4采血器软管长度应不小于600mm ,软管内径应不小于2. 7mm.壁厚应不小于0. 5mm.
4.1.2 外观
4.1.2.1采血器软管应柔软透明.光洁,无明显机械杂质.异物、扭结,其透明度应能保证发现气泡和回血。
4.1.22瓶塞穿刺针与采血针内外表面应光洁。
4.1.23采 血针针尖应锋利、无毛边、毛刺和弯钩。
4.1.3出气器件
采血器的出气器件应装有阻止空气中尘埃进入采血容器的空气过滤器。
4.1.4采血器针柄应有针尖斜面方向的指示标记。
4.1.5 密合性
采血器内腔通入高于大气压力50kPa的气压,15s内不应泄漏。
4.1.6连接牢固性
4.1.6.1采血 器各连接处应能承受20N的静态轴向拉力,持缕15s,不断裂和脱落。
4.1.6.2采血器的瓶塞穿刺针针管与针柄之间的接合处应能承受90N的轴向拉力15s不脱落或松
4.1.7微粒含量
采血器内腔应洁净,00mL洗脱液中,15~25um微粒数不得超过300个,大于25μm的微粒数不得超过100个。
4.1.8保护套.
采血器各出入口应有保护套。
3.2产品 标记
符合本标准要求、出气器件与采血器分离的采血器产品标记为:
采血器TK-S YY 0115
符合本标准要求、出气器件与采血器为一体的采血器产品标记为:
采血器TK-C YY 0115
4技术要求
4.1使用性能 .
4.1.1尺寸
4.1.1.1采血 器瓶塞穿刺针针管长度应不小于35mm,外径应不小于2. 0mm,内径应不小于外径的70%。
4.1.1.2采血器的出气针针管长度应不大于25mm ,外径应不大于1. 6mm,内径应不小于0.9mm.
4.1.1.3采血器的采血针针管长度应不小于35mm,外径应不大于2.0mm,内径应不小于外径的70%。
4.1.1.4采血器软管长度应不小于600mm ,软管内径应不小于2. 7mm.壁厚应不小于0. 5mm.
4.1.2 外观
4.1.2.1采血器软管应柔软透明.光洁,无明显机械杂质.异物、扭结,其透明度应能保证发现气泡和回血。
4.1.22瓶塞穿刺针与采血针内外表面应光洁。
4.1.23采 血针针尖应锋利、无毛边、毛刺和弯钩。
4.1.3出气器件
采血器的出气器件应装有阻止空气中尘埃进入采血容器的空气过滤器。
4.1.4采血器针柄应有针尖斜面方向的指示标记。
4.1.5 密合性
采血器内腔通入高于大气压力50kPa的气压,15s内不应泄漏。
4.1.6连接牢固性
4.1.6.1采血 器各连接处应能承受20N的静态轴向拉力,持缕15s,不断裂和脱落。
4.1.6.2采血器的瓶塞穿刺针针管与针柄之间的接合处应能承受90N的轴向拉力15s不脱落或松
4.1.7微粒含量
采血器内腔应洁净,00mL洗脱液中,15~25um微粒数不得超过300个,大于25μm的微粒数不得超过100个。
4.1.8保护套.
采血器各出入口应有保护套。
标准图片预览



标准内容
中华人民共和国医药行业标准
一次性使用采血器
本标准参照采用国际标准1SO1135-3:1987《次性使用采血器》。主题内容与适用范围bzxZ.net
YY 0115—93
本标准规定了次性使用采血器的产品分类、技术要求、试验方法、检验规则和标志、包装、运输、贮存的要求。
本标准适用于以聚氯乙烯为主要原料的一次性使用采血器(以下简称“采血器”)。2引用标准
GB2828逐批检查计数抽样程序及抽样表(适用于连续批的检查)GB2829周期检查计数抽样程序及抽样表(适用于生产过程稳定性的检查)GB8368一次性使用输液器
GB/T14233.1医用输液、输血、注射器具检验方法第一部分:化学分析方法GB/T14233.2医用输液、输血、注射器具检验方法第二部分:生物试验方法ZBC48006医用高分子制品包装、标志、运输和贮存3产品分类
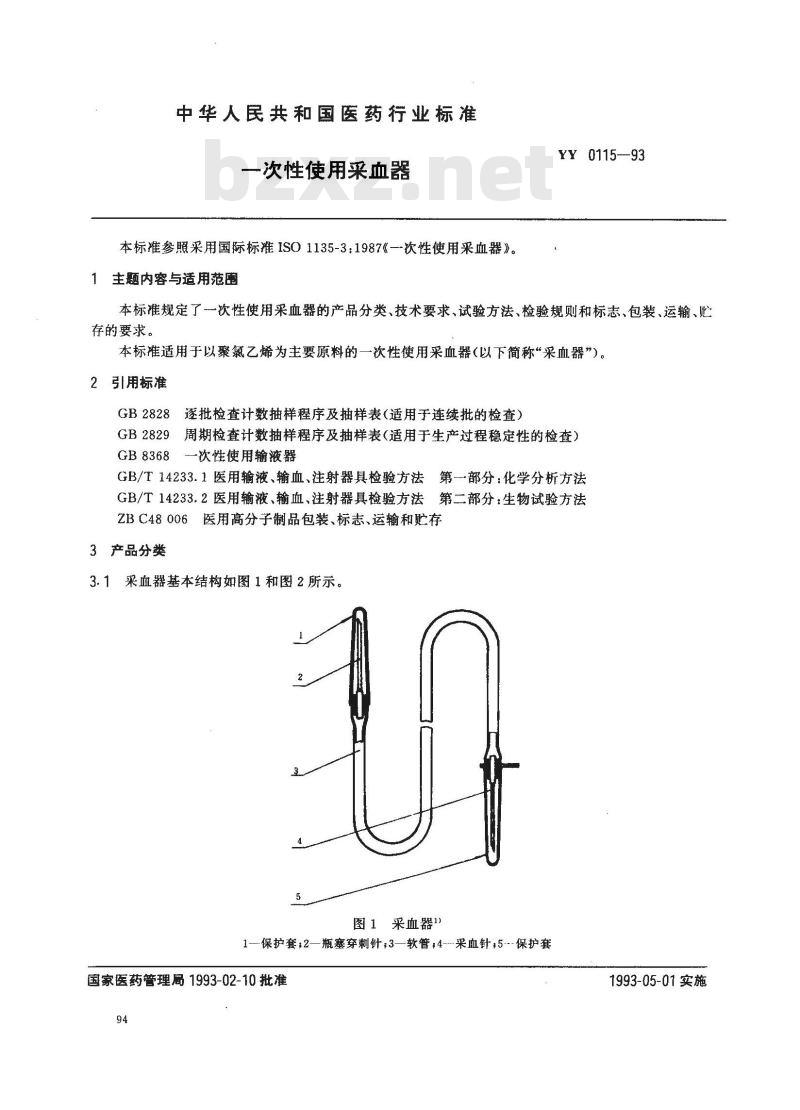
3.1采血器基本结构如图1和图2所示。图1采血器1)
1—保护套;2—瓶塞穿刺针,3—软管;4-采血针,5-保护套国家医药管理厨1993-02-10批准94
1993-05-01实施
YY 0115—93
88888888
图2出气器件2
1---空气过滤器,2—软管3-出气针:4保护套注:1)本示意图仅说明采血器的结构,并非为本标准规定的唯一型式。2)出气器件可与采血器的瓶塞穿刺针为一体。3.2产品标记
符合本标准要求、出气器件与采血器分离的采血器产品标记为:采血器TK-SYY0115
符合本标准要求、出气器件与采血器为体的采血器产品标记为:采血器TK-CYY0115
4技术要求
4.1使用性能
4.1.1尺寸
4.1.1.1采血器瓶塞穿刺针针管长度应不小于35mm,外径应不小于2.0mm,内径应不小于外径的70%。
4.1.1.2采血器的出气针针管长度应不大于25mm,外径应不大于1.6mm,内径应不小于0.9mm。4.1.1.3采血器的采血针针管长度应不小于35mm,外径应不大于2.0mm,内径应不小于外径的70%。
4.1.1.4采血器软管长度应不小于600mm,软管内径应不小于2.7mm。壁厚应不小于0.5mm。4.1.2外观
4.1.2.1采血器软管应柔软、透明、光洁,无明显机械杂质、异物、扭结,其透明度应能保证发现气泡和回血。
4.1.2.2瓶塞穿刺针与采血针内外表面应光洁。4.7.2.3采血针针尖应锋利、无毛边、毛刺和弯钩。4.1.3出气器件
采血器的出气器件应装有阻止空气中尘埃进入采血容器的空气过滤器。4.1.4采血器针柄应有针尖斜面方向的指示标记。4.1.5密合性
采血器内腔通人高于大气压力50kPa的气压,15s内不应泄漏。4.1.6连接牢固性
4.1.6.1采血器各连接处应能承受20N的静态轴向拉力,持续15s,不断裂和脱落。4.1.6.2采血器的瓶塞穿刺针针管与针柄之间的接合处应能承受90N的轴向拉力15s不脱落或松动。
4.1.7微粒含量
采血器内腔应洁净,200mL洗脱液中,15~25μm微粒数不得超过300个,大于25μm的微粒数不得超过100个。
4.1.8保护套
采血器各出入口应有保护套。
4.2溶出液化学性能
4.2.1还原物质
YY 0115--93
采血器溶出液20mL与同量空白对照液相比较,0.02mol/L的高锰酸钾消耗量不应超过1.5mL。4.2.2重金属
采血器溶出液所呈现的颜色不得超过空白对照液的颜色。4.2.3酸碱度
采血器溶出液与同批空白对照液作对照,pH值之差不得超过1.5。4.2.4不挥发物
采血器100mL溶出液中,不挥发物总量不得超过2mg。4.2.5氯化物
采血器溶出液所现的浑浊程度不得超过同量标准液所呈现的浑浊程度,标准液中氯离子的含量为 3μg/mL。
4.3采血器生物性能
4.3.1采血器应无菌,无菌有效期应不少于两年。4.3.2采血器应无热原。
4.3.3采血器应无异常毒性。
4.3.4采血器应无溶血作用。
4.3.5采血器环氧乙烷残留量每支应不大于0.5mg。5试验方法
5.1尺寸
以通用量具或专用量具检验。
5.2外观
5.2.1采血器软管、瓶塞穿刺针和采血针内外表面外观质量以目力检验。5.2.2将采血器的采血针在脱脂棉上拖拉,不得拉出纤维。5.3密合性
采血器各端封闭,通入50kPa气压,浸入20~30℃的水中15s,观察有无气泡溢出。5.4连接牢固性
5.4.1采血器一端固定,另一端施加20N的静态轴向拉力,持续15s。5.4.2将瓶塞穿刺针针柄固定,对针管施加90N的静态轴向拉力,持续15s,应符合5.3条规定。5.5微粒含量
按GB8368的附录 B进行。
5.6溶出液化学性能
按GB/T14233.1中对管状样品规定的方法进行。5.7生物性能
按GB/T14233.2规定的方法进行,其中环氧乙烷残留量按GB8368附录C进行。6检验规则
6.1采血器须经制造厂技术检验部门进行检查,合格后方可提交验收。6.2采血器必须成批提交检查,检查分为逐批检查和周期检查。6.3逐批检查
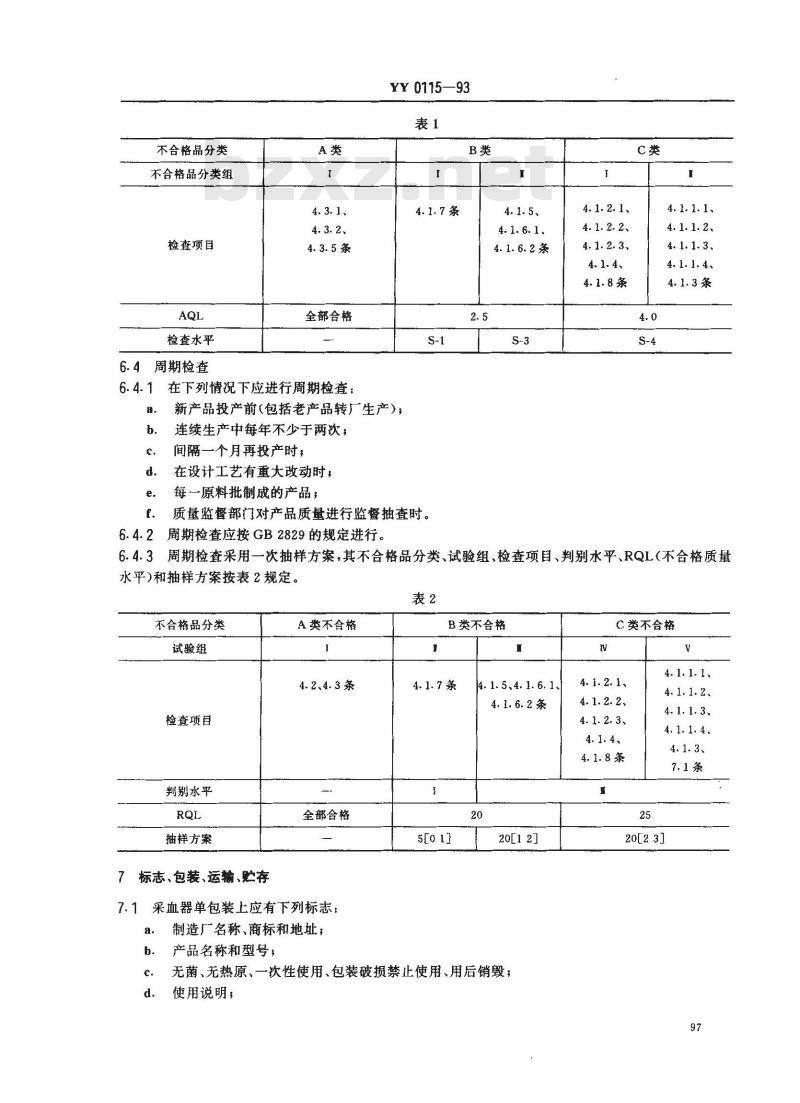
6.3.1逐批检查应按GB2828规定进行。6.3.2抽样方案严格性从正常检查抽样方案开始,其不合格品分类、检查项目、AQL(合格质量水乎)和检查水平按表1规定。
不合格品分类
不合格品分类组
检查项目
检查水平
6.4周期检查
全部合格
6.4.1在下列情况下应进行周期检查:a.
YY0115—93
4.1. 6.1.
4.1.6.2条
新产品投产前(包括老产品转厂生产),连续生产中每年不少于两次;
间隔一个月再投产时;
在设计工艺有重大改动时:
每一原料批制成的产品,
质量监督部门对产品质量进行监督抽查时。6.4.2周期检查应按GB2829的规定进行。S-3
4.1.2.1、
4.1.2.2、
4.1.2.3、
4. 1. 1. 1.
4.1.1.2、
4. 1. 1.3.
6.4.3周期检查采用一次抽样方案,其不合格品分类、试验组、检查项目、判别水平、RQL(不合格质量水平)和抽样方案按表2规定。
不合格品分类
试验组
检查项目
判别水平
抽样方案
标志、包装、运输、贮存
A类不合格
4.2、4.3条
全部合格
采血器单包装上应有下列标志:a.
制造厂名称、商标和地址;
产品名称和型号,
B类不合格
4.1.5、4.1.6.1
4.1.6.2条
20[12]
无菌、无热原、一次性使用、包装破损禁止使用、用后销毁;使用说明:
C类不合格
4. 1. 2. 1、
4. 1. 2. 2、
4.1.2.3、
4. 1. 1. 1.
4. 1. 1. 2、
4.1.1.3、
4. 1. 1, 4、
20[2 3]
YY0115—93
生产批号(以前六位数字表示年、月、日)或生产日期,f.
有效期。
其他要求应符合ZBC48006的规定。检验合格证不应装在单包装内。附加说明:
本标准由全国医用输液器具标准化技术委员会提出。本标准由国家医药管理局医用高分子产品质量检测中心负责起草。本标准主要起草人吴平、施燕平、林红。98
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
一次性使用采血器
本标准参照采用国际标准1SO1135-3:1987《次性使用采血器》。主题内容与适用范围bzxZ.net
YY 0115—93
本标准规定了次性使用采血器的产品分类、技术要求、试验方法、检验规则和标志、包装、运输、贮存的要求。
本标准适用于以聚氯乙烯为主要原料的一次性使用采血器(以下简称“采血器”)。2引用标准
GB2828逐批检查计数抽样程序及抽样表(适用于连续批的检查)GB2829周期检查计数抽样程序及抽样表(适用于生产过程稳定性的检查)GB8368一次性使用输液器
GB/T14233.1医用输液、输血、注射器具检验方法第一部分:化学分析方法GB/T14233.2医用输液、输血、注射器具检验方法第二部分:生物试验方法ZBC48006医用高分子制品包装、标志、运输和贮存3产品分类
3.1采血器基本结构如图1和图2所示。图1采血器1)
1—保护套;2—瓶塞穿刺针,3—软管;4-采血针,5-保护套国家医药管理厨1993-02-10批准94
1993-05-01实施
YY 0115—93
88888888
图2出气器件2
1---空气过滤器,2—软管3-出气针:4保护套注:1)本示意图仅说明采血器的结构,并非为本标准规定的唯一型式。2)出气器件可与采血器的瓶塞穿刺针为一体。3.2产品标记
符合本标准要求、出气器件与采血器分离的采血器产品标记为:采血器TK-SYY0115
符合本标准要求、出气器件与采血器为体的采血器产品标记为:采血器TK-CYY0115
4技术要求
4.1使用性能
4.1.1尺寸
4.1.1.1采血器瓶塞穿刺针针管长度应不小于35mm,外径应不小于2.0mm,内径应不小于外径的70%。
4.1.1.2采血器的出气针针管长度应不大于25mm,外径应不大于1.6mm,内径应不小于0.9mm。4.1.1.3采血器的采血针针管长度应不小于35mm,外径应不大于2.0mm,内径应不小于外径的70%。
4.1.1.4采血器软管长度应不小于600mm,软管内径应不小于2.7mm。壁厚应不小于0.5mm。4.1.2外观
4.1.2.1采血器软管应柔软、透明、光洁,无明显机械杂质、异物、扭结,其透明度应能保证发现气泡和回血。
4.1.2.2瓶塞穿刺针与采血针内外表面应光洁。4.7.2.3采血针针尖应锋利、无毛边、毛刺和弯钩。4.1.3出气器件
采血器的出气器件应装有阻止空气中尘埃进入采血容器的空气过滤器。4.1.4采血器针柄应有针尖斜面方向的指示标记。4.1.5密合性
采血器内腔通人高于大气压力50kPa的气压,15s内不应泄漏。4.1.6连接牢固性
4.1.6.1采血器各连接处应能承受20N的静态轴向拉力,持续15s,不断裂和脱落。4.1.6.2采血器的瓶塞穿刺针针管与针柄之间的接合处应能承受90N的轴向拉力15s不脱落或松动。
4.1.7微粒含量
采血器内腔应洁净,200mL洗脱液中,15~25μm微粒数不得超过300个,大于25μm的微粒数不得超过100个。
4.1.8保护套
采血器各出入口应有保护套。
4.2溶出液化学性能
4.2.1还原物质
YY 0115--93
采血器溶出液20mL与同量空白对照液相比较,0.02mol/L的高锰酸钾消耗量不应超过1.5mL。4.2.2重金属
采血器溶出液所呈现的颜色不得超过空白对照液的颜色。4.2.3酸碱度
采血器溶出液与同批空白对照液作对照,pH值之差不得超过1.5。4.2.4不挥发物
采血器100mL溶出液中,不挥发物总量不得超过2mg。4.2.5氯化物
采血器溶出液所现的浑浊程度不得超过同量标准液所呈现的浑浊程度,标准液中氯离子的含量为 3μg/mL。
4.3采血器生物性能
4.3.1采血器应无菌,无菌有效期应不少于两年。4.3.2采血器应无热原。
4.3.3采血器应无异常毒性。
4.3.4采血器应无溶血作用。
4.3.5采血器环氧乙烷残留量每支应不大于0.5mg。5试验方法
5.1尺寸
以通用量具或专用量具检验。
5.2外观
5.2.1采血器软管、瓶塞穿刺针和采血针内外表面外观质量以目力检验。5.2.2将采血器的采血针在脱脂棉上拖拉,不得拉出纤维。5.3密合性
采血器各端封闭,通入50kPa气压,浸入20~30℃的水中15s,观察有无气泡溢出。5.4连接牢固性
5.4.1采血器一端固定,另一端施加20N的静态轴向拉力,持续15s。5.4.2将瓶塞穿刺针针柄固定,对针管施加90N的静态轴向拉力,持续15s,应符合5.3条规定。5.5微粒含量
按GB8368的附录 B进行。
5.6溶出液化学性能
按GB/T14233.1中对管状样品规定的方法进行。5.7生物性能
按GB/T14233.2规定的方法进行,其中环氧乙烷残留量按GB8368附录C进行。6检验规则
6.1采血器须经制造厂技术检验部门进行检查,合格后方可提交验收。6.2采血器必须成批提交检查,检查分为逐批检查和周期检查。6.3逐批检查
6.3.1逐批检查应按GB2828规定进行。6.3.2抽样方案严格性从正常检查抽样方案开始,其不合格品分类、检查项目、AQL(合格质量水乎)和检查水平按表1规定。
不合格品分类
不合格品分类组
检查项目
检查水平
6.4周期检查
全部合格
6.4.1在下列情况下应进行周期检查:a.
YY0115—93
4.1. 6.1.
4.1.6.2条
新产品投产前(包括老产品转厂生产),连续生产中每年不少于两次;
间隔一个月再投产时;
在设计工艺有重大改动时:
每一原料批制成的产品,
质量监督部门对产品质量进行监督抽查时。6.4.2周期检查应按GB2829的规定进行。S-3
4.1.2.1、
4.1.2.2、
4.1.2.3、
4. 1. 1. 1.
4.1.1.2、
4. 1. 1.3.
6.4.3周期检查采用一次抽样方案,其不合格品分类、试验组、检查项目、判别水平、RQL(不合格质量水平)和抽样方案按表2规定。
不合格品分类
试验组
检查项目
判别水平
抽样方案
标志、包装、运输、贮存
A类不合格
4.2、4.3条
全部合格
采血器单包装上应有下列标志:a.
制造厂名称、商标和地址;
产品名称和型号,
B类不合格
4.1.5、4.1.6.1
4.1.6.2条
20[12]
无菌、无热原、一次性使用、包装破损禁止使用、用后销毁;使用说明:
C类不合格
4. 1. 2. 1、
4. 1. 2. 2、
4.1.2.3、
4. 1. 1. 1.
4. 1. 1. 2、
4.1.1.3、
4. 1. 1, 4、
20[2 3]
YY0115—93
生产批号(以前六位数字表示年、月、日)或生产日期,f.
有效期。
其他要求应符合ZBC48006的规定。检验合格证不应装在单包装内。附加说明:
本标准由全国医用输液器具标准化技术委员会提出。本标准由国家医药管理局医用高分子产品质量检测中心负责起草。本标准主要起草人吴平、施燕平、林红。98
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
