YY 0321.2-2009
基本信息
标准号: YY 0321.2-2009
中文名称:一次性使用麻醉用针
标准类别:医药行业标准(YY)
标准状态:现行
出版语种:简体中文
下载格式:.zip .pdf
下载大小:829595

标准分类号
关联标准
出版信息
相关单位信息
标准简介
YY 0321.2-2009.Single use needle for anaesthesia.
YY0321的本部分规定了公称外径为0.4mm~2.1mm的用于人体硬脊膜外腔神经阻滞(简称硬膜外麻醉)、蛛网膜下腔阻滞(简称腰椎麻醉)、硬膜外和腰椎联合麻醉、神经阻滯局部麻醉进行穿刺、注射药物的一次性使用麻醉用针(以下简称麻醉用针)的要求。
2规范性引用文件
下列文件中的条款,通过YY0321本部分的引用而成为本部分的条款,凡是注日期引用文件,其随后的所有修改单(不包括勘误的内容)或修订版均不适用于本部分,然而,鼓励根据本部分达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本部分。
GB/T 191包装储运图示标志.
GB/T 1962.1注射器 、注射针及其他医疗器械6%(鲁尔)圆锥接头第1部分:通用要求
GB/T 1962.2注射器 、注射针及其他医疗器械6%(鲁尔)圆锥接头第 2部分:锁定接头
GB/T 6682分析实验室 用水规格和试验方法
GB/T 14233.1医用输液 .输血、注射器具检验方法第1部分:化学分析方法
GB/T 14233.2医用输液 、输血、注射器具检验方法第 2部分:生物学试验方法
GB/T 16886.1医疗器械生物学评价 第 1部分:评价与试验
GB/T 18457制 造医疗器械用不锈钢针管
YY/T 0313- 1998 医用高分子产 品包装、标志、运输和贮存
YY0466医疗器械用于医疗器械标签、标记和提供信息的符号
3分类与标记
3.1分类
一次性使用麻醉针可分为:
a) 硬膜外穿刺针;
b) 腰椎穿刺针;
c) 联合麻醉套针;
d) 神经阻滞穿刺针。
3.2标记.
3.2.1产 品型号
产品型号标记由产品名称代号和分类代号组成。
产品名称代号:麻醉用针以AN表示;
分类代号:硬膜外穿剌针以E表示;腰椎穿刺针以s表示;联合麻醉套针以E/SI表示;神经阻滞
穿刺针以N表示.
YY0321的本部分规定了公称外径为0.4mm~2.1mm的用于人体硬脊膜外腔神经阻滞(简称硬膜外麻醉)、蛛网膜下腔阻滞(简称腰椎麻醉)、硬膜外和腰椎联合麻醉、神经阻滯局部麻醉进行穿刺、注射药物的一次性使用麻醉用针(以下简称麻醉用针)的要求。
2规范性引用文件
下列文件中的条款,通过YY0321本部分的引用而成为本部分的条款,凡是注日期引用文件,其随后的所有修改单(不包括勘误的内容)或修订版均不适用于本部分,然而,鼓励根据本部分达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本部分。
GB/T 191包装储运图示标志.
GB/T 1962.1注射器 、注射针及其他医疗器械6%(鲁尔)圆锥接头第1部分:通用要求
GB/T 1962.2注射器 、注射针及其他医疗器械6%(鲁尔)圆锥接头第 2部分:锁定接头
GB/T 6682分析实验室 用水规格和试验方法
GB/T 14233.1医用输液 .输血、注射器具检验方法第1部分:化学分析方法
GB/T 14233.2医用输液 、输血、注射器具检验方法第 2部分:生物学试验方法
GB/T 16886.1医疗器械生物学评价 第 1部分:评价与试验
GB/T 18457制 造医疗器械用不锈钢针管
YY/T 0313- 1998 医用高分子产 品包装、标志、运输和贮存
YY0466医疗器械用于医疗器械标签、标记和提供信息的符号
3分类与标记
3.1分类
一次性使用麻醉针可分为:
a) 硬膜外穿刺针;
b) 腰椎穿刺针;
c) 联合麻醉套针;
d) 神经阻滞穿刺针。
3.2标记.
3.2.1产 品型号
产品型号标记由产品名称代号和分类代号组成。
产品名称代号:麻醉用针以AN表示;
分类代号:硬膜外穿剌针以E表示;腰椎穿刺针以s表示;联合麻醉套针以E/SI表示;神经阻滞
穿刺针以N表示.
标准图片预览




标准内容
ICS 11. 040. 20
中华人民共和国医药行业标准
YY0321.2—2009
代替YY0321.2—2000
一次性使用麻醉用针
Single-use needle for anaesthesia2009-06-16发布
国家食品药品监督管理局
2010-12-01实施
YY0321分为以下几个部分:
一次性使用麻醉穿刺包;
:一次性使用麻醉针;
一次性使用麻醉用过滤器。
本部分为YY0321的第2部分。
本部分代替YY0321.22000岁-—饮性使用麻酵用针》。YY0321本部分与YY0321.2:2000租比主要变化如下YY 0321. 2—2009
扩大了基本尺寸针管长度范围(YY0321--2000的3.1表1,本部分的3.4表1);针管韧性试验条件作了部分修改(YY0321--2000的4.2.1,本部分的5.2.2表3);针管外表面要求作了修改(YY0321--2000的4.5.4,本部分的5.2.4);增加了针尖斜面与针管与针座平面位置的偏差值(YY 0321--2000 的 4.5.2,本部分的5.4.4);
增加了腰椎穿刺针的流量指标(本部分的5.5);调整了衬芯与村芯座连接牢固度的拉力指标(YY0321--20004.2.2表2,本部分的5.6表5);
无菌、热原的试验进行了修改(YY0321—2000的4.3.1、4.3.2,本部分的7.1、7.2)。本部分的附录 A、附录 B、附录 C、附录 D为规范性附录。本部分由国家食品药品监督管理局提出。本部分由全国医用注射器(针)标准化技术委员会归口。本部分起草单位:上海埃斯埃医械塑料制品有限公司、浙江康德莱医疗器械股份有限公司。本部分起草人:曹贤明、张锦生、张洪辉。本部分于2000年9月首次发布,2009年第一次修订。-TKAONTKAca
1范围
一次性使用麻醉用针
YY0321.2-2009
YY0321的本部分规定了公称外径为0.4mm~2.1mm的用于人体硬脊膜外腔神经阻滞(简称硬膜外麻醉)、蛛网膜下腔阻滞(简称腰椎麻醉)、硬膜外和腰椎联合麻醉、神经阻滞局部麻醉进行穿刺,注射药物的一次性使用麻醇醉用针(以下简称麻醉用针>的要求。2规范性引用文件bzxz.net
下列文件中的条款,通过YY0321本部分的引用而成为本部分的条款,凡是注日期引用文件,其随后的所有修改单(不包括勘误的内容)或修订版均不适用于本部分,然而,鼓励根据本部分达成协议的各方研究是否可使用这些文件的最新版本。凡是不往日期的引用文件,其最新版本适用于本部分。GB/T101包装储运图示标志
GB/T1962.1注射器、注射针及其他医疗器械6%(臀尔)圆锥接头第1部分:通用要求GB/T1962.2注射器、注射针及其他医疗器械6%(解尔)圆锥接头第2部分:锁定接头GB/T6682分析实验室用水规格和试验方法GB/T14233.1医用输液、输血、注射器具检验方法第1部分:化学分析方法GB/T14233.2医用输液、输迹,注射器具检验方法第2部分,生物学试验方法GB/T16886.1医疗器械生物学评价第1部分:评价与试验GB/T18457制造医疗器械用不锈钢针管YY/T0313—1998医用高分子产品包装、标志,运输和忙存YY0466医疗器械用于医疗器械标签、标记和提供信息的符号3分类与标记
3.1分类
一次性使用麻醉针可分为:
a)硬膜外穿刺针;
b)腰椎穿刺针:
c)联合麻醉套针;
d)神经阻滞穿刺针。
3.2标记
3.2.1产品型号
产品型号标记由产品名称代号和分类代号组成。产品名称代号:麻醉用针以AN表示:分类代号:硬膜外穿刺针以E表示腰椎穿刺针以S表示;联合麻醉套针以E/SⅡ表示,神经阻滞穿刺针以 N 表示。
注:Ⅱ型刃口的腰摊穿刺针应在分类代号后加注刃口型式代号。标记示例1:一次性使用麻酵用针——硬膜外穿刺针:AN-E
标记示例2:一次性使用麻醇用针·一一硬膜外芽斓针和Ⅱ型刃口腰椎穿刺针组合的联合麻醉套针:AN-E/SI
YY0321.2—2009
3.2.2产品规格
产品规格标记以针管公称外径×针管长度表示,单位为毫米。标记示例:针管公称外径为0.5mm,针管长度为110mm的一次性使用麻醉用针:0.5×110
3.3结构型式
麻醉用针的结构型式和部件名称如图1~图4所示。贝型式
刻度线
衬芯座:
针座;
针管;
衬芯。
图硬膜外穿刺针示意图
刃口型式
村芯座:
针座,
3—针管,
4——衬芯。
图2腰椎穿刺针示意图
-KAONTKAca-
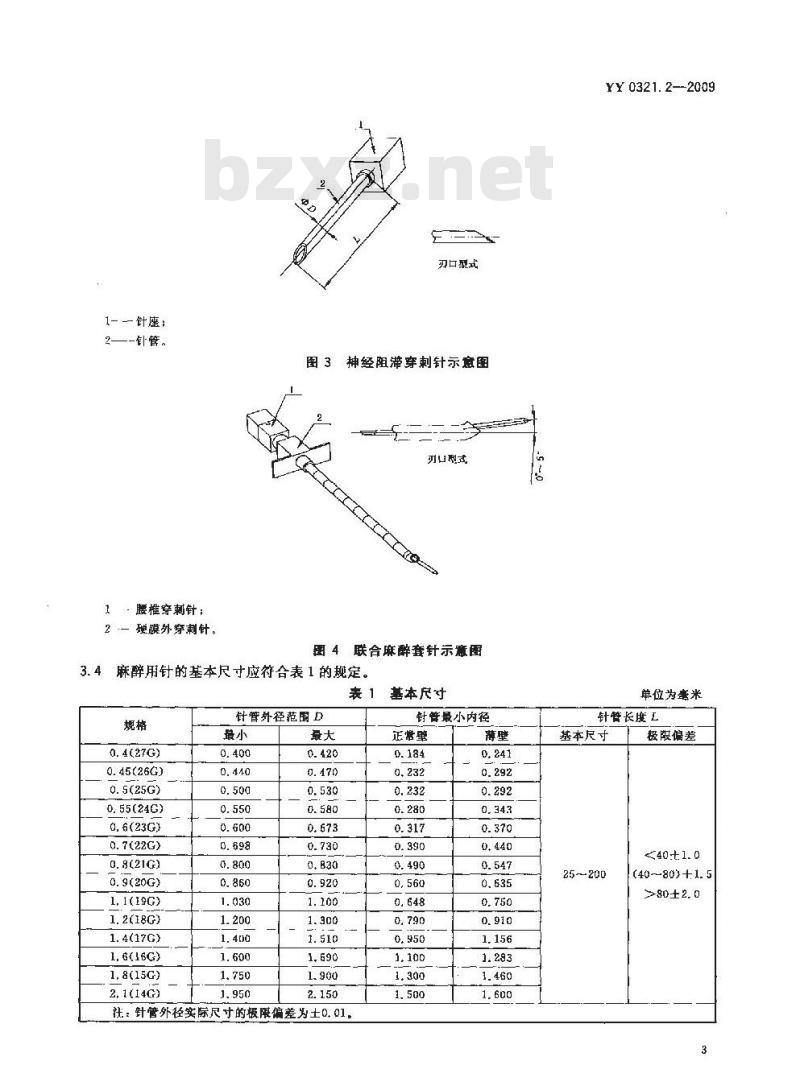
1-——针座:
2—-针管。
1腰推穿刺针;
2—硬膜外穿刺针。
刃口型式
图3神经阻滞穿刺针示意图
刃型式
围 4联合麻醉套针示意图
3.4麻醉用针的基本尺寸应符合表1的规定。表1
0.45(26G)
0.55(24G)
1,1(19G)
2,1(14G)
针管外径范围D
注:针管外径实际尺寸的极限偏差为土0.01.基本尺寸
针管最小内径
正常壁
YY 0321. 2--2009
单位为塞米
针管长度L
基本尺寸
25~200
极限偏差
(40--803+1. 5
YY0321.2-—2009
4材料
制造麻醉用针的材料应满足第5章、第6章、第7章的要求。5物理性能
5.1针座、衬芯座
5.1.1针座圆锥接头应符合GB/T1962.1或GB/T1962.2的要求。5.1.2用正常或矫正视力观察,针座和衬芯座应无毛边,塑流和气泡等缺陷。5.2针管
5.2.1刚性
按GB/T18457规定的试验时,针管的挠度值应不大于表2的规定。刚性试验条件
跨距/ml
荷载/N
晨大挠度/mm
跨距/mm
荷载/N
最大挠度/mm
0.45(26G)
0.55(24G)
在表3规定的试验条件下,按GB/T18457规定的试验时,针管不得折断。5.2.2
表3韧性试验条件
0.45(26G)
0.55(24G)
固定支点和荷载作用点之间的距离/mm8
-TTKAONTKAca-
2. 1(14G)
注:固定针管的夹具不得损伤针管。表3(续)
YY 0321.2--2009
固定支点和载作用点之间的距离/mm25
5.2.3耐腐蚀性按GIB/I18457规定的试验时,针管浸泡的部位不得有腐蚀痕迹5.2.4用正常或矫正视力观察,针管外表面应滑,无金属加「过程中的杂质,5.2.5硬膜外穿刺针针管的刻度线应清晰、无断线,刻度线尺寸应符合图1的规定。5.3衬芯
5.3.1衬芯表面应光滑,能自由通过穿刺针内腔,手感试验无阻滞现象。5.3.2采用不锈钢材料的衬芯,其耐腐蚀性应符合5.2.3的要求。5.4针尖
5.4.1用3倍放大镜检查时,针尖应无毛刺、平头和弯钩。5.4.2硬膜外穿刺针针尖斜面的内圆弧上应无尖锐的边锋,用应规格的麻醇导管从针座锥孔处插入,至穿出针尖斜面10mm后,回抽导管,应不损伤导管。5.4.3硬膜外或腰椎穿刺针的村心尖端不得樊出针管刃口斜面。5.4.4硬膜外穿刺针和I型刃口的腰椎穿刺针,如图1、图2所示的轴A一A、B一B应互相平行,偏差不应超过土15°。
5.5流量
Ⅱ型刃口的腰椎穿刺针按附录 A 试验,以相对压强 100 kPa 的水压经针座内圆锥接头处注人针管,水从针管另一端通孔处流出的流冠应符合表4的规定。表 4 流量
针管规格
5.6连接牢固度
流量/(mL/min)
麻醇用针的针管与针座、衬芯与衬芯座连接应牢固,在连接处施加表5规定的轴向静拉力,持续10 s,两者不应分离。
表 5 连接牢固度
针管与针座
针营外径/rnm
0. 4~0. 5
0, 55~~0. 6
0. 7--2. 1
拉力/N
村芯外径/mm
20. 5~1. 0
村芯与村芯座
拉力/N
YY 0321.2-—2009
5.7琳醉用针的针管与针座连接应正直,用正常或矫正规力观察应无明显的歪斜。5.8微粒污染
麻醉用针内腔应洁净,按附录8试验时,≥5μm的微粒数不得超过100个/mL。5.9色标
麻醉用针以颜色表示针管的公称外径,其识别的色标应符个表6的规定。注:色标可在针座,衬芯座或保护套任-部件上表示。表6识别色标
6化学性能
金属离子
按 GB/T 14233.1中的比色法试验时,检验液呈现的颜色应不超过质量浓度p(Pb\T)-5 Pg/mL的标准对照液。
按GB/T14233.1中的原子吸收分光光度法试验时,镉的含量应不超过0.1g/mL。6.2酸碱度
按 GB/T 14233. 1 中的酸度计法试验时,检验液与空白液 pH值之差应不超过 1. 0。6.3环氧乙烷残留量
麻醉用针经环氧乙烷灭菌后,按照GB/T11233.1进行试验,其残留量应不大于0.1mg。生物性能
在新产品、材料来源和配方改变时,应按GB/T16886.1的规定对细胞毒性、皮内刺激反应、迟发性超敏反应、全身急性毒性和血液相容性进行生物学评价。7.1每个经初包装的麻醉针应通过一灭菌的确认和常规控使产品无荫。注 1: 适宜的灭菌确认和常现控制见 GB 18278,GB 18279 和 GH 18280。注2GB/T14233.2中规短了无菌试验方法,该方选可用于型式检验而不适宜于出厂检验。7.2菌内毒素
按GB/T14233.2 中的疑聚法试验,-次性使用麻醉用针---腰推穿刺针细菌内毒素限量每件不6
-TrKAONrKAca-
YY 0321.2-2009
超过2.15EU,硬膜外穿刺针以及神经阻滞穿刺针的细菌内毒素限量每件不超过20EU8标志,使用说明书
8.1标患
8.1.1 韧包装
韧包装至少应包括:
α)制造名称、地址和/或商标;6)产品名称、型号和规格;
c)产品注册证号、执行标准号:d)生产批号或日期;
失效年月:
“一次性使用\字样和/或图形符号;g)“无菌”“火菌方法\的字样和/或图形符号;h)“包装破损、禁止使用”,“用后销毁”等字样。8.1.2中包装
若使用中包装时中包装副至少应有8.1.1中规定的信息和数量。8.1.3外包装
外包装至少应包括:
制造广名称、地址(或)商标;a)
b)产品名称、型号、规格;
毛重和数量;
体积(长×宽×高);
产品注册证号、执行标准号;
生产批号或日期;
灭菌批号或日期;
h)失效年月;
)“-次性使用”,“无菌”字样或图形符号;“易碎物品”,“怕雨”,“向上”等字样或图示标志应符合GB/T191的有关规定。8.2使用说明书
使用说明书至少应有下列信息:a)产品名称;
医疗器械生产企业许可证号、产品注册证号、执行标准号;b)
产品性能、主要结构和适用范围;e
使用方法、注意事项
失效期限;
f)其他说明和必要的告信息和说明;贮存条件。
9包装
9.1麻醉用针的包装应符合YY/T0313一1998中5.1和5.3的规定,若采用环氧乙烷灭菌,单包装的材料应选用具有透析功能的材料。9.2每支(套)麻酵用针应装人一初包装内。9.3初包装内不应有肉眼可见异物。9.4若干数量的麻醛用针应装人一中包装内。7
YY 0321. 2—2009
5中包装内应有使用说明书和合格证。9.5
运输和存
10.1.麻醉包在运输时应防止重压、阳光直晒和雨雪浸淋。10.2麻醉包应贮存在无腐蚀性气体、通风良好、清洁的环境内。8
-TTKAONKACa=
A.1原理
附录A
(规范性附录)
流量试验方法
将水在一定压力下,通过被测件内腔,计算该被测件单位时间内流出的水量。A.2试验仪器
接头。
YY0321.2—2009
流量测试仪:水压在0kPa300kPa可调控,压力允差土5%,出水口有一个6%的外圆锥的
最小刻度为0
试验步骤
开启仪器电源
将被测件装在仪器出水口6%的外圆锥接头调整水压至标准规定值
选定测低的间。
启动测关,让水从被测件出可端注人量简内达到规是的时间白动关闭读取量筒内水量。
YY0321.2—2009
B.1原理
附录B
(规范性附录)
微粒含量测定方法
这一方法是通过冲洗被测件,收集被测件洗脱液中的粒子,并对其计数来评价微粒污染。B.2试验仪器
粒子计数器(电阻法或光阻法)有搅拌系统,…-次取样量不小于1mL。B.3冲洗液
猜净水(蒸馏水或纯水)或质量浓度为9/I.的氯化钠溶液。B.4试验步骤
用洁净的注射器取60L冲洗液,经被测件流人洁净的计数器的样品池中,即得洗脱液。对样品池内洗脱液中25m的粒子计数,总取样量不少于15mL。10
-irKAoNirKAca=
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
中华人民共和国医药行业标准
YY0321.2—2009
代替YY0321.2—2000
一次性使用麻醉用针
Single-use needle for anaesthesia2009-06-16发布
国家食品药品监督管理局
2010-12-01实施
YY0321分为以下几个部分:
一次性使用麻醉穿刺包;
:一次性使用麻醉针;
一次性使用麻醉用过滤器。
本部分为YY0321的第2部分。
本部分代替YY0321.22000岁-—饮性使用麻酵用针》。YY0321本部分与YY0321.2:2000租比主要变化如下YY 0321. 2—2009
扩大了基本尺寸针管长度范围(YY0321--2000的3.1表1,本部分的3.4表1);针管韧性试验条件作了部分修改(YY0321--2000的4.2.1,本部分的5.2.2表3);针管外表面要求作了修改(YY0321--2000的4.5.4,本部分的5.2.4);增加了针尖斜面与针管与针座平面位置的偏差值(YY 0321--2000 的 4.5.2,本部分的5.4.4);
增加了腰椎穿刺针的流量指标(本部分的5.5);调整了衬芯与村芯座连接牢固度的拉力指标(YY0321--20004.2.2表2,本部分的5.6表5);
无菌、热原的试验进行了修改(YY0321—2000的4.3.1、4.3.2,本部分的7.1、7.2)。本部分的附录 A、附录 B、附录 C、附录 D为规范性附录。本部分由国家食品药品监督管理局提出。本部分由全国医用注射器(针)标准化技术委员会归口。本部分起草单位:上海埃斯埃医械塑料制品有限公司、浙江康德莱医疗器械股份有限公司。本部分起草人:曹贤明、张锦生、张洪辉。本部分于2000年9月首次发布,2009年第一次修订。-TKAONTKAca
1范围
一次性使用麻醉用针
YY0321.2-2009
YY0321的本部分规定了公称外径为0.4mm~2.1mm的用于人体硬脊膜外腔神经阻滞(简称硬膜外麻醉)、蛛网膜下腔阻滞(简称腰椎麻醉)、硬膜外和腰椎联合麻醉、神经阻滞局部麻醉进行穿刺,注射药物的一次性使用麻醇醉用针(以下简称麻醉用针>的要求。2规范性引用文件bzxz.net
下列文件中的条款,通过YY0321本部分的引用而成为本部分的条款,凡是注日期引用文件,其随后的所有修改单(不包括勘误的内容)或修订版均不适用于本部分,然而,鼓励根据本部分达成协议的各方研究是否可使用这些文件的最新版本。凡是不往日期的引用文件,其最新版本适用于本部分。GB/T101包装储运图示标志
GB/T1962.1注射器、注射针及其他医疗器械6%(臀尔)圆锥接头第1部分:通用要求GB/T1962.2注射器、注射针及其他医疗器械6%(解尔)圆锥接头第2部分:锁定接头GB/T6682分析实验室用水规格和试验方法GB/T14233.1医用输液、输血、注射器具检验方法第1部分:化学分析方法GB/T14233.2医用输液、输迹,注射器具检验方法第2部分,生物学试验方法GB/T16886.1医疗器械生物学评价第1部分:评价与试验GB/T18457制造医疗器械用不锈钢针管YY/T0313—1998医用高分子产品包装、标志,运输和忙存YY0466医疗器械用于医疗器械标签、标记和提供信息的符号3分类与标记
3.1分类
一次性使用麻醉针可分为:
a)硬膜外穿刺针;
b)腰椎穿刺针:
c)联合麻醉套针;
d)神经阻滞穿刺针。
3.2标记
3.2.1产品型号
产品型号标记由产品名称代号和分类代号组成。产品名称代号:麻醉用针以AN表示:分类代号:硬膜外穿刺针以E表示腰椎穿刺针以S表示;联合麻醉套针以E/SⅡ表示,神经阻滞穿刺针以 N 表示。
注:Ⅱ型刃口的腰摊穿刺针应在分类代号后加注刃口型式代号。标记示例1:一次性使用麻酵用针——硬膜外穿刺针:AN-E
标记示例2:一次性使用麻醇用针·一一硬膜外芽斓针和Ⅱ型刃口腰椎穿刺针组合的联合麻醉套针:AN-E/SI
YY0321.2—2009
3.2.2产品规格
产品规格标记以针管公称外径×针管长度表示,单位为毫米。标记示例:针管公称外径为0.5mm,针管长度为110mm的一次性使用麻醉用针:0.5×110
3.3结构型式
麻醉用针的结构型式和部件名称如图1~图4所示。贝型式
刻度线
衬芯座:
针座;
针管;
衬芯。
图硬膜外穿刺针示意图
刃口型式
村芯座:
针座,
3—针管,
4——衬芯。
图2腰椎穿刺针示意图
-KAONTKAca-
1-——针座:
2—-针管。
1腰推穿刺针;
2—硬膜外穿刺针。
刃口型式
图3神经阻滞穿刺针示意图
刃型式
围 4联合麻醉套针示意图
3.4麻醉用针的基本尺寸应符合表1的规定。表1
0.45(26G)
0.55(24G)
1,1(19G)
2,1(14G)
针管外径范围D
注:针管外径实际尺寸的极限偏差为土0.01.基本尺寸
针管最小内径
正常壁
YY 0321. 2--2009
单位为塞米
针管长度L
基本尺寸
25~200
极限偏差
(40--803+1. 5
YY0321.2-—2009
4材料
制造麻醉用针的材料应满足第5章、第6章、第7章的要求。5物理性能
5.1针座、衬芯座
5.1.1针座圆锥接头应符合GB/T1962.1或GB/T1962.2的要求。5.1.2用正常或矫正视力观察,针座和衬芯座应无毛边,塑流和气泡等缺陷。5.2针管
5.2.1刚性
按GB/T18457规定的试验时,针管的挠度值应不大于表2的规定。刚性试验条件
跨距/ml
荷载/N
晨大挠度/mm
跨距/mm
荷载/N
最大挠度/mm
0.45(26G)
0.55(24G)
在表3规定的试验条件下,按GB/T18457规定的试验时,针管不得折断。5.2.2
表3韧性试验条件
0.45(26G)
0.55(24G)
固定支点和荷载作用点之间的距离/mm8
-TTKAONTKAca-
2. 1(14G)
注:固定针管的夹具不得损伤针管。表3(续)
YY 0321.2--2009
固定支点和载作用点之间的距离/mm25
5.2.3耐腐蚀性按GIB/I18457规定的试验时,针管浸泡的部位不得有腐蚀痕迹5.2.4用正常或矫正视力观察,针管外表面应滑,无金属加「过程中的杂质,5.2.5硬膜外穿刺针针管的刻度线应清晰、无断线,刻度线尺寸应符合图1的规定。5.3衬芯
5.3.1衬芯表面应光滑,能自由通过穿刺针内腔,手感试验无阻滞现象。5.3.2采用不锈钢材料的衬芯,其耐腐蚀性应符合5.2.3的要求。5.4针尖
5.4.1用3倍放大镜检查时,针尖应无毛刺、平头和弯钩。5.4.2硬膜外穿刺针针尖斜面的内圆弧上应无尖锐的边锋,用应规格的麻醇导管从针座锥孔处插入,至穿出针尖斜面10mm后,回抽导管,应不损伤导管。5.4.3硬膜外或腰椎穿刺针的村心尖端不得樊出针管刃口斜面。5.4.4硬膜外穿刺针和I型刃口的腰椎穿刺针,如图1、图2所示的轴A一A、B一B应互相平行,偏差不应超过土15°。
5.5流量
Ⅱ型刃口的腰椎穿刺针按附录 A 试验,以相对压强 100 kPa 的水压经针座内圆锥接头处注人针管,水从针管另一端通孔处流出的流冠应符合表4的规定。表 4 流量
针管规格
5.6连接牢固度
流量/(mL/min)
麻醇用针的针管与针座、衬芯与衬芯座连接应牢固,在连接处施加表5规定的轴向静拉力,持续10 s,两者不应分离。
表 5 连接牢固度
针管与针座
针营外径/rnm
0. 4~0. 5
0, 55~~0. 6
0. 7--2. 1
拉力/N
村芯外径/mm
20. 5~1. 0
村芯与村芯座
拉力/N
YY 0321.2-—2009
5.7琳醉用针的针管与针座连接应正直,用正常或矫正规力观察应无明显的歪斜。5.8微粒污染
麻醉用针内腔应洁净,按附录8试验时,≥5μm的微粒数不得超过100个/mL。5.9色标
麻醉用针以颜色表示针管的公称外径,其识别的色标应符个表6的规定。注:色标可在针座,衬芯座或保护套任-部件上表示。表6识别色标
6化学性能
金属离子
按 GB/T 14233.1中的比色法试验时,检验液呈现的颜色应不超过质量浓度p(Pb\T)-5 Pg/mL的标准对照液。
按GB/T14233.1中的原子吸收分光光度法试验时,镉的含量应不超过0.1g/mL。6.2酸碱度
按 GB/T 14233. 1 中的酸度计法试验时,检验液与空白液 pH值之差应不超过 1. 0。6.3环氧乙烷残留量
麻醉用针经环氧乙烷灭菌后,按照GB/T11233.1进行试验,其残留量应不大于0.1mg。生物性能
在新产品、材料来源和配方改变时,应按GB/T16886.1的规定对细胞毒性、皮内刺激反应、迟发性超敏反应、全身急性毒性和血液相容性进行生物学评价。7.1每个经初包装的麻醉针应通过一灭菌的确认和常规控使产品无荫。注 1: 适宜的灭菌确认和常现控制见 GB 18278,GB 18279 和 GH 18280。注2GB/T14233.2中规短了无菌试验方法,该方选可用于型式检验而不适宜于出厂检验。7.2菌内毒素
按GB/T14233.2 中的疑聚法试验,-次性使用麻醉用针---腰推穿刺针细菌内毒素限量每件不6
-TrKAONrKAca-
YY 0321.2-2009
超过2.15EU,硬膜外穿刺针以及神经阻滞穿刺针的细菌内毒素限量每件不超过20EU8标志,使用说明书
8.1标患
8.1.1 韧包装
韧包装至少应包括:
α)制造名称、地址和/或商标;6)产品名称、型号和规格;
c)产品注册证号、执行标准号:d)生产批号或日期;
失效年月:
“一次性使用\字样和/或图形符号;g)“无菌”“火菌方法\的字样和/或图形符号;h)“包装破损、禁止使用”,“用后销毁”等字样。8.1.2中包装
若使用中包装时中包装副至少应有8.1.1中规定的信息和数量。8.1.3外包装
外包装至少应包括:
制造广名称、地址(或)商标;a)
b)产品名称、型号、规格;
毛重和数量;
体积(长×宽×高);
产品注册证号、执行标准号;
生产批号或日期;
灭菌批号或日期;
h)失效年月;
)“-次性使用”,“无菌”字样或图形符号;“易碎物品”,“怕雨”,“向上”等字样或图示标志应符合GB/T191的有关规定。8.2使用说明书
使用说明书至少应有下列信息:a)产品名称;
医疗器械生产企业许可证号、产品注册证号、执行标准号;b)
产品性能、主要结构和适用范围;e
使用方法、注意事项
失效期限;
f)其他说明和必要的告信息和说明;贮存条件。
9包装
9.1麻醉用针的包装应符合YY/T0313一1998中5.1和5.3的规定,若采用环氧乙烷灭菌,单包装的材料应选用具有透析功能的材料。9.2每支(套)麻酵用针应装人一初包装内。9.3初包装内不应有肉眼可见异物。9.4若干数量的麻醛用针应装人一中包装内。7
YY 0321. 2—2009
5中包装内应有使用说明书和合格证。9.5
运输和存
10.1.麻醉包在运输时应防止重压、阳光直晒和雨雪浸淋。10.2麻醉包应贮存在无腐蚀性气体、通风良好、清洁的环境内。8
-TTKAONKACa=
A.1原理
附录A
(规范性附录)
流量试验方法
将水在一定压力下,通过被测件内腔,计算该被测件单位时间内流出的水量。A.2试验仪器
接头。
YY0321.2—2009
流量测试仪:水压在0kPa300kPa可调控,压力允差土5%,出水口有一个6%的外圆锥的
最小刻度为0
试验步骤
开启仪器电源
将被测件装在仪器出水口6%的外圆锥接头调整水压至标准规定值
选定测低的间。
启动测关,让水从被测件出可端注人量简内达到规是的时间白动关闭读取量筒内水量。
YY0321.2—2009
B.1原理
附录B
(规范性附录)
微粒含量测定方法
这一方法是通过冲洗被测件,收集被测件洗脱液中的粒子,并对其计数来评价微粒污染。B.2试验仪器
粒子计数器(电阻法或光阻法)有搅拌系统,…-次取样量不小于1mL。B.3冲洗液
猜净水(蒸馏水或纯水)或质量浓度为9/I.的氯化钠溶液。B.4试验步骤
用洁净的注射器取60L冲洗液,经被测件流人洁净的计数器的样品池中,即得洗脱液。对样品池内洗脱液中25m的粒子计数,总取样量不少于15mL。10
-irKAoNirKAca=
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。