YY/T 0188. 11-1995
基本信息
标准号: YY/T 0188. 11-1995
中文名称:药品检验操作规程 第11部分:澄明度检查法
标准类别:医药行业标准(YY)
标准状态:现行
出版语种:简体中文
下载格式:.zip .pdf
下载大小:178043

标准分类号
关联标准
出版信息
相关单位信息
标准简介
YY/T 0188. 11-1995.Operating methods for the tests and assays of drugs Part 11:Tests for the clarilty of soiutlons.
1范围
YY/T 0188. 11规定了药物的各种注射液.注射用无菌粉针剂及其原料药、滴眼剂的澄明度检查方法。
YY/T 0188. 11适用于药物制成的水(醇)溶剂型注射液(包括输液)、油溶剂型注射液、混悬型注射液、注射用无菌粉针剂及其原料药、滴眼剂的澄明度检查。
2引用标准
中华人民共和国药典(1995年版)WS1- -362(B- -121)-91澄明度检查细则和判断标准
3定义
YY/T 0188. 11采用下列定义。
3.1白块用规定的检查方法,能看到有明显的平面或梭角的白色物质。
3.2自点
不能辨清平面或楼角的按白点计.但有的白色物质虽不易看清平面校角(如球形),但与上述白块同等大小或更大者,应作白块论。在检查中见似有似兀或若隐若现的微细物,不作白点计数。
3.3 微盘白点50 mL或50 mL以下注射液,在规定的检查时间内仅见到3个或3个以下的白点者,作为微社白点100 mL或100 mL以上注射液,在规定检查时间内仅见到5个或5个以下的白点时,作为微量白点。
3.4少量白点药液澄明,白点数量 比微量白点较多,在规定检查时间内较难准确计数者。
3.5微量沉积物某些生化制剂或商分 子化合物制剂,静置后有微小的质点沉积,轻轻倒转时有烟雾状细线浮起,轻摇即散失者。
3.6异物包括玻璃屑、纤维、色点、色块及其他外来异物。
3.7特殊异物金属屑及 明显可见的玻璃屑、玻璃块、玻璃砂、硬毛或粗纤维等异物。金属屑有-面闪光者即是,玻璃屑有闪烁性或有棱角的透明物即是。
3.8贮存期产品出厂后的产品。
4检查装置
4.1光源采用日光灯。无色溶液注射剂、滴眼剂于光照度为1 00~1 500 lx的位咒,透明塑料容器或有色溶液注射剂于光照度为2 00~3 000 lx的位置,塑料容器或有色溶液滴眼剂于光照度(除正文中另有规定外)为2 000~4 000 lx的位置,用目检视。
1范围
YY/T 0188. 11规定了药物的各种注射液.注射用无菌粉针剂及其原料药、滴眼剂的澄明度检查方法。
YY/T 0188. 11适用于药物制成的水(醇)溶剂型注射液(包括输液)、油溶剂型注射液、混悬型注射液、注射用无菌粉针剂及其原料药、滴眼剂的澄明度检查。
2引用标准
中华人民共和国药典(1995年版)WS1- -362(B- -121)-91澄明度检查细则和判断标准
3定义
YY/T 0188. 11采用下列定义。
3.1白块用规定的检查方法,能看到有明显的平面或梭角的白色物质。
3.2自点
不能辨清平面或楼角的按白点计.但有的白色物质虽不易看清平面校角(如球形),但与上述白块同等大小或更大者,应作白块论。在检查中见似有似兀或若隐若现的微细物,不作白点计数。
3.3 微盘白点50 mL或50 mL以下注射液,在规定的检查时间内仅见到3个或3个以下的白点者,作为微社白点100 mL或100 mL以上注射液,在规定检查时间内仅见到5个或5个以下的白点时,作为微量白点。
3.4少量白点药液澄明,白点数量 比微量白点较多,在规定检查时间内较难准确计数者。
3.5微量沉积物某些生化制剂或商分 子化合物制剂,静置后有微小的质点沉积,轻轻倒转时有烟雾状细线浮起,轻摇即散失者。
3.6异物包括玻璃屑、纤维、色点、色块及其他外来异物。
3.7特殊异物金属屑及 明显可见的玻璃屑、玻璃块、玻璃砂、硬毛或粗纤维等异物。金属屑有-面闪光者即是,玻璃屑有闪烁性或有棱角的透明物即是。
3.8贮存期产品出厂后的产品。
4检查装置
4.1光源采用日光灯。无色溶液注射剂、滴眼剂于光照度为1 00~1 500 lx的位咒,透明塑料容器或有色溶液注射剂于光照度为2 00~3 000 lx的位置,塑料容器或有色溶液滴眼剂于光照度(除正文中另有规定外)为2 000~4 000 lx的位置,用目检视。
标准图片预览



标准内容
YY/T0188.11—1995
本标准是依据《中华人民共和国药典》(1995年版)和中华人民共和国卫生部部标准WS1一362(B—121)—91《澄明度检查细则和判断标准》制定的,由ZBC10007—89化学药及抗生素的制剂的检查法》中的注射剂澄明度检查法与滴眼剂澄明度检查法合并列出另立的标准。本标准对各剂型注射液、注射用无菌粉针剂及其原料药以及滴眼剂等制剂澄明度检查法,作了详细的说明与规定,是统一药品检验操作的规范化工作指南。本标准对原标准进行较大的改动有:1.增加了对检查装置的说明与规定;2.增加了注射用无菌原料药的澄明度检查,3.在第3章定义中,将“特大异物”归入“特殊异物”4.对特殊品种的判断,删除了复方甘油磷酸钠注射液和水解蛋白注射液本标准从生效之日起,同时代替ZBC10007—89。本标准由国家医药管理局提出并归口。本标准起草单位:无锡市第四制药厂。本标准主要起草人:沈佩英。
本标准于1989年3月首次发布,于1995年7月第一次修订。179
1范围
中华人民共和国医药行业标准
药品检验操作规程
第11部分:澄明度检查法
Operating methods for the tests and assays of drugsPart 11:Tests for the clarity of solutionsYY/T0188.111995
代替ZBC10007--89
本标准规定了药物的各种注射液、注射用无菌粉针剂及其原料药、滴眼剂的澄明度检查方法。本法适用于药物制成的水(醇)溶剂型注射液(包括输液)、油溶剂型注射液、混悬型注射液、注射用无菌粉针剂及其原料药、滴眼剂的澄明度检查。2引用标准
中华人民共和国药典(1995年版)WS1-362(B—121)-91澄明度检查细则和判断标准3定义
本标准采用下列定义。
3.1白块用规定的检查方法,能看到有明显的平面或棱角的白色物质。3.2白点不能辨清平面或棱角的按白点计。但有的白色物质虽不易看清平面、校角(如球形),但与上述白块同等大小或更大者,应作白块论。在检查中见似有似无或若隐若现的微细物,不作白点计数。3.3微量白点50mL或50mL以下注射液,在规定的检查时间内仅见到3个或3个以下的白点者,作为微量白点;100mL或100mL以上注射液,在规定检查时间内仅见到5个或5个以下的白点时,作为微量白点:
3.4少量白点药液澄明,白点数量比微量白点较多,在规定检查时间内较难准确计数者。3.5微量沉积物某些生化制剂或高分子化合物制剂,静暨后有微小的质点沉积,轻轻倒转时有烟雾状细线浮起,轻摇即散失者。
3.6异物包括玻璃屑、纤维、色点、色块及其他外来异物。3.7特殊异物金属屑及明显可见的玻璃屑、玻璃块、玻璃砂、硬毛或粗纤维等异物。金属屑有一面闪光者即是,玻璃屑有闪烁性或有棱角的透明物即是。3.8贮存期产品出厂后的产品。
4检查装置
4.1光源采用日光灯。无色溶液注射剂、滴眼剂于光照度为1000~15001x的位置,透明塑料容器或有色溶液注射剂于光照度为2000~30001x的位置,塑料容器或有色溶液滴眼剂于光照度(除正文中另有规定外)为2000~40001x的位置,用目检视。国家医药管理局1995-07-11批准180
1996-05-01实施此内容来自标准下载网
YY/T0188.11-1995
采用伞棚式装经,两面或单面用,见中华人民共和国药典附录。4.2式样
4.3背景
4.4距离
为不反光黑色。在背部右侧和底部为不反光白色(供检查有色异物)。供试品至人眼距离为20~25cm。
4.5检查
应在避光室内或暗处进行。
5检查规则
5.1检查人员条件
5.1.1视力远距离和近距离视力测验,均为0.9或0.9以上(不包括矫正后视力),色盲测验应无色盲。
5.1.3澄明度检查操作人员应经有关澄明度检查法的全面培训,能正确掌握判断标准,熟练掌握操作方法,方可上岗操作。
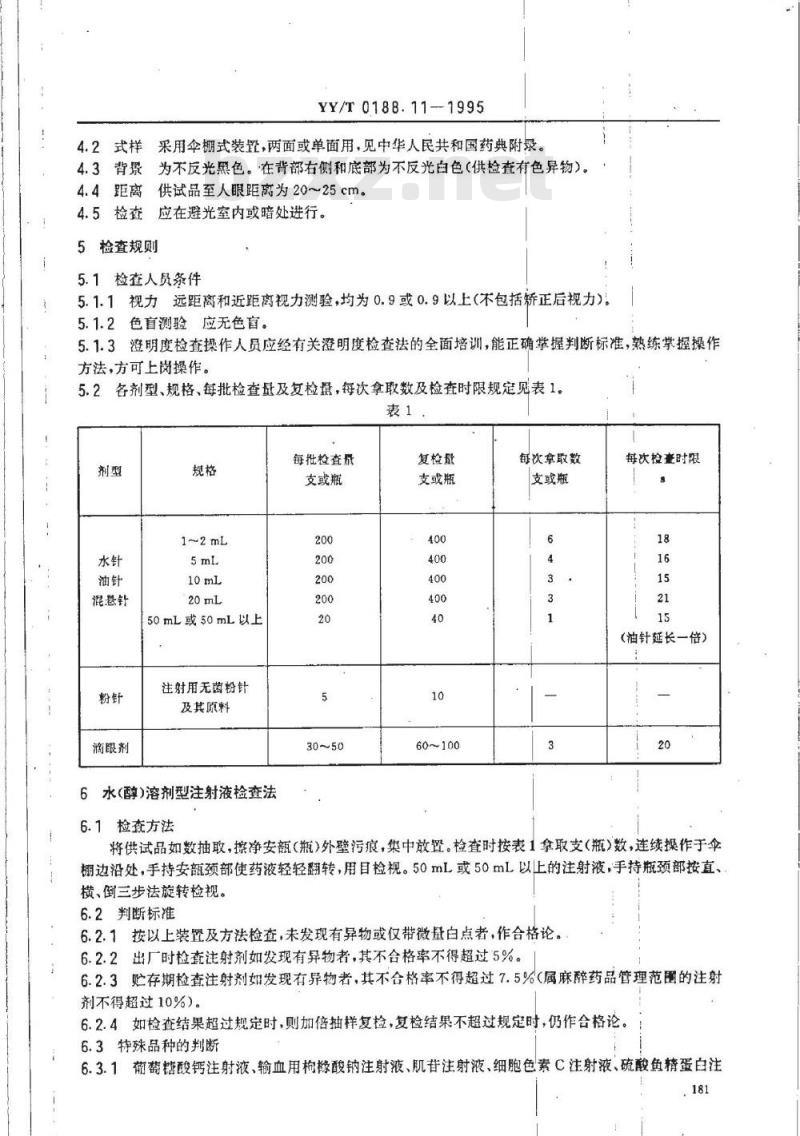
5.2各剂型、规格、每批检查量及复检量,每次拿取数及检查时限规定见表1。表1
混悬针
滴眼剂
50mL或50mL以上
注射用无菌粉针
及其原料
6水(醇)溶剂型注射液检查法
每批检查量
支或瓶
复检量
支或瓶
60~100
每次拿取数
支或瓶
每次捡壹时限
(油针延长一倍)
6.1检查方法
将供试品如数抽取,擦净安瓶(瓶)外壁污痕,集中放暨。检查时按表1拿取支(瓶)数,连续操作于伞棚边沿处,手持安颜颈部使药液轻轻翻转,用目检视。50mL或50mL以上的注射液,手持瓶颈部按直、横、倒三步法旋转检视。
6.2判断标准
6.2.1按以上装置及方法检查,未发现有异物或仅带微量白点者,作合格论。6.2.2出厂时检查注射剂如发现有异物者,其不合格率不得超过5%。6.2.3贮存期检查注射剂如发现有异物者,其不合格率不得超过7.5%(属麻醉药品管理范围的注射剂不得超过10%)。
6.2.4如检查结果超过规定时,则加倍抽样复检,复检结果不超过规定时,仍作合格论。6.3特殊品种的判断
6.3.1葡萄糖酸钙注射液、输血用枸橡酸钠注射液、肌苷注射液、细胞色素C注射液、硫酸鱼精蛋白注181
YY/T0188.11—1995
射液、肝素钠注射液、乳酸钠注射液在药液澄明的情况下,仅带有少量白点者,作合格论。6.3.2胰岛素注射液,在药液澄明的情况下,仅带少量白点及短小纤维状物者,作合格论。6.3.3盐酸精氨酸注射液,在药液澄明的情况下,仅带少量白点及短小纤维(经摇动即能分散)者,作合格论。
6.3.4右旋糖酐类注射液,带有轻微乳光及微量白点者,作合格论。7油溶剂型注射液检查法
检查方法按水(醇)溶剂型注射液检查方法,其检查时限延长一倍。如有结晶析出,可在80℃以下水浴中加热30min,振摇,放冷至20~30℃检查,若结晶不溶者判为不合格。8混悬型注射液检查法
按水(醇)溶剂型注射液的检查方法及检查时限,检查色、块等异物。9注射用无菌粉针及无菌粉末原料药检查法9.1准备工作
9.1.1澄明水或溶剂的制备取重蒸馏水或溶剂,用4号或5号玻璃垂熔漏斗,或孔径为0.8μm滤膜连续过滤,过滤水或溶剂经澄明度检查,无毛、点等异物。9.1.2注射器及针头加水或溶剂用的注射器及针头应洁净,并经抽取制备好的澄明水或溶剂检查潘明度,无毛、点等异物的方可使用。9.2检查方法
9.2.1注射用无菌粉针在超净台内操作,取供试品5支(瓶),擦净容器外壁,小心开启,避免玻璃屑等异物落入容器中,按各品种的规定,分别注入规定量预先制备好的澄明水或溶剂,使药粉全部溶解,用手指持容器一端,于伞棚边沿轻轻旋转,使容器内药液形成旋流,随即用目检视,先与黑色背景,后与白色背景对照检查。
9.2.2无菌粉末原料药在超净台内操作,取洁净具塞瓶子5个,按各品种的规定,分别注入规定量预先制备好的澄明水或溶剂,照注射用无菌粉针项下方法操作,记录瓶中毛、点数,作为空白,然后分别加入规定量的供试品,使完全溶解,同法操作,扣除空白,即得。9.3注意事项
-9.3.1小瓶装粉针剂,打开铝盖,用清洁绸布将橡皮塞外壁擦净避免异物带入。检查澄明度时,由于针刺橡皮塞的掉屑,可不计入色点数内。9.3.2安颜粉针在未打开前须预先反复倒转观察,如发现玻璃屑者作特殊异物论,未发现者再作进一步检查。在打开安甄时,带进的玻璃屑,检查澄明度时,可不计入玻璃屑数内。9.3.3注射用无菌粉针剂或无菌粉末原料药澄明度检查时,溶液在摇匀后,如显轻微混浊,或有肉眼可见微粒,可于室温静置30min或于25℃土2℃,每隔5min振摇30s,使之溶解,30min内再观察,但不得用超声波助溶。轻轻旋转不得有可见的烟雾状旋涡产生,且其浊度不得超过规定的浊度对照管。9.4判断标准
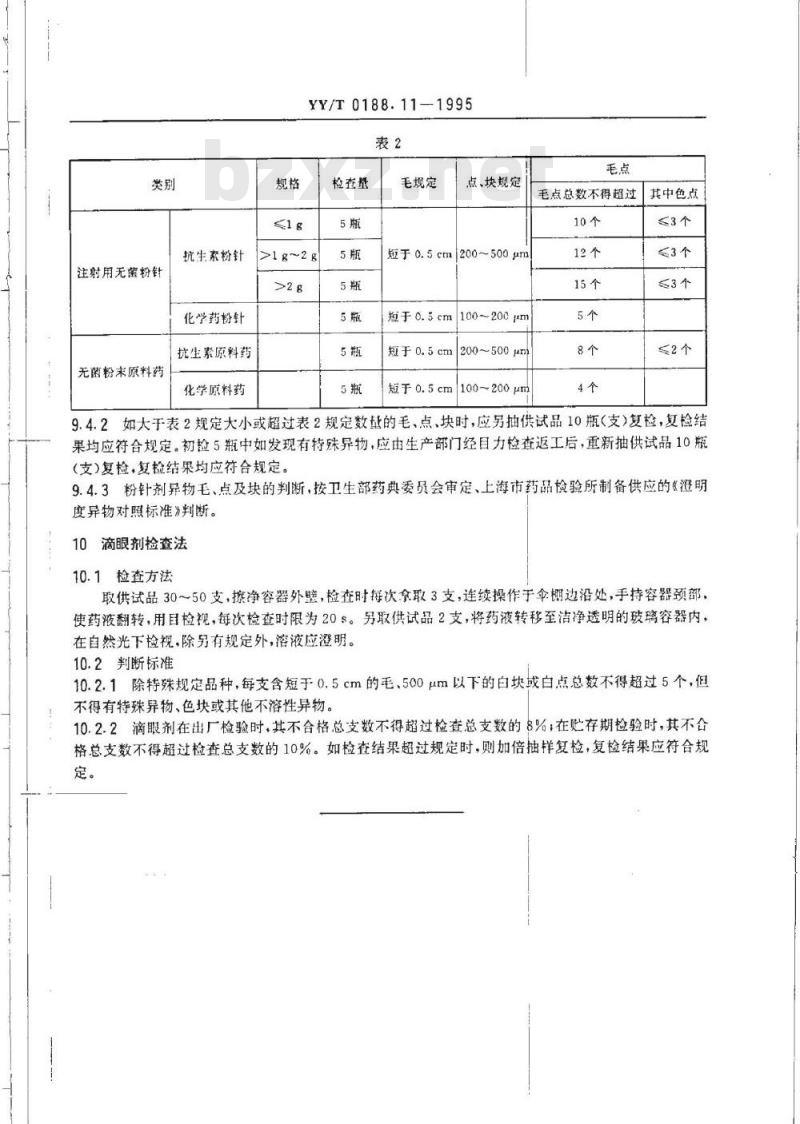
9.4.1抗生素粉针剂、化学药粉针剂及其原料药每瓶(支)所含毛白点、白块、色点总数不得超过表2规定。
注射用无菌粉针
抗生素粉针
化学药粉针
抗生素原料药
无菌粉末原料药
化学原料药
YY/T0188.11-1995
检在量
>1g~2g
毛规定
点、块规定
短于0.5cm200~500μm
短于0.5cm100~200m
短于0.5cm
200500
短于0.5cm
1100~200μm
毛点总数不得超过
其中色点
9.4.2如大于表2规定大小或超过表2规定数量的毛、点、块时,应另抽供试品10瓶(支)复检,复检结果均应符合规定。初检5瓶中如发现有特殊异物,应由生产部门经目力检查返工后,重新抽供试品10瓶(支)复检,复检结果均应符合规定。9.4.3粉针剂异物毛、点及块的判断,按卫生部药典委员会审定、上海市药品检验所制备供应的《澄明度异物对照标准》判断。
10滴眼剂检查法
10.1检查方法
取供试品30~50支,擦净容器外壁,检查时每次盒取3支,连续操作于伞树边沿处,手持容器颈部,使药液翻转,用目检视,每次检查时限为20s。另取供试品2支,将药液转移至洁净透明的玻璃容器内,在自然光下检视,除另有规定外,溶液应没明。10.2判断标准
10.2.1除特殊规定品种,每支含短于0.5cm的毛、500μm以下的白块或白点总数不得超过5个,但不得有特殊异物、色块或其他不溶性异物。10.2.2滴眼剂在出厂检验时,其不合格总支数不得超过检查总支数的8%,在贮存期检验时,其不合格总支数不得超过检查总支数的10%。如检查结果超过规定时,则加倍抽样复检,复检结果应符合规定。
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
本标准是依据《中华人民共和国药典》(1995年版)和中华人民共和国卫生部部标准WS1一362(B—121)—91《澄明度检查细则和判断标准》制定的,由ZBC10007—89化学药及抗生素的制剂的检查法》中的注射剂澄明度检查法与滴眼剂澄明度检查法合并列出另立的标准。本标准对各剂型注射液、注射用无菌粉针剂及其原料药以及滴眼剂等制剂澄明度检查法,作了详细的说明与规定,是统一药品检验操作的规范化工作指南。本标准对原标准进行较大的改动有:1.增加了对检查装置的说明与规定;2.增加了注射用无菌原料药的澄明度检查,3.在第3章定义中,将“特大异物”归入“特殊异物”4.对特殊品种的判断,删除了复方甘油磷酸钠注射液和水解蛋白注射液本标准从生效之日起,同时代替ZBC10007—89。本标准由国家医药管理局提出并归口。本标准起草单位:无锡市第四制药厂。本标准主要起草人:沈佩英。
本标准于1989年3月首次发布,于1995年7月第一次修订。179
1范围
中华人民共和国医药行业标准
药品检验操作规程
第11部分:澄明度检查法
Operating methods for the tests and assays of drugsPart 11:Tests for the clarity of solutionsYY/T0188.111995
代替ZBC10007--89
本标准规定了药物的各种注射液、注射用无菌粉针剂及其原料药、滴眼剂的澄明度检查方法。本法适用于药物制成的水(醇)溶剂型注射液(包括输液)、油溶剂型注射液、混悬型注射液、注射用无菌粉针剂及其原料药、滴眼剂的澄明度检查。2引用标准
中华人民共和国药典(1995年版)WS1-362(B—121)-91澄明度检查细则和判断标准3定义
本标准采用下列定义。
3.1白块用规定的检查方法,能看到有明显的平面或棱角的白色物质。3.2白点不能辨清平面或棱角的按白点计。但有的白色物质虽不易看清平面、校角(如球形),但与上述白块同等大小或更大者,应作白块论。在检查中见似有似无或若隐若现的微细物,不作白点计数。3.3微量白点50mL或50mL以下注射液,在规定的检查时间内仅见到3个或3个以下的白点者,作为微量白点;100mL或100mL以上注射液,在规定检查时间内仅见到5个或5个以下的白点时,作为微量白点:
3.4少量白点药液澄明,白点数量比微量白点较多,在规定检查时间内较难准确计数者。3.5微量沉积物某些生化制剂或高分子化合物制剂,静暨后有微小的质点沉积,轻轻倒转时有烟雾状细线浮起,轻摇即散失者。
3.6异物包括玻璃屑、纤维、色点、色块及其他外来异物。3.7特殊异物金属屑及明显可见的玻璃屑、玻璃块、玻璃砂、硬毛或粗纤维等异物。金属屑有一面闪光者即是,玻璃屑有闪烁性或有棱角的透明物即是。3.8贮存期产品出厂后的产品。
4检查装置
4.1光源采用日光灯。无色溶液注射剂、滴眼剂于光照度为1000~15001x的位置,透明塑料容器或有色溶液注射剂于光照度为2000~30001x的位置,塑料容器或有色溶液滴眼剂于光照度(除正文中另有规定外)为2000~40001x的位置,用目检视。国家医药管理局1995-07-11批准180
1996-05-01实施此内容来自标准下载网
YY/T0188.11-1995
采用伞棚式装经,两面或单面用,见中华人民共和国药典附录。4.2式样
4.3背景
4.4距离
为不反光黑色。在背部右侧和底部为不反光白色(供检查有色异物)。供试品至人眼距离为20~25cm。
4.5检查
应在避光室内或暗处进行。
5检查规则
5.1检查人员条件
5.1.1视力远距离和近距离视力测验,均为0.9或0.9以上(不包括矫正后视力),色盲测验应无色盲。
5.1.3澄明度检查操作人员应经有关澄明度检查法的全面培训,能正确掌握判断标准,熟练掌握操作方法,方可上岗操作。
5.2各剂型、规格、每批检查量及复检量,每次拿取数及检查时限规定见表1。表1
混悬针
滴眼剂
50mL或50mL以上
注射用无菌粉针
及其原料
6水(醇)溶剂型注射液检查法
每批检查量
支或瓶
复检量
支或瓶
60~100
每次拿取数
支或瓶
每次捡壹时限
(油针延长一倍)
6.1检查方法
将供试品如数抽取,擦净安瓶(瓶)外壁污痕,集中放暨。检查时按表1拿取支(瓶)数,连续操作于伞棚边沿处,手持安颜颈部使药液轻轻翻转,用目检视。50mL或50mL以上的注射液,手持瓶颈部按直、横、倒三步法旋转检视。
6.2判断标准
6.2.1按以上装置及方法检查,未发现有异物或仅带微量白点者,作合格论。6.2.2出厂时检查注射剂如发现有异物者,其不合格率不得超过5%。6.2.3贮存期检查注射剂如发现有异物者,其不合格率不得超过7.5%(属麻醉药品管理范围的注射剂不得超过10%)。
6.2.4如检查结果超过规定时,则加倍抽样复检,复检结果不超过规定时,仍作合格论。6.3特殊品种的判断
6.3.1葡萄糖酸钙注射液、输血用枸橡酸钠注射液、肌苷注射液、细胞色素C注射液、硫酸鱼精蛋白注181
YY/T0188.11—1995
射液、肝素钠注射液、乳酸钠注射液在药液澄明的情况下,仅带有少量白点者,作合格论。6.3.2胰岛素注射液,在药液澄明的情况下,仅带少量白点及短小纤维状物者,作合格论。6.3.3盐酸精氨酸注射液,在药液澄明的情况下,仅带少量白点及短小纤维(经摇动即能分散)者,作合格论。
6.3.4右旋糖酐类注射液,带有轻微乳光及微量白点者,作合格论。7油溶剂型注射液检查法
检查方法按水(醇)溶剂型注射液检查方法,其检查时限延长一倍。如有结晶析出,可在80℃以下水浴中加热30min,振摇,放冷至20~30℃检查,若结晶不溶者判为不合格。8混悬型注射液检查法
按水(醇)溶剂型注射液的检查方法及检查时限,检查色、块等异物。9注射用无菌粉针及无菌粉末原料药检查法9.1准备工作
9.1.1澄明水或溶剂的制备取重蒸馏水或溶剂,用4号或5号玻璃垂熔漏斗,或孔径为0.8μm滤膜连续过滤,过滤水或溶剂经澄明度检查,无毛、点等异物。9.1.2注射器及针头加水或溶剂用的注射器及针头应洁净,并经抽取制备好的澄明水或溶剂检查潘明度,无毛、点等异物的方可使用。9.2检查方法
9.2.1注射用无菌粉针在超净台内操作,取供试品5支(瓶),擦净容器外壁,小心开启,避免玻璃屑等异物落入容器中,按各品种的规定,分别注入规定量预先制备好的澄明水或溶剂,使药粉全部溶解,用手指持容器一端,于伞棚边沿轻轻旋转,使容器内药液形成旋流,随即用目检视,先与黑色背景,后与白色背景对照检查。
9.2.2无菌粉末原料药在超净台内操作,取洁净具塞瓶子5个,按各品种的规定,分别注入规定量预先制备好的澄明水或溶剂,照注射用无菌粉针项下方法操作,记录瓶中毛、点数,作为空白,然后分别加入规定量的供试品,使完全溶解,同法操作,扣除空白,即得。9.3注意事项
-9.3.1小瓶装粉针剂,打开铝盖,用清洁绸布将橡皮塞外壁擦净避免异物带入。检查澄明度时,由于针刺橡皮塞的掉屑,可不计入色点数内。9.3.2安颜粉针在未打开前须预先反复倒转观察,如发现玻璃屑者作特殊异物论,未发现者再作进一步检查。在打开安甄时,带进的玻璃屑,检查澄明度时,可不计入玻璃屑数内。9.3.3注射用无菌粉针剂或无菌粉末原料药澄明度检查时,溶液在摇匀后,如显轻微混浊,或有肉眼可见微粒,可于室温静置30min或于25℃土2℃,每隔5min振摇30s,使之溶解,30min内再观察,但不得用超声波助溶。轻轻旋转不得有可见的烟雾状旋涡产生,且其浊度不得超过规定的浊度对照管。9.4判断标准
9.4.1抗生素粉针剂、化学药粉针剂及其原料药每瓶(支)所含毛白点、白块、色点总数不得超过表2规定。
注射用无菌粉针
抗生素粉针
化学药粉针
抗生素原料药
无菌粉末原料药
化学原料药
YY/T0188.11-1995
检在量
>1g~2g
毛规定
点、块规定
短于0.5cm200~500μm
短于0.5cm100~200m
短于0.5cm
200500
短于0.5cm
1100~200μm
毛点总数不得超过
其中色点
9.4.2如大于表2规定大小或超过表2规定数量的毛、点、块时,应另抽供试品10瓶(支)复检,复检结果均应符合规定。初检5瓶中如发现有特殊异物,应由生产部门经目力检查返工后,重新抽供试品10瓶(支)复检,复检结果均应符合规定。9.4.3粉针剂异物毛、点及块的判断,按卫生部药典委员会审定、上海市药品检验所制备供应的《澄明度异物对照标准》判断。
10滴眼剂检查法
10.1检查方法
取供试品30~50支,擦净容器外壁,检查时每次盒取3支,连续操作于伞树边沿处,手持容器颈部,使药液翻转,用目检视,每次检查时限为20s。另取供试品2支,将药液转移至洁净透明的玻璃容器内,在自然光下检视,除另有规定外,溶液应没明。10.2判断标准
10.2.1除特殊规定品种,每支含短于0.5cm的毛、500μm以下的白块或白点总数不得超过5个,但不得有特殊异物、色块或其他不溶性异物。10.2.2滴眼剂在出厂检验时,其不合格总支数不得超过检查总支数的8%,在贮存期检验时,其不合格总支数不得超过检查总支数的10%。如检查结果超过规定时,则加倍抽样复检,复检结果应符合规定。
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。