YY 0465-2003
基本信息
标准号: YY 0465-2003
中文名称:一次性使用空心纤维血浆分离器
标准类别:医药行业标准(YY)
标准状态:现行
出版语种:简体中文
下载格式:.zip .pdf
下载大小:648265

标准分类号
关联标准
出版信息
相关单位信息
标准简介
YY 0465-2003.
YY 0465规定了一次性使用空心纤维血浆分离器的术语和定义、要求、试验方法、检验规则、标志及包装、运输、贮存。
YY 0465适用于一次性使用空心纤维血浆分离器(简称血浆分离器),本产品配合血浆分离装登用来治疗各种免疫、代谢失调及某些中毒等危重病人进行治疗性血浆置换。
2规范性引用文件
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注8期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。
GB/T 191-2000包装 储运图示标志
GB/T2828--1987逐批检查计数抽样程序及抽样表(适用于连续批的检查)
GB/T2829---2002周期检查计数抽样程字及抽样表(适用于生产过程稳定的检查)
GB/T13074--1991血液净化术语.血液透析和血液滤过
GB/T 14233.1-1998医用输液 、输血.注射器具检验方法第1部分:化学分析方法
GB/T 14233.2- -1993 医用输液 输血、注射器具检验方法第二部分 .生物检验方法
GB/T 16886. 1- -2001医疗 器械生物学评价第1部分.评价与试验
GB18278--2000医疗保健产品灭菌确认和常规控制要求湿热灭菌
GB 18279--2000医疗器械 环氧乙烷灭 菌确认和常规控制
GB 18280- -2000医疗保健产品灭菌确认和常规控制要求辐射灭菌
ISO8637:1989血液透析器、血液滤过器和血液浓缩器
3术语和定义
下列术语和定义适用于本标准。
3.1
血浆分离plasmaseparation用来治疗各种免疫.代谢失调及某些中毒等危重病人进行治疗性血浆置換。
32
筛选率ftering rate超滤液中溶质浓度与血液中榕质浓度的比值.
33
血浆分离装置plasmaseparation system由血液监护、体液平衡、血浆分离器等系统组成的装置。
34
血浆分离器plasmaseparator用高分子聚合物膜制成的用于分离血液中的大分子蛋白的器件。
3.5
滤过率filtration rate
YY 0465规定了一次性使用空心纤维血浆分离器的术语和定义、要求、试验方法、检验规则、标志及包装、运输、贮存。
YY 0465适用于一次性使用空心纤维血浆分离器(简称血浆分离器),本产品配合血浆分离装登用来治疗各种免疫、代谢失调及某些中毒等危重病人进行治疗性血浆置换。
2规范性引用文件
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注8期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。
GB/T 191-2000包装 储运图示标志
GB/T2828--1987逐批检查计数抽样程序及抽样表(适用于连续批的检查)
GB/T2829---2002周期检查计数抽样程字及抽样表(适用于生产过程稳定的检查)
GB/T13074--1991血液净化术语.血液透析和血液滤过
GB/T 14233.1-1998医用输液 、输血.注射器具检验方法第1部分:化学分析方法
GB/T 14233.2- -1993 医用输液 输血、注射器具检验方法第二部分 .生物检验方法
GB/T 16886. 1- -2001医疗 器械生物学评价第1部分.评价与试验
GB18278--2000医疗保健产品灭菌确认和常规控制要求湿热灭菌
GB 18279--2000医疗器械 环氧乙烷灭 菌确认和常规控制
GB 18280- -2000医疗保健产品灭菌确认和常规控制要求辐射灭菌
ISO8637:1989血液透析器、血液滤过器和血液浓缩器
3术语和定义
下列术语和定义适用于本标准。
3.1
血浆分离plasmaseparation用来治疗各种免疫.代谢失调及某些中毒等危重病人进行治疗性血浆置換。
32
筛选率ftering rate超滤液中溶质浓度与血液中榕质浓度的比值.
33
血浆分离装置plasmaseparation system由血液监护、体液平衡、血浆分离器等系统组成的装置。
34
血浆分离器plasmaseparator用高分子聚合物膜制成的用于分离血液中的大分子蛋白的器件。
3.5
滤过率filtration rate
标准图片预览




标准内容
YY0465--2003
本标准的尺寸、机械性能.渗透性能的试验方法参照TS18637:1089《血液透析器,血液滤过器和血液浓缩器》的有关规定,化学性能参照GB83681998《一次性倬用输液器的有关规定,生物学性能参照GB/T16886.1—2001医疗器械生物学评价第1部分:评价与试验》巾的有关规定本标准的附录A、附录B、附录C是规范性附录本标准由国家食品药品监督管理局提出。本标准由全国医用体外循环设备标准化技术委员会归二。本标准白大津市泌尿外科研究所和大津泰达生物医学工程殿份有限公司负责起节。本标准主要起草人·顾汉卿、所茉珠、米惠飞、竺惕明、高增丽,1范围
一次性使用空纤维瓶浆分离器
YY0465—2003
本标准规定了一欢性使用空心纤维血紧分离器的术语和定义要求,试验方法,检验规则、标志及包装,运翰、此存。
本标准适用于一次性使用空心纤维血浆分离器(简称血浆分离器),本产品配合血浆分离装叠用来治疗各种免疫、代谢失调及某些中毒等危重病人进行治疗性血浆整换。2规范性引用文件
下列文件中的条款通过本标准的引用而我为本标窄的条款。凡是注扫期的引用文件,其随后所有的修改单(不包括勘误的内奔)或修汀版均不活用下本标准,然面,鼓励根据本标准达试协议的各方研究是否可使用这些文性的最新版本。凡是不注日期的引用文件,其最新版本适罚于本标准。GB/T191—2000包装懒运图示标志GB/T2828-1987燃批检查计数拍样程序及抽样表(透消于连续拢的查)GB/T2829一2002周期检查计数抽样程序及掘样表(适用于生产过程稳定的检查)GB/T13074-1991迦净化本语,血被读析租血滤过GB/T14233、1—1998医用输液、输痴,注射器具控验方法第!部分:化学分析法GB/T 14233.2----1993
医用輪液,输血、注射器其检验方法第二部分·生物捡验方法践疗器械生物学评价第1部分·评价与试验GB/T16886.1---200
GB18278—2000医疗保健产品火菌确认和常规控制要戏混热灭菌GB18279-2000
医疗器械环氧艺烷灭菌确认和常规控制医疗保产品灰菌确认和常规控制要求辐射灭菌GB18280—2000
1508637:1989血疫透析器、血液滤过器和血液教缩器3术语和定义
下列术语和定义适用于本标难
血浆分离plasaseparatiu
用衰治疗登种免疫,代谢失调及基些中毒等危重病人进行治疗性垂聚置换。32
筛选率fileringrate
超液中质液度与血中溶质滋度的比值。33
自辣分离装翼patpartiostste
l血液监护、体液平衡、和浆分离器等系统组成的装置。34
血浆分离器playmaseparatnr
用高分子聚合物膜制或的用于分离耻液中的大分了蛋白的器件,3.5
滤过率fitrati rate
FKNIKAa
YY 0465—2003
作单位时间内血聚分离器能将血液中的某些物质滤低的量。3.6
跨膜压transmembrane pressure血浆分离器的半透膜两侧的我体韵水压装37
面租e
吸浆分离器内半透膜与血波接触的面,以孕方长为单佐的计算。3.8
血案容量blonkl mpartmeit yolun心在设定磨压时充满血聚分离器的血液容积:39
血液流率bleud fluu ratc
在单位时间内流经血浆分离器的血浓景.以mL/mn表示,3.10
模拟血液mitationblood
人工配置近似血液中所含毒索物质的液体,3
洗脱获lerng nad
以注射用水没滤待谢器件后陷液体。4分类与命名
4.1型式
血浆分离器的型式为空心纤维型。4.2血浆分离器的基本舒数
4. 2 1血浆分离蛋的有效膜面积削浆夺离器的有效膜面积不低于公称膜面积的。4. 2. 2血案分离器的血流率
血浆分离器的血流应大于200 mL/min,4. 2. 3血浆分两器减过滋流率
渐浆分离器滤过液流率成大于 ml./r!n,4. 2 4血紧分离器的血室容素
血浆分离器的症室容教不大于 mI-4. 3血浆分离器的基本尽寸
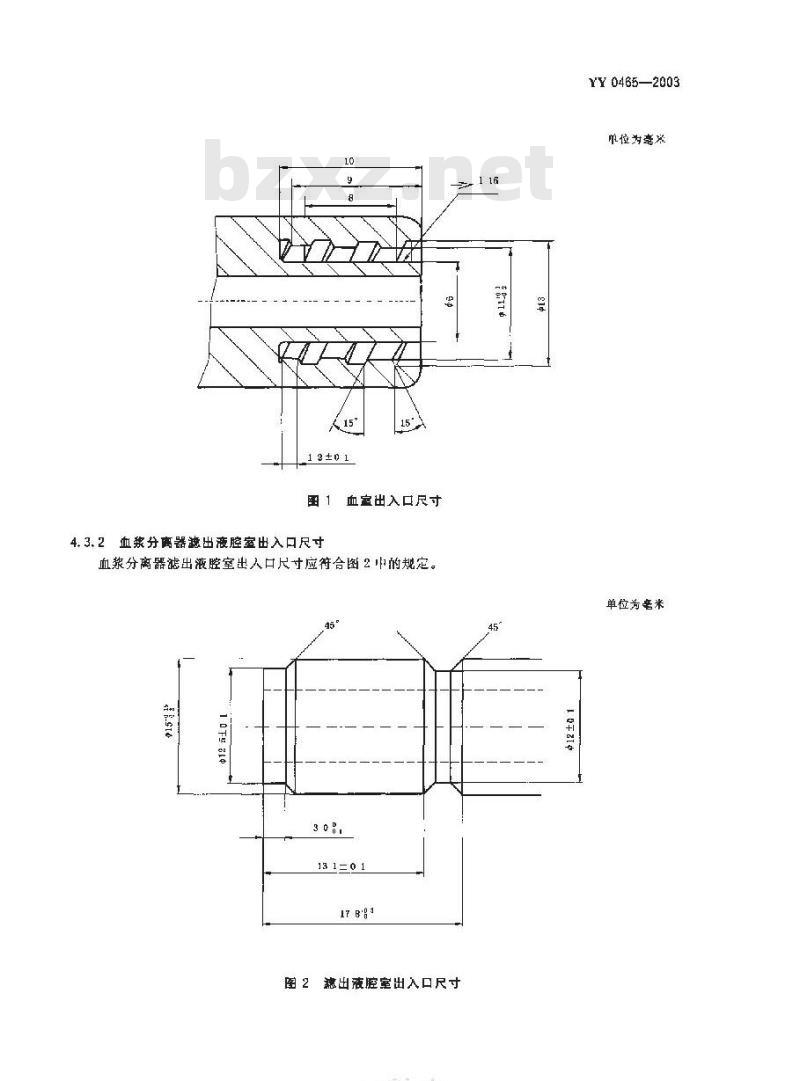
4 1 血浆分离器血室出入口片寸迎浆分离器血室出,人口尺寸应符合离1的规定,10
12±01
图1血室出入口尺寸
4. 3. 2血浆分离器范出液腔室出入口尺寸血浆分离器滤出液腔室出人口尺寸应符合图2 中的规定。45
13 1=0 1
图2滤出液腔室出入口尺寸
rKAoNiiKAca
YY0465—2003
单位为毫
单位为老米
YY 0465--2003
型号命名
5要求
5.1外澳
膜公称面积,m
··系列代号
血浆分离器的外壳应透明,表面光错,滋林通道内不得简肉眼可的杂质。5.2尺寸
而浆分离器的有救膜面积应衍合4.2.1的规定。5.3盘藍容量
率容氧应符合 4.2 4 的规定,
5.4微粒
而浆分离器内腔应沾许,100 mL,洗脱液 15 μm~25 剂m1 的微粒数不得超过200个,大于25 μm的微粒数不得超过100个。
55血浆分离器的化学性能
5.5.1还原物质(易氧化物)
检验液和空白波消耗高锰酸钾游液[c(KMnr),>=0.002mal/I.]的体积之差应不超过2.0ml55.2金属离子
55.21原子吸牧分光光度计(AAS)或相当的方法进行测定时,检验液中锁、整、铅,需的总含量虚不超过 1 μg/ml。辐的含量应不超过0 1 μg/ml.。5.5,2 2比色分析方法,试验液卓现的题色应不超过质量浓度p(Pb2/ )=1. g/ml.标准对照液。553酸威度
检验液与空白液pH值之龚应不超1。5.5,4蒸发残渣
蒸发残谱的总量应不超过2mg。
5.55紫外吸光度
检验液的吸光度应不大10.1.
5.5.6环氧乙烷残留量
浆分离器用环氧之烷泥,环氧乙烷残留量避不大于15/名。5.6助浆分离器的生物性能
561生物学评价
血浆分离器成按GB/T16886.1--2091的规定要求进行生物学评价。5.6.2无兹
浆分离器应无菌,
5.6.3无致热原
血浆分离器应尤致热原。
57血浆分离器的密封性能
51血浆分离器血室承受压力
it浆分离器血室应能承受 100 k 的就验压力。57.2血浆分离器出腔室承受压力应策变正斥100 kPa,负压低于大气压93 3 kPa的验照小。5. 8 血浆分离器潜还性能
YY 0465-2003
奥浆分离器当跨膜压9.3kPa.纽流率150mL/mln时.0.5m赚面积的直浆分离器其渗透性能应符合以下要求:
5. 8. 1血浆滤过率
血浆滤过率应大手40mL/min
5, 8. 2总酸白筛选系数
总蛋血筛选系数多0.8。
5. 9 血浆分离器耐漏性能
血浆分离器在℃~5心溢度范国内不应有婆膨和破裂。6试验方法
61外观
日成符合51的规定。
6.2尺寸
血浆分离器的有效膜面积按式(1)算:S = rDL +n× 10-
式中;
S—有效膜面积,单位为乎方米(n\)一察心纤继内经单位齿旁米(
L-----空心纤维有效长度,单位为毫术(mm);R——空心纤维根数。
6 3血室容量检验
血液创、滤出液侧均充填经过脱气而不留气泡的充填滤,放置601m11,先使滤乌液侧处于密闭状态后,来用如压空气(约50kIa)将迎液衡的水排测盘(需减去滤出液谢渗透到血液侧的最)。应符合53的规定。
6,4微粒
按录 A进行应符合5 4的规定。
6 5化学性能试验方法
651试孩制备瑕-灭菌后的产品和玻璃烧瓶连成-一循环系统,房密于封性减出滚出口,按公称纤继面积1m约用500mL生理盐水比例邮人生理盐水并保持在37℃C士1℃,通过动泵作用于一殷尽可能短的用硅橡胶管1.,使水以1L/h的流录循环2h。取50ml循环液稀释至1000mL备用。652还原物质(葛氧化物)试验
接GB/ 14233. 1—1S98 中 5.2,2方法兰规定进行,应符合 5.5.1的要求。6. 5. 3金离离子试验
6531原子吸收分光光度法为中裁方法,检验液的吸光度应不大于0.1,应符合5.5.2.1的要求。6.5.3.2比包+按GB/T14233.1-1998中5.5.1法规定进行,应符合5.522的要求。6. 5. 3 酸碱度
按GB/T142331*-1998中5.4,1方法一规定进行,应符合5,5.3的要求,6.5.4蒸发残液
按GB/T1423311998规定进行,庞符合5.5.4要求,6. 5.5紫外吸光度
HTTKAONKAa
YY0465—2003
按 GR/T 14233 1--1998 中规定在 250 nm~320 nm 波长范围内进行,应符合 5. 5. 5要求。6.5.6环氧乙烷残留量
按GB/T14233.1—1998第三篇的万法进行,应符合556要求。66生物性能试验方法
66.1生物学评价
企业产品注册时应按GB/T16886.12001的规定内容进行生物学性能的评价。若需要进行试验应进行:
6.6.1.1细跑毒性,按GB/T14233.2—1993中第7章的规定进行,应≤1级。6 6.1,2皮内刺激,按(:H/F 12233 2一1993 中第 8 章的观定进行,应无刺激作用。6 6.13致敏试验按 CB/T 12233.2—1993 中第 9章的规定进行,应无致敏物。6. 6. 1. 4急性声性试验,按 G13/ T 14233 2一1993 中第 5 章的现定进行,应无急性会身毒性应。6 6. 1 5血液相容性,溶血试验按 GB/T 14233 2—1993 中第 6 章的规定选行,溶证率≤5%。6.6.2无菌试验
主浆分离器按(:H/T18278—2C00或GB/T182792000或GB/T18280—2093确认过的火菌过程便其尤菌。其后对每一生产批的灭菌程序进行监控。66.3无热原试验
应对销售前的血浆分离器进行无热原程序确认,其后生产厂须定期进行热原试验:以保证器件无热原。
67密封性能试验
接ISO86371989中5.3机械性能试验方法进行,应符合57的规定。6 8渗透性能试验
6.8.1血浆滤过率试验
按附录的方法进行,应符合三81的规定!6. 8 2总蛋白筛选系数试验
按附求(的方法进行,应符合5.82的规定6. 9耐温试验
将血浆分离器放人℃冰箱中3min,然后放人50℃恒温箱中3h,取出后恢复至室温进行观察并做斥力试验,应符合5.9的规定,
7检验规则bzxz.net
71出厂检验
7 1.1出检验为逐挑检验。
71.2山检验以每月产量为·-捡查批。713避批检验应符含GI/T2828有关规定:7. 1. 4 检查采用一次性抽样方案,其检查分类,检查项目,合格质年水平(AQ1.)和检查水平按表 1规定。
7 2周期检验
7 2. 1 在下列情况 下应进行周期检验:a)产品注册挝:
b)在1.艺配方或材料有重大变动可能影响产品质量时:c)正常生产时每年的不少于一次;d)停产半年以上恢复生产时:
e)国家质量监再部门提出要求时:7. 2. 2
检查分类
试验组
检查项目
检查水平
出厂检验抽样方案
全部含格
YY 0465--2003
周期检查采用一次抽样方案,其检查分类、不合格质量水平(RQL)和判别水平按表2规定表2周期检验抽样方案
检查分类
检查项目
判圳水半
检查期
30(A.=0 R.=1)
每年一次
45(A4.=0 R. =1)
每半年一次
40(4. =1 R. =2)
每半年一次
72.3周期检查应在逐批检吉合格后进行,周期检查不合格的处理按GB/T2829进行。724
按GB/T16886.1—2001中37的要求进行生物学性能再评价。8标志
每只血浆分离器在外壳明显位应有下列标志:a)
制造厂名称,地址和商标,
产品名称和型号
生产批号和日期:
灭菌方法和有效期:
有效面积,
最高使用压力!
一次性使用,
产品注册号:
8.2合格证上应有下列标志:
制造厂名称:
产品名称、型号:
c)检验员代码1
d)检验R期。
8.3外包装箱上应有下列标志
a)制造厂名,地址,
b)产品名称和型凸:
e),
FTKAONKAca-
YY0465—2003
d)毛重;
体积(长×宽×高);
生产批号和灭菌日期,
g)产品合格证和有效期;
h):产品注册号;
1)产品标准编号;
J)一次性使用字样:
“小心轻放”、“切勿重压”、“怕湿”等字样或标志,应符合GB/T191规定。k)
包装、运输、贮存
9.1包装
91.1血浆分离器单包装
每只血浆分离器应用复合薄膜袋封装,密封后再装入包装盒,盒内应有使用说明书和检验合格证各一份。
血浆分离器外包装
外包装采用瓦楞包装箱。
2运输
运输方式按订货合同规定,运输中应防止重压并避免碰撞和雨雪淋袭9.3贮存
包装好的血浆分离器应贮存在相对湿度不超过80%,无腐蚀性气体,阴凉、干燥,通风良好、清洁的环境内。血浆分离器在符合贮存规定的条件下,灭菌有效期为2年。A, 1康理
附录A
(规范性附录)
血浆分离器微粒含量测定方法
YY 0465—2003
这一方法是通过冲洗内腔液体通道表面,收集通道表面洗脱被中的粒子,并对其计数米评价污染。A,2试验仪器
仅端与装如图A.1所示。
空气过滤器:
进气针,
氧化钠注射液,
过滤装量,
三通开关,
聚氧乙.渐软管,
被测血浆分剪器。
微粒计数器,
取样杯。
图A1微粒含量测定装置
YY04652003
焦 2. 1也阻式粒子计数器:有搅拌系统,一次取样量为 1l mL,可同时对 15 μm~25 μm 和大于25μm的微粒计数,
A.2 2过滤装置-内装直径 50 mm,径0. 45 μm的微孔滤膜,A.2.3冲洗液·氯化钠注射液。
4.24聚氟乙烯软管:软管长1m,外径35mm~4mm。A.2.5三通转换川关。
A.3步骤
过滤装置通过瓶寒穿刺器与装有氣化钢注射液的被瓶工连接,过滤装下端接三通转换刀关,下接软节至微粒计数器取样杯,A3.2用100mL冲洗浓冲洗过滤器、三通转携川关和软带社韧孩试骑冲洗液应不少于 2 LA 3. 3在约 1 m静压头下,使冲识液通过较管20 mL,流品液流人数器的圾杯中即得本底液,测定100ml.本底液中微粒数。
注试验底法点环境污染。
3.4重复A3,5的步骤,以两次计数的半均值为100 ml.本底液中微粒含量。A.35使进气口密封,将血浆分离器的进液端与二道转换开关的另一接头连接,13.6在1m静斤头下,使冲洗滋过血聚离器200mL,流出泄流人计数器4mL.用注射用水棉释至100mI的取样杯中即得洗脱液,谢定100mI.洗脱涨中的微效数:A4结果表示
洗脱液与本底液微粒读数之差为舒就液中的微橙含量。B.1自的
附录B
(规范性附录》
血浆分离器透性能的测定
通过滋定了解而滋的血紧分离值和蛋白筛选率。B 2 设备与仪器
I. 2 1 浓珠血泵,
B 2 2 500 mI. 量简。
B.2.3负压泵
B.2.41 Cco mL盛液简,
B.2.5血液回路导带。
B3试剂
新鲜猪而500 mL加2%草酸钾制备戒新鲜抗凝猪血。B.4操作步骤
YY 0465—2003
将血波回路导管进血出血口接人而浆分离器进血出血口,动静脉管插人露有抗凝猪血容器。B. 4. 1
B.4.2将血液回路导管、泵管接人血泵滚珠泵头。B 4,3将血浆分离器出液口上端有寒于塞住,下端接人负束,间接有盛液瓶。B, 4. 4将血泵肩动,血流量为 150 mL/min,负压录启动,跨膜压 9. 3 kPa,运转 3 nun 停止工作,B.4.5把滤出液体清理到盛液瓶,有望简计里。B 5结果表示
计量超过120mL血聚渗透性能为合格。FKNrKAc
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
本标准的尺寸、机械性能.渗透性能的试验方法参照TS18637:1089《血液透析器,血液滤过器和血液浓缩器》的有关规定,化学性能参照GB83681998《一次性倬用输液器的有关规定,生物学性能参照GB/T16886.1—2001医疗器械生物学评价第1部分:评价与试验》巾的有关规定本标准的附录A、附录B、附录C是规范性附录本标准由国家食品药品监督管理局提出。本标准由全国医用体外循环设备标准化技术委员会归二。本标准白大津市泌尿外科研究所和大津泰达生物医学工程殿份有限公司负责起节。本标准主要起草人·顾汉卿、所茉珠、米惠飞、竺惕明、高增丽,1范围
一次性使用空纤维瓶浆分离器
YY0465—2003
本标准规定了一欢性使用空心纤维血紧分离器的术语和定义要求,试验方法,检验规则、标志及包装,运翰、此存。
本标准适用于一次性使用空心纤维血浆分离器(简称血浆分离器),本产品配合血浆分离装叠用来治疗各种免疫、代谢失调及某些中毒等危重病人进行治疗性血浆整换。2规范性引用文件
下列文件中的条款通过本标准的引用而我为本标窄的条款。凡是注扫期的引用文件,其随后所有的修改单(不包括勘误的内奔)或修汀版均不活用下本标准,然面,鼓励根据本标准达试协议的各方研究是否可使用这些文性的最新版本。凡是不注日期的引用文件,其最新版本适罚于本标准。GB/T191—2000包装懒运图示标志GB/T2828-1987燃批检查计数拍样程序及抽样表(透消于连续拢的查)GB/T2829一2002周期检查计数抽样程序及掘样表(适用于生产过程稳定的检查)GB/T13074-1991迦净化本语,血被读析租血滤过GB/T14233、1—1998医用输液、输痴,注射器具控验方法第!部分:化学分析法GB/T 14233.2----1993
医用輪液,输血、注射器其检验方法第二部分·生物捡验方法践疗器械生物学评价第1部分·评价与试验GB/T16886.1---200
GB18278—2000医疗保健产品火菌确认和常规控制要戏混热灭菌GB18279-2000
医疗器械环氧艺烷灭菌确认和常规控制医疗保产品灰菌确认和常规控制要求辐射灭菌GB18280—2000
1508637:1989血疫透析器、血液滤过器和血液教缩器3术语和定义
下列术语和定义适用于本标难
血浆分离plasaseparatiu
用衰治疗登种免疫,代谢失调及基些中毒等危重病人进行治疗性垂聚置换。32
筛选率fileringrate
超液中质液度与血中溶质滋度的比值。33
自辣分离装翼patpartiostste
l血液监护、体液平衡、和浆分离器等系统组成的装置。34
血浆分离器playmaseparatnr
用高分子聚合物膜制或的用于分离耻液中的大分了蛋白的器件,3.5
滤过率fitrati rate
FKNIKAa
YY 0465—2003
作单位时间内血聚分离器能将血液中的某些物质滤低的量。3.6
跨膜压transmembrane pressure血浆分离器的半透膜两侧的我体韵水压装37
面租e
吸浆分离器内半透膜与血波接触的面,以孕方长为单佐的计算。3.8
血案容量blonkl mpartmeit yolun心在设定磨压时充满血聚分离器的血液容积:39
血液流率bleud fluu ratc
在单位时间内流经血浆分离器的血浓景.以mL/mn表示,3.10
模拟血液mitationblood
人工配置近似血液中所含毒索物质的液体,3
洗脱获lerng nad
以注射用水没滤待谢器件后陷液体。4分类与命名
4.1型式
血浆分离器的型式为空心纤维型。4.2血浆分离器的基本舒数
4. 2 1血浆分离蛋的有效膜面积削浆夺离器的有效膜面积不低于公称膜面积的。4. 2. 2血案分离器的血流率
血浆分离器的血流应大于200 mL/min,4. 2. 3血浆分两器减过滋流率
渐浆分离器滤过液流率成大于 ml./r!n,4. 2 4血紧分离器的血室容素
血浆分离器的症室容教不大于 mI-4. 3血浆分离器的基本尽寸
4 1 血浆分离器血室出入口片寸迎浆分离器血室出,人口尺寸应符合离1的规定,10
12±01
图1血室出入口尺寸
4. 3. 2血浆分离器范出液腔室出入口尺寸血浆分离器滤出液腔室出人口尺寸应符合图2 中的规定。45
13 1=0 1
图2滤出液腔室出入口尺寸
rKAoNiiKAca
YY0465—2003
单位为毫
单位为老米
YY 0465--2003
型号命名
5要求
5.1外澳
膜公称面积,m
··系列代号
血浆分离器的外壳应透明,表面光错,滋林通道内不得简肉眼可的杂质。5.2尺寸
而浆分离器的有救膜面积应衍合4.2.1的规定。5.3盘藍容量
率容氧应符合 4.2 4 的规定,
5.4微粒
而浆分离器内腔应沾许,100 mL,洗脱液 15 μm~25 剂m1 的微粒数不得超过200个,大于25 μm的微粒数不得超过100个。
55血浆分离器的化学性能
5.5.1还原物质(易氧化物)
检验液和空白波消耗高锰酸钾游液[c(KMnr),>=0.002mal/I.]的体积之差应不超过2.0ml55.2金属离子
55.21原子吸牧分光光度计(AAS)或相当的方法进行测定时,检验液中锁、整、铅,需的总含量虚不超过 1 μg/ml。辐的含量应不超过0 1 μg/ml.。5.5,2 2比色分析方法,试验液卓现的题色应不超过质量浓度p(Pb2/ )=1. g/ml.标准对照液。553酸威度
检验液与空白液pH值之龚应不超1。5.5,4蒸发残渣
蒸发残谱的总量应不超过2mg。
5.55紫外吸光度
检验液的吸光度应不大10.1.
5.5.6环氧乙烷残留量
浆分离器用环氧之烷泥,环氧乙烷残留量避不大于15/名。5.6助浆分离器的生物性能
561生物学评价
血浆分离器成按GB/T16886.1--2091的规定要求进行生物学评价。5.6.2无兹
浆分离器应无菌,
5.6.3无致热原
血浆分离器应尤致热原。
57血浆分离器的密封性能
51血浆分离器血室承受压力
it浆分离器血室应能承受 100 k 的就验压力。57.2血浆分离器出腔室承受压力应策变正斥100 kPa,负压低于大气压93 3 kPa的验照小。5. 8 血浆分离器潜还性能
YY 0465-2003
奥浆分离器当跨膜压9.3kPa.纽流率150mL/mln时.0.5m赚面积的直浆分离器其渗透性能应符合以下要求:
5. 8. 1血浆滤过率
血浆滤过率应大手40mL/min
5, 8. 2总酸白筛选系数
总蛋血筛选系数多0.8。
5. 9 血浆分离器耐漏性能
血浆分离器在℃~5心溢度范国内不应有婆膨和破裂。6试验方法
61外观
日成符合51的规定。
6.2尺寸
血浆分离器的有效膜面积按式(1)算:S = rDL +n× 10-
式中;
S—有效膜面积,单位为乎方米(n\)一察心纤继内经单位齿旁米(
L-----空心纤维有效长度,单位为毫术(mm);R——空心纤维根数。
6 3血室容量检验
血液创、滤出液侧均充填经过脱气而不留气泡的充填滤,放置601m11,先使滤乌液侧处于密闭状态后,来用如压空气(约50kIa)将迎液衡的水排测盘(需减去滤出液谢渗透到血液侧的最)。应符合53的规定。
6,4微粒
按录 A进行应符合5 4的规定。
6 5化学性能试验方法
651试孩制备瑕-灭菌后的产品和玻璃烧瓶连成-一循环系统,房密于封性减出滚出口,按公称纤继面积1m约用500mL生理盐水比例邮人生理盐水并保持在37℃C士1℃,通过动泵作用于一殷尽可能短的用硅橡胶管1.,使水以1L/h的流录循环2h。取50ml循环液稀释至1000mL备用。652还原物质(葛氧化物)试验
接GB/ 14233. 1—1S98 中 5.2,2方法兰规定进行,应符合 5.5.1的要求。6. 5. 3金离离子试验
6531原子吸收分光光度法为中裁方法,检验液的吸光度应不大于0.1,应符合5.5.2.1的要求。6.5.3.2比包+按GB/T14233.1-1998中5.5.1法规定进行,应符合5.522的要求。6. 5. 3 酸碱度
按GB/T142331*-1998中5.4,1方法一规定进行,应符合5,5.3的要求,6.5.4蒸发残液
按GB/T1423311998规定进行,庞符合5.5.4要求,6. 5.5紫外吸光度
HTTKAONKAa
YY0465—2003
按 GR/T 14233 1--1998 中规定在 250 nm~320 nm 波长范围内进行,应符合 5. 5. 5要求。6.5.6环氧乙烷残留量
按GB/T14233.1—1998第三篇的万法进行,应符合556要求。66生物性能试验方法
66.1生物学评价
企业产品注册时应按GB/T16886.12001的规定内容进行生物学性能的评价。若需要进行试验应进行:
6.6.1.1细跑毒性,按GB/T14233.2—1993中第7章的规定进行,应≤1级。6 6.1,2皮内刺激,按(:H/F 12233 2一1993 中第 8 章的观定进行,应无刺激作用。6 6.13致敏试验按 CB/T 12233.2—1993 中第 9章的规定进行,应无致敏物。6. 6. 1. 4急性声性试验,按 G13/ T 14233 2一1993 中第 5 章的现定进行,应无急性会身毒性应。6 6. 1 5血液相容性,溶血试验按 GB/T 14233 2—1993 中第 6 章的规定选行,溶证率≤5%。6.6.2无菌试验
主浆分离器按(:H/T18278—2C00或GB/T182792000或GB/T18280—2093确认过的火菌过程便其尤菌。其后对每一生产批的灭菌程序进行监控。66.3无热原试验
应对销售前的血浆分离器进行无热原程序确认,其后生产厂须定期进行热原试验:以保证器件无热原。
67密封性能试验
接ISO86371989中5.3机械性能试验方法进行,应符合57的规定。6 8渗透性能试验
6.8.1血浆滤过率试验
按附录的方法进行,应符合三81的规定!6. 8 2总蛋白筛选系数试验
按附求(的方法进行,应符合5.82的规定6. 9耐温试验
将血浆分离器放人℃冰箱中3min,然后放人50℃恒温箱中3h,取出后恢复至室温进行观察并做斥力试验,应符合5.9的规定,
7检验规则bzxz.net
71出厂检验
7 1.1出检验为逐挑检验。
71.2山检验以每月产量为·-捡查批。713避批检验应符含GI/T2828有关规定:7. 1. 4 检查采用一次性抽样方案,其检查分类,检查项目,合格质年水平(AQ1.)和检查水平按表 1规定。
7 2周期检验
7 2. 1 在下列情况 下应进行周期检验:a)产品注册挝:
b)在1.艺配方或材料有重大变动可能影响产品质量时:c)正常生产时每年的不少于一次;d)停产半年以上恢复生产时:
e)国家质量监再部门提出要求时:7. 2. 2
检查分类
试验组
检查项目
检查水平
出厂检验抽样方案
全部含格
YY 0465--2003
周期检查采用一次抽样方案,其检查分类、不合格质量水平(RQL)和判别水平按表2规定表2周期检验抽样方案
检查分类
检查项目
判圳水半
检查期
30(A.=0 R.=1)
每年一次
45(A4.=0 R. =1)
每半年一次
40(4. =1 R. =2)
每半年一次
72.3周期检查应在逐批检吉合格后进行,周期检查不合格的处理按GB/T2829进行。724
按GB/T16886.1—2001中37的要求进行生物学性能再评价。8标志
每只血浆分离器在外壳明显位应有下列标志:a)
制造厂名称,地址和商标,
产品名称和型号
生产批号和日期:
灭菌方法和有效期:
有效面积,
最高使用压力!
一次性使用,
产品注册号:
8.2合格证上应有下列标志:
制造厂名称:
产品名称、型号:
c)检验员代码1
d)检验R期。
8.3外包装箱上应有下列标志
a)制造厂名,地址,
b)产品名称和型凸:
e),
FTKAONKAca-
YY0465—2003
d)毛重;
体积(长×宽×高);
生产批号和灭菌日期,
g)产品合格证和有效期;
h):产品注册号;
1)产品标准编号;
J)一次性使用字样:
“小心轻放”、“切勿重压”、“怕湿”等字样或标志,应符合GB/T191规定。k)
包装、运输、贮存
9.1包装
91.1血浆分离器单包装
每只血浆分离器应用复合薄膜袋封装,密封后再装入包装盒,盒内应有使用说明书和检验合格证各一份。
血浆分离器外包装
外包装采用瓦楞包装箱。
2运输
运输方式按订货合同规定,运输中应防止重压并避免碰撞和雨雪淋袭9.3贮存
包装好的血浆分离器应贮存在相对湿度不超过80%,无腐蚀性气体,阴凉、干燥,通风良好、清洁的环境内。血浆分离器在符合贮存规定的条件下,灭菌有效期为2年。A, 1康理
附录A
(规范性附录)
血浆分离器微粒含量测定方法
YY 0465—2003
这一方法是通过冲洗内腔液体通道表面,收集通道表面洗脱被中的粒子,并对其计数米评价污染。A,2试验仪器
仅端与装如图A.1所示。
空气过滤器:
进气针,
氧化钠注射液,
过滤装量,
三通开关,
聚氧乙.渐软管,
被测血浆分剪器。
微粒计数器,
取样杯。
图A1微粒含量测定装置
YY04652003
焦 2. 1也阻式粒子计数器:有搅拌系统,一次取样量为 1l mL,可同时对 15 μm~25 μm 和大于25μm的微粒计数,
A.2 2过滤装置-内装直径 50 mm,径0. 45 μm的微孔滤膜,A.2.3冲洗液·氯化钠注射液。
4.24聚氟乙烯软管:软管长1m,外径35mm~4mm。A.2.5三通转换川关。
A.3步骤
过滤装置通过瓶寒穿刺器与装有氣化钢注射液的被瓶工连接,过滤装下端接三通转换刀关,下接软节至微粒计数器取样杯,A3.2用100mL冲洗浓冲洗过滤器、三通转携川关和软带社韧孩试骑冲洗液应不少于 2 LA 3. 3在约 1 m静压头下,使冲识液通过较管20 mL,流品液流人数器的圾杯中即得本底液,测定100ml.本底液中微粒数。
注试验底法点环境污染。
3.4重复A3,5的步骤,以两次计数的半均值为100 ml.本底液中微粒含量。A.35使进气口密封,将血浆分离器的进液端与二道转换开关的另一接头连接,13.6在1m静斤头下,使冲洗滋过血聚离器200mL,流出泄流人计数器4mL.用注射用水棉释至100mI的取样杯中即得洗脱液,谢定100mI.洗脱涨中的微效数:A4结果表示
洗脱液与本底液微粒读数之差为舒就液中的微橙含量。B.1自的
附录B
(规范性附录》
血浆分离器透性能的测定
通过滋定了解而滋的血紧分离值和蛋白筛选率。B 2 设备与仪器
I. 2 1 浓珠血泵,
B 2 2 500 mI. 量简。
B.2.3负压泵
B.2.41 Cco mL盛液简,
B.2.5血液回路导带。
B3试剂
新鲜猪而500 mL加2%草酸钾制备戒新鲜抗凝猪血。B.4操作步骤
YY 0465—2003
将血波回路导管进血出血口接人而浆分离器进血出血口,动静脉管插人露有抗凝猪血容器。B. 4. 1
B.4.2将血液回路导管、泵管接人血泵滚珠泵头。B 4,3将血浆分离器出液口上端有寒于塞住,下端接人负束,间接有盛液瓶。B, 4. 4将血泵肩动,血流量为 150 mL/min,负压录启动,跨膜压 9. 3 kPa,运转 3 nun 停止工作,B.4.5把滤出液体清理到盛液瓶,有望简计里。B 5结果表示
计量超过120mL血聚渗透性能为合格。FKNrKAc
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。