基本信息
标准号:
YY/T 0656-2008
中文名称:自动化血培养系统
标准类别:医药行业标准(YY)
标准状态:现行
出版语种:简体中文
下载格式:.zip .pdf
下载大小:1.11 MB
相关标签:
自动化
培养
系统

标准分类号
关联标准
出版信息
相关单位信息
标准简介
YY/T 0656-2008.Automated blood culture system.
YY/T 0656规定了自动化血培养系统的术语、定义、要求、试验方法、标志、标签和说明书、包装、运输和贮存。
YY/T 0656适用于临床实验室通过体外培养,检测人体血液或其他在正常条件下无菌的体液(以下称无菌体液)中微生物的自动化血培养系统(以下简称血培养系统),包括血培养设备及其所配套的培养基。
YY/T 0656所指微生物的范围是细菌和酵母样真菌。
2规范性引用文件
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。
GB4793.1测量、控制和试验室用电气设备的安全要求第1部分:通用要求
GB/T 14710医用电气设备环境要求及试验方法
3术语和定义
下列术语和定义适用于本标准。
3.1血培养blood culture临床实验室通过体外培养,检测人体血液或其他无菌体液中的微生物。
3.2血培养用培养基blood culture media用于体外培养人体血液或其他无菌体液中的微生物的培养基。
3.3自动化血培养系统automated blood culture system用于临床实验室在体外对人体血液或其他无菌体液中的微生物连续培养、自动检测和判断培养结果(阳性或阴性)的系统,该系统包括血培养仪及其相配套的培养基。
3.4血培养阳性blood culture positive血培养系统检测到血培养用培养基中有微生物存在。
3.5血培养阴性blood culture negative在培养周期内,血培养系统未能检测到血培养用培养基内有微生物存在。
3.6血培养假阳性false positive
标准内容
ICS11.100
中华人民共和国医药行业标准
YY/T0656—2008
自动化血培养系统
Automatedbloodculturesystem
2008-04-25发布
数码防61
国家食品药品监督管理局
2009-06-01实施
本标准由国家食品药品监督管理局提出。YY/T0656-2008
本标准由全国医用临床检验实验室和体外诊断系统标准化技术委员会(SAC/TC136)归口。本标准主要起草单位:美国BD公司、法国生物梅里埃公司、北京市医疗器械检验所。本标准主要起草人:童明庆、沈然、王辉、肖志强。1范围
自动化血培养系统
YY/T0656—2008
本标准规定了自动化血培养系统的术语、定义、要求、试验方法、标志、标签和说明书、包装、运输和存。
本标准适用于临床实验室通过体外培养,检测人体血液或其他在正常条件下无菌的体液(以下称无菌体液)中微生物的自动化血培养系统(以下简称血培养系统),包括血培养设备及其所配套的培养基。本标准所指微生物的范围是细菌和酵母样真菌。2规范性引用文件
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。GB4793.1测量、控制和试验室用电气设备的安全要求第1部分:通用要求GB/T14710医用电气设备环境要求及试验方法3术语和定义
下列术语和定义适用于本标准。3.1
血培养bloodculturebZxz.net
临床实验室通过体外培养,检测人体血液或其他无菌体液中的微生物3.2
血培养用培养基bloodculturemedia用于体外培养人体血液或其他无菌体液中的微生物的培养基。3.3
自动化血培养系统automatedbloodculturesystem用于临床实验室在体外对人体血液或其他无菌体液中的微生物连续培养、自动检测和判断培养结果(阳性或阴性)的系统,该系统包括血培养仪及其相配套的培养基。3.4
血培养阳性bloodculturepositive血培养系统检测到血培养用培养基中有微生物存在3.5
血培养阴性bloodculturenegative在培养周期内,血培养系统未能检测到血培养用培养基内有微生物存在。3.6
血培养假阳性falsepositive
血培养系统判断血培养阳性,但染色镜检及转种后未见微生物存在。3.7
false negative
血培养假阴性
血培养系统判断血培养阴性,但染色镜检及转种后发现微生物存在。1
YY/T0656-2008
4要求
4.1正常工作条件
正常工作条件应满足下列要求:a)环境温度:在说明书中明确;b)相对湿度:在说明书中明确;电源电压:220V±22V,50Hz±1Hzc
大气压力:在说明书中明确。
4.2系统功能
4.2.1具有连续孵育功能。
4.2.2自动监测和判断培养结果(培养阳性和培养阴性)。4.2.3培养阳性应有明确的习式。4.2.4应提供温度失控报
4.3阳性培养结果的重烤
血培养系统对标准菌标的检测
4.4血培养用培养
光菌试验
血培养系统对未进骨接种的血增养用应为阴性。
4.5培养基的稳
4.5.1用到效期
4.5.2未进行按机
在血培养泰统中进行培养,结果均基按产品
明书要求
个月内的血培养用培养基对标难菌株的检测绪果应为阳性
用到效期后
4.6温度准确度波
内血培养用培养基的检时结果
果应为阴性
温度准确度度波动应满足下列
a)血培养系统注
度准确度偏差应不
b)温度波动
4.7外观
4.7.1血培养仪
天超过3.0%
血培养仪外观应待
刻要求
应整洁,无划痕文身和标识清晰;a)
紧固件连接应牢
4.7.2血培养用培养基
过+15℃:
,不得有松动。
血培养用培养基外观应符合下列要求:盛装血培养用培养基的容器的外观应整洁,文字符号标识清晰a)
盛装血培养用培养基的容器应无裂缝、出封性好,无漏液、渗液;b)
c)血培养用培养基内的液体无浑浊、无絮状沉淀、清澈透明。4.8环境试验
应符合GB/T14710中适用环境组别的要求。4.9电气安全
应符合GB4793.1的要求。
5试验方法
5.1试验条件
按照4.1规定的正常工作条件进行。5.2系统功能
开机后逐项验证,应符合4.2的要求。5.3阳性培养结果的重复性试验
YY/T0656—2008
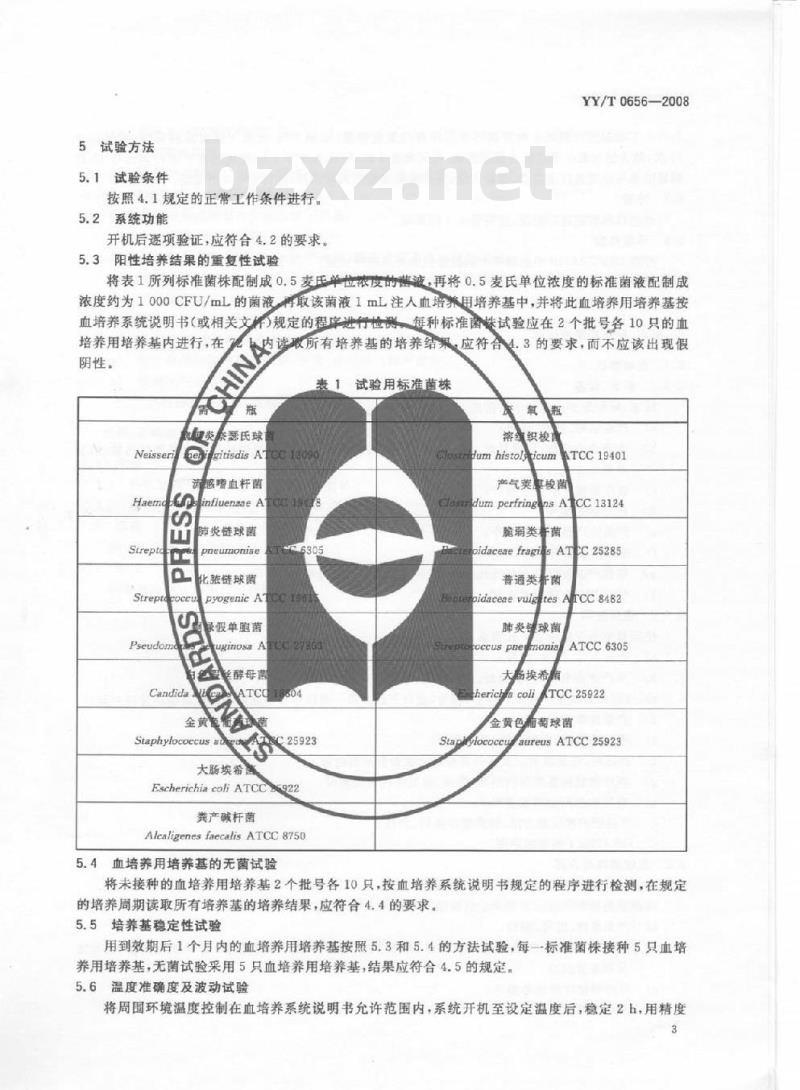
将表1所列标准菌株配制成0.5麦氏单位浓皮的蕾液,再将0.5麦氏单位浓度的标准菌液配制成浓度约为1000CFU/mL的菌液利取该菌液1mL注入血增养用培养基中,并将此血培养用培养基按血培养系统说明书(或相关文师)规定的程序进行检测,每种标准菌试验应在2个批号各10只的血培养用培养基内进行,在7元
内读取所有培养基的培养结果应符合4.3的要求,而不应该出现假NIH
阴性。
表1试验用标准菌株
泰泰慧氏球
Neissen
Strept
Strept
Pseudon
itisdisAT
感嗜血杆菌
influenaaeA
肺炎链球菌
pneumonise
化脓链球菌
PvogenicA
录假单胞菌
osaAC2
丝醇母菌
Candida
金黄意
Staphylococcus ad
大肠埃希菌
LNC25923
Escherichia coli ATCC5922
粪产碱杆菌
Alcaligenes faecalis ATCC87505.4血培养用培养基的无菌试验
资维织梭章
Humhisto/ticum
TCC19401
产气英康梭菌
dum perfring
nsATCC13124
脆期类存菌
SATCC25285
pidaceae fragi
普通类桥菌
oidaceae vulgtesArCC8482
肺炎球菌
pecuspne
大岛埃希金
ATCC6305
KTCC25922
金黄色霜萄球菌
Stapiylococeu
aureusATCC25923
将未接种的血培养用培养基2个批号各10只,按血培养系统说明书规定的程序进行检测,在规定的培养周期读取所有培养基的培养结果,应符合4.4的要求。5.5培养基稳定性试验
用到效期后1个月内的血培养用培养基按照5.3和5.4的方法试验,每一标准菌株接种5只血培养用培养基,无菌试验采用5只血培养用培养基,结果应符合4.5的规定。5.6温度准确度及波动试验
将周国环境温度控制在血培养系统说明书允许范围内,系统开机至设定温度后,稳定2h,用精度3
YY/T0656—2008
为0.1的温度计测试血培养用培养基所在位置的温度,每隔30s记录1次温度测量值,连续记录10次,最大值与最小值之差为温度波动;每天测量2次,间隔不少于6h,连续测量5d,计算所有10次测量结果与设定温度值之差,取最大值,为准确度偏差的测量结果,应符合4.6的规定。5.7外观
通过目视检查进行验证,应符合4.7的要求。5.8环境试验
按照GB/T14710中适用环境试验组别的要求进行试验。5.9电气安全
按照GB4793.1的试验方法进行。6标志、标签和使用说明
6.1血培养仪
6. 1.1标志、标签
标志、标签至少应包括下列信息:a)产品名称、型号、规格;
b)生产企业名称、注册地址、生产地址、联系方式(国外产品尚需提供驻华办事机构的名称、地址及联系方式);
医疗器注册证书编号:
产品标准编号;
产品生产日期或者编号:
电源连接条件,输人功率:
g)依据产品特性应当标注的图形、符号以及其他相关内容;h)GB4793.1的要求适用。
使用说明
使用说明至少应包括下列信息:产品名称、型号、规格
b)生产企业名称、注册地址、生产地址、联系方式及售后服务单位:e)
《医疗器械生产企业许可证》编号(进口产品及第一类医疗器械除外)、医疗器械注册证书编号:产品标准编号:
产品的性能、主要结构、适用范围;e)
禁忌症、注意事项以及其他需要警示或者提示的内容;f)
医疗器械标签所用的图形、符号、缩写等内容的解释;安装和使用说明或者图示;
产品维护和保养方法,特殊储存条件、方法;D
GB4793.1的要求适用。
6.2血培养用培养基
6.2.1标识标签
培养基的销售包装标签至少应包括以下内容产品名称、型号、规格;
生产企业名称、注册地址、生产地址、联系方式(国外产品尚需提供驻华办事机构的名称、地址b)
及联系方式);
医疗器械注册证书编号:
d)产品标准编号;
e)产品生产日期或批(编)号:f)产品有效期限;
依据产品特性应当标注的图形、符号以及其他相关内容。g)
6.2.2使用说明
培养基的使用说明至少应包括以下内容:a)产品名称、型号、规格;
生产企业名称、注册地址、生产地址、联系方式及售后服务单位;YY/T0656—2008
《医疗器械生产企业许可证》编号(进口产品及第一类医疗器械除外)、医疗器械注册证书编号:产品标准编号:
产品的性能、主要结构、适用范围;禁忌症、注意事项以及其他需要警示或者提示的内容,医疗器械标签所用的图形、符号、缩写等内容的解释;使用说明或者图示;
产品特殊储存条件、方法。
7包装、运输和购存
7.1包装
7.1.1外包装箱应能保证产品不受自然损坏。7.1.2随机文件应至少包括产品说明书、装箱清单。7.2运输
按订货合同规定的要求进行运输。7.3贮存
按制造商规定的条件进行贮存。5
YY/T0656—2008
参考文献
[1]Centers for Disease Control Increase in national hospital discharge survey rates for septicemia-UnitedStates,1979-1987.MMWR.199039.31-34.[2]
AronsonMD,BorDH.Blood cultures.AnnalsIntMed.1987106:246-253[3]
Bryan CS. Clinical implications of positive blood cultures. Clin Microbial Rev 1989,2:329-353.
Washington JA II,Ilstrup DM. Blood cultures:issues and controversies.Rey Infect Dis[[4]
1986;8:792-802
WeinsteinMP,MurphyJR,RellerLB,LichensteinKA.Clinical significance of positive cultures:a comprehensive analysis of 5o0 episodes of bacte[6]
remia and fungemia in adults,I.Laboratory and epidemiologic observations.Rev Infect Dis1983:5.35-53.
Ilstrup DM. Statistical methods employed in the study of blood culture media. In:Washing[
ton A11.ed.The detection of septicemia,West Palm Beach:CRCPress1978;31-39[8] Arkin CF,Wachtel MS.How many paticnts are necessary to assess test performance? JAMA1990;263275-278.
YY/T0656-2008
中华人民共和国医药
行业标准
自动化血培养系统
YY/T0656—2008
中国标准出版社出版发行
北京复兴门外三里河北街16号
邮政编码:100045
网址spc.net.cn
电话:6852394668517548
中国标准出版社秦皇岛印刷厂印刷各地新华书店经销
开本880×12301/16印张0.75字数12千字2008年11月第一版2008年11月第一次印刷书号:155066-2-19178定价14.00元如有印装差错由本社发行中心调换版权专有侵权必究
举报电话:(010)68533533
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。






 ✕
✕