基本信息
标准号:
SN/T 1672.8-2013
中文名称:进出口医用设备检验规程 第8部分:超声诊断和理疗设备
标准类别:商检行业标准(SN)
标准状态:现行
出版语种:简体中文
下载格式:.rar .pdf
下载大小:1.47 KB
相关标签:
进出口
医用
设备
检验
规程
超声
诊断
理疗

标准分类号
关联标准
出版信息
相关单位信息
标准简介
SN/T 1672.8-2013 进出口医用设备检验规程 第8部分:超声诊断和理疗设备
SN/T1672.8-2013
标准内容
中华人民共和国出入境检验检疫行业标准SN/T1672.8-—2013
代替SN/T1430.1-2004
进出口医用设备检验规程
第8部分:超声诊断和理疗设备
Rules for the inspection of import and export medical equipment-Part 8:Ultrasonic diagnostic and physiotherapy equipment2013-11-06发布
集志真力
中华人民共和国
国家质量监督检验检疫总局
2014-06-01实施
SN/T1672α进出口医用设备检验规程》共分为8个部分:第1部分:通用要求,bzxz.net
一第2部分:全身螺旋CT扫描仪;第3部分:经颅多普勒血液分析仪;一第4部分:B型超声诊断设备;一第5部分:医用诊断X射线机:第6部分:医疗诊断用磁共振设备;第7部分:医用内窥镜;
一第8部分:超声诊断和理疗设备。本部分为SN/T1672的第8部分。
本部分按照GB/T1.1—2009给出的规则起草。SN/T1672.8—2013
请注意本文件的某些内容可能涉及专利。本文件的发布机构不承担识别这些专利的责任。本部分代替SN/T1430.1—2004《进口医疗器械检验规程:医用超声诊断和治疗设备》。本部分与SN/T1430.1一2004相比.除编辑性修改外主要技术变化如下:修改了标准的名称、适用范围;增加了电磁兼容、环保、能效等方面的要求:修改了检验项目、检验内容、检验方法;规定了多种检验监管模式和检验方式。本部分由国家认证认可监督管理委员会提出并归口。本部分起草单位:中华人民共和国浙江出人境检验检疫局。本部分主要起草人:李炳强、钮隽、许健、张昊、汤卫平。本部分所代替标准的历次版本发布情况为:SN/T1430.1—2004。
1范围
进出口医用设备检验规程
第8部分:超声诊断和理疗设备
SN/T1672.8—2013
SN/T1672的本部分规定了进出口医用超声诊断和理疗设备的抽样、检验及判定。本部分适用于进出口医用超声诊断和理疗设备的进出口检验2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注目期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB/T2828.1计数抽样检验程序第1部分按接收质量限(AQL)检索的逐批检验抽样计划GB9706.1一2007医用电气设备第1部分:安全通用要求GB9706.7—2008
医用电气设备第2-5部分:超声理疗设备安全专用要求GB9706.9—2008医用电气设备第2-37部分:超声诊断和监护设备安全专用要求GB9706.152008
医用电气设备第1工部分:安全通用要求并列标准:医用电气系统安全要求
GB/T16846—2008医用超声诊断设备声输出公布要求SN/T0002—2004进出口机电商品检验规程编写的基本规定YY0505医用电气设备第1-2部分安全通用要求并列标准3术语和定义
电磁兼容要求和试验
GB9706.1-2007及SN/T00022004界定的以及下列术语和定义适用于本文件。3.1
检验批inspectionlot
为实施抽样检验而汇集的同一规格,型号,任相同生产条生产的单位产品称为检验批,简称批。3.2
型式试验模式modeoftypetest
按规定的周期依据国家技术规范的强制性要求进行型式试验,按现场检验规定对产品进行抽批检验,并对企业的质量管理体系实施监督的合格评定活动。3.3
抽样检验模式modeofsamplinginspection按国家技术规范的强制性要求,对进出口商品进行逐批或抽批实施抽样,检验和检查的合格评定活动。
符合性验证模式modeofcomplianceinspection按国家技术规范的强制性要求,查验检验单证和凭证是否与货物相符,必要时可进行抽查检验,并实施监督的合格评定活动。
SN/T1672.8-2013
4总要求
4.1安全要求
医用超声诊断和理疗设备的安全要求应满足GB9706.1,GB9706.15和GB9706.7或GB9706.9的规定,适用时应考虑使用国家(地区)的差异。2电磁兼容性要求
医用超声诊断和理疗设备的电磁兼容特性参照GB9706.7或GB9706.9和YY0505的规定,适用时应考虑使用国家(地区)的差异。3其他要求
适用时,还应符合使用国家(地区)有关技术法规对医用超声诊断和理疗设备的环保、能效、性能等的规定。
5检验与试验
5.1检验监管模式的选取
5.1.1进出口医用超声诊断和理疗设备的检验监管模式有:型式试验模式、抽样检验模式和符合性验证模式。5.1.2进出口医用超声诊断和理疗设备的检验监管模式的选取应符合国家相关规定。5.2检验方式
不同检验监管模式下的检验方式为:型式试验模式:型式试验和开箱检验;a)
抽样检验模式:逐批或抽批抽样检验;b)
符合性验证模式:证单\查验和开箱检验5.3
型式试验
5.3.1抽样
从定型产品中随机抽取1台代表性样品进行检测。5.3.2检验内容
安全检测
按GB9706.1、GB9706.15和GB9706.7或GB9706.9进行全部适用项目的检测,适用时应考虑使用国家(地区)的差异,
5.3.2.2电磁兼容检测
按GB9706.7或GB9706.9和YY0505进行全部适用项目的检测,适用时应考虑使用国家(地区)的差异。
1)证单指国家实施许可制度的证明文件。2
环保、能效、性能检测
SN/T1672.8—2013
按照使用国家(地区)对医用超声诊断和理疗设备的环保、能效、性能等的规定进行全部适用项目检测。
5.3.3结果判定
如所有检测均合格,则判型式试验合格,否则为不合格。5.3.4不合格处置
判为型式试验不合格的,允许整改后重新提交检测。5.4抽样检验
5.4.1抽样
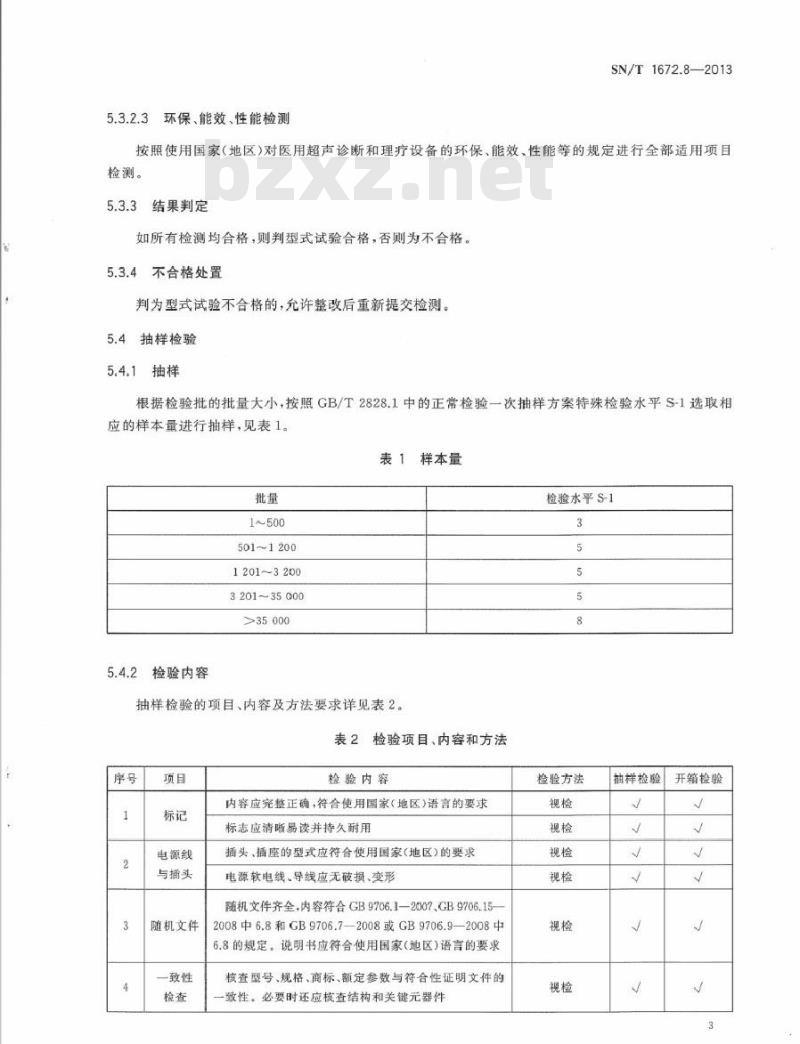
根据检验批的批量大小,按照GB/T2828.1中的正常检验一次抽样方案特殊检验水平S-1选取相应的样本量进行抽样,见表1。
表1样本量
501~1200
1201~3200
320135000
>35000
5.4.2检验内容
抽样检验的项目、内容及方法要求详见表2。表2
检验项目、内容和方法
电源线
与插头
随机文件
一致性
检验内容
内容应完整正确,符合使用国家(地区)语言的要求标志应清晰易读并持久耐用
插头、插座的型式应符合使用国家(地区)的要求电源软电线、导线应无破损、变形随机文件齐全,内容符合GB9706.1—2007、GB9706.15-2008中6.8和GB9706.7-2008或GB9706.9—2008中6.8的规定。说明书应符合使用国家(地区)语言的要求核查型号、规格、商标、额定参数与符合性证明文件的致性。必要时还应核查结构和关键元器件检验水平S-1
检验方法
抽样检验
开箱检验
SN/T1672.8—2013
保护接地、
功能接地
和电位
连续漏电
流和患者
辅助电流
电介质
声输出
检验内容
表2(缕)
保护接地阻抗、电位均衡导线连接装置、功能接地端子及其标记应符合GB9706.12007中第18章的规定依同设备类别,在正常工作温度下,对地漏电流、外壳漏电流及惠者辅助电流应特合GB9706.1-2007中19.3的相应规定。
具有安全功能的绝缘依不回的绝缘类最因能承受CB9706.1-2007中20.3所规定的试验电压,历时1min,无击穿或闪络现象。适用时,试验至少应包括:1)带电部件(设备的网电源部分和已保护接地购可触及金属部件之间:
2)带电部件(设备的网电源部分)和未保护接地外壳部件之间;
3)应用部分(惠告电路)和带电部分之间检验方法
GB9706.1—2007
第18章
GB9706.1-2007
第19章
GB9706.1—2007
第20章
医用理疗设备的手持式治疗头不需要的超声辅射的GB
9706.7—2008
空间峰值时间平均声强小于100mWlem第35章
医用诊断设备的声输出数据准确度符合GB9706.92008中50.2.危险输出的防止符合GB9706.9200851.2和51.4的规定
医用理疗设备:应符合GB9706.72008中423符台
性试验的要求
医用诊断设备:应符合GB9706.9-2008中42.3的测量要求
声输出公布资料应行合GB/T16846-2008中4.2.2的要求
GB9706.9—2008
第50章、第51章
GB0706.72008
第42章
GB9706.9—2008
第2章
注:以上项目如与使用国家(地区)技术法规有差异,接使用国家(地区)技术法规检验。5.4.3
结果判定
所有检验项目合格,则判抽样检验合格,否则为不合格。5.4.4不合格处置
抽样检验
开箱检验
判为抽样检验不合格的,在法律法规允许的前提下,经技术处理后,允许重新提交检验一次5.5开箱检验
5.5.1抽样
根据检验批的批量大小,按照GB/T2828.1申的特殊检验水平S-1选取相应的样本量进行抽样(见表1)。如选取的样本量大于批量时,对该检验批进行全数检验。4
检验内容
开箱检验的项目、内容及方法要求详见表2。3结果判定
所有检验项目合格,则判开箱检验合格,否则为不合格。5.5.4不合格处置
SN/T1672.8—2013
判为开箱检验不合格的,在法律法规允许的前提下,经技术处理后,允许重新提交检验一次。合格批判定及有效期
6.1无论采取何种检验监管模式,只有该模式中的全部检验合格,方可判定该批产品合格,否则判定该批产品不合格。
2合格检验批的有效期为12个月。6.2
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。






 ✕
✕