标准分类号
关联标准
出版信息
相关单位信息
标准简介
标准号:SN/T 5117-2019
标准名称:进出口食用动物、饲料 链霉素类(链霉素、二氢链霉素)药物残留测定 液相色谱-质谱∕质谱法
英文名称:Determination of streptomycin, dihydrostreptomycin residues in live animals and
feeds for import and export-HPLC MS/MS method
标准格式:PDF
发布时间:2019-09-03
实施时间:2020-03-01
标准大小:5280K
标准介绍:本标准规定了链霉素、二氢链霉素药物残留量的液相色谱-质谙/质谱测定方法
本标准适用于猪、牛、羊、兔、鸡血清及猪、牛、羊、兔尿液,以及玉米粉、小麦粉、高粱粉饲料中链霉素、二氢链霉素药物残留量的測定和确证。
2规范性引用文
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅所注日期的版本适用于本
文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件
GB/T6682分析实验室用水规格和试验方法
3原理
试样中残留的链霉素、二氢链霉素经混合提取液提取,HIB固相萃取柱净化,经水淋洗、甲醇洗脱
定容后供液相色谱-质谱/质谱法测定,外标法定量,
4试剂与材料
4.1乙腈:高效液相色谱纯
4.2甲酸:高效液相色谱纯
4.3甲醇:高效液相色谱纯,
4.4磷酸二氢钾(KH2PO4)
4.5三氯乙酸
4.6盐酸(HC1)。
4.7氢氧化钠(NaOH)
标准内容
ICS67.120
中华人民共和国出入境检验检疫行业标准SN/T5117—2019
进出口食用动物、饲料
链霉素类
链霉素、二氢链霉素)药物残留测定液相色谱-质谱/质谱法
Determination of streptomycin, dihydrostreptomycin residues in live animals andfeedsforimportandexport-HPLCMS/MSmethod业标准信息服务平台
2019-09-03发布
中华人民共和国海关总署
2020-03-01实施
本标准按照GB/T1.1—2009给出的规则起草。本标准由中华人民共和国海关总署提出并归口本标准起草单位:中华人民共和国大连海关、沈阳农业大学,SN/T5117—2019
本标准主要起草人:徐静,孙兴权,苏明明,田宏哲,杨璐,李一尘,肖珊珊,代弟,曹际娟。行业标准信息服务平台
1范围
进出口食用动物、饲料链霉素类(链霉素、三氢链霉素)药物残留测定液相色谱-质谱/质谱法
本标准规定了链霉素、二氢链霉素药物残留量的液相色谱-质谱/质谱测定方法。SN/T 5117—2019
本标准适用于猪、牛、羊、兔、鸡血清及猪、牛、羊、兔尿液,以及玉米粉、小麦粉、高粱粉饲料中链霉素、二氢链霉素药物残留量的测定和确证。2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅所注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB/T6682分析实验室用水规格和试验方法3原理
试样中残留的链霉素、二氢链霉素经混合提取液提取,HLB固相萃取柱净化,经水淋洗、甲醇洗脱、行业标准信息服务平台
定容后供液相色谱-质谱/质谱法测定,外标法定量。试剂与材料
乙晴:高效液相色谱纯。
甲酸:高效液相色谱纯。
甲醇:高效液相色谱纯。
磷酸二氢钾(KH,PO.)。
三氯乙酸。
4.6盐酸(HCI)。
氢氧化钠(NaOH)
氨水(NH,·H2O)
4.9乙二胺四乙酸二钠盐(Na2·EDTA)4.10提取液:10mmol/LKH,PO溶液(含0.4mmol/LEDTA和2%三氯乙酸),称取2.72gKH,PO4,加人2L水,用1mol/LHCI溶液调节pH值为4.0.再加人0.3g乙二胺四乙酸二钠盐(含2个结晶水)和40g三氯乙酸,混匀即可。4.110.1%甲酸:取1.0mL甲酸溶于1L水中即可。4.12链霉素标准物质:CAS号57-92-1,纯度98.0%4.13双氢链霉素标准物质:CAS号128-46-1,纯度99.0%。4.14标准储备溶液的配制:分别准确称取适量的标准物质,用水配制成100ug/mL的标准储备溶液1
SN/T5117—2019
置于一4℃避光保存,有效期1个月。4.15混合标准溶液的配制:取适量标准储备溶液(4.14)至100mL容量瓶中,用水定容至刻度,配制成混合标准溶液,各组分浓度均为1g/mL。一4℃避光保存,有效期5天。4.16标准工作溶液的配制:根据需要,吸取一定量的混合标准溶液(4.15),用空白基质提取液稀释至所需浓度,临用现配。
4.17HLB固相萃取柱或相当者:60mg,3mL。使用前依次用3mL甲醇、5mL超纯水预洗活化4.18滤膜:0.22μm,水相。
水:GB/T6682规定的一级水。
仪器和设备
5.1高效液相色谱串联二级质谱仪:配有电喷雾离子源(ESI)。5.2电子天平:感量分别为0.01g,0.0001g。5.3离心机:转速8500r/min以上。5.4
涡旋震荡器。
5.5氮吹仪。
固相萃取装置。
5.7 pH计。
5.810mL塑料离心管。
试样的制备与保存
6.1试样制备
无菌采集待检动物非抗凝(8mL),分离血清于洁净容器内作为试样,加封并标明标记。尿液样品(≥5mL)装人洁净容器内加封并标明标记。饲料样品(≥500g)经粉碎机粉碎,过20目筛,混匀,密封,作为试样,标明标记。在制样的探作过中,应防止样品受到污染或发生残留物含量的变化6.2试样保存
空意服务平
血清和尿液样品于一20℃以下条件下保存。饲料样品专带温下保存测定步骤
7.1提取
称取约2g(精确至0.01)样品于50mL具塞离心管中,准确加人8mL提取液(4.10).涡旋温荡提取3min后,8500r/min离心5min,倾出上清液。重复提取一次,合并上清液。上清液用氨水4.8)调至pH3~4,待净化
7.2净化
将提取液转移到已活化的HLB固相萃取柱(4.17),流速控制在1d/s左右,用3mL水淋洗,弃去流出液,用5mL甲醇(4.3)洗脱,洗脱液收集于10mL刻度塑料离心管(5.8)中,并于45℃氮气吹干,用1mL水溶解残渣,过微孔滤膜(4.18)后,待上机检测。2
7.3测定
液相色谱条件
SN/T5117—2019
色谱柱:AtlantisHilicSilica,150mmX2.1mm(内径),粒度3μm,或相当者:b)
色谱柱温度:40℃;
流动相:梯度洗脱条件见表1:
流速:0.3mL/min;
进样量:20uL;
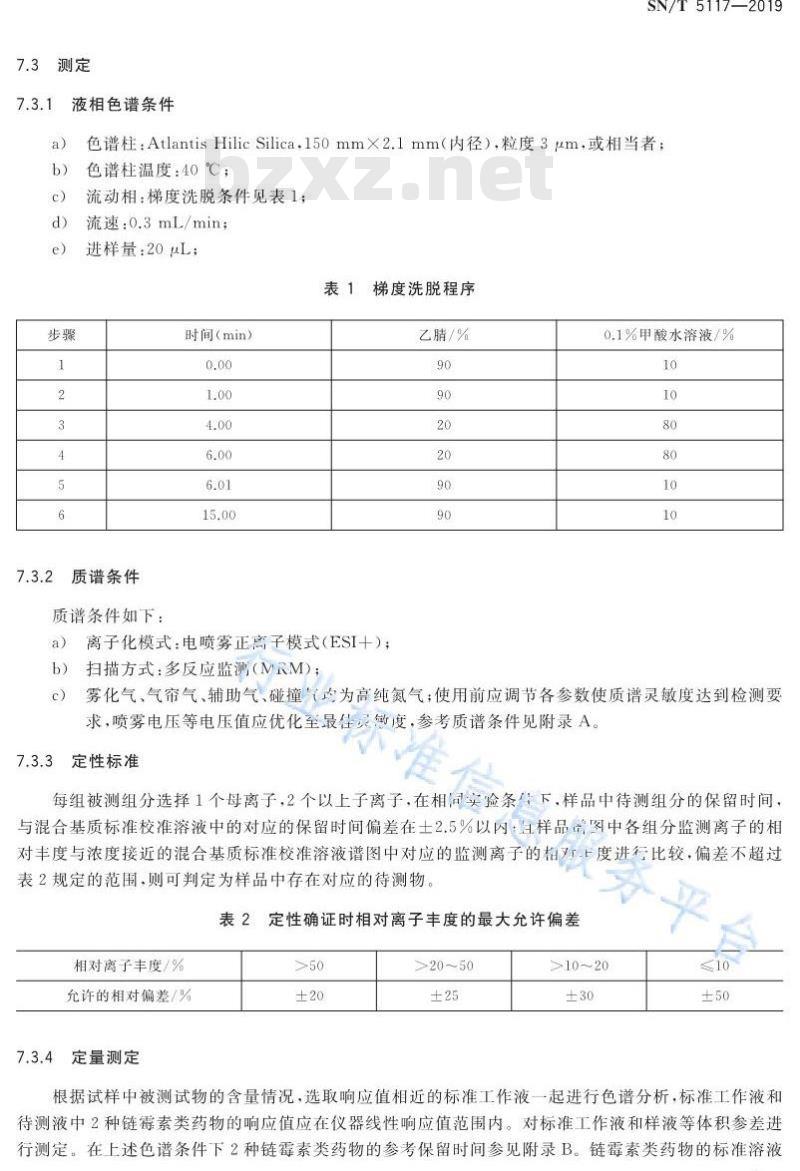
梯度洗脱程序
时间(min)
质谱条件
质谱条件如下:
a)离子化模式:电喷雾正高子模式(ESI十)b)扫描方式:多反应监测(MRM);乙腈/%
0.1%甲酸水溶液/%
雾化气、气帘气、辅助气、碰撞内为高纯氮气:使用前应调节各参数使质谱灵敏度达到检测要c)
求,喷雾电压等电压值应优化至最佳灵敏度,参考质谱条件见附录A。7.3.3
定性标准
每组被测组分选择1个母离子,2个以上子离子,在相同实验条生下,样品中待测组分的保留时间与混合基质标准校准溶液中的对应的保留时间偏差在士2.5%以内样品管图中各组分监测离子的相对丰度与浓度接近的混合基质标准校准溶液谱图中对应的监测离子的相已度进行比较,偏差不超过表2规定的范围,则可判定为样品中存在对应的待测物表2定性确证时相对离子丰度的最大允许偏差相对离子丰度/%
允许的相对偏差/%
7.3.4定量测定bzxZ.net
>20~50
>10~20
根据试样中被测试物的含量情况,选取响应值相近的标准工作液一起进行色谱分析,标准工作液和待测液中2种链霉素类药物的响应值应在仪器线性响应值范围内。对标准工作液和样液等体积参差进行测定。在上述色谱条件下2种链霉素类药物的参考保留时间参见附录B。链霉素类药物的标准溶液3
SN/T5117—2019
的多反应监测(MRM)色谱图参见附录B。7.3.5空白试验
分别取阴性的血清、尿液和饲料样品2g,按7.1和7.2操作。8
结果计算
用色谱数据处理机或按式(1)计算,计算结果需扣除空白值:X,=A Xc,xV
式中:
试样中被测组分含量,单位为微克每于克(rg/kg);样品溶液中被测组分的峰面积;标准工作溶液中被测组分的浓度,单位为纳克每毫升(ng/mL);样品溶液最终定容体积,单位为毫升(mL);标准工作溶液中被测组分的峰面积;最终样液所代表的试样质量,单位为克(g)。·(1)
方法的性能指标
业标性信息服务平台
测定低限
本方法2种链霉素类药物的测定低限均为10.0μg/kg。9.2
回收率
精密度
本方法精密度的实验数据见附录C。4
电喷雾离子源参考条件:
a)雾化气:65psi
辅助气:65L/min;
气帘气:28psi;
电喷雾电压:5500V;
离子源温度:550℃。
组分名称
链霉素
二氢链霉素
附录A
(资料性附录)
电喷雾离子源参考条件!
SN/T5117—2019
被测物监测离子对、保留时间、去簇电压、碰撞气能量和碰撞室出口电压定性离子对
582.3/263.5*
582.3/246.5
584.4/263.4*
584.4/245.5
保留时间
去袭电压(DP)
碰撞能量(CE)
碰撞室出口
电压(CXP)
*为定量离子对,对于不同质谱仪器,质谱参数可能存在差异,测定前应该将质谱参数优化到最佳行业标准信息服务平台
1)非商业性声明:表B.1所列参数是用5500QTRAP质谱仪完成的,此处列出试验用仪器型号仅是为了提供参考.并不涉及商业目的,鼓励标准使用者尝试采用不同厂家或型号的仪器。5
SN/T5117—2019
附录B
(资料性附录)
标准物质多反应检测(MRM)色谱图582. 3/263.5
582.3/246.5
标准信息服务平台
图B.1链霉素标准溶的多应检测(MRM)色谱图(提取离子流图)6
S88R8CSANTd
584. 4/263. 4
584. 4/246.5±
SN/T 5117—2019
二氢链霉素标准溶液的多反应检测(MRM)色谱图(提取离子流图)行业标准信息服务平台
SN/T5117—2019
添加水平/
化合物
链霉素
二氢链霉素
化合物
链霉素
二氢链霉素
化合物
链霉素
二氢链霉素
μg/kg
附录C
(规范性附录)
2种链霉素类药物添加回收率和精密度(n=6)2种链霉素类药物在动物血清中的回收率和精密度(n=6)回收率范围
70.2~81.5
75.4~91.2
66.2~84.1
82.1~97.0
85.0~104.5
69.8~84.7
75.6~90.0
68.2~85.6
71.0~79.9
88.5~93.6
79.5~100.0
78.8~91.9
76.3~89.4
71.6~90.0
68.4~83.0
73.3~89.1
74.8~83.8
69.8~86.0
67.5~82.1
82.0~94.5
73.0~95.0
77.3~93.3
79.0~89.3
72.2~84.0
76.4~92.6
80.5~94.5
2种链霉素类药物在动物尿液中的回收率和精密度(n=6)添加水平/
69.5-88.5
70.2~81.5
71.8~89.1
76.0~93.3
回收率范围/
70.0~83.0
74.0~92.0
76.0-87.0
65.8~84.7
77.5~93.5
86.1~100.2
82.5~93.0
71.8~89.1
69.2~85.2
78.5~86.3
65.8-80.3
71.0~81.4
70.0~85.2
73.8~85.1
2种链需素类药物在饲料中的回收率和精密度(n=6)添加水平
玉米粉
66.7~82.9
76.7~86.5
76.7~86.5
78.8~91.0
回收率范围
小麦粉
69.9~84.7
69.8~84.4
71.2~84.4
80.4~92.4
高粱粉
68.2~84.1
75.0~88.3
76.0~90.8
74.3~88.3
相对标准
偏差范围/
相对标准
偏差范围/
相对标准
馆美范围/
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。






 ✕
✕