基本信息
标准号:
SN/T 5121-2019
中文名称:进出口食用动物、饲料中伊维菌素残留测定 液相色谱-质谱∕质谱法
标准类别:商检行业标准(SN)
标准状态:现行
出版语种:简体中文
下载格式:.zip .pdf
下载大小:4.68 MB
相关标签:
进出口
食用动物
饲料
菌素
残留
测定
色谱
质谱
质谱法

标准分类号
关联标准
出版信息
相关单位信息
标准简介
标准号:SN/T 5121-2019
标准名称:进出口食用动物、饲料中伊维菌素残留测定 液相色谱-质谱∕质谱法
英文名称:Determination of Ivermectin residue in live animal and feed for import and export-LC-MS/MS method
标准格式:PDF
发布时间:2019-09-03
实施时间:2020-03-01
标准大小:5243K
标准介绍:本标准规定了进出口食用动物、饲料中伊维菌素残留测定液相色谱质谱/质谱法
本标准适用于进出口食用动物(如猪、牛、羊、兔、鸡、鸭)血液以及动物饲料中伊维菌素的测定和2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅所注日期的取本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件
GB/T6682分析实验室用水规格和试验方法
3原理
试样经乙腈涡旋振荡提取后,液相色谱质谱/质谱法检测和确证,内标峰面积法定量
4试剂材料
除非另有说明,所用试剂均为分析纯,水为GB/T6682规定的一级水
1乙腩:高效液相色谱级。
4.2甲酸
44氯化钠
4.55mmol/l乙酸铵+0.1%甲酸水溶液:称取0.385g乙酸铵于烧标中,用水溶解,转移至1000ml容量瓶中,用水洗涤烧杯至少3次,直至洗净,并将洗液全部转移至100容量瓶中,再加入1mL甲酸于1000mL容量瓶中
标准内容
ICS71.040.40
中华人民共和国出入境检验检疫行业标准SN/T 5121—2019
进出口食用动物、饲料中伊维菌素残留测定液相色谱-质谱/质谱法
Determination of Ivermectin residue in live animal and feed foimportandexportLC-MS/MSmethod行业标准信息服务平台
2019-09-03发布
中华人民共和国海关总署
2020-03-01实施
本标准是照按GB/T1.1—2009起草。前言
SN/T5121—2019
请注意本文件的某些内容可能涉及专利,本文件的发布机构不承担识别这些专利的责任。本标准由中华人民共和国海关总署提出并归口。本标准起草单位:中华人民共和国重庆海关。本标准主要起草人:李光满、夏明星、陈宗祥、唐璜、王安良、郑小玲、熊英、周树予、李应国。行业标准信息服务平台
1范围
进出口食用动物、饲料中伊维菌素残留测定液相色谱-质谱/质谱法
SN/T 5121—2019
本标准规定了进出口食用动物、饲料中伊维菌素残留测定液相色谱-质谱/质谱法。本标准适用于进出口食用动物(如猪、牛、羊、兔、鸡、鸭)血液以及动物饲料中伊维菌素的测定和确证。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅所注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB/T6682分析实验室用水规格和试验方法3原理
试样经乙睛涡旋振荡提取后,液相色谱-质谱/质谱法检测和确证,内标峰面积法定量。4试剂材料
新业标准信
除非另有说明,所用试剂均为分析纯,水为GB/T6682规定的一级水。4.1乙:高效液相色谱级。
4.2甲酸。
4.3乙酸铵。
4.4氯化钠。
4.55mmol/L乙酸铵+0.1%甲酸水溶液:称取0.385g乙酸铵于免杯,中,用水溶解,转移至1000mL容量瓶中,用水洗涤烧杯至少3次,直至洗净,并将洗液全部转移至1000瓶中,再加入1mL甲酸于1000mL容量瓶中,用水定容。4.6标准物质:伊维菌素(Ivermetine,CAS号:70288-86-7),纯度均大于96%,伊维菌案同位素内标(lvermetin-d2),纯度大于98%。4.7标准储备液:准确称取伊维菌素标准品0.1g(精确到0.0001g).用乙睛(4.1)充分溶解,稀释定容于100mL容量瓶中,配制成浓度为1mg/mL的标准储备液;另将伊维菌素同位素内标标准品10mg用乙睛(4.1)充分溶解,稀释定容于10mL容量瓶中,配制成浓度为1mg/mL的伊维菌素同位素内标标准储备液,最后分别将定容后的标准储备液倒入棕色试剂瓶中,一18℃以下避光保存。4.8标准中间储备液:准确移取100μL伊维菌素标准储备液(4.7)和100μL伊维菌素内标标准储备液(4.7)于两个100mL容量瓶中,用乙晴稀释定容,分别配成1/mL的伊维菌系标准中间储备液和1ug/mL伊维菌素同位素内标标准中间储备液,溶液置于棕色试剂瓶中,一18℃以下避光保存。4.9含内标的标准工作液:根据需要用乙(4.1)将伊维菌素标准中间储备液(4.8)稀释成合适的浓度的混合标准工作曲线溶液,同时每个标液里面添加等量伊维菌素同位素内标标准中间储备液标准中间1
SN/T5121—2019
储备液(4.8),每个标液中伊维菌素同位素内标浓度为20μg/L,伊维菌素浓度参考线性浓度范围为5μg/L~50ug/L,临用时现配。
4.10基质标准工作液:选择不含伊维菌素的样品5份,按照本标准7.1进行处理至取上清液5mL氮气吹干”(不用添加伊维菌素内标),分别加入1mL不同浓度含内标的标准工作液(4.9),超声溶解残渣,过0.22um滤膜(4.11)后,配置成基质标准工作液,临用时现配。4.11微孔滤膜:有机系,0.22μm。5仪器与设备
5.1液相色谱-质谱/质谱仪:配电喷雾离子源(ESI)。5.天平:感量为0.0001g和0.01mg。5.3冷冻离心机:转速不低于8000r/min。5.4旋涡混匀器。
5.5超声波清洗器。
5.6氮吹仪。
试样制备与保存
6.1试样制备
6.1.1饲料:从所取样品中取出具有代表性样品适量,磨碎混匀后,装人洁净的塑料袋中,样品数量15g,密封,并标记。
6.1.2血液:动物血液用肝素钠抗凝采血管收集,样品数量15mL,密封,并标记。6.2试样保存
业标准信息服
饲料常温保存.待检血液试样于4保存,留存血液试样于一18℃冷冻保存。7分析步骤
7.1提取
7.1.1血液
称取2.0g(精确到0.01g)试样和0.5g氯化钠(4.4)于50mL离心管,加入4uL的伊维菌素同位素内标中间储备液(4.8.相当于伊维菌素同位素内标质量为4ng)、3mL水和10mmL乙肺(4.1).旋涡混匀2min,振荡提取30min,以8000r/min在10℃以下条件冷冻离心5min,取上清液5mL氧气吹干,加人1.0mL乙睛(4.1),超声溶解残渣过0.22um滤膜(4.11)后,供液相色谱-质谱/质谱代洲走和确证。
7.1.2饲料
称取2.0g(精确到0.01g)试样和3.0g氯化钠(4.4)于50mL离心管中,加人40μL的伊维菌素同位素内标中间储备液(4.8,相当于伊维菌素同位素内标质量为4ng)、7.5mL水和10mL乙晴(4.1),旋涡混匀2min,振荡提取30min,以8000r/min在10℃以下条件冷冻离心5min,取上清液5mL氮气吹干,加入1.0mL乙睛(4.1),超声溶解残渣,过0.22um滤膜(4.11)后,供液相色谱-质谱/质谱仪测定和确证。
7.2测定和确证
液相色谱-质谱/质谱参考条件
液相色谱参考条件
参考条件如下:
色谱柱:Cig柱,100mmX4.6mm(内径).2.6pm,或相当者SN/T 5121—2019
流动相:A:5mmol/L乙酸铵+0.1%甲酸水溶液(4.5);B:乙睛(4.1),梯度洗脱程序见表1。b)
流速:0.4mL/min。
柱温:30℃。
进样量:20μL。
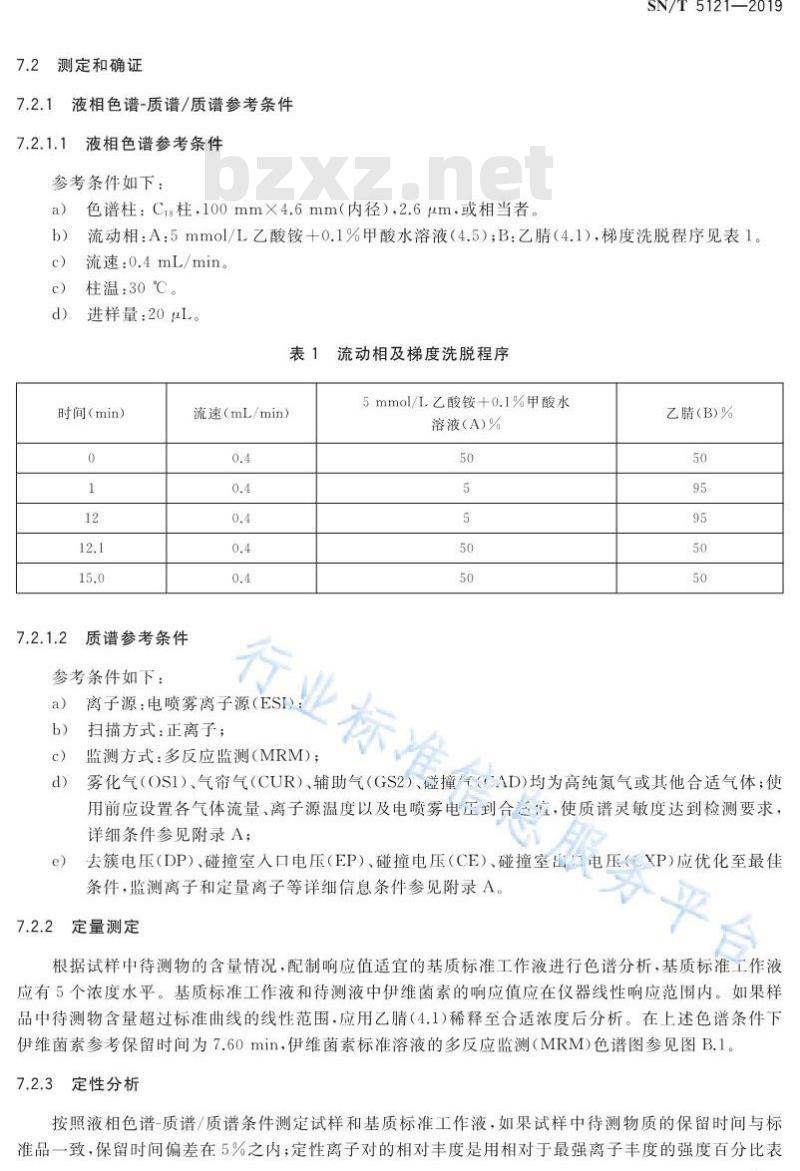
表1流动相及梯度洗脱程序
时间(min)
流速(mL/min)
5mmol/L乙酸铵+0.1%甲酸水
溶液(A)%
乙睛(B)%
行业标准
质谱参考条件wwW.bzxz.Net
参考条件如下:
a)离子源:电喷雾离子源(ESIb)扫描方式:正离子;
监测方式:多反应监测(MRM);d)雾化气(OS1)、气帘气(CUR)、辅助气(GS2)、微撞气(AD)均为高纯氮气或其他合适气体;使用前应设置各气体流量、离子源温度以及电喷雾电压到合值,使质谱灵敏度达到检测要求,详细条件参见附录A;
e)去簇电压(DP)、碰撞室人口电压(EP)、碰撞电压(CE)、碰撞室出电压(XP)应优化至最佳条件,监测离子和定量离子等详细信息条件参见附录A。7.2.2
定量测定
根据试样中待测物的含量情况,配制响应值适宜的基质标准工作液进行色谱分析,基质标准工作液应有5个浓度水平。基质标准工作液和待测液中伊维菌素的响应值应在仪器线性响应范围内。如果样品中待测物含量超过标准曲线的线性范围.应用乙睛(4.1)稀释至合适浓度后分析。在上述色谱条件下伊维菌素参考保留时间为7.60min.伊维菌素标准溶液的多反应监测(MRM)色谱图参见图B.1。7.2.3定性分析
按照液相色谱-质谱/质谱条件测定试样和基质标准工作液,如果试样中待测物质的保留时间与标准品一致,保留时间偏差在5%之内:定性离子对的相对丰度是用相对于最强离子丰度的强度百分比表3
SN/T5121—2019
示,应当与浓度相当标准工作溶液的相对丰度一致,相对丰度充许偏差不超过表2规定的范围,则可判断试样中存在对应的待测物。
表2定性确证时相对离子丰度的最大充许偏差相对离子丰度/%
允许的相对偏差/%
7.3空白试验
除不加试样外,均按上述操作步骤进行。结果计算和表达
>20~50
>10~20
用仪器软件处理数据或按内标法绘制标准曲线,以各基质标准工作液与内标物溶液色谱峰面积比值为横坐标,以各基质标准工作液与内标物溶液浓度比值为纵坐标绘制标准曲线,将样液中分析物与内标物峰面积比值代人曲线方程,计算出样液中分析物与内标物浓度比值,因内标物浓度已知,进而得出样液中分析物浓度C,代人公式(1)中,计算结果须扣除空白值X
式中:
(C-C) XV
试样中待测物质的含量,单位为微克每千克(ug/kg);从标准曲线得到的待测物质的溶液浓度,单位为微克每升(g/L);从标准曲线得到的空白试验待测物质的溶液浓度,单位为微克每升(ug/L):V
样液最终定容体积单位为毫升(mL);m
最终样液所代表的试样质量单位为克(g)。标准信息
结果保留三位有效数字。
测定低限和回收率
9.1测定低限
本方法的测定低限:食用动物(如猪、牛、羊、免、鸡、鸭)为10μg/kg。
9.2回收率
(1)
激以舒岛物饲料中限检出限均
收务平
采用本方法对食用动物(如猪、牛、羊、兔、鸡、鸭)血液以及动物饲料等基质进行回收率试验·国收率数据参见附录C。
10精密度
在重复性条件下获得的两次独立结果绝对差值不超过算数平均值的10%。4
质谱参考条件
电喷雾电压(IS):5500V:
碰撞气压力(CAD):Medium;
雾化气压力(GS1):50Psi;
气帘气压力(CUR):20Psi;
辅助气压力(GS2):50Psi;
离子源温度(TEM):600℃:
附录A
(资料性附录)
质谱参考条件!
SN/T5121—2019
监测离子对、去族电压(DP)、碰撞室人口电压(EP)、碰撞电压(CE)、碰撞室出口电压(CXP见表A.1。
化合物
伊维菌素
d2-伊维菌
素内标
母离子(Q1)
定性、定量离子对以及CE、DP、EP、CXP参考值检测模式
正离子
正离子
子离子(Q3)
注:表中带*的离子为定量离对于不同质谱仪器,仪器参数可能存在差异,测定前应将质谱参数优化到最佳。业标准信息服务平台
1)非商业性声明:附录A所列参考质谱条件是在ABAPI4000QTRAP型液质联用仪上完成的,此处列出试验用仪器型号仅为提供参考,并不涉及商业目的,鼓励标准使用者尝试不同厂家或型号的仪器,5
SN/T5121—2019
附录B
(资料性附录)
伊维菌素标准溶液和同位素内标溶液多反应监测(MRM)色谱图伊维菌素标准溶液和同位素内标溶液多反应检测(MRM)色谱图见图B.1。XIu bl M- ( 2kIr4, 2J2.2u2/SJ.72U UuID. IVeIIe, 1-1 aII EMIrph 2 (e LL1DJHil ul D1su/ Ml 1IuILu 2piy?577
892.8569.7
Mwx. +d.r cp
行业标准信息服务平台
Mux2as.3upe
图B.1伊维菌素(10μg/L)标准溶液和伊维菌素同位素内标(20μg/L)溶液的多反应监测(MRM)色谱图SN/T5121—2019
行业标准信息服务平台
SN/T5121—2019
添加水平
附录C
(资料性附录)
不同基质中伊维菌素添加回收率试验数据回收率
79.0~89.9
87.0~89.0
92.0~96.5
74.0~83.5
80.5~88.3
86.5~94.2
73.7~78.9
82.0~88.0
79.2~86.5
81.2~86.0
颗粒饲料
预混饲料
浓缩饲料
添加水平
回收率
82.0~89.0
80.2~89.4
72.8~85.6
85.8~90.2
71.5~82.7
81.0~92.0
78.6~85.9
74.0~79.5
87.2~91.0
79.0~87.5
业标准信息服务平台
86-2~89.2
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。






 ✕
✕