基本信息
标准号:
SN/T 1460-2015
中文名称:输入性蚊类携带西尼罗病毒与圣路易脑炎病毒的检测方法
标准类别:商检行业标准(SN)
标准状态:现行
出版语种:简体中文
下载格式:.zip .pdf
下载大小:3.79 MB
相关标签:
输入
蚊类
携带
西尼罗
病毒
脑炎
检测
方法

标准分类号
关联标准
出版信息
相关单位信息
标准简介
SN/T 1460-2015.Detection methods for west nile virus and St.Louis encephalitis virus carried by imported mosquitoes.
1范围
SN/T 1460规定了国境口岸输入性蚊类携带西尼罗病毒与圣路易脑炎病毒检测的生物安全要求、检测对象、检测方法、结果的报告。
SN/T 1460适用于检验检疫机构对输入性蚊类体内携带西尼罗病毒与圣路易脑炎病毒检测和报告,对口岸发现的蚊类检测西尼罗病毒与圣路易脑炎病毒也可参照执行
2规范性引用文件
下列文件对于本文件的应用是必不可少的。儿是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 6682分析实验室用水规格和试验方法
GB 19489实验室生物安 全通用要求
WS 233微 生物和生物医学实验室生物安全通用准则
3术语和定义
下列术语和定义适用于本C件。
3.1输入性蚊类imported mosquitocs
通过入境交通工具、集装箱、货物及行李带人境内的库蚊、伊蚊展蚊类。
3.2西尼罗病毒west nile virus; WN
西尼罗热的病原体,属黄病毒科黄病毒属,为单链RNA病毒。西尼罗病毒分两个基因型,导致人类感染西尼罗病毒的分离株主要为I型。主要分布于非洲、中东.西亚和北美。
3.3圣路易脑炎病毒St.Luis encephalitis virus;SLEV
圣路易脑炎的病原体,属黄病毒科黄病毒属,为单链RNA病毒。主要分布于北美洲。
标准内容
中华人民共和国出入境检验检疫行业标准SN/T1460—2015
代替SN/T1460-2004
输入性蚊类携带西尼罗病毒与圣路易脑炎病毒的检测方法
Detection methods for west nile virus and St.Louis encephalitis virus carried byimportedmosquitoeswwW.bzxz.Net
2015-09-02发布
中华人民共和国
国家质量监督检验检疫总局
2016-04-01实施
本标准按照GB/T1.1一2009给出的规则起草。SN/T1460—2015
本标准代替SN/T14602004&输人性蚊类携带西尼罗病毒与圣路易脑炎病毒的检测方法》。本标准与SN/T1460一2004相比,主要变化如下:增加了规范性引用文件;
对生物安全要求进行了修订,删除了在生物安全3级实验室的操作要求,增加了生物安全实验室设计原则、病毒核酸分子检测操作要求、实验室设施和设备,检测工作的安全防护和实验室废弃物处理的要求;
—对病毒核酸分子检测方法进行了修订,增加了实时荧光RT-PCR方法;—删除了附录A。
本标准由国家认证认可监督管理委员会提出并归口。本标准起草单位:中华人民共和国宁波出人境检验检疫局。本标准主要起草人:郑剑宁、胡群、李红、裘炯良本标准所代替标准的历次版本发布情况为:SN/T1460—2004。
1范围
输入性蚊类携带西尼罗病毒与圣路易脑炎病毒的检测方法
本标准规定了国境口岸输人#
对象、检测方法、结果的报告。SN/T1460—2015
炎病毒检测的生物安全要求、检测路勇网
对输入性蚊类体内携带西尼罗病毒与圣路易脑炎病毒检测和报告,对本标准适用于检验检疫机构
口岸发现的蚊类检测西尼罗病毒与圣路易脑炎病毒让2规范性引用文件
下列文件对于本文件的应用是必不可少的可参照携行
生日期的引用文件,仅注日期的版本适用于本文于本文件。
件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用GB/T6682分析实验室用水规格和试验方法GB19489
实验室生物安全通用要求
微生物和生物医学实验室生物安全通用准则3术语和定义
下列术语和定义适用于本文作
importedmosquitoes
输入性蚊类
通过人境交通工具、集装箱、货物及行带人境内的库蚊,伊蚊属蚊类。3.2
westnilewirus;wN
西尼罗病毒
西尼罗热的病原体,属黄病毒科黄病毒属,为单链RNA病毒。西尼罗病毒分两个基因型,导致人类感染西尼罗病毒的分离株主要为工型。主要分布于非洲中东、西亚和北美。3.3
圣路易脑炎病毒
St.Luis encephalitis wirus;SLEV圣路易脑炎的病原体,属黄病毒科黄病毒属,为单链RNA病毒。主要分布于北美洲。4缩略语
下列缩略语适用于本文件,
Ct值:循环阅值(cyclethreshold)DEPC:焦碳酸二乙酯(diethylPyrocarbonate)FAM.6-羧基-荧光素(6-carboxy-fluorescein)1
SN/T1460—2015
RT-PCR:逆转录聚合酶链式反应(reversetranscription polymerasechainreaction)TAMRA:四甲基罗丹明(tramethylrhodamine)5检测对象
输人性蚊类。
6生物安全要求
实验室及检验应遵照以下生物安全要求:生物安全实验室设计原则应遵照GB19489的规定。a)
b)实验室设施和设备应遵照GB19489规定的BSL-2实验室要求。实验室废弃物处理应遵照GB19489对废物处置的要求,c)
检测工作的安全防护应遵照WS233型规定的二级生物安全个体防护要求。d
病毒核酸分子检测检测操作要求应遵照相关国家标准的规定。病毒核酸分子检测一
仪器和设备
需要如下仪器设备:
-普通RT-PCR方法和实时荧光RT-PCR方法荧光定量PCR仪;
PCR仪;
二级生物安全柜:
普通冰箱;
70℃超低温冰箱;
普通台式离心机;
高速冷冻离心机(离心力可达12000g):微量可调移液器(0.1μL~2.5μL、1μL~20μL、10μL~200μL、200μL~1000μL);涡旋器;
电泳仪:
凝胶成像分析系统;
高压灭菌锅。
主要试剂
除另有规定外,所有化学试剂均采用分析纯。实验用水应符合GB/T6682中一级水的规格。用于PCR(包括核酸抽提)时所用的水应是无RNA酶的水。
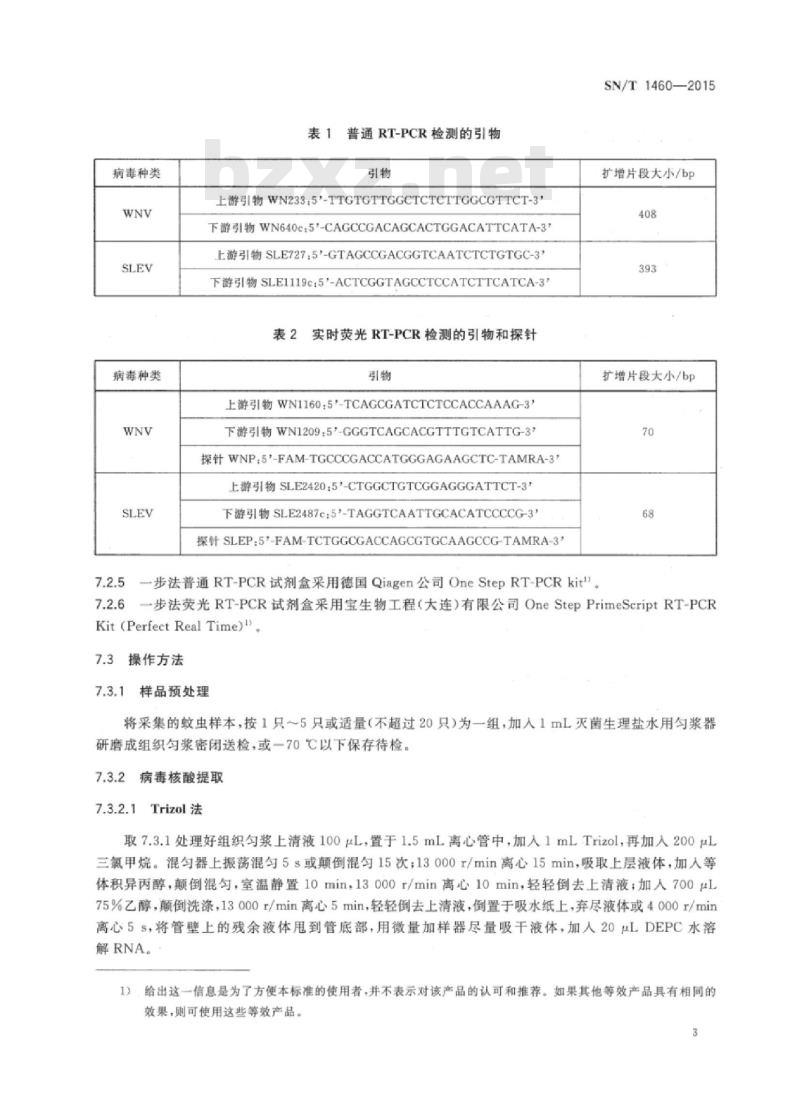
7.2.3核酸提取试剂为Trizol总RNA提取试剂或商品化的病毒RNA提取试剂盒。7.2.4引物和探针为根据表1和表2的序列进行合成引物和探针,加无RNA酶的超纯水配制成20μmol/L的储存液。
病毒种类
病毒种类
表1普通RT-PCR检测的引物
上游引物WN233:5'-TTGTGTTGGCTCTCTTGGCGTTCT-3下游引物WN640c:5'-CAGCCGACAGCACTGGACATTCATA-3上游引物SLE727:5*-GTAGCCGACGGTCAATCTCTGTGC-3”下游引物SLE1119c:5'-ACTCGGTAGCCTCCATCTTCATCA-3”实时荧光RT-PCR检测的引物和探针表2
上游引物WN1160:5*-TCAGCGATCTCTCCACCAAAG-3下游引物WN1209.5*-GGGTCAGCACGTTTGTCATTG-3探针WNP:5°-FAM-TGCCCGACCATGGGAGAAGCTC-TAMRA-3”上游引物SLE2420:5*-CTGGCTGTCGGAGGGATTCT-3*下游引物SLE2487c:5'-TAGGTCAATTGCACATCCCCG-3探针SLEP:5\-FAM-TCTGGCGACCAGCGTGCAAGCCG-TAMRA-3*一步法普通RT-PCR试剂盒采用德国Qiagen公司OneStepRT-PCRkit\SN/T1460—2015
扩增片段大小/bp
扩增片段大小/bp
一步法荧光RT-PCR试剂盒采用宝生物工程(大连)有限公司OneStepPrimeScriptRT-PCR7.2.6
Kit(PerfectReal Time)l
操作方法
7.3.1样品预处理
将采集的蚊虫样本,按1只一5只或适量(不超过20只)为一组,加人1mL灭菌生理盐水用勺浆器研磨成组织勾浆密闭送检,或一70C以下保存待检。病毒核酸提取
7.3.2.1Trizol法
取7.3.1处理好组织勾浆上清液100μL,置于1.5mL离心管中,加人1mLTrizol,再加人200μL三氯甲烷。混匀器上振荡混勾5s或颠倒混勾15次;13000r/min离心15min,吸取上层液体,加人等体积异丙醇,颠倒混匀,室温静置10min,13000r/min离心10min,轻轻倒去上清液:加人700μL75%乙醇,颠倒洗涤,13000r/min离心5min,轻轻倒去上清液,倒置于吸水纸上,弃尽液体或4000r/min离心5S,将管壁上的残余液体甩到管底部,用微量加样器尽量吸干液体,加人20μLDEPC水溶解RNA
给出这一信息是为了方便本标准的使用者,并不表示对该产品的认可和推荐。如果其他等效产品具有相同的1)
效果,则可使用这些等效产品
SN/T1460—2015
试剂盒提取法
按商品试剂盒说明书操作。
普通RT-PCR检测方法
反应体系
检测输人性蚊类中西尼罗病毒与圣路易脑炎病毒的普通RT-PCR反应体系见表3。表3普通RT-PCR反应体系
5倍浓度的一步RT-PCR缓冲液
dNTP混合液(1ommol/L)
上游引物(20μmol/L)
下游引物(20μmol/L)
无RNA酶水
一步RT-PCR酶混合物
RNA酶抑制剂
样品RNA
反应体积
检测过程中分别设阳性对照、阴性对照。阳性SLEV核昔酸序列通过载体构建和件7.3.3.2
反应参数
50C30min95℃15m
7min,4℃保存。
转录合成的
录结束局
PCR产物的琼脂糖温胶电泳
取5μLPCR扩增产物用
加样量/pL
WNV和SLEV病毒株或根据WNV和
RNA片段
5%的琼脂糖凝胶
电泳C
量标准物作对照,推荐使用PUCDNA/MSPC结果。
实时荧光RT-PCR检测方法
反应体系
阻性对照为无RNA酶的DEPC水。
s.72℃1min.35个循环.72℃
mL溴化乙锭,EB),并加DNA分子电泳池约0.5h凝胶成像系统观察检测输人性蚊类中西尼罗病毒与圣路易脑炎病毒的实时荧光RT-PCR反应体系见表4表4
2倍浓度的一步RT-PCR混合液
Tag酶
逆转录酶
上游引物(20μmol/L)
实时荧光RT-PCR反应体系
加样量/μL
下游引物(20μmol/L)
探针(20μmol/L)
ROX荧光校正染料
无RNA酶水
样品RNA
反应体积
表4(续)
检测过程中分别设阳性对照、阴性对照,阳性对照为WNV和
SLEV核苷酸序列通过载体构建和体反应条件
将加好样的PCR反应管分别转移到Prism7500型全自动荧光定量PCR检团荧光通道无.校正荧光通道ROX。光定量PC
夜为例说明
SN/T1460—2015
加样量/μL
EV病毒株或根据WNV和
为无RNA酶的DEPC水。
片度,对服
测仪上进行扩增反应,程序设置为以ABI格带光信号设置
报告荧光通道FAM.萍灭基
立按实际机型进行反应程序设
于其地型号的我光定量PCR仪
置,没有ROX荧光通道的荧光定量FCR仅不进行ROX的设置
步法实时荧光RT-PCR反应条
循环:选择FAM通道于72C延伸时收集荧光信号8结果判定及报告
普通RT-PCR
对样品进行RT-PCR检测.如果团性条带,而样品未出现预期大小的扩增条带时照和
卡群品
性基因。报告为“西尼罗病毒核酸医性C普通RTPCRPCR法)”
如果阴性对照和空白对照未出现条带阳戏
s.52℃30s.72℃40s.45个
未出现条带,用
性对照出现预期大小的扩增
中未检
到西尼
罗病毒或圣路易脑炎病毒特异
法)\或\圣路易
卤炎病毒核酸阴性(普通RT
出现预期
的扩增条带,而样品出现预期大小的扩增条带,则可判定样品中检测到西尼罗病毒或圣路易脑炎病毒特异性基因。报告为“西尼罗病毒核酸阳性(普通RT-PCR法)\或“圣路易脑炎病毒核酸阳性(普通RT-PCR法)”。8.2
实时荧光RT-PCR
基线设定
以阅值线刚好超过正常阴性对照扩增曲线的最高点或根据仪器噪音情况调整设定基线8.2.2质量控制
反应结果应同时符合以下条件,否则试验视为无效:给出这一信息是为了方便本标准的使用者,并不表示对该产品的认可和推荐。如果其他等效产品具有相同的2
效果,则可使用这些等效产品。5
SN/T1460—2015
阴性对照无扩增曲线:
阳性对照Ct值≤35并有明显扩增曲线。结果判定及报告
检验结果按以下要求判定和报告:a
阴性:Ct值为未检出或大于45,且无明显扩增曲线,报告为“西尼罗病毒核酸阴性(荧光RT-PCR法)”或“圣路易脑炎病毒核酸阴性(荧光RT-PCR法)”。阳性:检测样品Ct值≤40,并有明显扩增曲线,报告西尼罗病毒核酸阳性(荧光RT-PCR法)”或“圣路易脑炎病毒核酸阳性(荧光RT-PCR法)”检测样品出现荧光增幅曲线的Ct值介于40~45之间,应重新进行检测。若重新检测的Ct值仍介于40~45之间,并有明显扩增曲线,则按阳性结果报告,否则为阴性。SN/T1460-2015
中华人民共和国出人境检验检疫行业标准
输入性蚊类携带西尼罗病毒与圣路易脑炎病毒的检测方法
SN/T1460—2015
中国标准出版社出版
北京市朝阳区和平里西街甲2号(100029)北京市西城区三里河北街16号(100045)总编室:(010)68533533
网址spc.net.cn
中国标准出版社秦皇岛印刷厂印刷普
开本880×12301/16
印张0.75
字数14千字
2016年3月第一版
2016年3月第一次印刷
印数1-1100
书号:155066·2-29872
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。






 ✕
✕