基本信息
标准号:
SN/T 4161-2015
中文名称:国境口岸副溶血性弧菌实时荧光PCR方法
标准类别:商检行业标准(SN)
标准状态:现行
出版语种:简体中文
下载格式:.zip .pdf
下载大小:5.55 MB
相关标签:
国境
口岸
溶血性
弧菌
实时
荧光
PCR
方法

标准分类号
关联标准
出版信息
相关单位信息
标准简介
SN/T 4161-2015.Detection method for vibrio parahaemolyticus by real-time fluorescence PCR at frontier ports.
1范围
SN/T 4161规定了国境口岸副溶血性弧菌实时荧光PCR检验的对象、标本的采集、运输和保存,操作方法及结果报告。
SN/T 4161适用于国境口岸副溶血性弧菌感染的筛选检测。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 4789.17-2003食品卫生微生物学检验肉与肉制品检验
GB/T 4789.20-2003食品卫生微生物学检验水产食品检验;
GB 19489实验室生物安全通用要求
SN/T1193基因检验实验室技术要求
WS/T 230临床诊断中聚合酶链反应(PCR)技术的应用
3术语和定义
下列术语和定义适用于本文件。
3.1副溶血性弧菌 vibrio parahaemolyticus
副溶血性弧菌,属弧菌科弧菌属,革兰染色阴性,兼性厌氧菌,为多形态杆菌或稍弯曲弧菌。临床上以急性起病、腹痛、呕吐、发烧、腹泻及水样便(重症者为黏液便或黏血便)为主要症状。
4缩略语
下列缩略语适用于本文件。
DNA:脱氧核糖核酸(deoxyribonucleic acid)
PCR:聚合酶链反应(Polymerase Chain Reaction)
Taq DNA polymerase:Taq DNA聚合酶
标准内容
中华人民共和国出入境检验检疫行业标准SN/T4161-2015
国境口岸副溶血性弧菌实时荧光PCR方法
Detection methodfor vibrio parahaemolyticusbyreal-timefluorescencePCRatfrontierports
2015-02-09发布
中华人民共和国
国家质量监督检验检疫总局
2015-09-01实施
本标准按照GB/T1.1一2009给出的规则起草。本标准由国家认证认可监督管理委员会提出并归口。本标准起草单位:中华人民共和国江西出入境检验检疫局。本标准主要起草人:胡婷、杨春华、刘岚、孙思扬、谢玉萍、徐菱菱、周延。SN/T4161—2015
1范围
国境口岸副溶血性弧菌实时荧光PCR方法
SN/T4161—2015
本标准规定了国境口岸副溶血性弧菌实时荧光PCR检验的对象、标本的采集、运输和保存,操作方法及结果报告。
本标准适用于国境口岸副溶血性弧菌感染的筛选检测。规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB/T4789.17—2003食品卫生微生物学检验肉与肉制品检验GB/T4789.20一2003食品卫生微生物学检验水产食品检验GB19489实验室生物安全通用要求SN/T1193
WS/T230
术语和定义
基因检验实验室技术要求
临床诊断中聚合酶链反应(PCR)技术的应用下列术语和定义适用于本文件。3.1
副溶血性弧菌
vibrioparahaemolyticus
副溶血性弧菌,属弧菌科弧菌属,革兰染色阴性,兼性厌氧菌,为多形态杆菌或稍弯曲弧菌。临床上以急性起病、腹痛、呕吐、发烧、腹泻及水样便(重症者为黏液便或黏血便)为主要症状。缩略语
下列缩略语适用于本文件。
DNA:脱氧核糖核酸(deoxyribonucleicacid)PCR:聚合酶链反应(PolymeraseChainReaction)TagDNApolymerase:TaqDNA聚合酶5
检测对象
疑似副溶血弧菌感染者的临床标本,如粪便疑似副溶血弧菌污染环境标本,如水样,以及食品。1
SN/T4161—2015
6实验室生物安全和PCR防污染要求实验室生物安全应符合GB19489的规定。PCR防污染措施按WS/T230和SN/T1193的规定执行。
7仪器与器材
实时荧光定量PCR仪及配套PCR反应管。生物安全柜。
高速冷冻离心机:最大转速1
台式离心机(离心速度900g)
涡旋振荡器。
恒温水浴锅。
高压灭菌锅。
低温冰箱、冷藏、冷冻冰箱。
可调式微量加样器。
8试剂
生理盐水:蒸馏水和NaCI配制浓度为0.8.1
阳性对照品:人工制备含副溶血弧菌检测序列的质8.3
阴性对照品:灭菌双蒸水ddH2O。8.4
EDTA-Na2的混合液
DNA提取液:含0.9%NaCI
1和01%
检测程序
样品的采集
粪便样本
采集病人发病早期新鲜粪便于
5g8g,水样便采集1mL~3mL。
一次性无菌采便
管内,成形便采集
经旋转,有可见粪便的棉拭放人采便管内。采亦可用湿润的直肠棉拭插人直肠内3cm~5cm处并轻轻便管外表贴上带有唯一标识号码的标签,直接用于检测,或保存,或送检。9.1.2水样标本
水样用无菌容器采集3mL~5mL,密闭后外表贴上带有唯一识别标识号码的标签,直接用于检测,或保存,或送检。
食品标本
肉与肉制品的取样方法按GB/T4789.17一2003中的规定。9.1.3.2
各种水产食品及其制品的取样方法按GB/T4789.20一2003中5.1的规定。9.2样本的运转与保存此内容来自标准下载网
样本运输采用冰壶加冰密封运输。对于不立即检测的样本,应保存于一20℃待检2
样本的前处理
粪便样本
SN/T4161—2015
挑取米粒大小粪便,放置于有0.5mL生理盐水的离心管中,振荡混匀,16200g离心2min。去尽上清,沉淀用于核酸提取。
水样样本
取标本3mL,16200g离心2min。去尽上清,沉淀用于核酸提取。9.3.3
食品样本
以无菌方法取肉类或水产品组织样品0.1g,用0.2mL无菌生理盐水离心管中研磨,然后100℃沸水中加热5min8000g离心3min,上清用于以后的荧光PCR反应9.4样本的DNA提取
在标本的前处理沉淀中,加人100μLDNA提取液充分混勾,沸水浴10min。16200g离心5min,上清可直接用于荧光PCR反应。也可以使用商品化的DNA提取试剂盒并按照说明书操作。9.5实时荧光PCR检测
9.5.1待检测所需各种试剂充分融化后,请先将各试剂剂盒进行实时荧光PCR检测时,应根据9.5.2
开行离
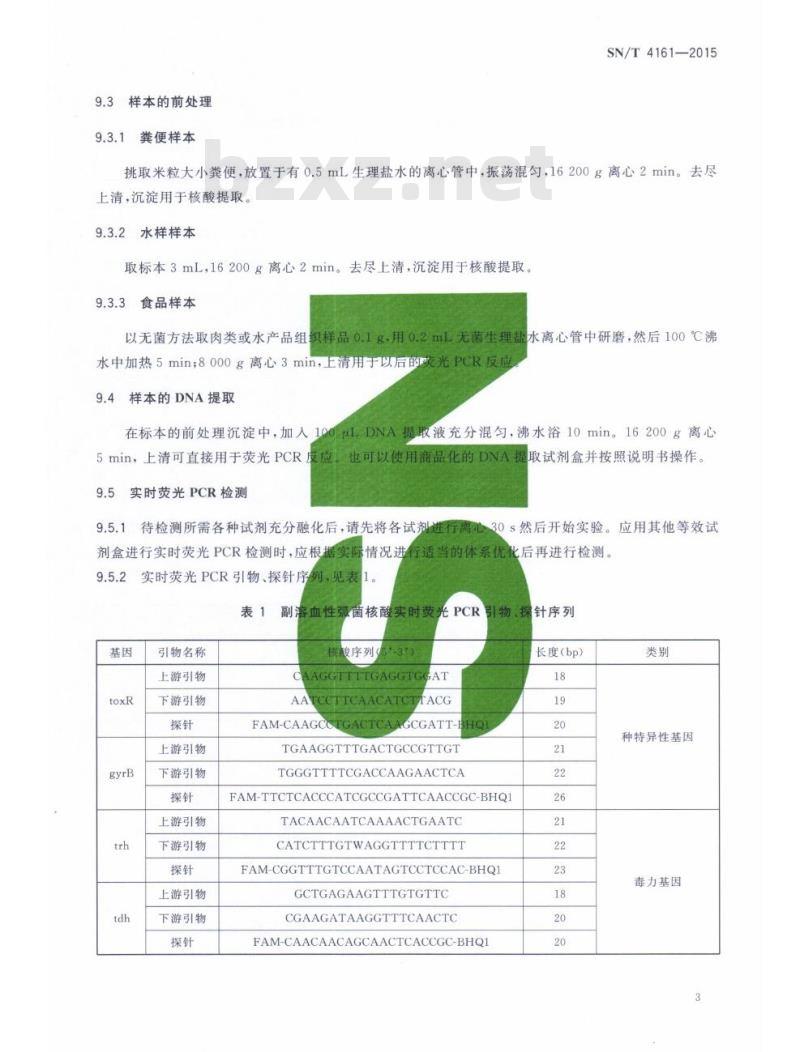
30s然后开始实验。应用其他等效试情况进行适当的体系优化后再进行检测。实时荧光PCR引物、探针序
学列,见表1。
表1副溶血性弧菌核酸实时荧光PCR引物、探针序列
引物名称
上游引物
下游引物
上游引物
下游引物
上游引物
下游引物
上游引物
下游引物
5~-3+)
核酸序列(5
CAAGGTTTTGAGGTG
AATCCTTCAACATO
FAM-CAAGCCTGACTCAAGCGATT-1
TGAAGGTTTGACTGCCGTTGT
TGGGTTTTCGACCAAGAACTCA
FAM-TTCTCACCCATCGCCGATTCAACCGC-BHQ1TACAACAATCAAAACTGAATC
CATCTTTGTWAGGTTTTCTTTT
FAM-CGGTTTGTCCAATAGTCCTCCAC-BHQ1GCTGAGAAGTTTGTGTTC
CGAAGATAAGGTTTCAACTC
FAM-CAACAACAGCAACTCACCGC-BHQI长度(bp)
种特异性基因
毒力基因
SN/T4161—2015
荧光PCR反应体系配置按表2中的顺序,依次加入。表2副溶血性弧菌核酸实时荧光PCR检测反应体系名称
2XPCRBuffer
上游引物(12.5μmol/L)
下游引物(12.5μmol/L)
探针(5μmol/L)
Nuclease-Free Water
总体系
TaKaRaPremixExTaqTM试剂盒中组分。给出这一信息是为了方便本标准的使用者,并不表示对该产品的唯一认可,如果其他等效产品具有相同的效果,则可使用这些等效产品。9.5.4:设立阴性对照和阳性对照9.5.5荧光PCR反应:将加好样的PCR反应管分别转移到荧光定量PCR检测仪上进行扩增反应。荧光通道检测选择:FAM通道。荧光PCR扩增程序按照表3中的程序进行设置,反应总体积为25μL。9.5.6首先进行种特异性基因检测,若检测为阳性,则继续进行毒力基因检测;若种特异性基因检测为阴性,则无需进行毒力基因检测。副溶血性弧菌核酸实时荧光PCR的反应程序表3
扩增及荧光收集
结果判定及报告
反应温度
是否采集荧光信号
循环数
阴性对照Ct值应显示0,阳性对照Ct值≤36并有典型的扩增曲线,否则此次检测结果无效,需重做。
当同时进行的阳性对照以及阴性实验结果正常,本方法检验结果判定如下:检测样品有明显的荧光增幅曲线,且Ct值≤36时,判为阳性;检测样品荧光增幅曲线的Ct值介于36和40之间时,建议采用浓缩方式处理核酸样本,再重新进行实时荧光RT-PCR检测。若重新检测的Ct值有明显减少趋势,且曲线有明显的对数增长期,判为阳性。此类样本建议用其他方法进一步验证;否则判为阴性;检测样品无荧光增幅现象,判为阴性。本方法报告模式如下:
SN/T4161—2015
若种特异性基因toxR/gyrB两者之一结果为阳性,且毒力基因trh/tdh两者之一结果为阳性即报告副溶血性弧菌核酸阳性且含毒力基因;若种特异性基因toxR/gyrB两者之一结果为阳性,且毒力基因检测为阴性则报告为副溶血性弧菌核酸阳性,但不含毒力基因;一若种特异性基因toxR/gyrB检测均为阴性,则报告为副溶血性弧菌阴性
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。






 ✕
✕