中华人民共和国出入境检验检疫行业标准SN/T4519-2016
出口动物源食品中利巴韦林残留量的测定液相色谱-质谱/质谱法
Determination of ribavirin residue in foodstuffs of animal origin for export-LC-MS/MSmethod
2016-06-28发布
中华人民共和国
国家质量监督检验检疫总局
2017-02-01实施
本标准按照GB/T1.1—2009给出的规则起草。SN/T4519—2016
请注意本文件的某些内容可能涉及专利。本文件的发布机构不承担识别这些专利的责任。本标准由国家认证认可监督管理委员会提出并归口。本标准起草单位:中华人民共和国福建出入境检验检疫局、中华人民共和国东山出入境检验检疫局、中华人民共和国厦门出人境检验检疫局、中华人民共和国绍兴出入境检验检疫局、福建圣农发展股份有限公司。
本标准主要起草人:刘正才、杨方、潘迎芬、林永辉、陈旭东、徐敦明、任明兴、吕小玲。1范围
出口动物源食品中利巴韦林残留量的测定液相色谱-质谱/质谱法
SN/T4519—2016
本标准规定了动物源食品中利巴韦林残留量的液相色谱质谱/质谱的测定方法。本标准适用于鸡肉、肝脏、肾、蛋、猪肉、鳗鱼、虾等动物源食品中利巴韦林残留量的测定和确证。2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件GB/T6682分析实验室用水规格和试验方法3方法提要
试样中残留的利巴韦林代谢物经酸性磷酸酯酶水解成利巴韦林原药,与样品中残留的利巴韦林原药一起,经三氯乙酸乙晴混合溶液提取,经苯硼酸固相萃取小柱净化,液相色谱-质谱/质谱进行测定,同位素内标法定量。
4试剂和材料
除非另有说明,所用试剂均为分析纯,水为GB/T6682规定的一级水。4.1
甲醇:色谱纯。
2乙睛:色谱纯。
甲酸:色谱纯。
三氯乙酸。
5氨水:含量为25%~28%
乙酸铵:色谱级纯。
酸性磷酸酯酶(phosphataseacid,fromwheatgerm,活力:≥0.4unit/mg.CAS号:9001-77-8)。3酸性磷酸酯酶溶液(100ug/mL):准确称取酸性磷酸酯酶(4.7)5mg,置50mL容量瓶中,用水溶4.8
解并稀释至刻度,摇匀,配制成100μg/mL的酶解液,4℃~8℃冰箱中保存9三氟乙酸溶液(20g/L,pH4.8):称取20g三氯乙酸,加水约950mL使其溶解,用氨水调pH至4.9
4.8(±0.1),再加水定容至1000mL。4.10PBA苯硼酸固相萃取小柱洗脱液,甲酸-水-甲醇溶液(体积比2:8:90):准确量取2mL甲酸和8mL水加入90mL的甲醇中,混匀后备用4.11乙酸铵缓冲溶液(2.0mol/L+pH4.8):称取乙酸铵77.0g,水约450mL使其溶解,用乙酸调pH至4.8(士0.1),再加水定溶至500mL。4.12乙酸铵缓冲溶液(0.25mol/LpH8.5):称取乙酸铵9.06g,加水约450mL使其溶解,用氨水调pH至8.5士0.1),再加水定容至500ml。7
SN/T4519—2016
4.13标准物质:利巴韦林(ribavirin;CAS号:36791-04-5),纯度大于98.0%。4.14同位素内标标准物质:利巴韦林-13C,纯度大于99.0%。5标准储备液(100μg/mL):准确称取利巴韦林标准品(4.13)10mg(精确至0.1mg),置100ml容4.15
量瓶中,用甲醇溶解并稀释至刻度,摇匀,配制成100ug/mL的标准储备液,一18℃冰箱中保存,有效期为1年。
4.16标准中间液(1.0μg/mL):用移液管吸取标准储备液(4.15)1mL置100mL容量瓶中,用甲醇稀释至刻度,摇勾得到1.0μg/mL标准中间液,置4℃8℃冰箱中保存,有效期为3个月。4.17内标储备液:准确称取利巴韦林-13C,标准品(4.14)10mg(精确至0.1mg),置100mL容量瓶中,用甲醇溶解并稀释至刻度,播匀,配制成100μg/mL的内标标准储备液,一18℃冰箱中保存,有效期为1年。
4.18内标中间溶液(1.0μg/mL):移取1.00mL的内标标准储备液(4.17)至100mL容量瓶中,用甲醇稀释至刻度,置4℃~8
℃冰箱中保存,有效期为3个月。4.19标准工作液:临用时根据需要,移取适量的标准中问溶液(4.16)和内标中间溶液(4.18),用乙睛稀释至合适浓度,使用前配制。
4.20PBA苯硼酸固相苯取小柱:100mg/3mlL,或相当者:使用前依次用3mL乙腈,3mL乙腈-1%甲酸(体积比,3:1),3mL乙酸铵缓冲溶液(4.12))活化,并保持柱体湿润。注:可采用商品化的BondElutPBA固相举取小柱BondElutPBApartNo:12102127,USA7或等同性能的其他小柱。
滤膜:0.22um,有机系。
5仪器和设备
液相色谱-质谱/质仪:配电喷雾电离(ESI)源天平:感量0.1mg和0.01g。
组织捣碎机。
5.4高速冷冻离心机:转速8000/min5.5离心机5000r/min
5.6漩涡振荡器。
5.7pH计。
5.8氮吹仪。
固相萃取装置。
6试样制备与保存
6.1试样制备
肌肉、肝脏、肾放入组织捣碎机均质,充分混匀,均分成两份,分别装人清洁容器内,并标明标记;蛋类,虾去壳后取可食部分后放入组织捣碎机均质,充分混勾,均分成两份,分别装入清洁容器内,并标明标记。
制样操作过程中,应防止样品受到污染或发生残留物含量的变化6.2试样保存
试样于一18℃以下保存,新鲜或冷冻的组织样品可在2℃~6℃贮存72h。rKAoNiKAca
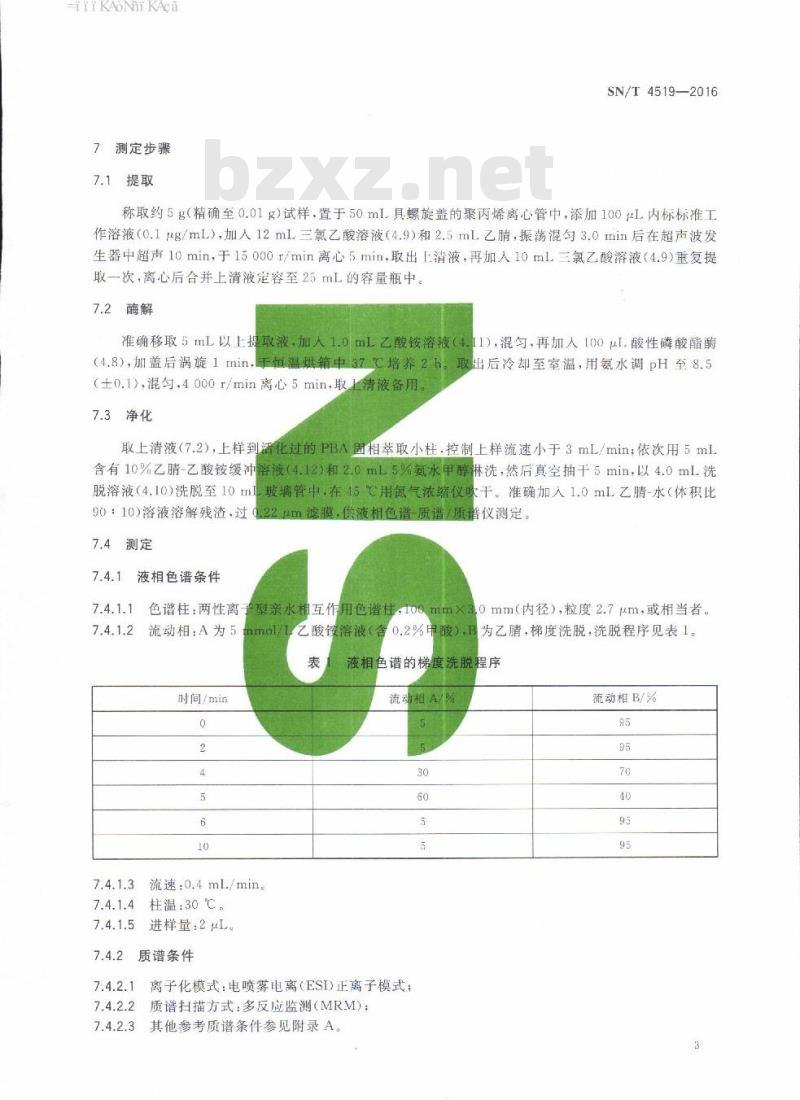
7测定步骤
7.1提取
SN/T4519—2016
称取约5g(精确至0.01g)试样,置于50mL具螺旋盖的聚丙烯离心管中,添加100L内标标准工作溶液(0.1μg/mL),加人12mL三氯乙酸溶液(4.9)和2.5mL乙睛,振荡混勾3.0min后在超声波发生器中超声10min,于15000r/min离心5min,取出上清液,再加入10mL三氯乙酸溶液(4.9)重复提取一次,离心后合并上清液定容至25mL的容量瓶中。7.2酶解
准确移取5mL以上提取液,加入1.0mL乙酸铵溶液(4.11),混匀,再加100μL酸性磷酸酯酶(4.8),加盖后涡旋1min,手恒温烘箱中37℃培养2h。取出后冷却至室温,用氨水调pH至8.5(士0.1),混匀,4000r/min离心5min,取上清液备用7.3净化
取上清液(7.2),上样到活化过的PBA固相萃取小柱,控制上样流速小于3mL/min;依次用5mlL含有10%乙腈-乙酸铵缓冲溶液(4.12)和2.0mL5%氨水甲醇淋洗,然后真空抽干5min,以4.0mL洗脱溶液(4.10)洗脱至10mL玻璃管中,在15℃用氮气浓缩仪吹干。准确加入1.0mL乙睛-水(体积比90:10)溶液溶解残渣,过0.22m滤膜.供液相色谱-质谱/质谱仪测定。7.4测定
液相色谱条件
子型亲水相互作用色谱柱
色谱柱:两性离
流动相:A为5
时间/min
流速:0.4mL/min
柱温:30℃。
进样量:2μL。
质谱条件
0mm(内径),粒度2.7μm,或相当者。乙酸铵溶液(含0.2%甲酸)1B
为乙,梯度洗脱,洗脱程序见表1。表
液相色谱的梯度洗脱程序
流动相A/路
离子化模式:电喷雾电离(ESI)正离子模式;质谱扫描方式:多反应监测(MRM);其他参考质谱条件参见附录A。
流动相B/%
-TTKAoNiKAca
SN/T4519—2016
7.4.3定性测定
被测组分选择1个母离子,2个以上子离子,在相同实验条件下,样品中待测物质的保留时间与标准校准溶液中对应浓度标准校准溶液的保留时间偏差在士2.5%之内;且样品谱图中各组分定性离子的相对丰度与浓度接近的标准校准溶液谱图中对应的定性离子的相对丰度进行比较,偏差不超过表2规定的范围,则可判定为样品中存在对应的待测物、表2定性确证时相对离子丰度的最大充许偏差相对离子丰度/%
允许的最大偏差/%
7.4.4定量测定
>10-20
内标法定量:用标准工作溶液分别进样,以分析化合物和内标化合物的峰面积比为纵坐标,以分析化合物和内标化合物的浓度比为横坐标作标准工作曲线,用标准工作曲线对样品进行定量,标准工作液和待测液中利巴韦林的响应值均应在仪器线性响应范围内。利巴韦林的保留时间、母离子和子离子参见附录A表A.1。利巴韦林的标准品选择离子流色谱图参见附录B图B.1。7.5空白试验
除不加试样外,均按7.1~7.4操作步骤进行。8结果计算和表述
试样中利巴韦林的残留总量利用数据处理系统计算或按式(1)计算,计算结果需扣除空白值。X_CXG,XAXA,XV
cXA,XA.Xm
式中:
样品中利巴韦林残留量,单位为微克每千克(ug/kg):e
标准工作溶液中利巴韦林的浓度,单位为纳克每毫升(ng/mL);样液中内标物的浓度,单位为纳克每毫升(ng/mL);样液中利巴韦林的峰面积;
标准工作溶液中内标物的峰面积;样品溶液最终定容体积,单位为毫升(mL):标准工作溶液中内标物的浓度,单位为纳克每毫升(ng/mL);样液中内标物的峰面积;
标准工作溶液中利巴韦林的峰面积;最终样液代表的试样质量,单位为克(g)。9测定低限和回收率
9.1测定低限
本方法中利巴韦林的测定低限为1.0ug/kg。9.2正确度(回收率)
不同基质中利巴韦林残留量在不同添加水平下的回收率试验数据参见附录C表C.1。4
-rKAONiKAca
质谱参考参数如下:
ESI正离了模式;
多反应监测(MRM);
电喷雾电压(IS):5500.0V;
离子源温度(TEM):500℃;
附录A
(资料性附录)
质谱参考参数\
雾化气压力(GS1):345kPa(50.00psi);辅助气压力(GS2):345kPa(50.00psi);气帘气压力(CUR):241kPa(35.00psi);监测离子对、去簇电压(DP)、碰撞电压(CE)见表A.1。表A.1
药物名称
利巴韦林
利巴韦林-\C
SN/T4519—2016
利巴韦林保留时间、定性定量离子对及去簇电压、碰撞能量保留时间
定性离子对
245.1>113.1
245.1>96.0
250.1>113.0
定量离子对
245.1>113.1
250.1≥113.0
去簇电压
碰撞电压
1)非商业性声明:附录A所列参考质谱条件是在WatcrsUItraUPLC-API5500型液质联用仪上完成的,此处列出试验用仪器型号仅为提供参考·并不涉及商业日的,鼓励标准使用者尝试不同厂家或型号的仪器。5
iKAONTKAca
SN/T4519—2016
附录B
(资料性附录)
利巴韦林标准物质的多反应监测(MRM)色谱图5×103
4×103
3×103-
2×103-
怕8.0×103
利巴韦林
m/z:245.1>96.1amu
时间/
时间/mi
利巴韦林
#/z:245.1113.1am
利巴韦林-
m/z250.1>113.0amm
时间/min
利巴韦林以及内标标准品(2ng/mL)的反应监测(MRM)色谱图iKAoNiiKAca
附录C
(资料性附录)
回收率
SN/T4519—2016
利巴韦林在鸡肉、鸡蛋、鸡肝、鸡肾、猪肉、鳗鱼、虾、蒸煮鸡尾串、皮蛋中回收率范围的试验数据,见表c.l。
样品名称
蒸煮鸡尾申
利巴韦林在不同基质中不同添加水平下的回收率范围添加水平/(g/kg)
回收率范围/%
77.8~107.0
81.0104.0
81.9~102.0
82.5~101.5
80.3~100.0
78.3~-102.0
82.0~100.5
80.4~93.4
78.6~102.0
78.5~95.0
76.6~89.9
81.8~101.0
82.0~100.5
80.7-93.8
81.7~103.0
80.0~-103.5
83.5-97.0
80.7-106.0
80.5~104.0
82.0~98.3
81.4107.0
80.0~101.5
77.6~91.8
79.7~103.0
82.0~98.0
80.9~95.9
SN/T4519—2016
Foreword
ThisstandardispreparedaccordingtoGB/T1.1-2009Please pay attention that some contents in this standard may refer to patents,The institution doesn'ttakeontheresponsibilityto indentifythesepatents.This standard is proposed by and is under the charge of the Certification and Accreditation adminis-tration of the People's Republic of China.This standard is drafted by Fujian Entry-Exit Inspection and Quarantine Bureau of the People'sRepublic of China,Dongshan Entry-Exit Inspection andQuarantineBureauof thePeople'sRepublicofChina,Xiamen Entry-Exit Inspection and Quarantine Bureau of the People's Republic of China.Shaoxing Entry-Exit Inspection and Quarantine Bureau of the People's Republic of China,Fujian sunnerdevelopmentCO.,LTD
This standard was mainly drafted by Liu Zhengcai,Yang Fang,Pan Yinfen,Lin Yonghui,Chen XudongXunDunming,RenMingxing,LvXiaolingNote:This Englishversion,a translationfrom theChinetextis solelyforguidance8
SN/T4519—2016
Determinationofribavirinresidueinfoodstuffsof animal origin for export-LC-MS/MS method
The standard specifies the sample preparationand determination of the ribavirinbyLC-MS/MS inani-mal tissues for export.
This standard is appiicable to the determination and confirmation of ribavirin in residues in chicken.liver,kidneyeggs,pork,fishandshrimpsNormativereferences
The following documents are necessary for this standard.For dated references,only dated editionsshall apply to this standard. For undated references,the latest edition of the normative document (in-cludingsubsequentamendments)referredtoapplies.GB/T6682Waterforanalytical laboratoryuse-Specificationand testmethods3Principle
Trichloroacetic acid-acetonitrile solution is used to extract the total residues of ribavirin in tested-samples and then was digestedby acid phosphatase.The extract was purified using phenyl boronicacid(PBA) SPE cartridge, The ribavirin is determined by LC-MS/MS,quantified by internal standardmethod.
Reagents andmaterials
Unless otherwise specified,all the reagent used should be analytical grade,water is the firsr gradewaterprescribedbyGB/T6682.
4.1Methanol:HPLCgrade.
SN/T4519—2016
Acetonitrile:HPLC gradebzxz.net
4.3Formicacid:HPLCgrade.
4.4 Trichloroacetic acid.
4.5Ammonia(25%~28%)
4.6Ammoniumacetate:HPLCgrade4.7Acid phosphatase(Phosphatase Acid,From Wheat Germ.Vitality:≥0.4unit/mg.CAS No:9001-77-8).
4.8Stock solutions of acid phosphatase (100 μg/mL):Weigh about 5.0mg acid phosphatasemate-rials(4.7)dissolvewith watertoa volumeof 504℃~8℃.
Thestocksolutionsstoreatapproximately4.9Trichloroacetic acid solution(20g/L.pH4.8):Weigh 20gtrichloroacetic acid,dissolve with950mLwaterandadjustedpH4.8(±0.1)with ammoniaanddiluteto1000mL,thenmixwell.4.10TheeluentofPBASPE(formicacid/water/methanol2:8:90.V/V/V):Pipet2.0mLformicacid and 8.0 mL water into90mLmethanol an4.112.0mol/Lammoniumacetatebuffermixwell.
solution:Weigh ammonium acetate 77.0 g.dissolve with450mLwaterandadjustedpH4.8(±0.1)withammoniaanddiluteto500m4.120.25mol/Lammoniumacetatebufferlution:Weigha
ammonium acetate 9.06 g,dissolve with450mLwaterandadjustedpH8.5(±0.1withammoniaanddiluteto500ml4.13Standard:ribavirin,CAsNo.36791-04-5.purity≥98.0%4.14
Isotopeinternalstandard:ribavirin-13Cs,purity≥99.0%4.15Stock solutionsof ribavirin(100 μg/mL):Weighabout 10.0mg ribavirin(4.13),dissolve withmethanol and then dilute with methanol to a volume of 1o0 mL.The stock solutions store at approxi-mately-18℃,can usefor12months.4.16Middle standard solution(1 μg/mL):Dilute 1.00 mL the stock standard solution (4.15)to100 mL with methanol.The stock solutions store at approximately4 ~8℃,can use for threemonths.
4.17Stock solutionsof ribavirin-13Cs(100μg/mL):Weighabout10.0mgribavirin-13Cs(4.14),dis-solvewithmethanolandthendilutewithmethanol toavolumeof10omL.Thestock solutions store10
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。






 ✕
✕