SN/T 3394-2012
基本信息
标准号: SN/T 3394-2012
中文名称:马秋波病毒实时荧光RT-PCR检测规程
标准类别:商检行业标准(SN)
标准状态:现行
出版语种:简体中文
下载格式:.zip .pdf
下载大小:282573

标准分类号
关联标准
出版信息
相关单位信息
标准简介
SN/T 3394-2012.Code of detecting machupo virus by real-time fluorescence RT-PCR.
1范围
SN/T 3394规定了国境口岸人出境人员或鼠类携带马秋波病毒的实时荧光RT-PCR快速检测方法,包括检测对象、标本采集和处理、检测程序、结果判定及报告。
SN/T 3394适用于国境口岸人出境人员或鼠类携带马秋波病毒的分子生物学检测。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB 19489实验室生物安 全通用要求
wS233微生物和生物医学实验室生物安全通用准则
可感染人类的高致病性病原微生物菌(毒)种或样本运输管理规定(2005卫生部)
3术语和定义
下列术语和定义适用于本文件。
3.1马秋波病毒machupo virus
属沙粒科,包括8种进化支,基因组为分节段双链RNA,由L(大)和S(小)片段组成,分别编码依赖RNA的RNA聚合酶、锌指蛋白和包膜糖蛋白、核蛋白。1962年首次在玻利维亚发现,故其引起的出血热又名玻利维亚出血热。该病毒由胼胝暮鼠(Calomyscallosus,又称白足鼠)携带传播,主要通过鼠的分泌物感染人类。
4缩略语
下列缩略语适用于本文件。
RT-PCR:逆转录聚合酶链式反应
Ct值:循环阈值,每个反应管的荧光信号达到设定阈值时所经历的循环数
RNA:核糖核酸
DEPC:焦碳酸二乙酪
FAM:6-羧基荧光素,一种荧光报告基团
BHQ:黑洞淬灭基团
1范围
SN/T 3394规定了国境口岸人出境人员或鼠类携带马秋波病毒的实时荧光RT-PCR快速检测方法,包括检测对象、标本采集和处理、检测程序、结果判定及报告。
SN/T 3394适用于国境口岸人出境人员或鼠类携带马秋波病毒的分子生物学检测。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB 19489实验室生物安 全通用要求
wS233微生物和生物医学实验室生物安全通用准则
可感染人类的高致病性病原微生物菌(毒)种或样本运输管理规定(2005卫生部)
3术语和定义
下列术语和定义适用于本文件。
3.1马秋波病毒machupo virus
属沙粒科,包括8种进化支,基因组为分节段双链RNA,由L(大)和S(小)片段组成,分别编码依赖RNA的RNA聚合酶、锌指蛋白和包膜糖蛋白、核蛋白。1962年首次在玻利维亚发现,故其引起的出血热又名玻利维亚出血热。该病毒由胼胝暮鼠(Calomyscallosus,又称白足鼠)携带传播,主要通过鼠的分泌物感染人类。
4缩略语
下列缩略语适用于本文件。
RT-PCR:逆转录聚合酶链式反应
Ct值:循环阈值,每个反应管的荧光信号达到设定阈值时所经历的循环数
RNA:核糖核酸
DEPC:焦碳酸二乙酪
FAM:6-羧基荧光素,一种荧光报告基团
BHQ:黑洞淬灭基团
标准图片预览




标准内容
中华人民共和国出入境检验检疫行业标准SN/T3394—2012
马秋波病毒实时荧光RT-PCR检测规程Code of detecting machupo virus by real-time fluorescence RT-PCR2012-12-12发布
中华人民共和国
国家质量监督检验检疫总局
2013-07-01实施
本标推按照CB/T 1.1—2009给出的规则起草SN/T3394—2012
请注意本文件的某些内容可能涉及专利。本文件的发布机构不承担识别这些专利的责任本标准由国家认证认可监督管理委员会提出并归口。本标准起草单位:中国检验检疫科学研究院,中华人民共和国福建出人境检验检疫局,中华人民共和国辽宁出人境检验检疫局。
本标准要起草人:姚李叫、韩辉、黄恩炯、张晓龙、杨宁曹晓梅、米峰林.高博.徐宝梁。1范围
马秋波病毒实时荧光RT-PCR检测规程SN/T 3394—2012
木标雅规定了国境口岸人出境人员或鼠类携带马秋波病毒的实时荧光RT-PCR快速检测方法,包括检测对象,标本采集和处理、检测程序,结果判定及报告。本标推适用于国境口岸人出境人员或鼠类携带马秋波病毒的分子牛物学检测。2规范性引用文件
下列文件对丁本文件的应用是必不可少的。凡是注口期的引用文件,仅注口期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GI319489实验室生物安全通用要求WS 233微生物和生物医学实验室生物安全通用准则可感染人类的高致病性病原微生物菌(毒)种或样木运输管理规定(2(,卫牛部)3术语和定义
下列术语和定义适用于本文件。3.1
machupo virus
马秋波病毒
属沙粒科,包括8种进化支,基因组为分节段双链RNA,山L(人)和S(小)片段组成,分别编码依赖RNA的 RNA 聚合酶、锌指蛋白私包膜糖蛋白,核蛋。1962年首次在玻利维亚发现故其引起的出而热又名玻利维亚出血热。该病毒山肼脏暮鼠(Cutomys cullosus·又称白足鼠)携带传播,主要通过鼠的分泌物感染人类。
4缩略语
下列缩略语适用于本文件,
RTPCR:逆转泵聚合酶链式反扇
Ct值:循环谢值,每个反应管的荧光信号达到设定值时所经历的循环数RNA:核糖核酸
DEPC:焦碳酸二乙酪
FAM:6-羧基荧光素.-种荧光报告基团BHQ:洞淬灭基团
5检测对象
疑似感染马秋波病毒的人出境人员以及疑似携带马秋波病毒的鼠。1
SN/T3394—2012
6生物安全要求
6.1检测工作中的个人防护按照GB194896.2实验室应遵循GB19489和WS233对生物安全3级(BSL-3)实验室的生物安全要求。6.3使用过的实验用品应遵照GB19489对废弃物的处理要求进行无害化处理。6.4样本运输应按照可《感染人类的高致病性病原微生物菌(毒)种或样本运输管理规定》的相关规定。7仪器和设备
7.1荧光定量PCR仪。
7.2生物安全柜。
7.3普通冰箱。
7.4一70℃及以下超低温冰箱。
7.5普通台式离心机。
7.6高速冷冻离心机(转速可达20000g7.7涡旋器。
7.8微量可调移液器(10、100叫,1009L)及配套带被芯吸头8试剂
8.1标准标本处理液:在新鲜配制的mLMEM中加人56
热灭活30min的胎牛血清2ml
2.50g/mE和1mlwww.bzxz.net
1mL庆大霉素(5000μg/mL)1ml两性素B(2链霉素10.000pg/mL),用7.5%炭酸氢钠溶液调至P7.2
QIAampViral
8.2核酸提取试剂:用德国Qiagen公司RNAKiL
青链霉索(青霉素G10.000U/ml
Ag Path IDTMOne step
8.3实时荧光RT-PCR试剂:用ABI公司的RT-PCRKit
8.4DEPC水。
8.5实时荧光RT-PCR引物及探针
上游引物PrimerF(5-3)ACCCTCAATGATGAAWCAAAGAAAG、下游引物PrimerR(5'3):AAGAGTGTGCTGCKCTGC及探针PTob(5-3FAMRAATCTTCTAAGCCAGACAGTGAATGCCTY-BHQI
注:引物序列中的简并碱基W表示A或T,R表示G或A.Y表示C或T。等效的其他检测试剂盒也可使用。9检测程序
9.1标本的采集、运输、处理及保存9.1.1人血清标本
无菌采集有出血热疑似症状的人静脉血2mL~5mL,室温静置30min使其凝固,然后500g离心10min,去除纤维蛋白和血红蛋白,收集血清于2ml.无菌螺口塑料管中,用耐低温油性记号笔记上编号,低温送到实验室,立即对血清标本进行核酸提取,如不能在2h内检测应存放在一70℃冰箱。1)由指定单位提供,给出这一信息是为了方便本标准的使用者,并不表示对该产品的认可。如果其他等效产品具有相同的效果,则可使用这些等效产品2
9.1.2鼠标本
SN/T 3394—2012
采集鼠类标本,三氯甲烷熏燕后分抹奇生虫,解剖取出肺组织,装人2mI.螺口塑料管内或小型塑料袋,用耐低温油性记号笔记上编号,于70℃以下运输。从一70 ℃容器中取山鼠肺标本,倒人研磨器中,加人 Hank':液!mI.吹洗,弃去液体后加人 1 mL标本处理液.反复研磨至组织碎片基本消失、随后将研磨液吸人 1,5 mL ePpendlorf 离心管,配平后置预冷1℃的离心机上,20 000g 离心10 miin。取上清液进行核酸提取,剩余的鼠内脏标本研磨液需保存在一70冰箱以备复查。
9.2病毒核酸提取
取血清标本或鼠标本研磨液140 μl.加人560 μI.裂解液(AV1.),在旋涡混合器上振荡15 s混匀,室温静置 10 mina
加人560 μl.无水乙醇终正反应,在旋涡混合器上振荡15s混勾。裂解后的液体分两次移人管柱,每次6coog离心1min,此时病毒R:NA会吸附在管杜底部的膜工。
加500μL洗液(AW1)至管柱上.6000g离心1min.弃AW1,加t500μl.洗波(AW2)至管柱上,20000g离心3min.弃去AW2.20000g离心1min以彻底去除残留在膜[乙醇。
加人 60 μL洗脱液(AVE)、空温静置1 min。将管柱置于1.5mL离心管上4℃下6000g离心1min,得到的RNA即可进行实时荧光RT-PCR检测。
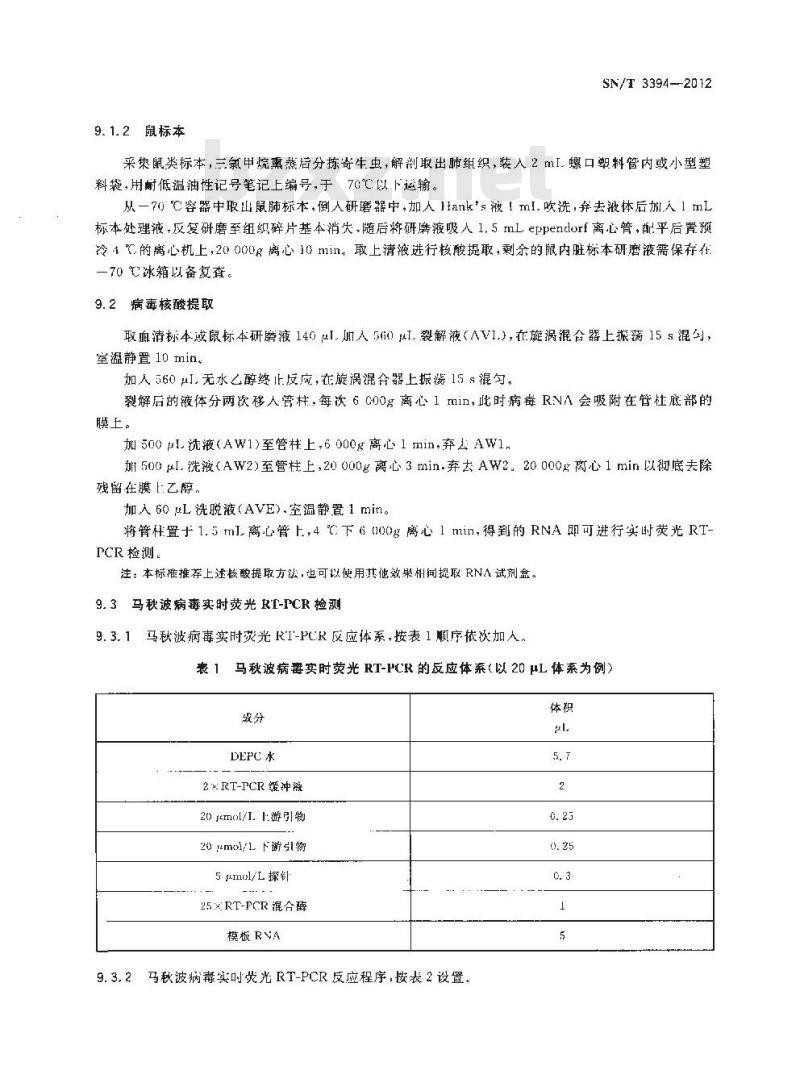
注:本标准推荐上述核酸提取方法,也可以使用其他效果相向提取 RNA 试剂盒。9.3马秋波病毒实时荧光RT-PCR检测9.3.1马秋波病毒实时荧光RI-PCR反应体系,按表1顺序依次加人。表 1马秋波病毒实时荧光 RT-PCR 的反应体系(以 20 μL 体系为例)成分
DEPC水
2×RT-PCR缓冲液
20 μmol/I. 游引物
20mol/1下游引物
5l/L探钮
25×RT-PCR 混合醇
模板RVA
9. 3. 2马秋波病毒实时荧光RT-PCR反应程序,接表 2 设置。体积
SN/T 3394—2012
逆转录
扩增及荧光收集
表 2马秋波病毒实时荧光 RT-PCR的反应程序反温度
93 ℃
循环数
注:程序设置是以ABII'risni73co型全自动荧光定举PcR检测仪为例说明,将费光信号设置为:ReporterDyelFAM.QnrnrhrrTsyel:NoNE,PassiveReference:RCX,其他型号的实时荧北PCR仪,可参考上速程序作适当调整。
10结果判定及报告
10.1基线和对照
根据使用不同的荧光定量PCR仪设定好基线,设定的般原则以阐值线刚好超过正常阴性对照扩增曲线的最高点,也可根据仪器噪音情况调整,阳性对照可为马秋波病毒核酸,也可为根据马秋波病母核苷酸序列体外合成的RNA片段,阴性刘照为不含马秋波病毒核酸的标本。10.2实时荧光RT-PGR反应的质量控制实验检测的结果应同时符合以下2个条件,否则试验结果无效:阴性对照无扩增曲线;
一一附性对照t值35并有明显扩增曲线、10.3实时荧光RT-PCR检测结果判定及报告实验检测的结果判定如下:
-阴性:无 Ct值或 Ct值40,且死明显扩增曲线,报告为马秋波病毒荧光RT-PCR检测阴性;附性:C1值≤40,并有明显扩增曲线,报告为马秋波病毒荧光RT-PCR检测阳性;疑似:Cl值在35~-40之间。疑似标本应重做,若重做结果仍为疑似,则报告为马秋波病毒荧光RT-PCR检测附性,
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
马秋波病毒实时荧光RT-PCR检测规程Code of detecting machupo virus by real-time fluorescence RT-PCR2012-12-12发布
中华人民共和国
国家质量监督检验检疫总局
2013-07-01实施
本标推按照CB/T 1.1—2009给出的规则起草SN/T3394—2012
请注意本文件的某些内容可能涉及专利。本文件的发布机构不承担识别这些专利的责任本标准由国家认证认可监督管理委员会提出并归口。本标准起草单位:中国检验检疫科学研究院,中华人民共和国福建出人境检验检疫局,中华人民共和国辽宁出人境检验检疫局。
本标准要起草人:姚李叫、韩辉、黄恩炯、张晓龙、杨宁曹晓梅、米峰林.高博.徐宝梁。1范围
马秋波病毒实时荧光RT-PCR检测规程SN/T 3394—2012
木标雅规定了国境口岸人出境人员或鼠类携带马秋波病毒的实时荧光RT-PCR快速检测方法,包括检测对象,标本采集和处理、检测程序,结果判定及报告。本标推适用于国境口岸人出境人员或鼠类携带马秋波病毒的分子牛物学检测。2规范性引用文件
下列文件对丁本文件的应用是必不可少的。凡是注口期的引用文件,仅注口期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GI319489实验室生物安全通用要求WS 233微生物和生物医学实验室生物安全通用准则可感染人类的高致病性病原微生物菌(毒)种或样木运输管理规定(2(,卫牛部)3术语和定义
下列术语和定义适用于本文件。3.1
machupo virus
马秋波病毒
属沙粒科,包括8种进化支,基因组为分节段双链RNA,山L(人)和S(小)片段组成,分别编码依赖RNA的 RNA 聚合酶、锌指蛋白私包膜糖蛋白,核蛋。1962年首次在玻利维亚发现故其引起的出而热又名玻利维亚出血热。该病毒山肼脏暮鼠(Cutomys cullosus·又称白足鼠)携带传播,主要通过鼠的分泌物感染人类。
4缩略语
下列缩略语适用于本文件,
RTPCR:逆转泵聚合酶链式反扇
Ct值:循环谢值,每个反应管的荧光信号达到设定值时所经历的循环数RNA:核糖核酸
DEPC:焦碳酸二乙酪
FAM:6-羧基荧光素.-种荧光报告基团BHQ:洞淬灭基团
5检测对象
疑似感染马秋波病毒的人出境人员以及疑似携带马秋波病毒的鼠。1
SN/T3394—2012
6生物安全要求
6.1检测工作中的个人防护按照GB194896.2实验室应遵循GB19489和WS233对生物安全3级(BSL-3)实验室的生物安全要求。6.3使用过的实验用品应遵照GB19489对废弃物的处理要求进行无害化处理。6.4样本运输应按照可《感染人类的高致病性病原微生物菌(毒)种或样本运输管理规定》的相关规定。7仪器和设备
7.1荧光定量PCR仪。
7.2生物安全柜。
7.3普通冰箱。
7.4一70℃及以下超低温冰箱。
7.5普通台式离心机。
7.6高速冷冻离心机(转速可达20000g7.7涡旋器。
7.8微量可调移液器(10、100叫,1009L)及配套带被芯吸头8试剂
8.1标准标本处理液:在新鲜配制的mLMEM中加人56
热灭活30min的胎牛血清2ml
2.50g/mE和1mlwww.bzxz.net
1mL庆大霉素(5000μg/mL)1ml两性素B(2链霉素10.000pg/mL),用7.5%炭酸氢钠溶液调至P7.2
QIAampViral
8.2核酸提取试剂:用德国Qiagen公司RNAKiL
青链霉索(青霉素G10.000U/ml
Ag Path IDTMOne step
8.3实时荧光RT-PCR试剂:用ABI公司的RT-PCRKit
8.4DEPC水。
8.5实时荧光RT-PCR引物及探针
上游引物PrimerF(5-3)ACCCTCAATGATGAAWCAAAGAAAG、下游引物PrimerR(5'3):AAGAGTGTGCTGCKCTGC及探针PTob(5-3FAMRAATCTTCTAAGCCAGACAGTGAATGCCTY-BHQI
注:引物序列中的简并碱基W表示A或T,R表示G或A.Y表示C或T。等效的其他检测试剂盒也可使用。9检测程序
9.1标本的采集、运输、处理及保存9.1.1人血清标本
无菌采集有出血热疑似症状的人静脉血2mL~5mL,室温静置30min使其凝固,然后500g离心10min,去除纤维蛋白和血红蛋白,收集血清于2ml.无菌螺口塑料管中,用耐低温油性记号笔记上编号,低温送到实验室,立即对血清标本进行核酸提取,如不能在2h内检测应存放在一70℃冰箱。1)由指定单位提供,给出这一信息是为了方便本标准的使用者,并不表示对该产品的认可。如果其他等效产品具有相同的效果,则可使用这些等效产品2
9.1.2鼠标本
SN/T 3394—2012
采集鼠类标本,三氯甲烷熏燕后分抹奇生虫,解剖取出肺组织,装人2mI.螺口塑料管内或小型塑料袋,用耐低温油性记号笔记上编号,于70℃以下运输。从一70 ℃容器中取山鼠肺标本,倒人研磨器中,加人 Hank':液!mI.吹洗,弃去液体后加人 1 mL标本处理液.反复研磨至组织碎片基本消失、随后将研磨液吸人 1,5 mL ePpendlorf 离心管,配平后置预冷1℃的离心机上,20 000g 离心10 miin。取上清液进行核酸提取,剩余的鼠内脏标本研磨液需保存在一70冰箱以备复查。
9.2病毒核酸提取
取血清标本或鼠标本研磨液140 μl.加人560 μI.裂解液(AV1.),在旋涡混合器上振荡15 s混匀,室温静置 10 mina
加人560 μl.无水乙醇终正反应,在旋涡混合器上振荡15s混勾。裂解后的液体分两次移人管柱,每次6coog离心1min,此时病毒R:NA会吸附在管杜底部的膜工。
加500μL洗液(AW1)至管柱上.6000g离心1min.弃AW1,加t500μl.洗波(AW2)至管柱上,20000g离心3min.弃去AW2.20000g离心1min以彻底去除残留在膜[乙醇。
加人 60 μL洗脱液(AVE)、空温静置1 min。将管柱置于1.5mL离心管上4℃下6000g离心1min,得到的RNA即可进行实时荧光RT-PCR检测。
注:本标准推荐上述核酸提取方法,也可以使用其他效果相向提取 RNA 试剂盒。9.3马秋波病毒实时荧光RT-PCR检测9.3.1马秋波病毒实时荧光RI-PCR反应体系,按表1顺序依次加人。表 1马秋波病毒实时荧光 RT-PCR 的反应体系(以 20 μL 体系为例)成分
DEPC水
2×RT-PCR缓冲液
20 μmol/I. 游引物
20mol/1下游引物
5l/L探钮
25×RT-PCR 混合醇
模板RVA
9. 3. 2马秋波病毒实时荧光RT-PCR反应程序,接表 2 设置。体积
SN/T 3394—2012
逆转录
扩增及荧光收集
表 2马秋波病毒实时荧光 RT-PCR的反应程序反温度
93 ℃
循环数
注:程序设置是以ABII'risni73co型全自动荧光定举PcR检测仪为例说明,将费光信号设置为:ReporterDyelFAM.QnrnrhrrTsyel:NoNE,PassiveReference:RCX,其他型号的实时荧北PCR仪,可参考上速程序作适当调整。
10结果判定及报告
10.1基线和对照
根据使用不同的荧光定量PCR仪设定好基线,设定的般原则以阐值线刚好超过正常阴性对照扩增曲线的最高点,也可根据仪器噪音情况调整,阳性对照可为马秋波病毒核酸,也可为根据马秋波病母核苷酸序列体外合成的RNA片段,阴性刘照为不含马秋波病毒核酸的标本。10.2实时荧光RT-PGR反应的质量控制实验检测的结果应同时符合以下2个条件,否则试验结果无效:阴性对照无扩增曲线;
一一附性对照t值35并有明显扩增曲线、10.3实时荧光RT-PCR检测结果判定及报告实验检测的结果判定如下:
-阴性:无 Ct值或 Ct值40,且死明显扩增曲线,报告为马秋波病毒荧光RT-PCR检测阴性;附性:C1值≤40,并有明显扩增曲线,报告为马秋波病毒荧光RT-PCR检测阳性;疑似:Cl值在35~-40之间。疑似标本应重做,若重做结果仍为疑似,则报告为马秋波病毒荧光RT-PCR检测附性,
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。